Темір: периодтық жүйедегі орны, атом құрылысы, таралуы, өндірісі, қасиеттері және қолданылуы



Темір

Мазмұны:
Периодтық жүйедегі орны және атом құрылысы
Табиғатта таралуы
Өнеркәсіпте алынуы
Физикалық қасиеттері
Химиялық қасиеттері
Темірдің маңызды қосылыстары
Қолданылуы
Құрамында темірі бар қосылыстар

Жалпы сипаттама. Периодтық жүйедегі орны және атом құрылысы
Темір - VIIIБ топ элементі, d - элемент. Темірдің валенттік электрондары сыртқы s-e және сырттан санағанда екінші деңгейдегі d-e болып табылады, сондықтан ол ауыспалы тотығу дәрежелерін көрсетеді.
Next
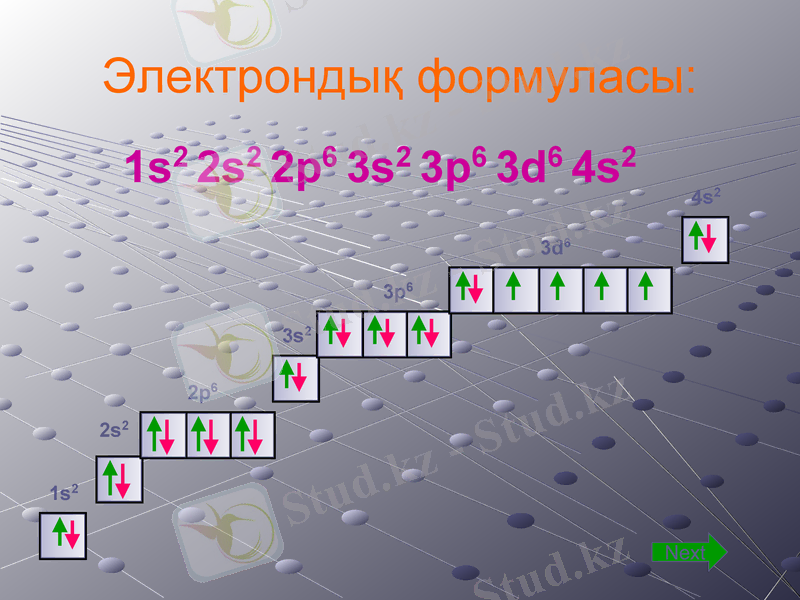
Электрондық формуласы:
1s2 2s2 2p6 3s2 3p6 3d6 4s2
1s2
2s2
2p6
3s2
3p6
3d6
4s2
Next

Темір химиялық реакцияларда 2 немесе 3 электрон беріп, өзінің тұрақты қосылыстарында +2 және +3 тотығу дәрежелерін көрсетеді:
Fe0 - 2e Fe2+
Fe0 - 3e Fe3+
Темірдің тотығу дәрежесі +6 (K2FeO4 - калий ферраты) болатын тұрақтылығы төмен қосылыстары белгілі.
Back

Табиғатта таралуы
Темір - табиғатта таралуы бойынша екінші металл. Оның жер қыртысындағы үлесі 5, 1%. Көптеген метеориттердің құрамында темір бар, сондықтан оны ертеде “аспан” және “жұлдыз” тасы деп атаған. Жер қыртысында темір көптеген минералдар түзеді. Темірдің маңызды өнеркәсіптік кендері: қызыл теміртас (Fe2O3), магниттік теміртас (Fe3O4), пирит (FeS2) . Елімізде темір кендерінің үлкен қоры Рудный темір кені бассейінінде және Орталық Қазақстанда бар. Қазіргі уақытта елімізде бірнеше жүздеген кен орындары мен кен ошақтары белгілі. Көптеген кен орындарында кендердің аз тереңдікте орналасуы оларды арзан ашық әдіспен өндіруге мүмкіндік береді.
Темір минералды сулардың құрамына сульфат (FeSO4) және гидрокарбонат Fe(HCO3) 2 түрінде кіреді.
Темір тұздары теңіз суларында бар, мұхит түбінде темірге бай табиғи шөгінділер кездеседі.
Next
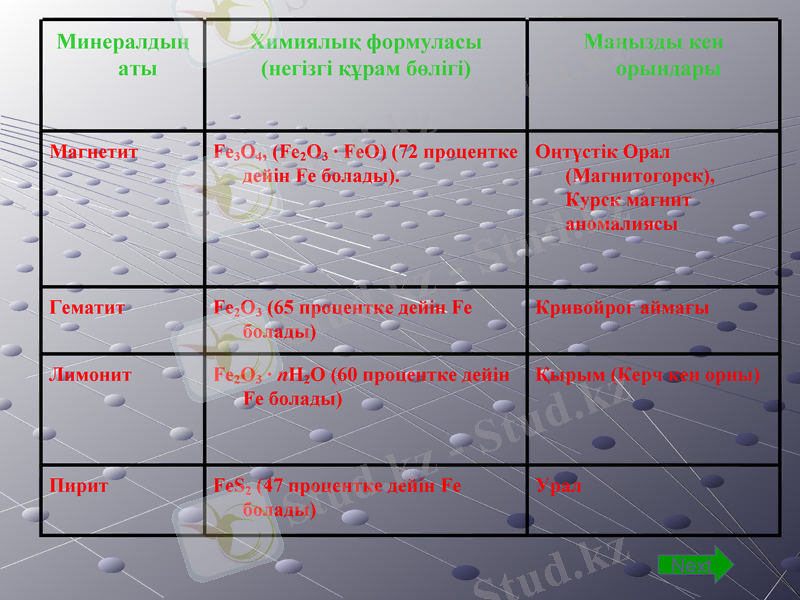
Минералдың аты
Химиялық формуласы
(негізгі құрам бөлігі)
Маңызды кен орындары
Магнетит
Fe3O4, (Fe2O3 ∙ FeO) (72 процентке дейін Fe болады) .
Оңтүстік Орал (Магнитогорск), Курск магнит аномалиясы
Гематит
Fe2O3 (65 процентке дейін Fe болады)
Кривойрог аймағы
Лимонит
Fe2O3 ∙ nH2O (60 процентке дейін Fe болады)
Қырым (Керч кен орны)
Пирит
FeS2 (47 процентке дейін Fe болады)
Урал
Next

Минералдар:
Магнетит
Гематит
Next

Лимонит
Пирит

Қазақстанда темірдің бай қоры бар, ол Торғай темір кенді бассейнінде және Орталық Қазақстанда орналасқан. Қазіргі кезде елімізде темірдің жүздеген кен орындары мен кен жылғалары белгілі болып отыр. Көптеген кен орындарындағы кеннің жер бетіне жақын жатуы оны арзан, ашық әдіспен өндіруге мүмкіндік береді.
Темір сульфат және гидрокарбонат түрінде минералды сулардың құрамына кіреді. Темір тұздары теңіз суларында да бар, сол сияқты мұхиттардың түбінде де темірге әжептәуір бай табиғи шөгінділер кездеседі.
Темір тірі организмдерде де болады. Ересек адамның денесінде 4-5 грамм темір бар. Оның 65%-і қандағы гемоглобиннің құрамына кіреді. Гемоглобин қанға қызыл түс береді және тыныс алу процесінде оттекті әр түрлі ұлпаларға тасымалдайды. Қанның құрамында темірдің жетіспеуі қан азаюына әкеліп, адам денсаулығын әлсіретеді.
Байланысқан күйдегі темір көптеген тағамдық өнімдерде: қара нан, картоп, алма, өрік, қарақұмық жармасында кездеседі. Бұл өнімдерді әркім өзінің тамақтану рационына кіргізіп, қан азаюының алдын алуға тиісті.
Back

Өнеркәсіпте алынуы:
Темірді 3 түрлі әдіспен алуға болады:
Пирометаллургиялық әдіспен:
оксидінен тотықсыздандыру арқылы:
Fe2O3 + 3H2 = 2Fe + 3H2O
соның ішінде алюминтермиялық әдіспен:
Fe2O3 + 2Al = Al2O3 + 2Fe
және көміртек (ІІ) оксидімен тотықсыздан-дыру арқылы:
Fe3O4 + 4CO = 3Fe + 4CO2
Back

Физикалық қасиеттері:
Темір - жылтыр, күміс түстес ақ металл, оның тығыздығы - 7, 87 г/см3. Балқу температурасы жоғары - 15390С. Темір иілімді, магниттелетін және оны жоғалтатын қасиеті бар, осыған орай техникада кеңінен қолданылады. Темірді электрмотор, электрмагнит трансформаторларының өзекшесін және микрофон мембранасын жасауға қолданылады. Іс жүзінде темірдің құймалары - шойын мен болат көбірек қолданылады.
Back

Химиялық қасиеттері:
I. Жай заттармен әрекеттесуі:
Темір оттекте жанғанда екі тотығу дәрежесін де (+2, +3) көрсетеді, ұшқын шашыратып жанады:
3Fe + 2O2 = Fe3O4
Next

Ылғалды ауада тат түзеді:
4Fe + 2H2O + 3O2 = 4FeO(OH)
Белсенді бейметалдар темірді тотықтырады:
2Fe + 3Cl2 = 2Fe3+ Cl3-
Fe + S = FeS
3Fe + C = Fe3C
Next

II. Күрделі заттармен әрекеттесуі:
Қатты қыздырылған темір су буымен әрекеттеседі:
Fe + H2O = FeO + H2
Концентрлі азот және күкірт қышқылдарында темір енжарланады, өйткені ерімейтін қосылыстардың қорғағыш қабатшасымен қапталады.
Сұйылтылған азот және күкірт қышқылдарымен әрекеттесіп, темір тотықсызданады:
Fe + 4HNO3(сұйық) = Fe(NO3) 3 + NO + 2H2O
Fe + H2SO4(сұйық) = FeSO4 + H2
Темір белсенділігі төмен металдарды олардың тұздарынан тотықсыздандырып, ығыстырып шығарады:
Fe + CuCl2 = FeCl2 + Cu
Back

Темірдің маңызды қосылыстары:
Темір (ІІ) оксиді немесе (FeO) - негіздік оксид, оңай тотығатын қара ұнтақ, оны мына реакция бойынша алады:
Fe2O3 + CO 2FeO + CO2
Қышқылдармен және қышқылдық оксидтермен әрекеттесіп тұз түзеді:
FeO + 2HCl = FeCl2 + H2O
FeO + CO2 = FeCO3
Next

Темір (ІІІ) оксиді Fe2O3 - амфотерлі оксид, бірақ негіздік қасиеті басымдау, ең тұрақты оксид, қызыл-қоңыр түсті, минералы гематит.
І. Алынуы: 1) 2Fe(OH) 3 = Fe2O3 + 3H2O
2) 3Fe + 2O2 = Fe3O4
3) 3Fe + 4HOH = Fe3O4 + 4H2
ІІ. Химиялық қасиеттері:
қышқылмен Fe2O3 + 3H2SO4 = Fe2(SO4) 3 + 3H2O
қышқылдық оксидпен Fe2O3 + 3SO3 = Fe2(SO4) 3
негізбен Fe2O3 + 2NaOH = 2NaFeO2 + H2O
Next

Темірдің гидроксидтері
Темірдің ІІ және ІІІ валентті оксидтеріне екі түрлі гидроксидтері сәйкес келеді.
Fe (II) гидроксиді - ақ түсті, ал Fe (III) гидроксиді - қызыл-қоңыр түсті. Олар суда ерімейтін заттар.
І. Алынуы. FeCl2 + 2NaOH = Fe(OH) 2 + 2NaCl
FeCl3 + 2NaOH = Fe(OH) 3 + 3NaCl
- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz