Химиялық және газдық коррозия: түрлері, кинетикасы, әсер ететін факторлар және қорғау әдістері



Химиялық коррозия
Жасаған: Баймухамбет Қырмызы
Борамбаева Сауле

Мазмұны:
Коррозия түрлері
Химиялық коррозия түрлері;
Газ коррозиясының кинетикасы;
Газ коррозиясына әсер ететін факторлар;
Металдар мен қорытпаларды газ коррозиясынан қорғау әдістері.

Коррозия түрлері
Химиялық коррозия
Электрохимиялық коррозия
Химиялық коррозия деп -металдың беткі қабатының сыртқы ортамен химиялық өзара əрекеттесуімен жүретін өзіндік бұзылуды айтады.
Металдардың электрхимиялық коррозиясы деп - металдардың электр өткізгіштігі ерітінді - электролиттердің сыртқы ортамен өзара əсерлесуі кезінде өзіндік бұзылуын айтады.

Химиялық коррозия түрлері
Газ коррозиясы
Бейэлекторлиттік коррозия
Жоғарғы температурада құрғақ газдармен (ауамен, отынның газ тəрізді жану өнімімен) металдың əрекеттесуі салдарынан болатын коррозия - газ коррозиясы деп аталады. Мысалы, іштен жану - қозғалтқыштың, жану камерасының, жану отынының газ өнімінің əсерінен болған реактивті тілке материалдарының коррозиясы.
Электр тогы жүрмейтін ортада металдың сұйықпен өзара əрекеттесуі кезінде (мұнай, мұнай өнімі, ерітілген күкірт, т. б. ), электролит еместерде химиялық коррозия жүреді. Коррозияның бұл түрі мұнай жəне газ тасымалдайтын көліктер мен оның шикізаттарын сақтайтын орындарда өте жиі кездеседі. Əсіресе, оның құрамында күкірті болса, осы коррозия түріне ұшырайды.

Металдардың газ коррозиясының кинетикасы
Көптеген металдар ауа оттегісімен өзара əсерлесуінен, тотық қабыршағымен қапталады. Алдымен металға жеткен оттегі молекулалары адсорбцияланады, яғни мономолекулярлы қабыршық пайда болып, оның беткі қабатына жабысады:
Ме (т) + О2 (г) = Ме (т) / 2Оадс.

Металдағы қабыршықты қалыңдығына байланысты былай бөледі:
§ жұқа (көрінбейтін) қалыңдық - мономолекулярлы қабаттан 40 нм-ге дейін;
§ орташа (көрінер-көрінбес түсті), оның қалыңдығы - 40 - 500 нм;
§ қалың (көрінетін қабат) қалыңдығы 500 нм-ден артық.

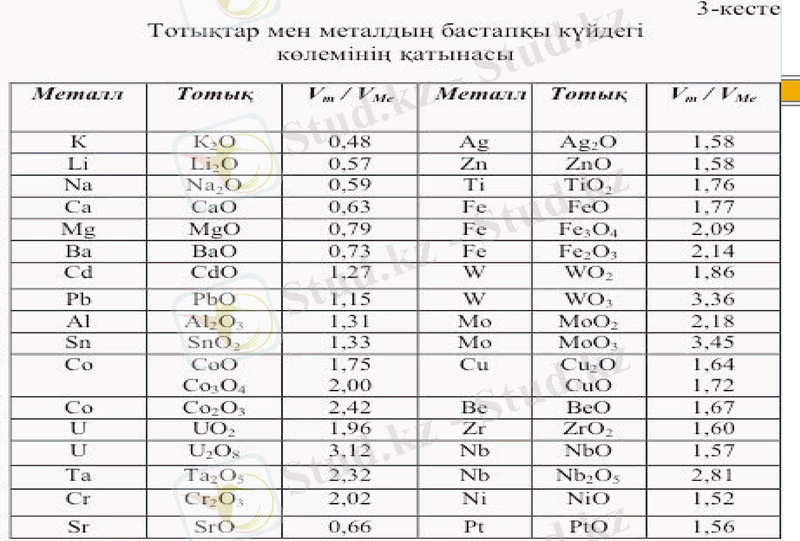
Тотықтың молекулярлы көлемін Vт деп, ал осыдан тотық молекуласы пайда болған металл көлемін VМе деп белгілеп, былай жазуға болады:
Vт / VМе > 1 болғанда, тұтас қабыршық пайда болады.
Vт / VМе < 1 болғанда, тұтас емес (кеуекті) қабыршық пайда болады.

Пайда болған тотық көлемі мен бастапқы металл қатынасын оңай есептеуге болады. 1г - атомдық металдың көлемі мынаған тең:
мұндағы А - металдың атомдық массасы;
ρМе - металдың тығыздығы.
Алынған тотықтың грамм-молекула көлемі мына теңдеумен анықталады:
мұндағы М - тотықтың грамм-молекулалық массасы;
n - тотықтағы металл атомдарының саны;
ρт - тотықтың тығыздығы.

Газ коррозиясына әсер ететін факторлар
Ішкі факторлар
Сыртқы факторлар
Ішкі факторларға - металдың өзімен тікелей байланысты, газ коррозиясына әсер ететін факторлар жатады. Мысалы қорытпаның табиғаты, химиялық және фазалық құрамы, оның құрылымы, беткі қабатының өңделуі, механикалық кернеулер- дің болуы, т. б.
Сырттан əсер ететін факторларға - коррозиялық ортаның құрамы мен коррозия жағдайларына байланысты факторлар жатады. Демек, газды ортаның құрамы, температура, ортаның қозғалыс жылдамдығы, қысым, т. б.

Газды ортаның құрамы
Жоғары температурада металдар оттегімен, су буларымен, көміртегі оксидтері жəне күкірт оксидтерімен өзара əрекеттеседі:
2Ме + О2 = 2МеО
Ме + СО2 = МеО + СО
Ме + Н2О = МеО + Н2
3Ме + SО2 = 2МеО + МеS
900°С кезінде темірдің, кобальт пен никелдің тотығу жылдамдығы мына қатармен өседі: Н2О → СО2 → О2 → SО2

Болаттар мен қорытпалардың коррозиясына құрамында су буы, көміртегі оксидтері мен күкірт оксидтерінен басқа, жану отынының өнімдері де айрықша əсер етуі мүмкін. Кейбір жағдайларда, мысалы сұйық отынның жануы кезінде (мазут, мұнай) күлдің мөлшерінің көп болуы - V2O5. Күл металға жабысып, ванадийлі коррозияны тудыра отырып, оның тотығу жылдамдығын арттырады. Оның себебі - V2O5 жеңіл балқуы, оның темірдегі тотық қабыршығын флюстеу қабілеттілігі (сұйық күйге өтуі) . Темірдің тотығу процесіне мына реакциямен қатысады:
Fe2O3 + V2O5 = 2FeVO4
4Fe + 3 V2O5 = 2Fe2O3 + 3V2O3
V2O3 + O2 = V2O5

Əр түрлі температуралық аралықта металдар əр түрлі тотықтанады. Тотығудың сызықтық заңы - натрий, кальций, магний үшін; параболалық - мыс, темір, никель үшін; логарифмдік - алюминий, мырыш, хром үшін дұрыс болады. Мыс 100°С температураға дейін логарифмдік заңдылық бойынша, ал 300-ден 1000°С-ға дейін - параболалық бойынша тотығады. Темір 400°С-қа дейін логарифмдік заңдылығы бойынша, ал 500-1100°С аралықта-параболалық заңдылығы бойынша тотығады.

Температура әсері
Коррозия жылдамдығының температураға байланыстылығы, экспоненттік заңына жақын, ол Аррениус теңдеуімен былай жазылады:
мұндағы k - химиялық реакция жылдамдығының константасы немесе диффузия коэффициенті;
A - тұрақты, 1/Т = 0 болғанда k-ға тең;
Q - химиялық реакцияның активтелу энергиясы немесе диффузия;
R - газ тұрақтысы, 1, 987 кал/моль немесе 8, 314 Дж/К·мольге тең;
T - абсолюттік температура.
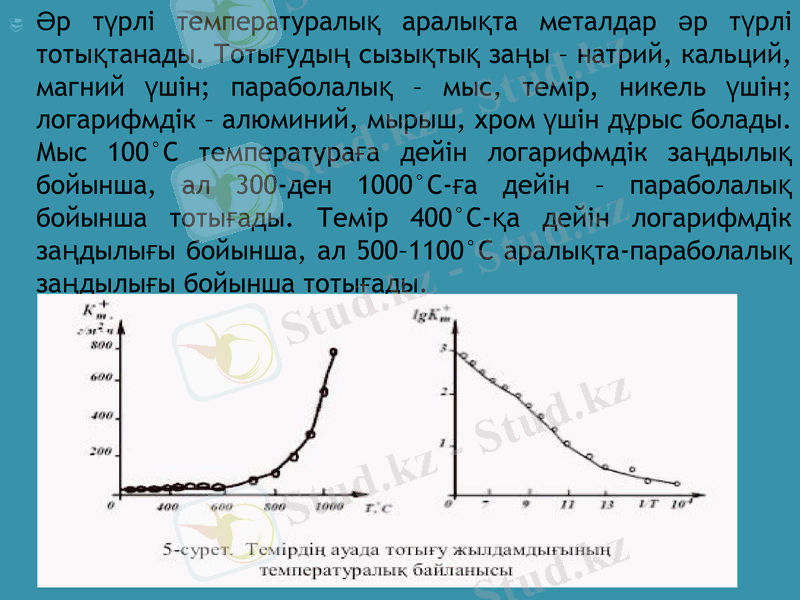
Əр түрлі температуралық аралықта металдар əр түрлі тотықтанады. Тотығудың сызықтық заңы - натрий, кальций, магний үшін; параболалық - мыс, темір, никель үшін; логарифмдік - алюминий, мырыш, хром үшін дұрыс болады. Мыс 100°С температураға дейін логарифмдік заңдылық бойынша, ал 300-ден 1000°С-ға дейін - параболалық бойынша тотығады. Темір 400°С-қа дейін логарифмдік заңдылығы бойынша, ал 500-1100°С аралықта-параболалық заңдылығы бойынша тотығады.

Металдар мен қорытпаларды газ коррозиясынан қорғау
қызуға төзімді етіп легірлеу ;
қорғаушы атмосфераларды қолдану;
арнайы қызуға төзімді қаптамалармен металдың беткі қабатын қаптау.

Қызуға төзімді етіп легирлеу
- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz