Кешенді қосылыстар мен комплексондардың химиялық негізі, биологиялық маңызы және фармация мен медицинадағы қолданылуы



ПРЕЗЕНТАЦИЯ
Тақырыбы: Кешенді қосылыстар. Кешенді қосылыстардың биологиялық ролі, фарм. препараттартарын алуда және анализдеу кезінде комплексондардың фармация мен медицинада қолданылуы. Гемоглабин және кобальттың комплексті қосылыстарының фармация мен медицинада қолданылуы, химиялық негізі.

Жоспар
Кіріспе;
Негізгі бөлім;
Кешенді қосылыстар, құрылымы.
Кешенді қосылыстардың номенклатурасы мен түрлері.
Кешенді қосылыстағы химиялық байланыс.
Химиялық қасиеттері.
Биологиялық маңызы; медицинада, фармацияда қолданылуы.
Қорытынды;
Қолданылған әдебиеттер.
Кіріспе
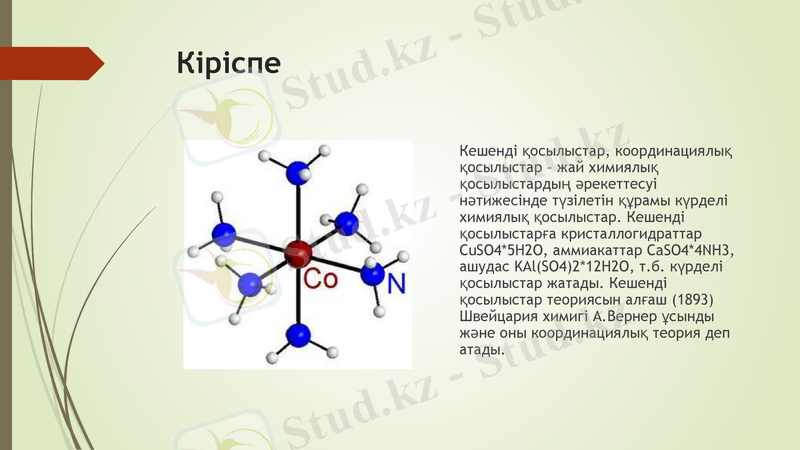
Кешенді қосылыстар, координациялық қосылыстар - жай химиялық қосылыстардың әрекеттесуі нәтижесінде түзілетін құрамы күрделі химиялық қосылыстар. Кешенді қосылыстарға кристаллогидраттар CuSO4*5H2O, аммиакаттар CaSO4*4NH3, ашудас KAl(SO4) 2*12H2O, т. б. күрделі қосылыстар жатады. Кешенді қосылыстар теориясын алғаш (1893) Швейцария химигі А. Вернер ұсынды және оны координациялық теория деп атады.

Құрылымы
Кешенді қосылыстар теориясын алғаш (1893) Швейцария химигі А. Вернер ұсынды және оны координациялық теория деп атады. Бұл теорияға сәйкес Кешенді қосылыстарда орт. орын алып тұрған ион немесе атом кешен түзуші деп, ал оның айналасына жиналған, яғни координацияланған иондарды немесе молекулаларды лигандалар деп атайды. Кешен түзушінің айналасына координациаланған лигандалардың жалпы саны оның координациялық саны деп аталады.
Комплекс түзілу реакциялары электрон жұптарының тасымалдануымен жүзеге асады және бұл комплексті қосылыстарының түзілуіне не бұзылуына әкеледі.
Комплксті қосылыстардың ерекшелігі болып, олардағы донорлы-акцепторлы механизм арқылы түзілген координациялық байланыстың болуы.

Комплекс қосылыстар
Комплексті қосылыстар ерітінді күйде болуға қабілетті, жай молекулалардан тұратын жоғары ретті қосылыстар деп қарастыуға болады.
Комплексті қосылыстар деп лигандалармен қоршалған орталық атомның болуымен ерекшеленетін, кристал күйде де, ерітінді түрінде де бола алатын қосылыс.
Кешенді ионның заряды сыртқы иондар зарядының қосындысына тең, бірақ мәні кері болады.

Кешен түзушінің зарядын табу үшін Кешенді қосылыстардың құрамына кіретін басқа иондардың барлығының зарядының алгебр. қосындысын шығарып, оған теріс мән қояды. Негізгі кешен түзушілерге хим. элементтердің периодтық жүйесінің қосымша топшаларында орналасқан d-элементтері жатады. Маңызды лигандтарға жататын полюсті молекулалар: H2O, NH3, CO, NO, NH2OH, т. б., аниондар: F, Cl-, Br-, Қ-, O2-, OH-, CN-, т. б. Полюсті молекулалар Кешенді қосылыстардың сыртқы сферасында аниондар немесе катиондар болуы кешен ионының зарядына байланысты. Егер қосылыстағы кешен ионының заряды оң болса, сыртқы сферада аниондар орналасады, ал кешен ионының заряды теріс болса, сыртқы сферада катиондар орналасады.

Химиялық байланыс
Комплекс қосылыстардың түзілуі орталық атом мен лиганда арасындағы донорлы-акцепторлы әсерлесуге байланысты. Әдетте электрон жұбының доноры лиганда болса, акцепторы бос орбитальды болатын орталық атом. Бұл байланыс өте берік және комплекстің еуі кезінде үзілмейді, оны координациялық байланыс деп атайды.

Изомерия Химиялық байланыс
Кешенді қосылыстарда δ-байланыстармен қатар донорлы-акцепторлы механизм бойынша π-байланыстар түзіледі. Мұндағы донор өзінің d-электрондарының лигандаға беруші метал ионы, ал акцептор -энергетикалық тиімді вакантты орбитальдары болатын лигандалар. Бұл байланысты дативті деп атайды.
Химиялық қасиеттері
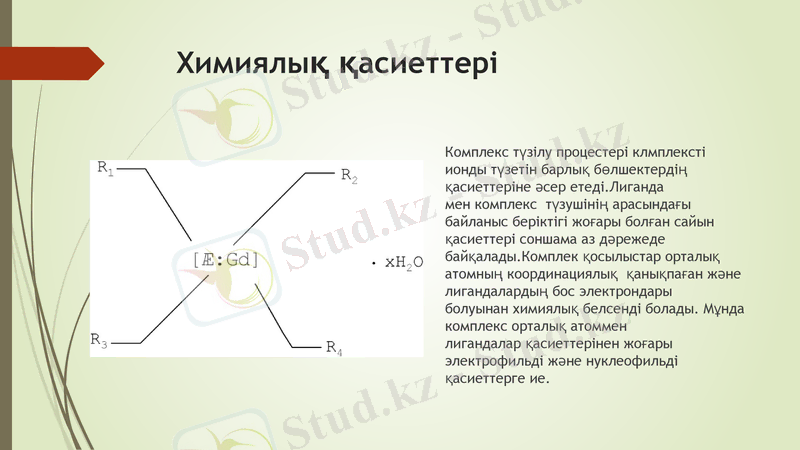
Комплекс түзілу процестері клмплексті ионды түзетін барлық бөлшектердің қасиеттеріне әсер етеді. Лиганда мен комплекс түзушінің арасындағы байланыс беріктігі жоғары болған сайын қасиеттері соншама аз дәрежеде байқалады. Комплек қосылыстар орталық атомның координациялық қанықпаған және лигандалардың бос электрондары болуынан химиялық белсенді болады. Мұнда комплекс орталық атоммен лигандалар қасиеттерінен жоғары электрофильді және нуклеофильді қасиеттерге ие.

Комплекс реагентпен әрекеттесу порцесі мына қосылсытар түзілгенде жүреді:
А) аз диссоциаланатын қосылыс;
Б) аз еритін қосылыс;
В) одан тұрақты қосылыс;
Г) тотығу-тотықсыздану өнімдері
Жай бөлшектерден құралған комплекс ионы олардың өлшемінен үлкен болады. Оның қасиеттері мен беткейіндегі заряд тығыздығы өзгереді. Жай бөлшектерден комплексті қышқылдар түзілгенде Н иондарымен байланыс энергиясы азаяды, қышқыл күші артады.

Қасиеттері
Комплексті қосылыстар тотығу-тотықсыздану реакцияларын көрсетеді:
[Cu(NH3) 4] ²⁺+Zn=[Zn(NH3) 4] ²⁺+Cu
Комплекс түзілу үрдісі d-элментерінің потенциал шамаларына күшті әсер етеді. Егер катиондардың тотықсызданған түрі, берілген лигандамен оның тотыққан түрімен салыстырғанда тұрақтырақ комплекс түзсе, онда потенциал шамасы өседі.
Лиганда табиғатына қарай:аквакомплекстер, аммиакаттар, ацидокомплекстер, гидрокомплекстер, макроцилді комплекстер болып бөлінеді.

Комплекс зарядының таңбасына қарай катионды-комплексті қосылыстағы комлексті катион[Co(NH3) 6] Cl3 анионды-комплексті қосылыстағы анион K[PF6], нейтрал-комплекс заряды 0-ге тең, сыртқы сферасы жоқ.

Жіктелуі
Кешенді қосылыстың белгілі бір класқа жатуына байланысты:
Комплексті қышқылдар H2[SiF6]
Кешенді негіздер [Ag(NH3) 2] OH
Кешенді тұздар K4[Fe(CN) 6]
А) кешен түзуші атом санынан қарай:монядролы-кешенді бөлшек құрамында бір атом кешен түзуші болады, мысалы-[Co(NH3) 6] Cl3; көп ядролы кешенді бөлшек құрамында бірнеше атом кешен түзуші болады.

Биологиялық маңызы
Ағзадағы химиялық элементтердің рөлі сан түрлі. Микроэлементтердің (C, O, N, H, S, P, Ca, CI, Mg, K, Na) ең негізгі функциясы терінің құрауы, осмос қысымын қалыпты ұстап тұру.
Микроэлементы (Cu, F, I, Fe, Mo, Zn, Br, Co), ферментер, гормондар, витаминдер құрамына кіреді де, зат алмасу, көбею, тері тыныс алу поцестеріне қатысады.
Макро және микроэлементтер-сүйек пен тіс ұлпаларының материалы.

K2[PtCl] 4 құрылымы
КҚ-ң биологиялық маңызы
Ағзада кездесетін кешенді қосылыстарда өтпелі металдар ионы болады: Mn, Co, Fe V. Бұл металдардың ағзада мөлшері аз, сондықтан кешенді қосылыстардың ағза өмірі үшін маңызы зор. Себебі: негізінен кешенді қосылыстардың қызметі-атом немесе бүтін молекуланы тасымалдайды, молекулаларды белгілі жерге бекітіп, поляризациялайды. Кешен түзуші металдар-өмірге қажеттелірге жатады.

Порфин
Тірі ағзалар үшін (жануарлар, бактериялар, өсімдіктер) порфин деп аталатын заттың төрт координациялық орныды алып отыратын металдардың кешенді қосылысының маңызы зор. Порфин тобы-пирролотәрізді циклді қосылыстар, =СН-топтарымен біріккен.
Порфиндердің туындылары-порфириндер. Адам ағзасында порифириннің І изомері ауытқу кезінде байқалады.
Таза порфириндер адам ағзасында ешқандай биологиялық белсенділік танытпайды. Олар тек металдармен қосылыс түзе отырып, әсер береді(гем-порфирин мен темір ионының комплексі) . Таза күйінде порфириндер жұмыртқа қабығының түсін беріп тұратын пигменттер, құс қанатындағы пигменттер күйінде болады.

Порфириндер
Порфириндер-қанық боялған қосылыстар. Оларға қазіргі кезде ароматты циклді қосылыстар жатады. Қызыл түсті порфириндерде пирролдар метинді көпіршелер арқылы өзара байланысқан, мұнда макроуикл-порфин деп аталады. Хлорофилдерде, жасыл түстілерде бір не екі пирролы гидрирленген және молекула хлорин деп аталады. Кобалиндер үшін, негізінен В12 дәрумені үшін төрт цикл де гидрирленген, бұл цикл коррин деп аталады.
Гемоглобин, миоглобин, каталаза цитохромдары мен пероксидазада порфириндер темір иондарымен -гем түрінде кешен түзеді. Хлорофилдер мен бактериохлорофилдерде магний бар. В12 дәруменінде орталық ион ретінде кобальт болады.

Гемоглобин
Атмосфералық оттегінің пайдаланылуы тірі ағзалар үшін маңызды биохимиялық үрдіс. Оттегі гемоглобин арқылы өкпеден бұлшықеттерге тасымалданады да, миоглобин бұлшықетінде бекітіліп тұрады. Гемоглобин мен миоглобин ферропротопорфин тобы бар темір(ІІІ) кешенді қосылыстары.

Темірдің кешенді қосылыстары
Темірдің кешенді қосылысы-, ісікті қайтаратын белсенді әсері бар.
Темірдің кешенді қосылысы онкологиялық ауруларды емдеудің көзі боп табылады. Ісікке қарсы препарат ретінде құрамында азолды ферроцендердің туындысы- ұсынылады. жалпы формуласы: R = H, X = CF3 немесе R = H, X = CHF-CF3 .

Натрий
Натрий сульфаты(глаубер тұзы) ішті босатқыш зат ретінде қолданылады. Бұл тұз асқазанға түседі де, осмос қысымын ұзақ уақыт бойы жоғары етеді. Соның арқасында асқазанда су мөлшері көп жиналып, калл массасы тезірек сыртқа шығады.
Натрий тетраборат антисептикалық зат ретінде қолданылады.

Мыс
Қазіргі кезеңде 25 мысты ақуыздар мен ферменттер бар. Ферменттердің бір бөлігі оттегімен әсерлесуді катализдейді.
Қазіргі таңда мысты ферменттер мен ақуыздардың 25 түрі белгілі. Ферменттердің бір бөлігі субстрат пен оттегінің әрекеттесуін белсендіртеді Бұл ферменттер органикалық қосылыстардың тотығуна қатысатын оттегі молекуласын белсендіртеді.
Үлкен концентрацияда мыстың ерімтал тұздары токсинді келеді. Бұл құбылыс мыстың ақуызбен ерімейтін бионеорганикалық хелаттар-альбунминаттар түзілуімен түсіндіріледі.

Медицина мен фармацияда қолданылуы
Биокомплекстік қосылыстар тұрақтылығы бойынша ажыратылады. Олардың кейбіреуінің тұрақты болғаны сонша, олар әрқашан да ағзада болып, белгілі бір функцияны атқарып тұрады.
Құрамына металл ионы кіретін көптеген ферменттер тірі ағзада келесі қызметтер атқарады:1) Олар ферменттердің активті орталығының электрофильді тобы болып келеді және субстрат молекулаларының теріс зарядталған бөліктерімен әсерлесуге мүкіндік береді.
Металл ионы фермент құрылымының каталитикалық активті коыормациясын қалыптастырады.
Кейде түрлі тотығу дәрежесін көрсететін метал иондары электрондар тасымалдауына қатысады.

- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz