Коферменттердің құрылысы мен қызметі: изоферменттер және мүше-спецификациялық ферменттер



ПРЕЗЕНТАЦИЯ
Тақырыбы: Коферменттердің құрылысы мен биологиялық функциясы. Изоферменттер. Мүше-спецификациялық ферменттер.

Жоспар
I. Кіріспе:
II. Негізгі бөлім:
Коферменттер туралы жалпы түсінік
Коферменттердің түрлері
Коферменттердің химиялық құрылымы мен қызметі
Коферменттердің классификациясы
Изоферменттер және олардың қымзеті
III. Қорытынды
IV. Пайдаланылған әдебиеттер

Коферменттер-құрамында белок жоқ органикалық қосылыстар көптеген ферменттер витаминге жатады немесе витаминдер туындысы болып табылады. Коферменттерге активтік тобы бар витаминдер тиаминпирофосфат (в1 витаминнің туындысы ), никотинамидті коферменттер (РР витамині бар) жатады.

I. Витаминдық коферменттер:
1. (НАД, НАДФ)
2. Флавиндік(ФАД, ФМН)
3. Тиаминдық(ТМФ, ТДФ, ТТФ)
4. Кобамидтық (метилкобаламин, дезоксикобаламин)
5. Пиродиксиндік(ПАЛФ, ПАМФ)
6. Фолаттық(ТГФК)
7. Хинондық(убихинон, пластохинон)

II. Витаминдік емес коферменттер:
1. Нуклеотидтер(УДФ-глюкоза, көмірсутектердің,
спирттердің нуклеотидтық туындылары ж/е т. б)
2. Моносахаридтердің фосфаттары(глюкоза-1, 6-дифосфат, 2, 3-дифосфоглицерат)
3. Металлпорфириндер(гемдер, хлорофилдер)
4. Пептидтер(глутатитон)

Витаминдық емес коферменттер:
1. коферменттер
НАД+ және НАДФ+ (НАД+ , НАДФ+ ) . Бұл коферменттердің активті бөлігі никотинамид (РР витамині) болып табылады.
НАД+ пен НАДФ+ тотықсызданған кезде придиннің төрт валенті азот үш валенттіге ауысады және субстраттағы гидрид-ион С4 күидегі никотинамидтік сақинаға ауысады.
НАД пен НАДФ-тің тотықсыздану реакциясы:
НАД +Н +Н НАД-Н+Н
НАДФ +Н +Н НАДФ-Н+Н

Тотыққан(I) және тотықсызданған(II) НАД пен НАДФ-тің формуласы:
2. ФАД және ФМН флавиндік коферменттер. Бұлардың пайда болу көзі-рибофлавин. ФАД және ФМН коферменттері әртүрлі апоферменттермен баиланысады да, флавопротидті ферменттер-флавиндік дегидро геназа түзеді. Қазіргі кезде флавопротеидтердің саны 80 шамасына жетеді
ФАД флавиндік коферменттер. ФАД , ФАД жане ФМН коферменттері әртүрлі.
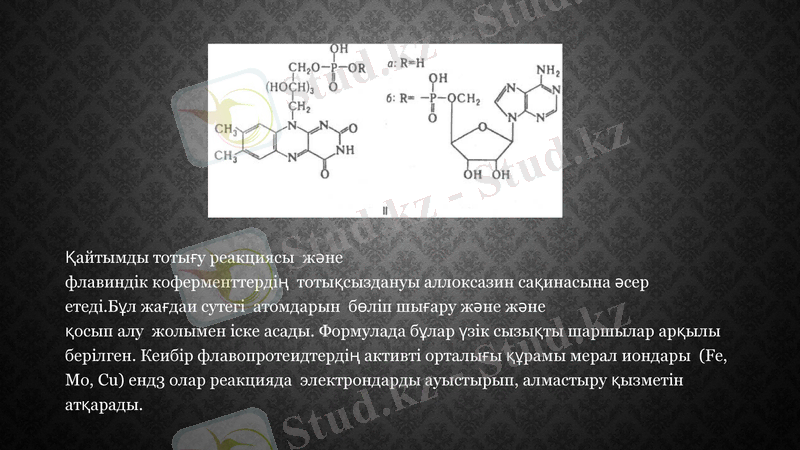
Қайтымды тотығу реакциясы және флавиндік коферменттердің тотықсыздануы аллоксазин сақинасына әсер етеді. Бұл жағдаи сутегі атомдарын бөліп шығару және және қосып алу жолымен іске асады. Формулада бұлар үзік сызықты шаршылар арқылы берілген. Кеибір флавопротеидтердің активті орталығы құрамы мерал иондары (Fe, Mo, Cu) енд3 олар реакцияда электрондарды ауыстырып, алмастыру қызметін атқарады.

3. Тиаминдық коферменттер(ТПФ, ТДФ, ТТФ)
H3C олар апоферменттпен мықты баиланысқан болады және простетикалық топ деп саналады. ТПФ молекуласындағы активті бөлік-тазол сақинасының - CH тобы сол топтың көмегімен ол субстаратпен байланысады.
ТПФ апоферментпен байланысып, декорбаксилаза түзеді. ТПФ - коферменті в1 витаминінің туындысы, оның тиазол сақинасында күкірт бар. Ол апоферментпен мықты баиланысқан.

4. Кобамидтік коферменттер.
Бұлардың пайда болу көзі-витамин В
Цианкобаламиннің орталық бөлігінің (1) және оның екі туындысы-коб- амидтік коферменттердің: метилкобаламин(2) мен 5’- (3) құрылыс нобайы. R’-5’-дезоксиаденозил; R-5, 6-
5. Пиридоксиндік коферменттер.
Бұл коферменттердің негізі В6 витамині, коферменттің құрамында бір-біріне ұқсас үш қосылыс: пиридоксин, пиридоксаль және пиридоксиамин кіреді.
В6 витаминнің негізгі активті туындысы пиридоксаль-5-фосфат болып саналады.

7. Липой қышқылы коферменті құрамында дисульфидтік топ бар, ол топ тотығып екі сульфгидрилдік топ (-SH) құрайды да, дигидролипой қышқылына айналады.
Липой қышқылы өзінің карбоксил тобы арқылы лизиннің ε-амин тобымен апоферментпен пептидтік байланыс жасайды және декарбоксилаза ферменті түзіледі.
Коферменттер
Оксидоредуктаза
Трансфераза
Гидролаза
Лиаза
Изомераза

В1 дәрумені (антиневриттік)
В1 дәрумені - тиамин. Антиневриттік дәрумен. 1912 жылы Функ алғаш рет кристалл түрінде бөліп алып, В1 дәруменінің құрамында аминотоптан басқа күкірт атомы болғандықтан, тиамин деп аталады.
В1 дәрумені -тиаминохлорид
В1 дәруменінің биологиялық белсенді түрі тиаминдифосфат (ТДФ) болып табылады. ТДФ күрделі екі ферменттік жүйенің - пируват және а - комплекстің құрамына кіреді. полимерфттік комплекс ацетил -SkoA және СО2 түзілетін пирожүзім қышқылының тотыға декарбоксилденуін катализдейді.
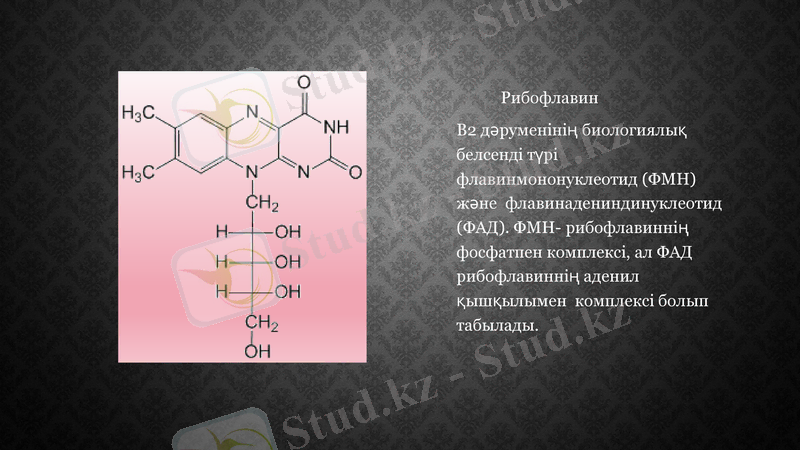
Рибофлавин
В2 дәруменінің биологиялық белсенді түрі флавинмононуклеотид (ФМН) және (ФАД) . ФМН- рибофлавиннің фосфатпен комплексі, ал ФАД рибофлавиннің аденил қышқылымен комплексі болып табылады.

В2 авитаминозының белгілері
Рибофлавиннің ас арқылы жеткіліксіз түсуі организмдегі органикалық заттардың тотығуын нашарлатып, зат алмасу процесін, әсіресе белоктар мен амин қышқылдарының алмасуын төмендетеді. В2 витамині авитаминозында адам шаршағыш келеді, бұлшық еттерден әл кетеді, жүрек еті әлсірейді, балалардың бойының өсуі тежеледі, салмақ қосуы төмендейді, шашы түсіп (алопеция), бас терісі қабыршақтанады (дерматит) . Адам организмінде рибофлавин жетпегенде көздің мөлдір қабығы мен бұршағында кератит, катаракта сияқты аурулар пайда болады, көз қызарып, жас ағып, көру процесі нашарлайды. Тілдің кілегей қабаты қабынады (глоссит), ауызы уылады, екі езудің терісі жарылып, қабынады (ауыздық ауруы) .

Биомедициналық қызметі
Пантотен қышқылы организм үшін өте қажет күрделі органикалық зат коэнзим - А-ның (HSKоA) құрамына енеді:
Коэнзим - А организмдегі негізгі зат алмасу процестеріне қатысады: май қышқылдарының катаболизмі мен анаболизміне, көмірсулар мен майлардың бір-біріне алмасуына өте қажет зат. Егер коэнзим - А организмде жектіліксіз түзілсе, онда зат алмасу процесі бұзылады.

В3 авитаминозының белгілері
Пантотен қышқылы авитаминозында адамдар мен жануарлар әр түрлі ауруларға шалдығады: денедегі түктер мен шаш түсіп, түсі өзгереді, терісі зақымданып, ішкі органдардың кілегей қабаты қабынады, жүйке жүйесі, ішкі секреция бездері зардап шегеді. В3 витаминінің организмде жетіспеуінің ең алғаш белгілері мынадай: адамдардың аяғының саусақтары жансызданып, шанши бастайды, кейінірек саусақтары мен табаны өте қатты ауырып, ол тізеге дейін көтеріледі.
В5 немесе РР дәрумені- никотин қышқылы.

Транскарбоксилдену реакциясы
Н дәруменінің авитаминозының белгілері:
Н дәрумені жетіспегенде адамдарда тері қабыну процесі, тырнақтың зақымдалуы, бұлшықеттің ауруы, шаршау, ұйқы басу, депрессия, анемия сияқты аурулар байқалады. БҰл құбылыстар күнделікті биотин енгізгенде тез жазылып кетеді.
С дәрумені - аскорбин қышқылы
Антискорбуттық дәрумен. С дәрумені (аскорбин қышқылы, антискорубтық дәрумен) . Химиялық құрылысы бойынша аскорбин қышқылы L- глюкозаның құрылысына жақын қышқылдың лактоны болып табылады.

Изоферменттер және олардың қымзеті
Изофермент немесе изоэнзим - бір ферменттің әр түрі, олардың полипептидтік құрылысында бір-бірінен айырмашылықтары, ферменттiң бiр реакциясын катализдейтiн көптiк формалары, бiрақ субстратқа, катализделетiн (белсендiлiк) реакцияның максимал жылдамдығына, электрофоретиялық қуаттылығына немесе реттегіш қасиеттерінің жақындығына, жеке алғанда физикалық және химиялық қасиеттері бойынша бiр-бiрiмен өзгешеліктерінің болуы. Олар бір түрге жататындардың ағзасында немесе жеке клеткасында кездеседі, олардың катализдік активтілігі әр түрлі болады.

- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz