Термодинамика негіздері және тасымалдау құбылыстары: идеал мен нақты газдар, энергия, энтропия және фазалық ауысулар



ТЕРМОДИНАМИКА НЕГІЗДЕРІ
Қарағанды мемлекеттік техникалық университеті
Физика кафедрасы

Идеал газдың ішкі энергиясы Газдың ұлғаю жұмысы
Термодинамиканың бірінші заңы
Жылусыйымдылқ теориясы
Карно циклы және оның ПӘК
Энтропия. Энтропииның ықтималды салыстырмалы күйімен байланысы Термодинамиканың екінші заңы және оның физикалық мәні
Дәріс жоспары

Идеал газдың ішкі энергиясы
Идеал газдың ішкі энергиясы оның молекулаларының кинетикалық энергиясынан тұрады
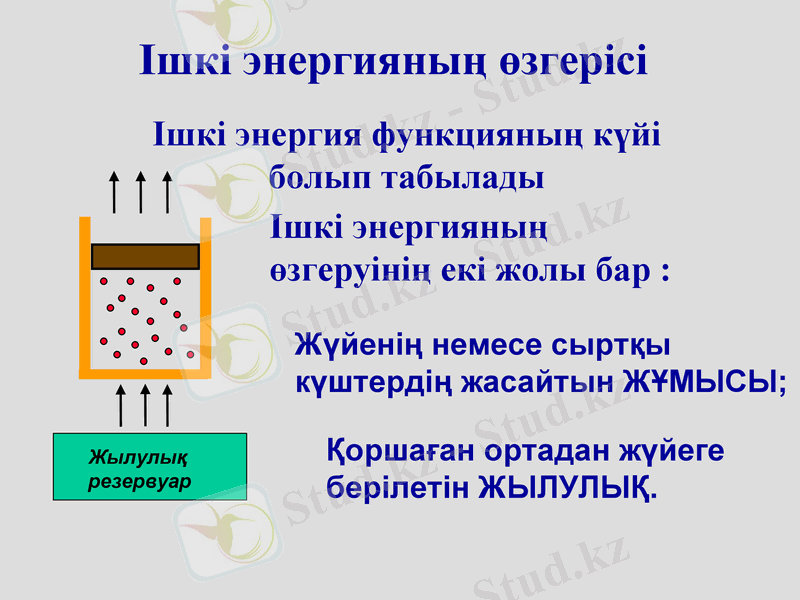
Ішкі энергияның өзгерісі
Ішкі энергия функцияның күйі болып табылады
Ішкі энергияның өзгеруінің екі жолы бар :
Жүйенің немесе сыртқы күштердің жасайтын ЖҰМЫСЫ;
Қоршаған ортадан жүйеге берілетін ЖЫЛУЛЫҚ.
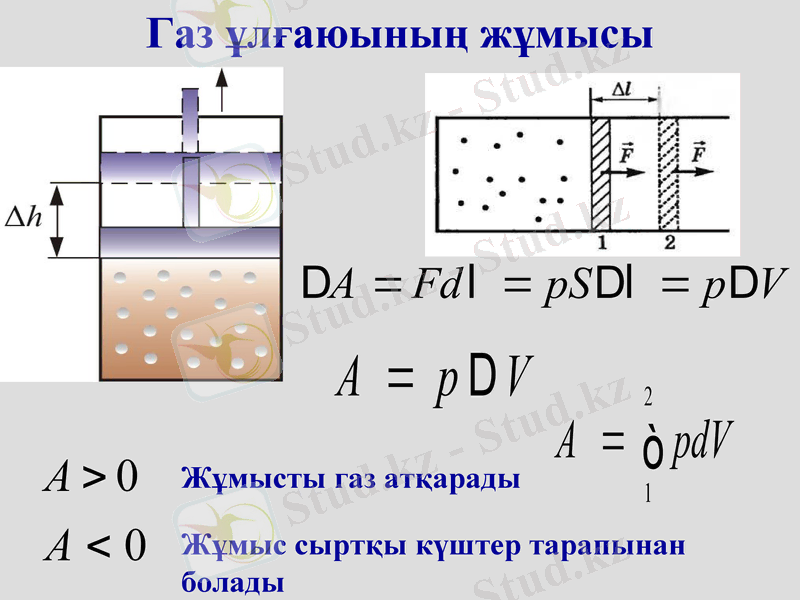
Газ ұлғаюының жұмысы
Жұмысты газ атқарады
Жұмыс сыртқы күштер тарапынан болады
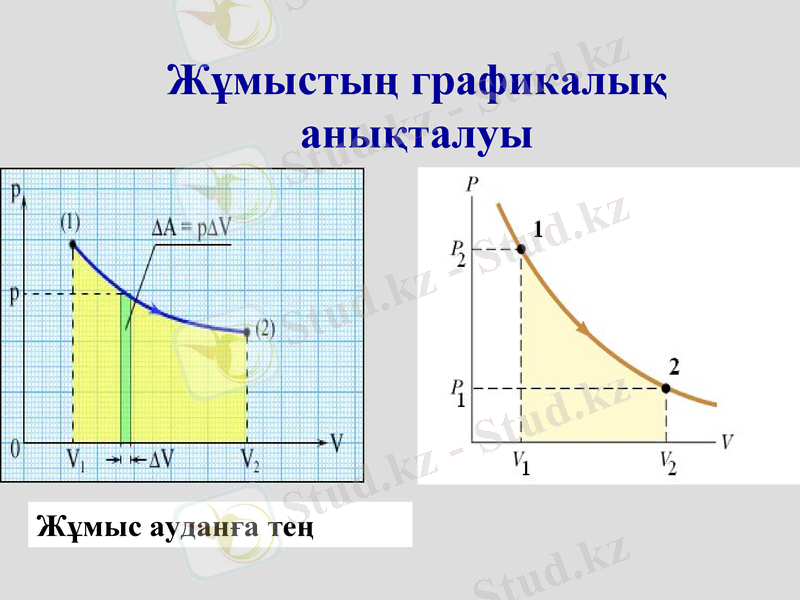
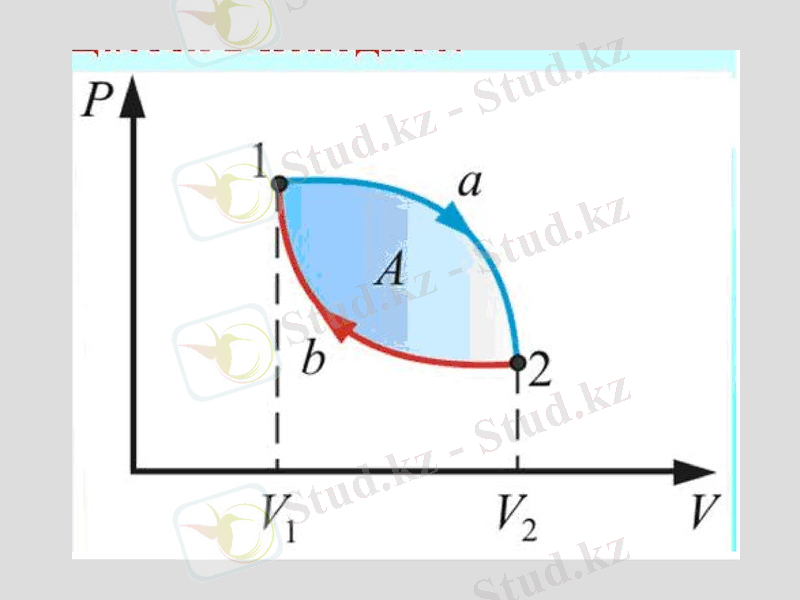
Жұмыстың графикалық анықталуы
Жұмыс ауданға тең
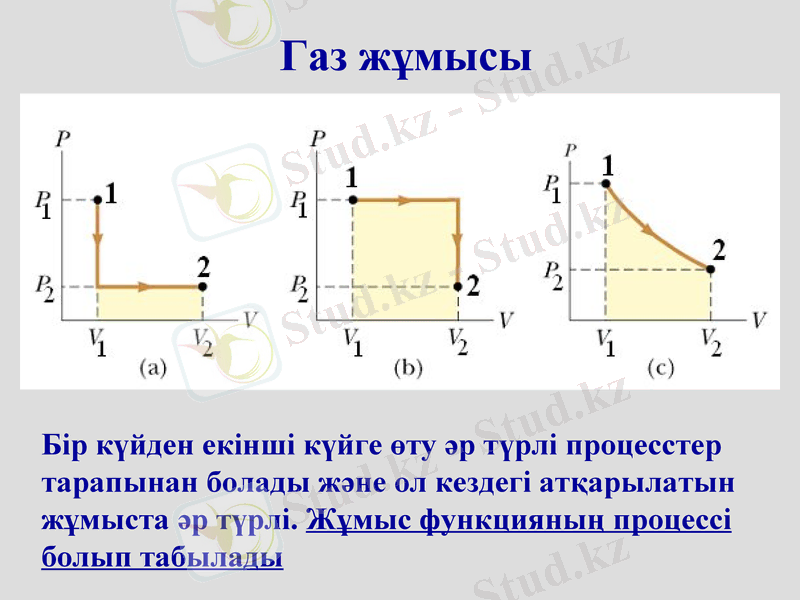
Бір күйден екінші күйге өту әр түрлі процесстер тарапынан болады және ол кездегі атқарылатын жұмыста әр түрлі. Жұмыс функцияның процессі болып табылады
Газ жұмысы
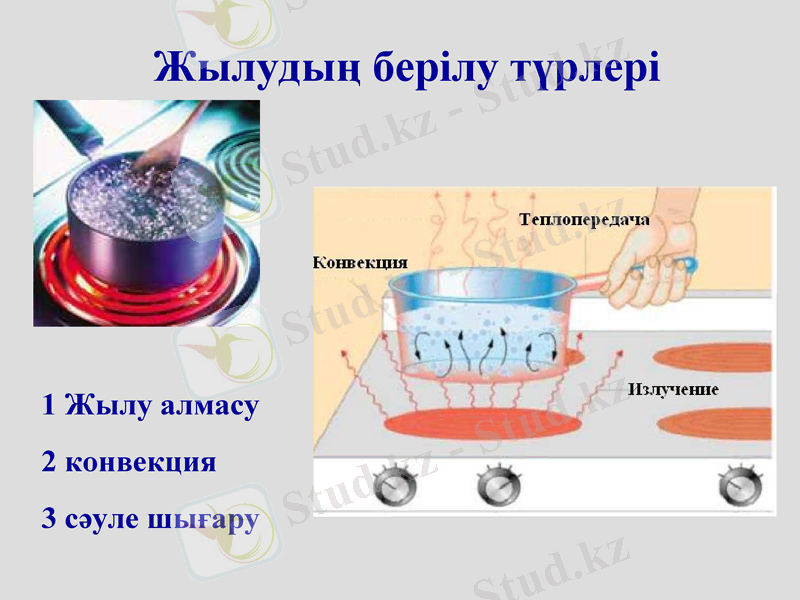
Жылудың берілу түрлері
1 Жылу алмасу
2 конвекция
3 сәуле шығару
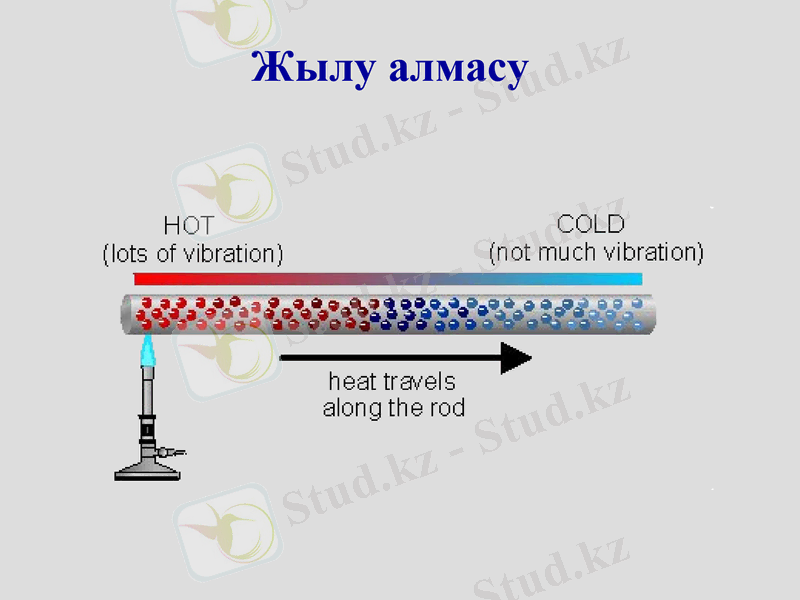
Жылу алмасу
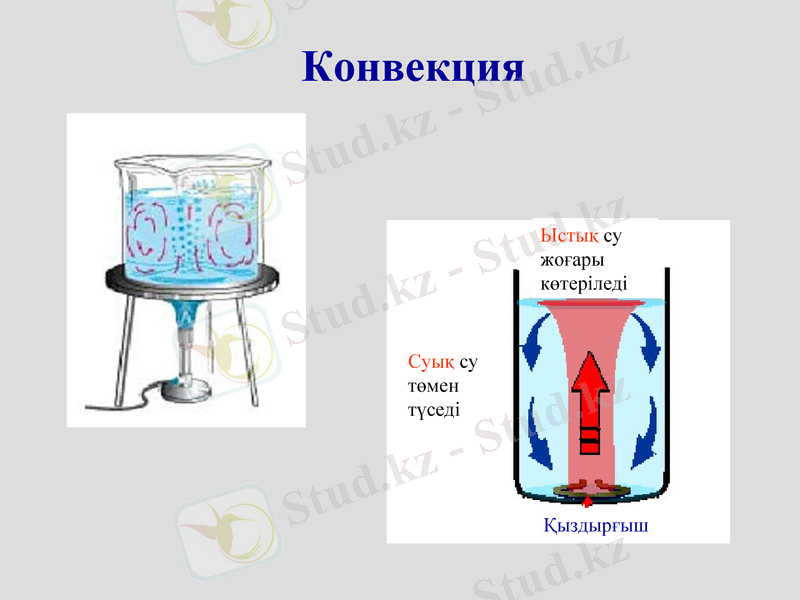
Конвекция
Ыстық су жоғары көтеріледі
Суық су төмен түседі
Қыздырғыш
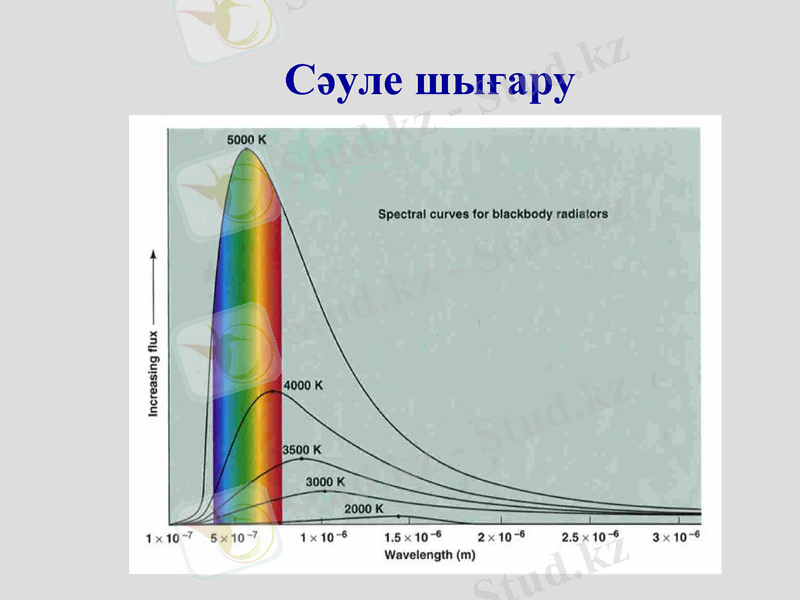
Сәуле шығару

Термодинамиканың бірінші заңы

Жылусыйымдылық
Меншікті жылусыйымдылық
Мольлық жылусыйымдылық
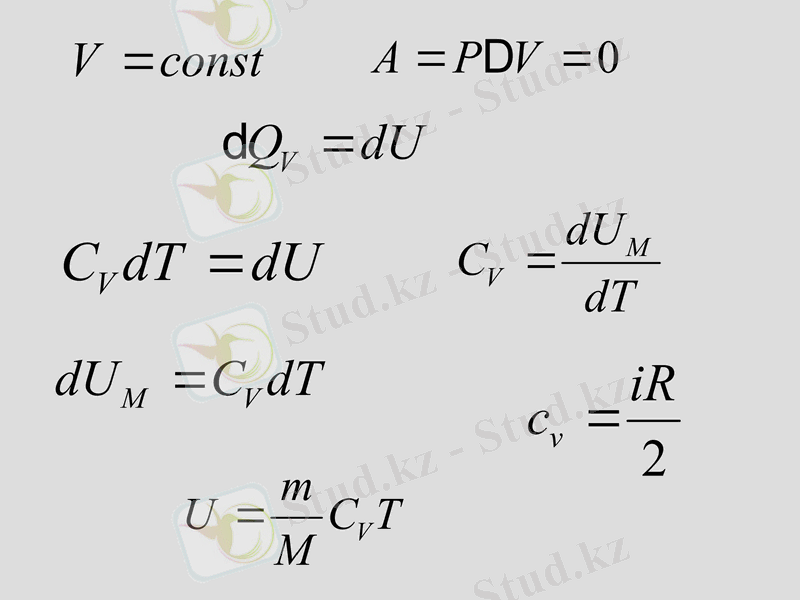
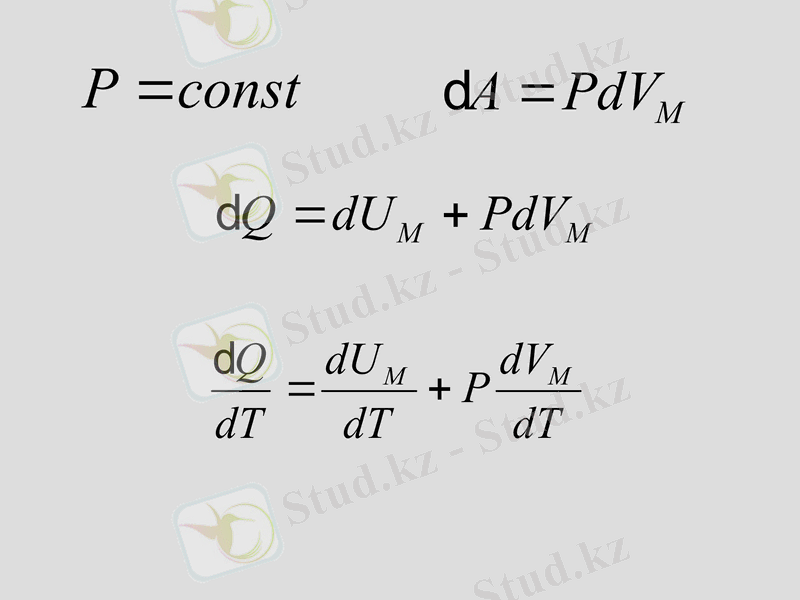
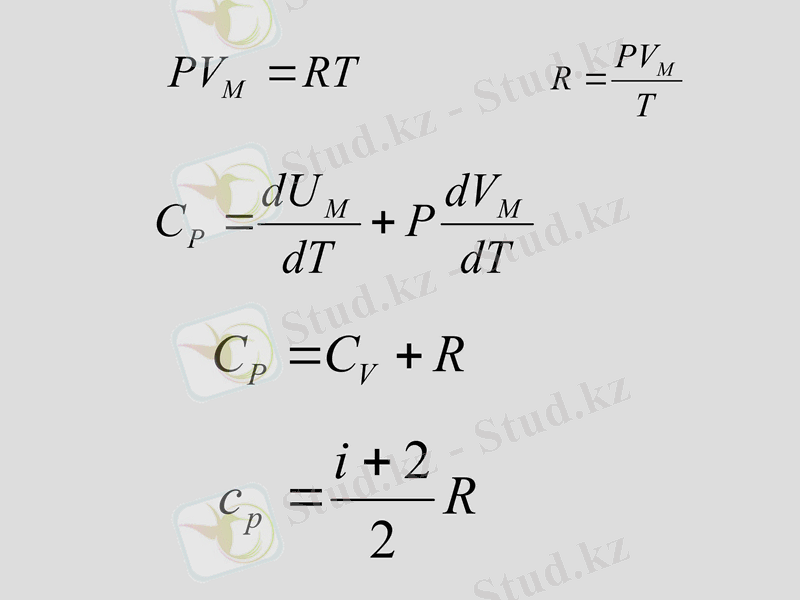

Жылусыйымдылық процесс түріне байланысты
Тұрақты көлемдегі мольдық жылусыйымдылық
Тұрақты қысымдығы мольдық жылусыйымдылық
Мольдық жылусыйымдылық арасындағы байланыс (Майер теңдеуі)
Пуассона коэффициенті (адиабата көрсеткіші)
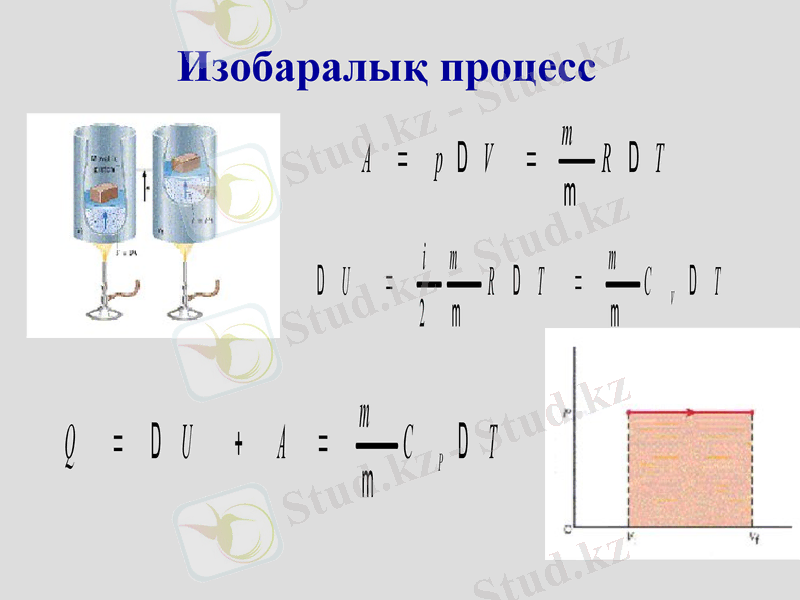
Изобаралық процесс
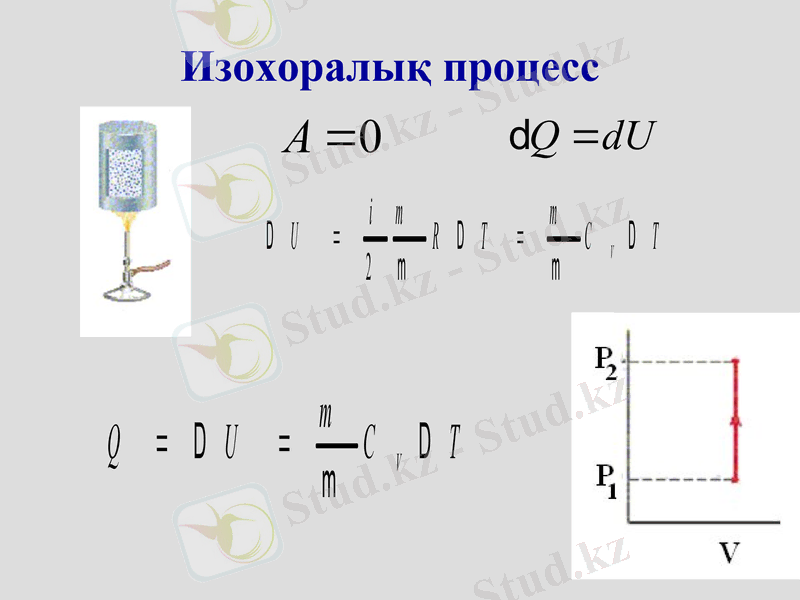
Изохоралық процесс
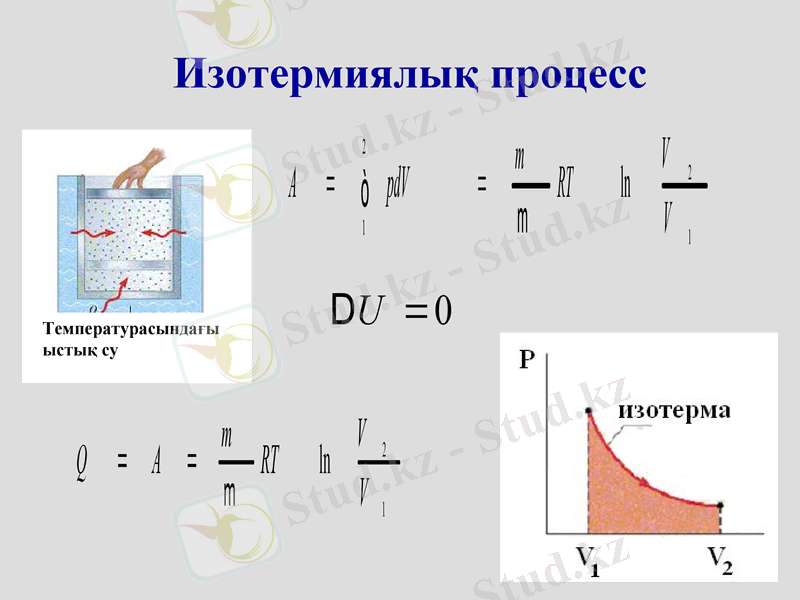
Изотермиялық процесс
Температурасындағы ыстық су

Адиабаталық процесс
Адиабаталық процесс кезінде қысымның ұлғаюы көлемнің кішіреуі мен температураның жоғарылауына тәуелді. Процесстің теңдеуі:

Энтропия
қайтымды процесс үшін
келтірілген жылу мөлшері
Клаузиус өлшем енгізді, оны энтропия деп атады:


Энтропия
Больцман энтропияны термодинамикалық ықтималдығымен байланыстырды :
Энтропия жүйенің біркелкілік емес шамасы; үлкен энтропия үлкен хаосқа соқтырады

Термодинамиканың екінші бастамасы
Суық денеден ыстық денеге жылу берілу мүмкін емес
Бір рет қана берілген жылудың көмегімен сыртқы ортаның қасиетін өзгертпей мәңгі қозғалтқыш алу мүмкін емес
Оқшауланған жүйедегі энтропия ондағы барлық процесстерде кеміді
Қайтымды процесстер үшін
Кайтымсыз процесстер үшін
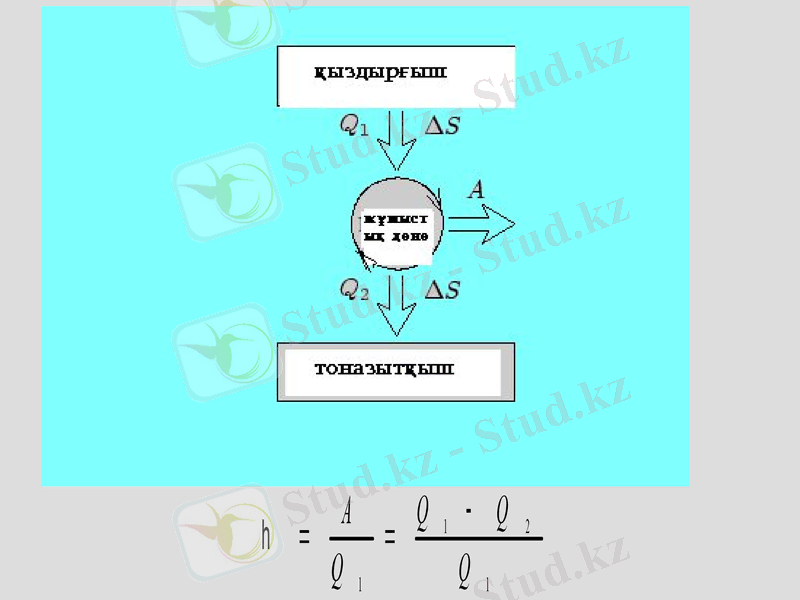
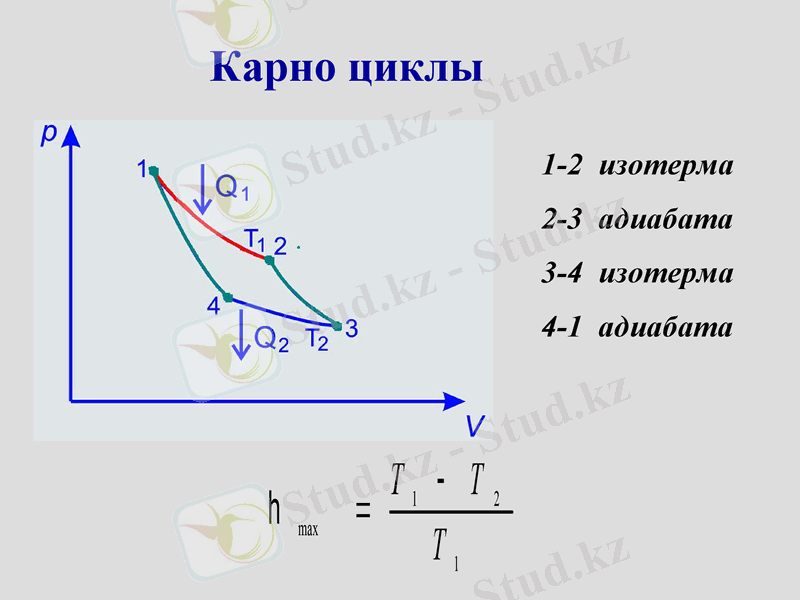
Карно циклы
1-2 изотерма
2-3 адиабата
3-4 изотерма
4-1 адиабата
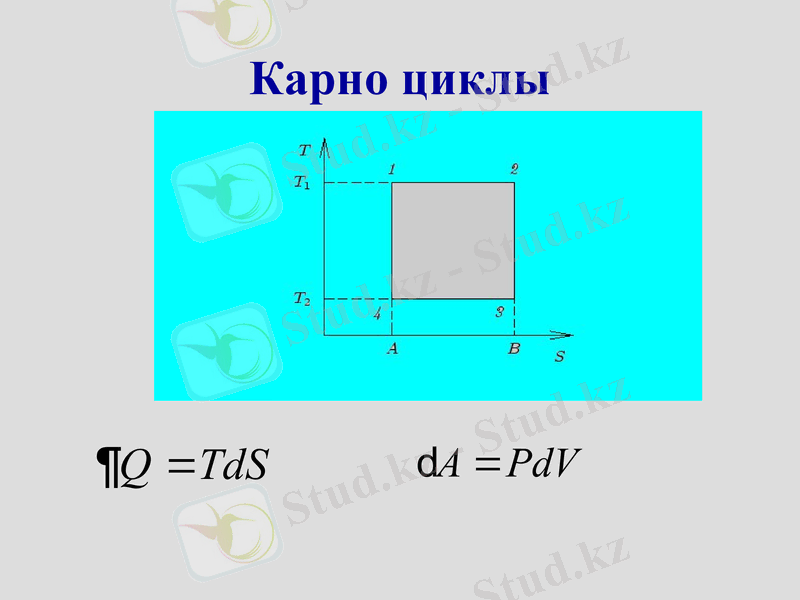
Карно циклы


ТАСЫМАЛДАУ ҚҰБЫЛЫСЫ.
НАҚТЫ ГАЗДАР

Дәріс жоспары
Эффективтік диаметр
Тасымалдау құбылысы
Молекуллрдың өзара әсерлесуі
Ван-дер-Ваальс теңдеуі
Ван-дер-Ваальс изотермасы
Фазалық ауысу
Күй диаграммасы
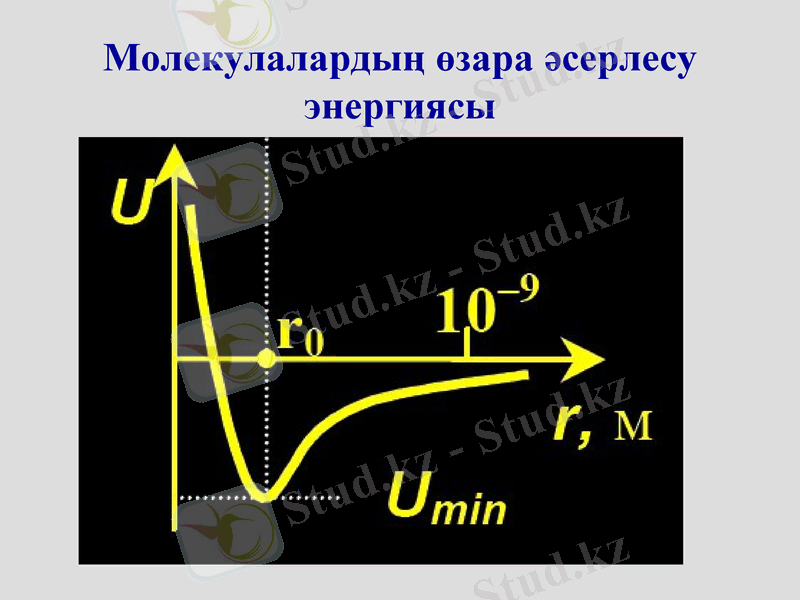
Молекулалардың өзара әсерлесу энергиясы
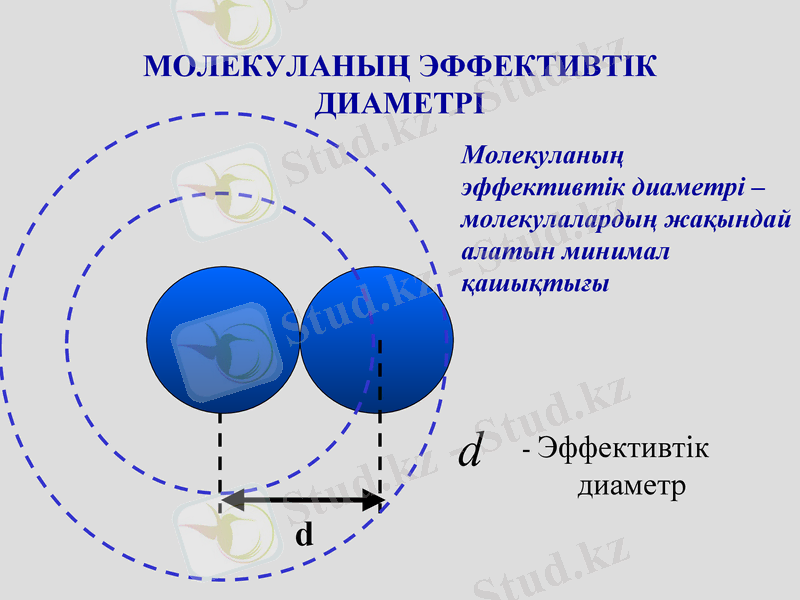
МОЛЕКУЛАНЫҢ ЭФФЕКТИВТІК ДИАМЕТРІ
d
Молекуланың эффективтік диаметрі - молекулалардың жақындай алатын минимал қашықтығы
- Эффективтік
диаметр
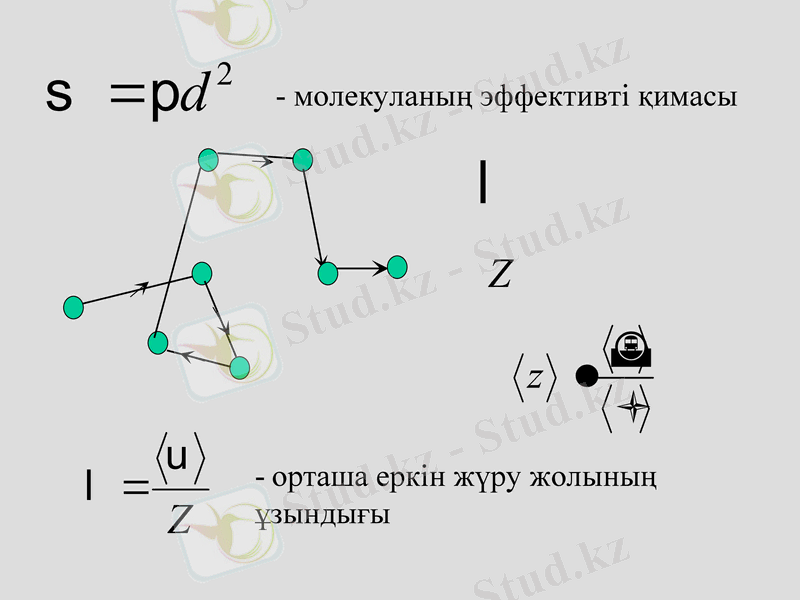
- молекуланың эффективті қимасы
- орташа еркін жүру жолының ұзындығы
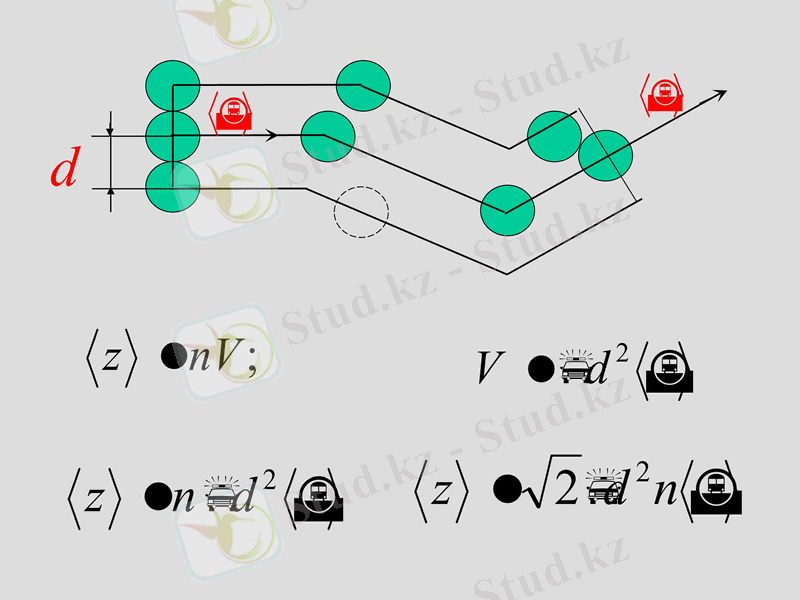
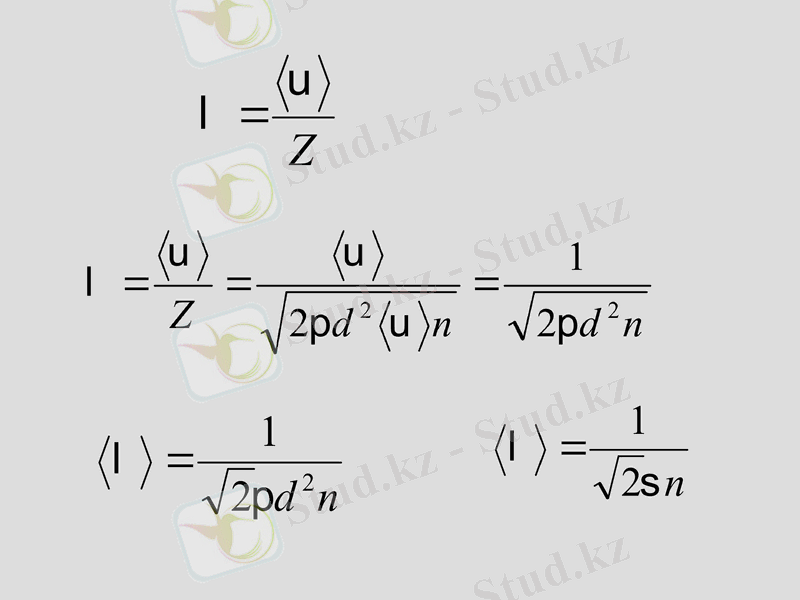

Орташа еркін жол ұзындығы

Тасымалдау құбылысы
Диффузия
Фик заңы

-диффузия коэффициенті
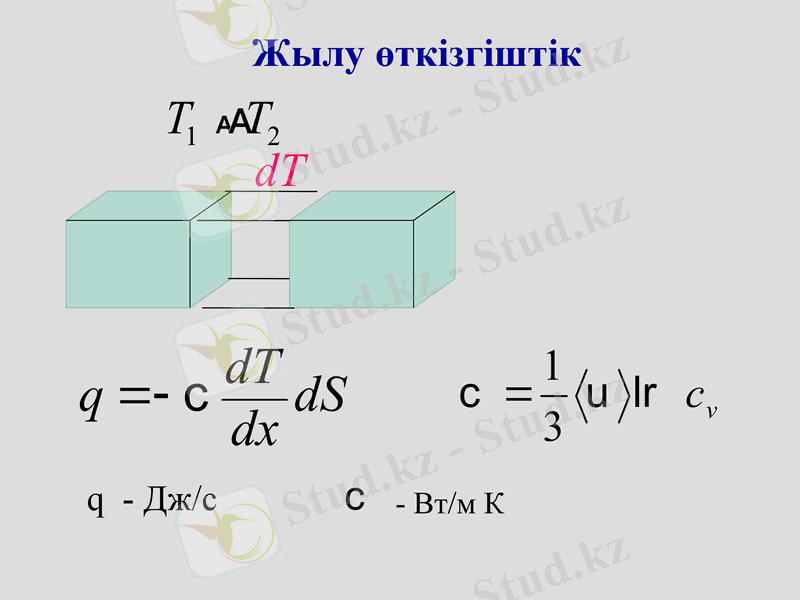
Жылу өткізгіштік
q - Дж/c
- Вт/м К
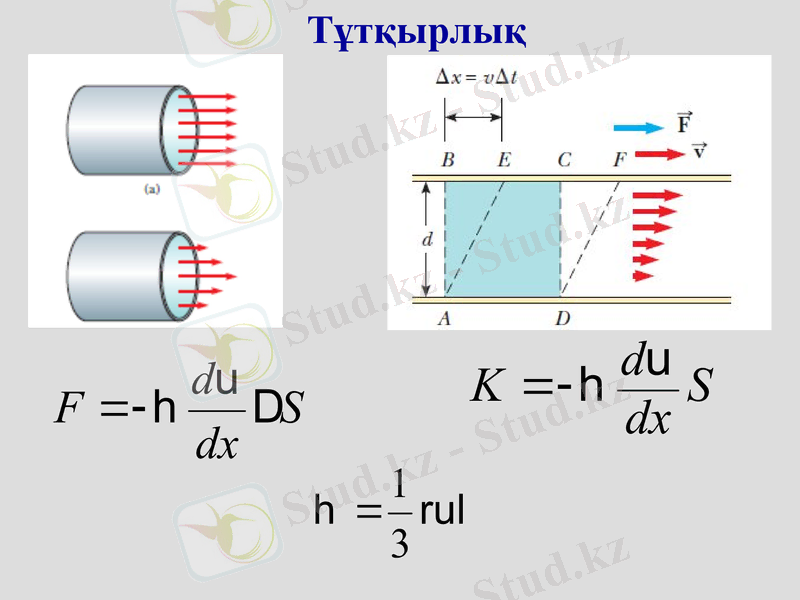
Тұтқырлық
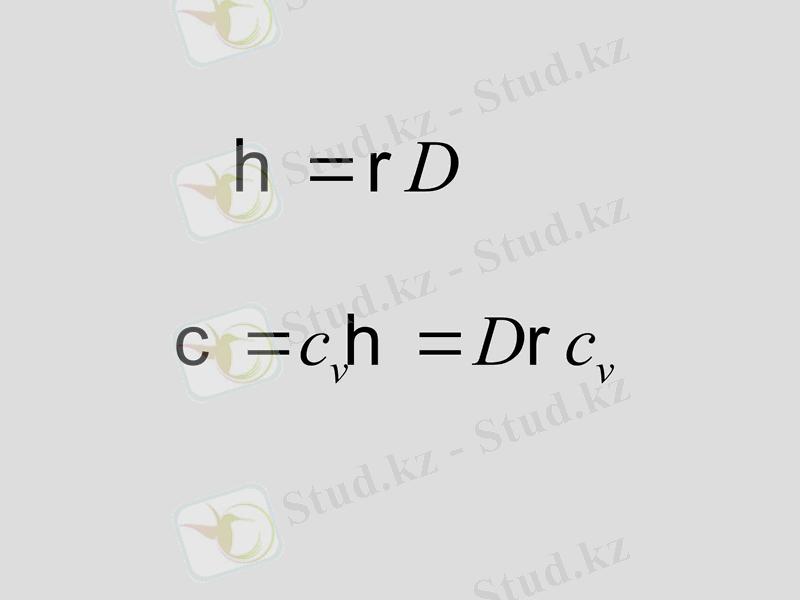
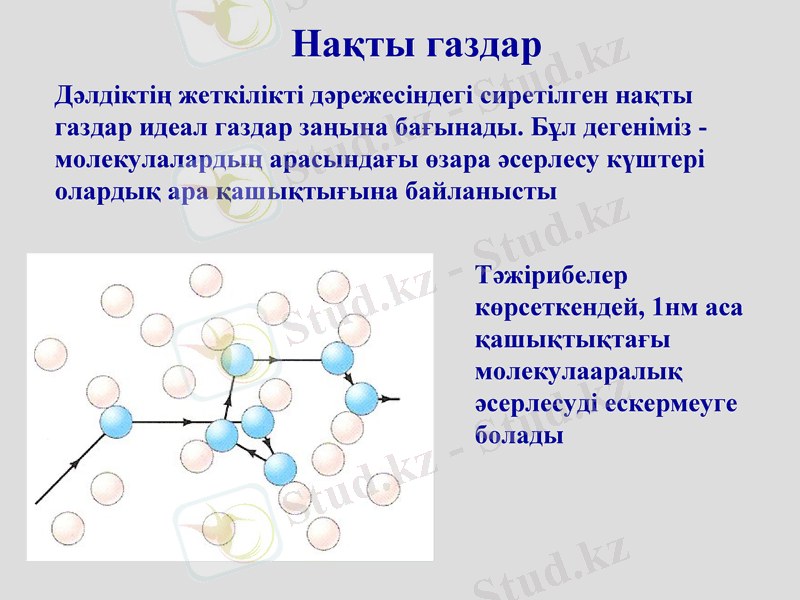
Нақты газдар
Дәлдіктің жеткілікті дәрежесіндегі сиретілген нақты газдар идеал газдар заңына бағынады. Бұл дегеніміз - молекулалардың арасындағы өзара әсерлесу күштері олардық ара қашықтығына байланыcты
Тәжірибелер көрсеткендей, 1нм аса қашықтықтағы молекулааралық әсерлесуді ескермеуге болады
Нақты газдар
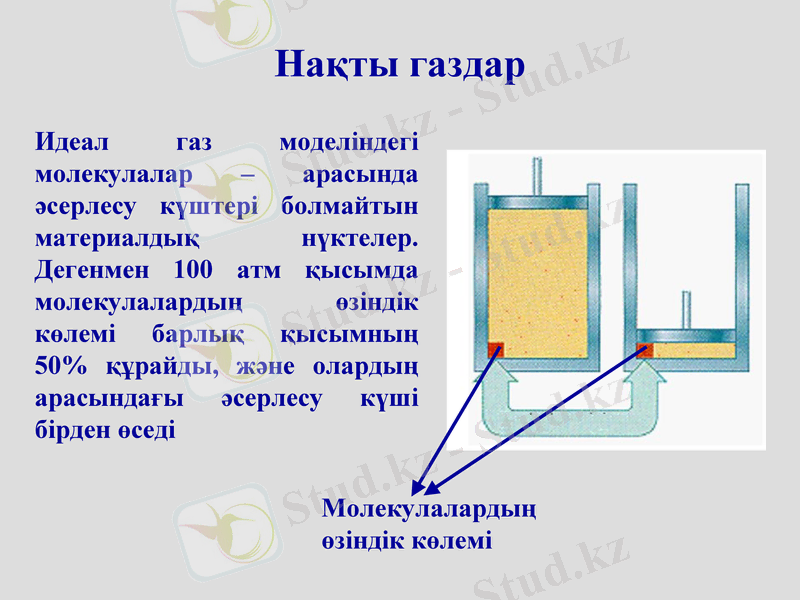
Молекулалардың өзіндік көлемі
Идеал газ моделіндегі молекулалар - арасында әсерлесу күштері болмайтын материалдық нүктелер. Дегенмен 100 атм қысымда молекулалардың өзіндік көлемі барлық қысымның 50% құрайды, және олардың арасындағы әсерлесу күші бірден өседі

Қысым ұлғайғанда сығылғaн газ көлемі молекулалардың өздері алатын көлемге теңеседі

Идеал газ күйінің теңдеуі төмен қысымда және жоғары температурадағы газдар әрекетін сипаттауға пайдалы.
Идеал газадың берілген күйден ауытқуы сығылу коэффициентімен Z сипатталады
Егер Z = 1 болса, идеал газ қасиетіне жақын болады
Сығылу коэффициенті Z 1-ден өзгеше болса, солғұрлым идеал газадан ауытқуы күштірек болады
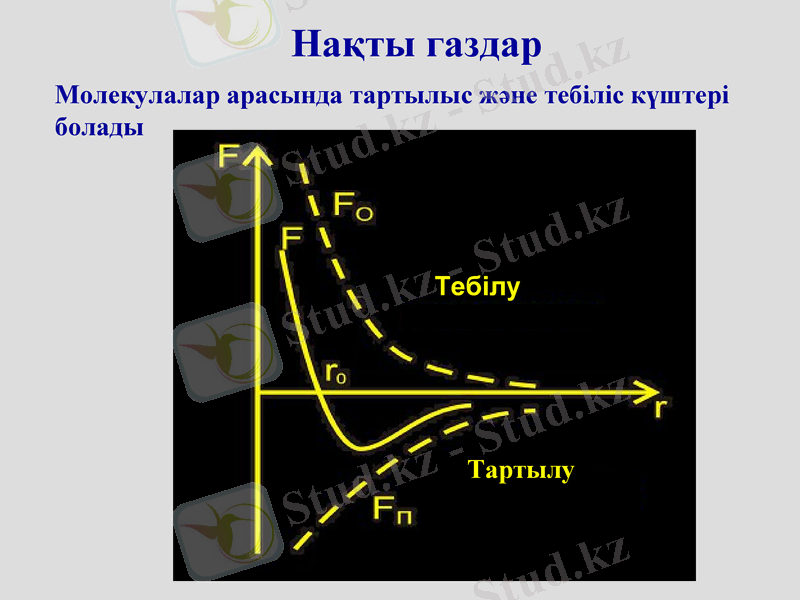
Нақты газдар
Молекулалар арасында тартылыс және тебіліс күштері болады

Молекулалардың потенциялдық және кинетикалық энергиялары арасындағы арақатынас агрегаттық күйлерге бөлу үшін сындық болып табылады

Нақты газ күйінің теңдеуі -Ван-дер-Ваальс теңдеуі
Нақты газдарда келесі ескерілу керек:
Бөлшектерде өз көлемі болады
Молекулалар арасында тартылыс және тебіліс күштері бар
Идеал газ күйінің теңдеуі
молекулалардың өз көлемі мен олардың әсерлесуі ескерілетіндей түрлендірілуі қажет
ВАН-ДЕР-ВААЛЬС ТЕҢДЕУІ
Газдың 1 молі үшін
Молекулалардың өзара әсерлесуін ескеру
Молекуланың өз көлеміне түзетілім
Газдың туынды массасы үшін
B-тұрақтысы молекула өлшеміне байланысты: үлкен молекула үшін оның мәні де үлкен
a-молекулалар арасындағы тартылыс күшінің шамасы
ВАН-ДЕР-ВААЛЬС ИЗОТЕРМАЛАРЫ
Ван-дер-Ваальса теңдеуі - 3-дәрежеде V қатысты, сондықтан 3 заттық түбірі болуы мүмкін
db жеріндегі ұлғаю қысым ұлғаюымен жүреді, оның физикалық мағынасы жоқ, сол себепті бірден ea
секірісі болады
ВАН-ДЕР-ВААЛЬС ИЗОТЕРМАЛАРЫ
Жоғары температураларда идеал газ изотермаларынан ауытқу кішірек көрсетілген
Нақты газдың ішкі энергиясы
- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz