Органикалық қосылыстардың кеңістіктік құрылысы мен стереохимиясы



С. Ж. Асфендияров атындағы Қазақ Ұлттық Медицина Университеті Химия кафедрасы
Орындаған:
Курс:
Топ:
Тексерген:

Органикалық қосылыстардың кеңістіктегі құрылысы

Молекуланың кеңістіктегі құрылымын және оның физикалық-химиялық қасиеттеріне әсерін стереохимия зерттейді.

Стереоизомерлер - құрамы мен олардың атомдарының қосылу реті бірдей болып, тиісті молекуладағы жекеленген бөліктердің кеңістіктегі орналасуы әртүрлі қосылыстар.

Стереоизомерлер
( тұрақтылығына қарай )
Конфигурациялық
Конформациялық
Бір не бірнеше жай байланыстардың төңірегінде айналғанда пайда болатын өзгешеліктерді есептемегендегі атомдардың кеңістіктегі орналасуы
Конфигурациясы белгілі молекуладағы атомдардың қарапайым δ-байланыстар төңірегінде айналуы салдарынан әртүрлі орналасулардың пайда болуы

Стереоизомерлер
( симметрияны елестетуіне қарай )
энантиомерлер
диастереомерлер
Стереоизомерлердің айырмашылығы белгілі бір затпен оның айнадағы бейнесі тәрізді болатын стереоизомерлер
Өзара энантиомер емес кеңістіктік изомерлердің түрі

Жазықтықта молекуланың кеңістіктік құрылысын бейнелеу үшін әртүрлі стереохимиялық және проекциялық формулалар қолданылады. Молекулалық модельдердің бірнеше түрі бар: 1. Шарөзекшелік нұсқа; 2. Дрейдинг нұсқасы; 3. Жартысфералық нұсқа.

Шарөзекшелік нұсқа - бұл типті нұсқаны атомның құрамына кіретін молекулаларды түсті шарлармен белгілеу. Шарларды химиялық байланыстарды білдіретін өзекшелермен қосады. Бұл нұсқа арқылы молекулалар арасындағы дәл бұрышты анықтауға болады, бірақ арасындағы химиялық байланыстардың ұзындығы жуықтап қана алынады.
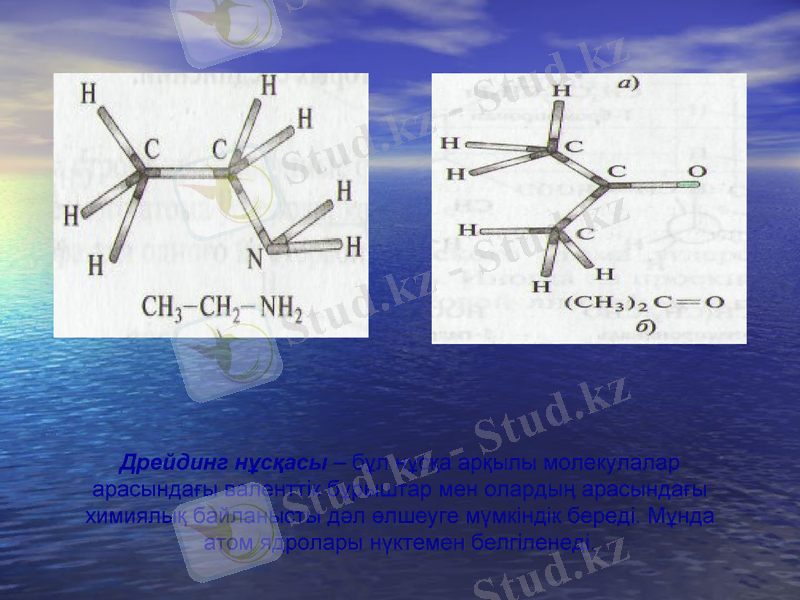
Дрейдинг нұсқасы - бұл нұсқа арқылы молекулалар арасындағы валенттік бұрыштар мен олардың арасындағы химиялық байланысты дәл өлшеуге мүмкіндік береді. Мұнда атом ядролары нүктемен белгіленеді.

Жартысфералық нұсқа ( Стюарт - Бриглеб нұсқасы) - нұсқа жарты сегментті шарлардан құралады, жарты сегменттерді өзара батырмалармен біріктіреді.
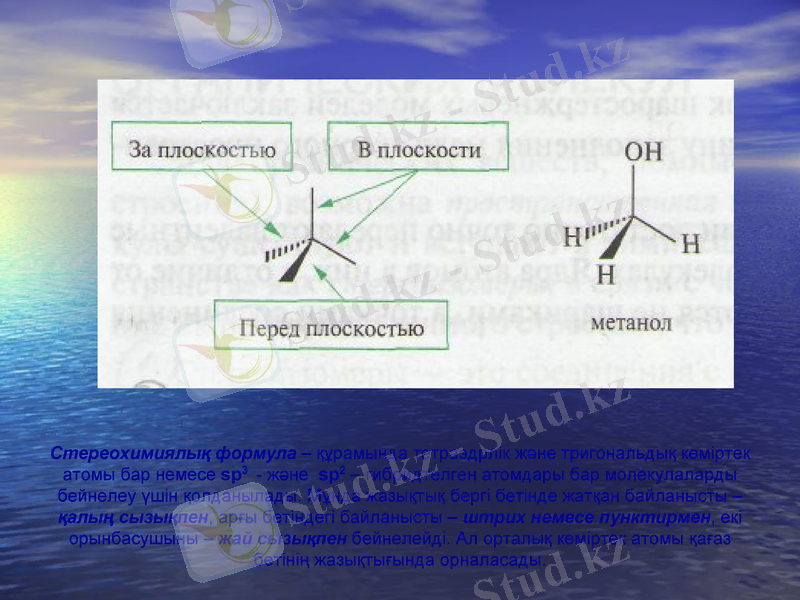
Стереохимиялық формула - құрамында тетраэдрлік және тригональдық көміртек атомы бар немесе sp3 - және sp2 - гибридтелген атомдары бар молекулаларды бейнелеу үшін қолданылады. Мұнда жазықтық бергі бетінде жатқан байланысты - қалың сызықпен, арғы бетіндегі байланысты - штрих немесе пунктирмен, екі орынбасушыны - жай сызықпен бейнелейді. Ал орталық көміртек атомы қағаз бетінің жазықтығында орналасады.
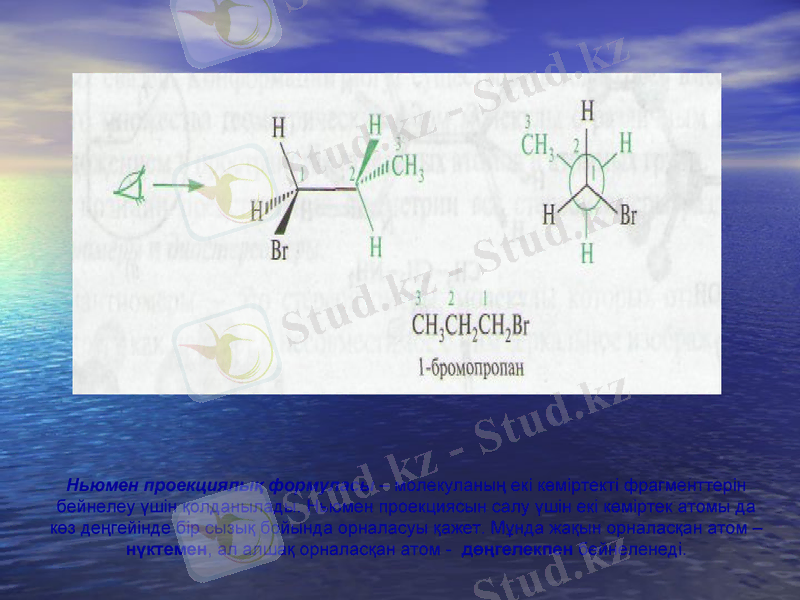
Ньюмен проекциялық формуласы - молекуланың екі көміртекті фрагменттерін бейнелеу үшін қолданылады. Ньюмен проекциясын салу үшін екі көміртек атомы да көз деңгейінде бір сызық бойында орналасуы қажет. Мұнда жақын орналасқан атом - нүктемен, ал алшақ орналасқан атом - дөңгелекпен бейнеленеді.

Перспективті формулалар - пропорциональды емес ұзартылған орталық байланысы бар екі көміртек атомды фрагменттерді бейнелеу үшін қолданылады.
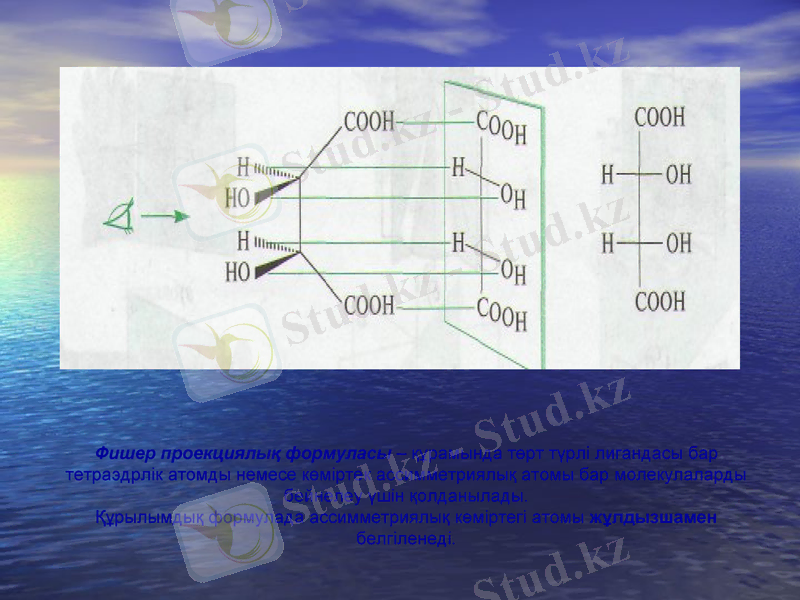
Фишер проекциялық формуласы - құрамында төрт түрлі лигандасы бар тетраэдрлік атомды немесе көміртек ассимметриялық атомы бар молекулаларды бейнелеу үшін қолданылады.
Құрылымдық формулада ассимметриялық көміртегі атомы жұлдызшамен белгіленеді.

Стереоизомерлер
( симметриялық элементтің болуына қарай )
Хиральді
Ахиральді
Симметрия жазықтықтары не орталықтары болмайтын молекулалар
Симметрия жазықтықтары не орталықтары бар молекулалар

Энантиомерия - зат ретіндегі екі молекуланың конфигурациясы және оның айнадағы көрінісі өзіне сәйкес химиясы өзара қатынаста болатын стереоизомерия. Қалыпты жағадайдағы энантиомерлер бірдей химиялық және физикалық қасиеттерді көрсетеді.

Энантиомерлер әртүрлі биологиялық қасиет көрсетеді. Энантиомерлерді атау үшін 2 түрлі номенклатура қолданылады.
Салыстырмалы конфигурация
немесе
D-, L- номенклатура
Абсолюттік конфигурация
немесе
R-, S- номенклатура

Салыстырмалы конфигурация немесе D-, L- номенклатура - қалыпты үлгі ретінде қабылданған глицеринді альдегидтің конфигурациясымен салыстыратын конфигурация.

Абсолюттік конфигурация немесе R-, S- номенклатура - табиғатта кездесетін молекулалардағы атомдардың кеңістіктік орналасуын анықтайды.

Поляриметрдің құрылыс схемасы : 1-натрийлік лампа, 2- поляризатор, 3- поляриметрлік түтік, 4- призма-анализатор
Полярланған жарықтың жазықтықты айналдыру таңбасын тәжірибе кезінде арнаулы өлшеуіш аспап көмегімен анықтайды және ол құрылғыны поляриметр деп атайды.

Агрегаттық күйінен тәуелсіз жағдайдағы, яғни газ, сұйық, кристалды түрінде кездесетін, тең сандық шамадағы энантиомер қоспасынан тұратын өнім рацемат деп аталады.

Рацематтарды энантиомерлерге бөлу әдістері: - физикалық немесе механикалық; - химиялық; - биологиялық.

Физикалық әдіс - ол кристалдарды таңдап, бөле ажырату, оны конгломераттар жағдайында қолданылады. Бұл әдістің қолданылу аясы шектеулі.

Химиялық әдіс - бұл әдісті қолданғанда молекулаға көмектесуші ретінде алдын-ала оптикалық белсенді затты қосып, оның қоспалы бірігу көмегімен жаңа хиралдық ортаны енгізеді. Осы тұста рацематтан екі диастереомер түзіледі.

Биологиялық әдіс - бұл әдіс кейбір заттың тек бір ғана энантиомерін өзіне қорек ретінде тұтынатын микроорганизмдердің биохимиялық өміріне, тіршілігіне негізделген.

Диастереомерия - оптикалық антиподтар жұбын құрастырмайтын кеңістіктегі изомерлердің бар болуы . Диастереомер - энантиомер болмайтын екі стереоизомер. Эпимеризация - диастереомерлердің бірін екіншісіне ауыстыру әрекеті.

Диастереомерлер
δ - диастереомер
Π - диастереомер
Барлық орынбасарлар хиральді орталықпен сигма байланыс арқылы қосылған диастереомерлер.
Барлық орынбасарлар хиральді орталықпен пи байланыспен қосылған диастереомерлер.

П- диастереомерлер - эпимеризация реакциясына п-байланысының үзілуі салдарынан жүреді. Оған цис- және транс- изомерлер мысал бола алады. п- диастереомерлерді белгілеу үшін E-, Z- жүйесін пайдаланады. HOOC H HOOC COOH \ / \ / C=C C=C / \ / \ H COOH H H транс-(Е) изомер цис-(Z) изомер фумар қышқылы малеин қышқылы

Конформация - конфигурациясы белгілі молекуладағы атомдардың қарапайым δ- байланыстар төңірегінде айналуы салдарынан әртүрлі орналасулардың пайда болуы.
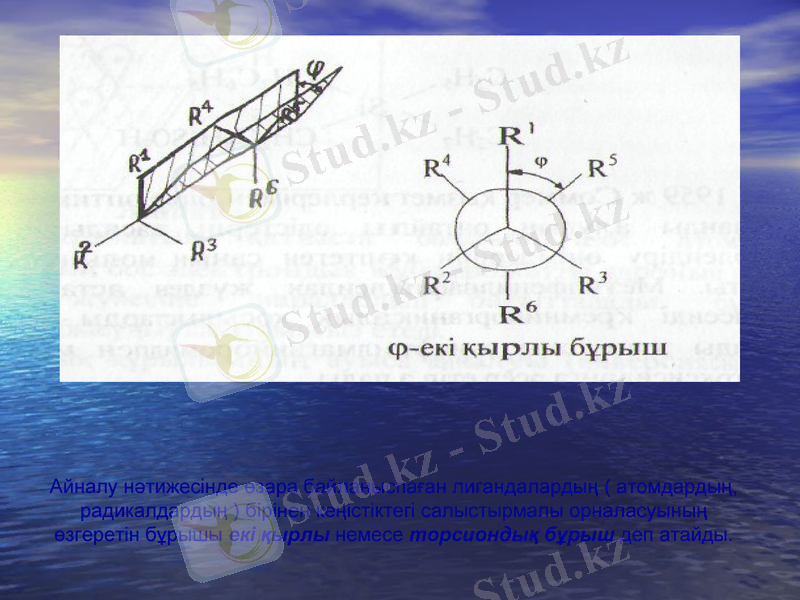
Айналу нәтижесінде өзара байланыспаған лигандалардың ( атомдардың, радикалдардың ) бірінен кеңістіктегі салыстырмалы орналасуының өзгеретін бұрышы екі қырлы немесе торсиондық бұрыш деп атайды.

- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz