Массалар әрекеттесу заңы және тура мен кері реакциялардың кинетикасы



Массалар
әрекеттесу заңы

І. Тура және кері реакциялар ІІ. Массалар әрекеттесу заңы

Тура және кері реакциялар
Химиялық реакцияның жүру механизмін және жылдамдығын зерттейтін химия ғылымының тарауын кинетика деп атайды. Аналитикалық реакциялардың жүруі үшін қажетті жағдайларды таңдау, химиялық процесстердің механизмін және оларды бағыттауды білу керек. Жүйенің бір күйден екінші күйге өтуі процесс деп аталады. Егер жүйе үздіксіз тізбекті тепе-теңдік күйлерден өтсе, ол процесс тепе-теңдік процесі деп аталады. Егер жүйені осы тепе-теңдік күйлерден тізбектеп өткізетін кері процесс мүмкін болса, ол қайтымды(кері) деп аталады, ал әрбір өзгеруі қоршаған ортаның күйінің өзгеруімен жүрсе, ол қайтымсыз (тура) реакция деп аталады. Барлық реалды процесстер қайтымсыз.
N
+
H
NH
тура
кері
2
2
3
2
3
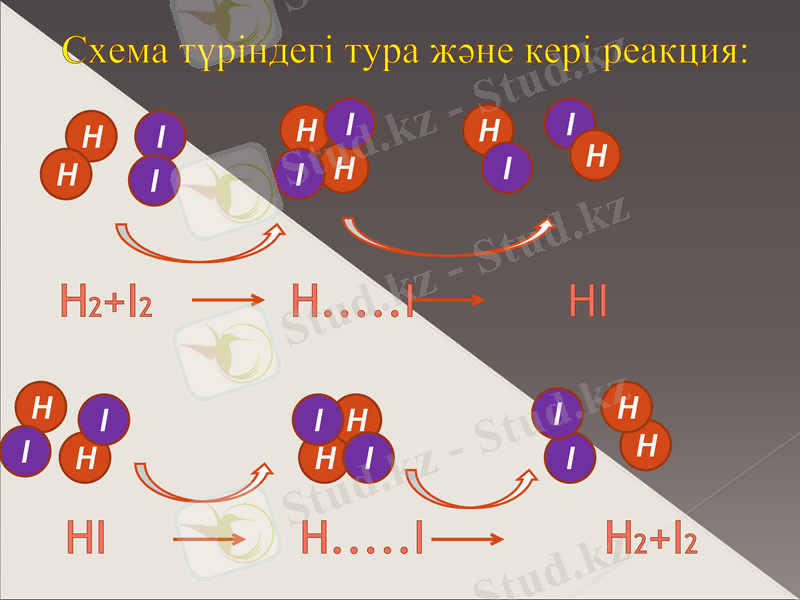
Схема түріндегі тура және кері реакция:
Н
Н
І
І
Н
Н
І
І
Н
І
І
Н
Н2+І2 Н . . . І НІ
Н
Н
Н
Н
Н
Н
І
І
І
І
І
І
НІ Н . . . І Н2+І2

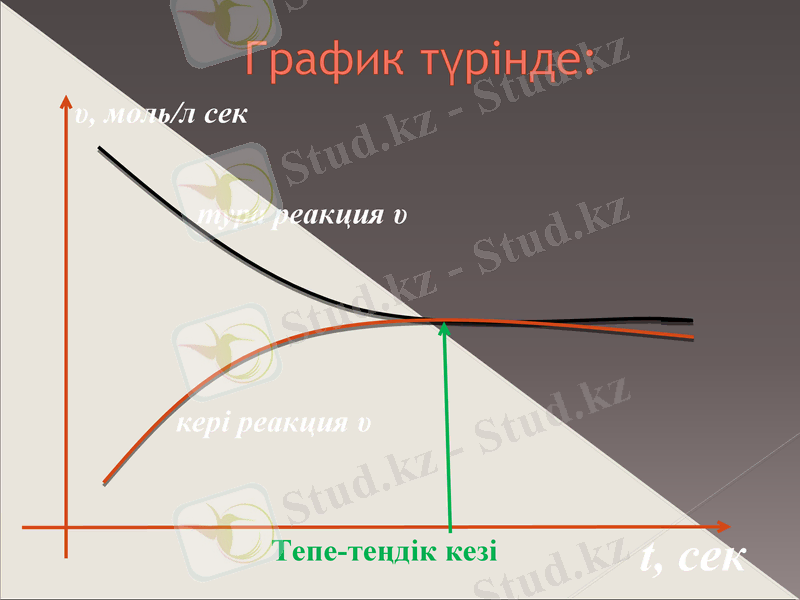
График түрінде:
υ, моль/л сек
t, сек
тура реакция υ
кері реакция υ
Тепе-теңдік кезі

Массалар әрекеттесу заңын көптеген ғалымдар зерттеген. Соның ішіндегі ең нәтижелісі Гульдберг пен Ваагенің зерттеулері. Олар былай деп жазған: «Біздің ойымызша, химиялық күштің ауқымын анықтау үшін, процесс үнемі қарама-қарсы екі бағытта жүру керек . . . Егер осындай процессте бір-біріне қарсы екі күш бар десек, бірі - өнімді түзуге күш жұмсаса, екіншісі сол өнімнен алғашқы заттарды қайта түзуге күш жұмсайды, сонымен қатар бұл күштер бірдей болған кезде, жүйеде тепе-теңдік орнайды. »

Аналитикалық химия үшін химиялық реакцияның жылдамдығына реакцияға түсетін заттардың концентра- циясының әсерін қарастыру қажет. Ол Массалар әрекеттесу заңымен анықталады. Массалар әрекеттесу заңы немесе әрекеттесуші массалар заңын ең алғаш 1807 жылы Норвегия ғалымдары Гульдберг пен Вааге және кейін орыс ғалымы Бекетов ұсынды.


Массалар әрекеттесу заңының дұрыс тұжырымы мынадай болады: берілген жағдайдағы химиялық реакцияның жылдамдығы, реакция теңдеуінің стехиометриялық коэффициентіне тең болатын дәрежелі әрекеттесуші заттардың активті концентрация- ларының көбейтіндісіне тура пропорционал.

Назар аударғаныңызға
көп рахмет!
- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz