Азот (N): атомдық құрылым, физико-химиялық қасиеттері, таралуы және қолданылуы



15 топ элементі
Пниктоген
Азот - N - Nitrogen

Элемент атауы- Азот (N) - Nitrogen
Период - ІІ
Тобы - 15
Атомдық масса - 14, 00674
Атомдық номер - 7
Электрондық конфигурациясы - 1s22s22p3
Балқу температурасы -209, 86°C
Қайнау температурасы -195, 8°C
Тотығу дәрежесі - +5, +4, +3, +2, +1, 0, -1, -2, -3
Азоттың тұрақты 2 изотобы бар :
14N - 99, 635% и 15N - 0, 365%.
Азот N
Тарихы
Азотты кім нақты ашқанын айту қиын, себебі 1772 жылы 3 ғалым азотқа бірдей тәжірибе жасаған. Олар Генри Кавендиш, Джозеф Пристли және Даниэль Резерфорд. Бірақ ешқандай ғалым өз тәжірибесін толықтай аяқтамаған.
«АЗОТ» атауын 1787 жылы А. Лавуазье ұсынған.
Г. Кавендиш
Д. Пристли
Д. Резерфорд

Таралуы
Азот - Күн Жүйесіндегі ең көп таралған 4-ші элемент ( сутек, оттек және гелийден кейінгі) .
Азот - жерде де кең таралған элемент.
Атмосфера құрамында 3, 87·1018 кг - 75, 6% (салмақ)
немесе 78, 08% (көлемі) ;
Биосферада (0, 7-1, 5) ·1018 кг;
Жердің мантия қабатында 1, 3·1019 кг;
Гидросферада 2·1016 кг (7·1014 кг қосылыс түрінде) .
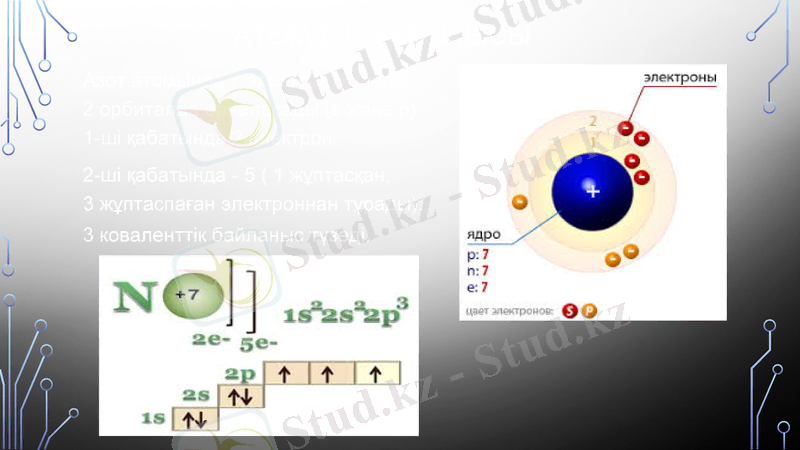
Азот атомында 7 электрон болады, 2 орбиталда орналасады (s және p) . 1-ші қабатында 2 электрон;
2-ші қабатында - 5 ( 1 жұптасқан, 3 жұптаспаған электроннан тұрады) .
АТОМДЫҚ ҚҰРЫЛЫСЫ
3 коваленттік байланыс түзеді.
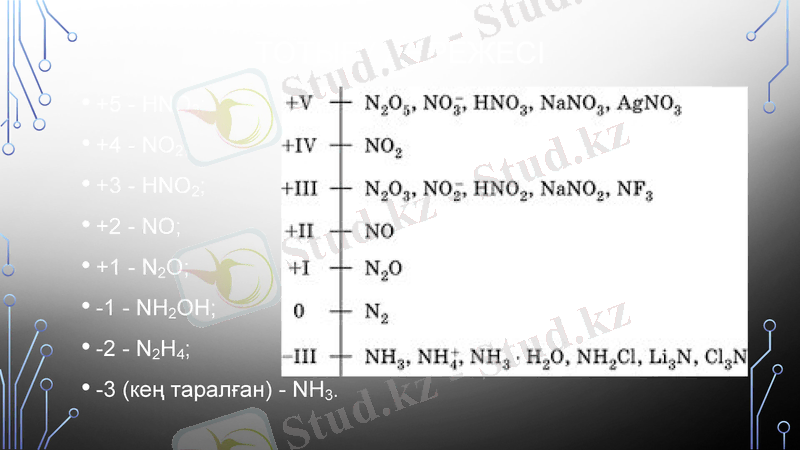
Тотығу дәрежесі
+5 - HNO3;
+4 - NO2;
+3 - HNO2;
+2 - NO;
+1 - N2O;
-1 - NH2OH;
-2 - N2H4;
-3 (кең таралған) - NH3.
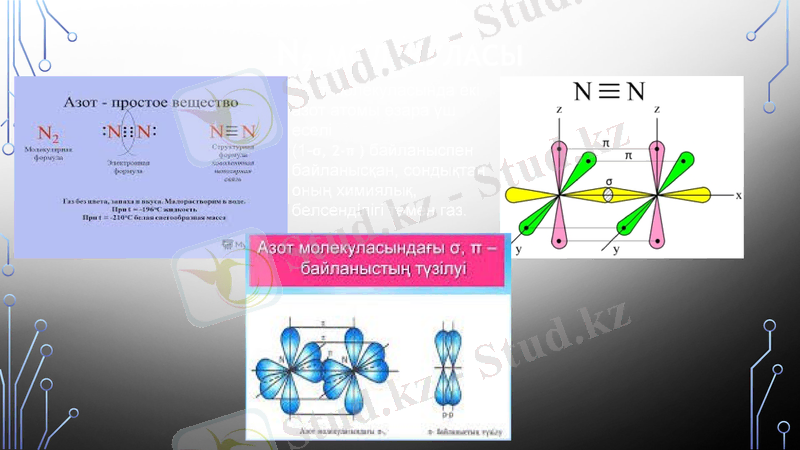
N2 молекуласы
Азот молекуласында екі азот атомы өзара үш еселі
(1-σ, 2-π ) байланыспен байланысқан, сондықтан оның химиялық, белсенділігі төмен газ.
N2 Алынуы
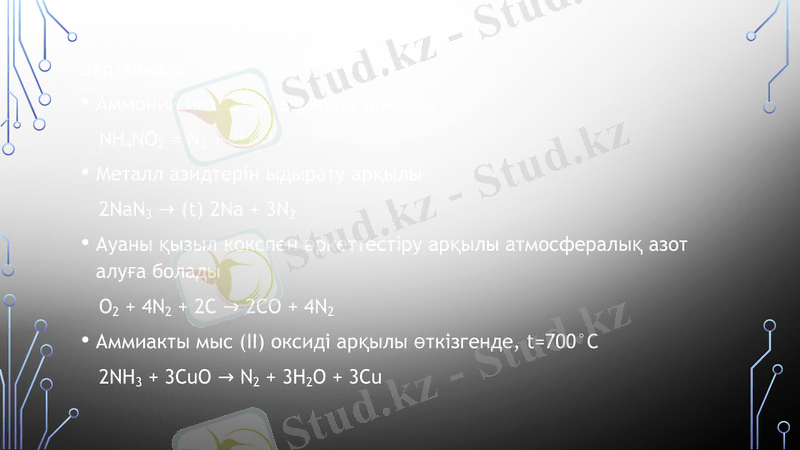
Зертханада
Аммоний нитратын ыдырату арқылы
NH4NO2 = N2 + 2H2O
Металл азидтерін ыдырату арқылы
2NaN3 → (t) 2Na + 3N2
Ауаны қызыл кокспен әркеттестіру арқылы атмосфералық азот алуға болады
O2 + 4N2 + 2C → 2CO + 4N2
Аммиакты мыс (II) оксиді арқылы өткізгенде, t=700°C
2NH3 + 3CuO → N2 + 3H2O + 3Cu

N2 қасиеті
Түссіз, иіссіз газ
Суда нашар ериді
Органикалық еріткіштерде ериді
Катализатор мен қыздыру қатысында металл және бейметаллмен әрекеттеседі

N2 Химиялық қасиеті
Қалыпты жағдайда N2 тек Li-мен әрекеттеседі
6Li + N2 = 2Li3N
Қыздырғанда N2 металлдармен әрекеттеседі
2Al + N2 = 2AlN
500°C температурада және улкен қысымда N2 сутекпен әрекеттеседі
N2 + 3H2 ↔ 2NH3
1000°C температурада N2 оттекпен, бормен, кремниймен әрекеттеседі
N2 + O2 ↔ 2NO

Түрлері
Байланысқан азот - молекулалық азоттан басқа кез келген химиялық қосылыстың құрамына кіретін азот.
Молекулалық азот - N2 молекуласы түріндегі азот.
Нәруыздық азот - нәруыз құрамындағы азот.
Нитраттық азот - қосылыстардың құрамына нитротоп түрінде кіретін азот.
Сіңімтал азот- өсімдіктер сіңіре алатын түрдегі азот.

N2 қолданылуы
Аммиак пен азоттың синтезіне
Жарылғыш заттарды өңдіруге
Төмен температура жасауға
Сұйық азот салқындатқыш жүйелер саласында
Минералды тыңайтқыштар өндіруге: калий нитраты (KNO3) ; натрий нитраты (NaNO3) ; аммоний нитраты (NH4NO3) ; кальций нитраты (Ca(NO3) 2) .
- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz