V-T диаграммасындағы (1-4) циклді p-V және p-T координаталарына көшіру: аралықтардың сипаттамасы, адиабаттық процесс пен идеал газ моделінің шектеулері


Есеп
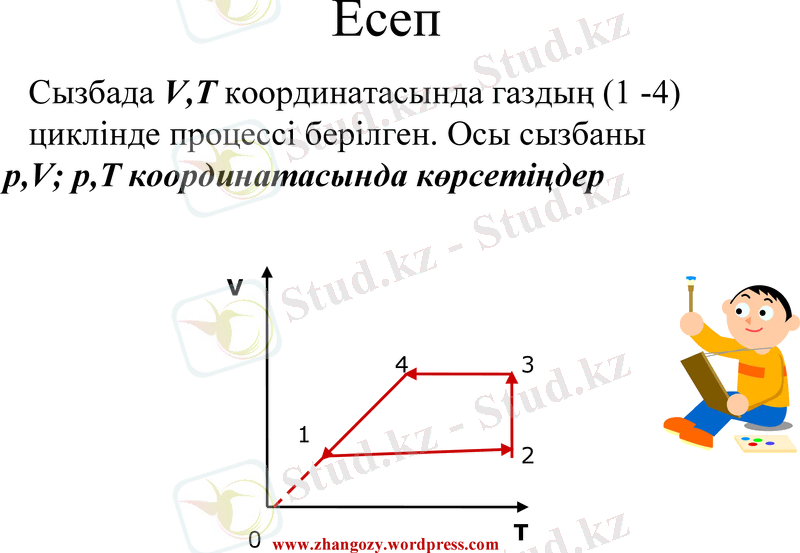
Сызбада V, T координатасында газдың (1 -4) циклінде процессі берілген. Осы сызбаны
p, V; p, T координатасында көрсетіңдер
V
T
1
4
3
2
0
www. zhangozy. wordpress. com
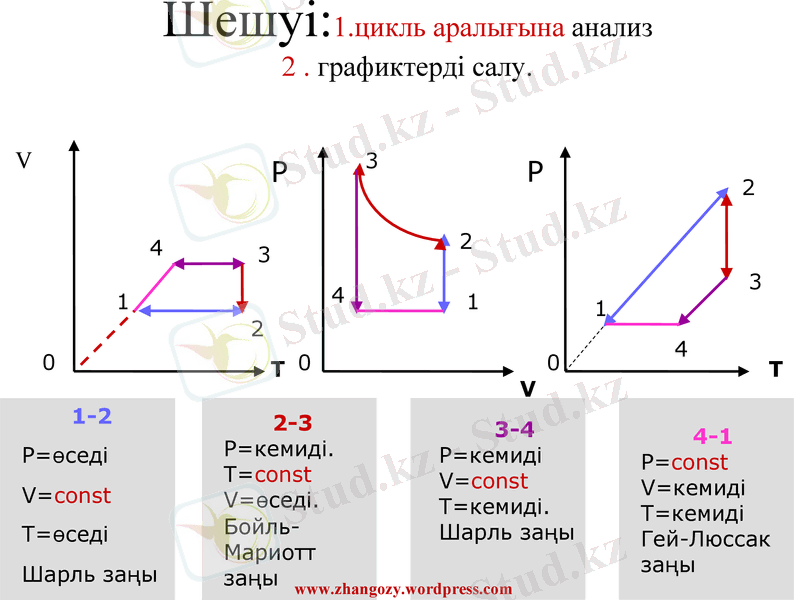
Шешуі:1. цикль аралығына анализ 2 . графиктерді салу.
V
T
V
T
Р
Р
0
0
0
1
2
3
4
1-2
P=өседі
V=const
T=өседі
Шарль заңы
2-3
P=кемиді.
T=const
V=өседі.
Бойль-Мариотт заңы
3-4
P=кемиді
V=const
T=кемиді.
Шарль заңы
4-1
P=const
V=кемиді
T=кемиді
Гей-Люссак заңы
1
2
3
4
1
2
3
4
www. zhangozy. wordpress. com

Аралық 1-2
Газ күйінің өзгеруі 1 ден 2 температураның артуы арқылы жүреді, бұл жағдайда көлем тұрақты.
Бұл аралық изохоралық ұлғаю.
p, V; p, T. координатасын саламыз
www. zhangozy. wordpress. com

Аралық 2-3
Газдың 2 күйден 3 өтуі температура тұрақты жағдайда өтеді, қысым кемігенде, көлем артады.
бұны изотермиялық ұлғаю деп атайды.
p, V; p, T. Графигін салайық.
www. zhangozy. wordpress. com

Аралық 3-4
Газдың 3 күйден 4 өттуі температураның. көлемнің кемуі арқылы жүреді.
Қысым тұрақты бұл изохоралық салқындау.
p, V; p, T. Графигін салайық
www. zhangozy. wordpress. com

Аралық 4-1
Газдың 4 күйден 1-ге өтуі температураның, көлемнің кемуі арқылы жүреді.
Қысым тұрақты. Бұл изобаралық сығылу деп аталады.
p, V; p, T. графигін саламыз
www. zhangozy. wordpress. com

Идеал газдың моделін қолдану шектілігі. Адиабаталық процесс. Пуассон теңдеуі.
Пән мұғалімі: Оңғарбай Ж.

Идеал газдың моделін қолдану шектілігі.
Әрбір физикалық модельдің қолданылу шегі болатыны белгілі. Сол сияқты идеал газ моделінің қолданылу шегі бар.
Идеал газдың моделін қолдану шектілігі қарастырылған есепке байланысты болмақ.
Егер қысым, көлем және температура арасында байланыс орнату қажет болса, онда газды бірнеше ондаған атмосфералық қысымға дейінгі дәлдікпен газды идеал деп алуға болады.
Егер фазалық кезеңдер (булану немесе конденсация, болмаса газдың тепе -теңдігі қарастырылатын болса ) онда газ қысымын тіпті бірнеше миллиметр сынап бағанасына дейінгі қысымда идеал газ моделін қолдануға болмайды.
www. zhangozy. wordpress. com

Адиабаталық процесс
Қоршаған ортамен жылу алмасынсыз өтетін процестерді адиабаталық процесс деп атайды.
dQ = 0
Адиабаталық процесс кезінде газ бен қоршаған ортаның арасында жылу алмасу болмайды.
www. zhangozy. wordpress. com
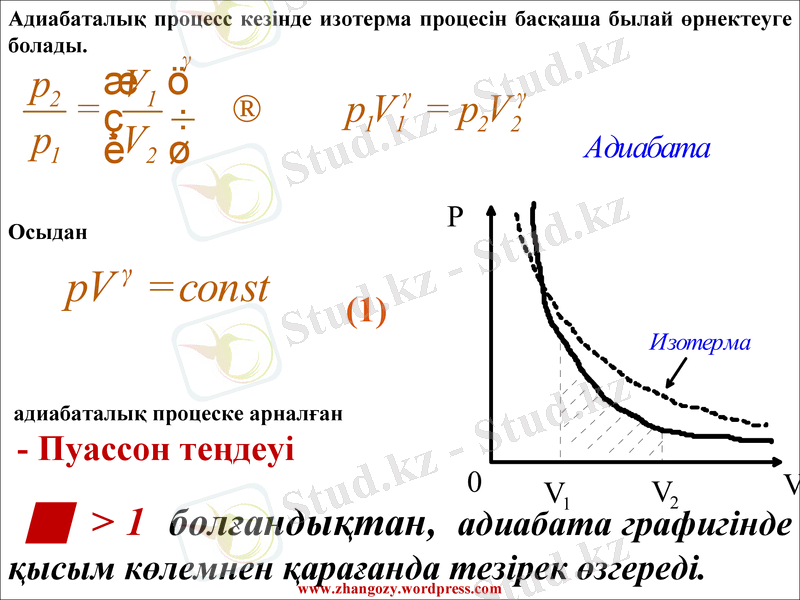
Адиабаталық процесс кезінде изотерма процесін басқаша былай өрнектеуге болады.
Осыдан
(1)
адиабаталық процеске арналған
- Пуассон теңдеуі
> 1 болғандықтан, адиабата графигінде қысым көлемнен қарағанда тезірек өзгереді.
www. zhangozy. wordpress. com

γ-адиабата көрсеткіші
Бір атомды идеал газ үшін адиабата көрсеткіші ү=5/3, екі атомды идеал газ үшін адиабата көрсеткіші ү=7/5, үш атомды идеал газ үшін адиабата көрсеткіші ү=4/3 болады, ал күрделі газдар үшін адиабата көрсеткіші молекуланың еркіндік дәрежесімен анықталады.
Адиабаталық процес кезінде адиабата көрсеткіші
ү=
R - универсал газ тұрақтысы
Сv-газдың тұрақты көлемдегі жылу сыйымдылығы
www. zhangozy. wordpress. com

Пуассон теңдеуін пайдаланып, адиабата көрсеткішін ескерсек идеал газ күйінің теңдеуін басқаша былай түрлендіреміз:
демек (2)
немесе (3)
Адиабаталық ұлғаю кезінде идеал газ салқындайды, ал сығылу кезінде -қызады.
www. zhangozy. wordpress. com

Назарларыңызға рахмет!
www. zhangozy. wordpress. com
- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz