Ақуыздардың құрылысы, құрамы және физико-химиялық қасиеттері



Белок. Белоктардың физикалық, химиялық қасиеттері.
Орындағандар: Орынбасар А. Е
Құрманбаева Д. Қ
Әлтаева А. Б
Қабылдаған: а. о Досмагулова К. К

Жоспар:
Белоктардың құрылысы
Белоктардың құрамы
Белоктардың қызметі
Химиялық қасиеттері

Фридрих Энгельс пікір бойынша: «Тіршілік - белок заттарының өмір сүру формасы».
Фридрих Энгельс
Ақуыз туралы алғашқы мәліметтер XVIII ғасырдан белгілі. 1745 ж. италиялық ғалым Беккори бидай ұнынан лейковина деген ақуызды бөліп шығарған.

Белок
молекулалары өте күрделі болатын аминқышқылдарынан құралған органикалық зат
аминқышқылдары қалдықтарынан күралған жоғары молекуларлық органикалық түзілістер.
Құрамында:
50, 6 - 54, 5% көміртек,
21, 5 - 23, 5% оттек,
6, 5 - 7, 3% сутек,
15 - 17, 6% азот,
0, 3 - 2, 5% күкірт бар, кейде фосфор кездеседі.
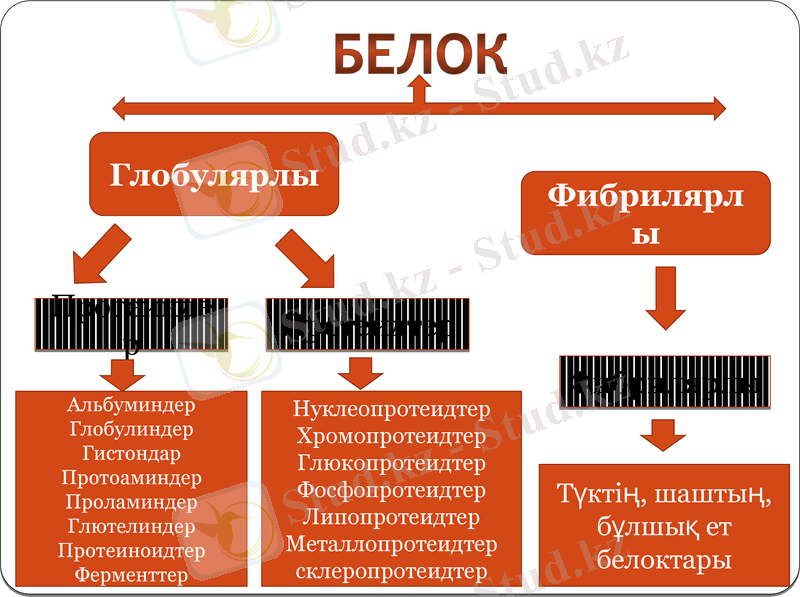
Белок
Глобулярлы
Фибрилярлы
Протеиндер
Протеидтер
Фибрилярлы
Альбуминдер
Глобулиндер
Гистондар
Протоаминдер
Проламиндер
Глютелиндер
Протеиноидтер
Ферменттер
Нуклеопротеидтер
Хромопротеидтер
Глюкопротеидтер
Фосфопротеидтер
Липопротеидтер
Металлопротеидтер
склеропротеидтер
Түктің, шаштың, бұлшық ет белоктары
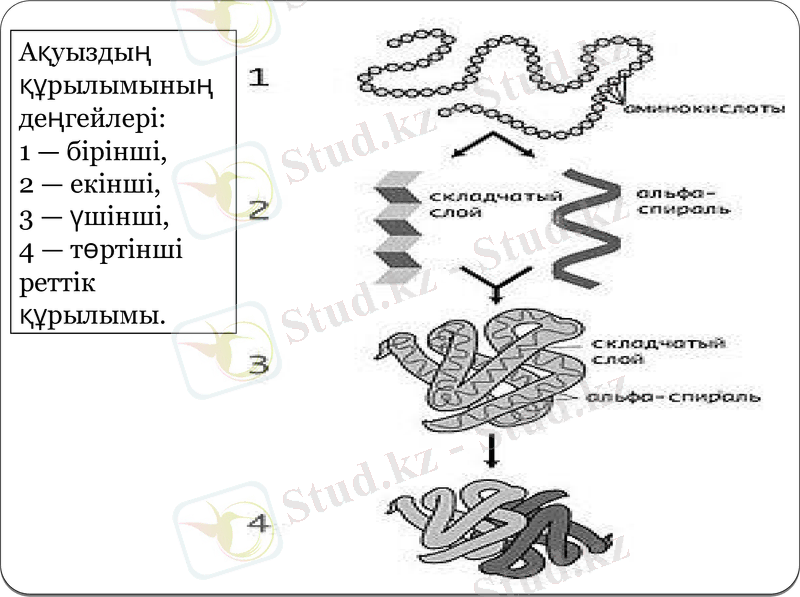
Ақуыздың құрылымының деңгейлерi:
1 - бірінші,
2 - екінші,
3 - үшінші,
4 - төртінші реттік құрылымы.
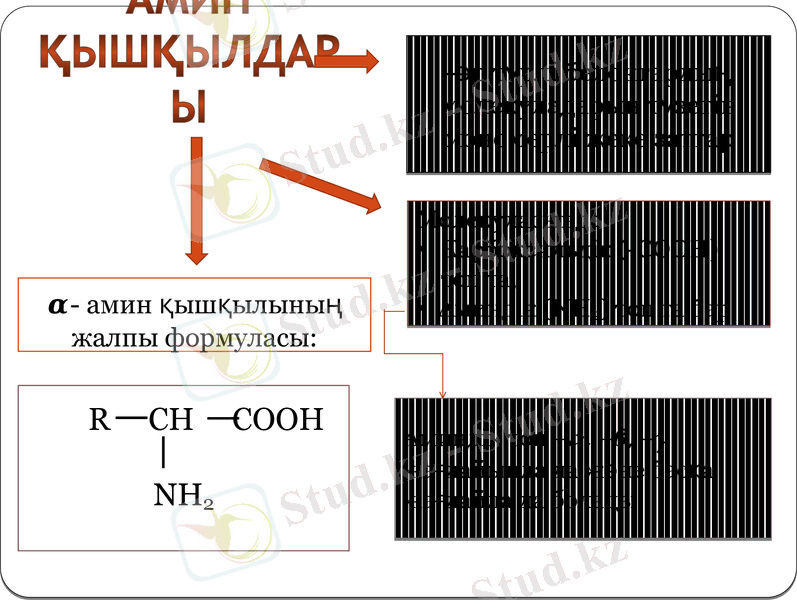
Амин қышқылдары
-әр түрлі белоктардың молекуладарын түзетін мономерлі жеке заттар
Молекуласында:
Карбоксильдік (-СООН) топ та,
Аминдік (NH2) топ та бар.
𝜶- амин қышқылының жалпы формуласы:
R CH COOH
NH2
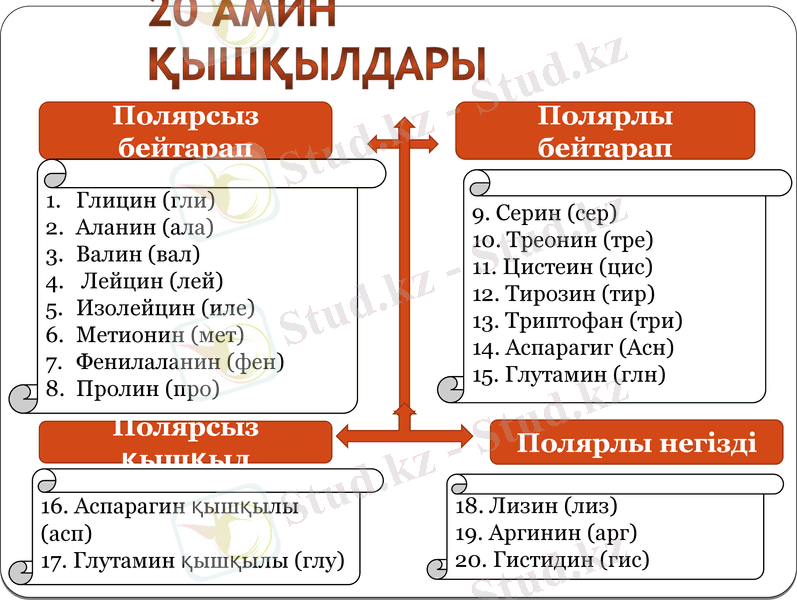
20 Амин қышқылдары
Полярсыз бейтарап
Полярлы бейтарап
Глицин (гли)
Аланин (ала)
Валин (вал)
Лейцин (лей)
Изолейцин (иле)
Метионин (мет)
Фенилаланин (фен)
Пролин (про)
9. Серин (сер)
10. Треонин (тре)
11. Цистеин (цис)
12. Тирозин (тир)
13. Триптофан (три)
14. Аспарагиг (Асн)
15. Глутамин (глн)
Полярсыз қышқыл
Полярлы негізді
16. Аспарагин қышқылы (асп)
17. Глутамин қышқылы (глу)
18. Лизин (лиз)
19. Аргинин (арг)
20. Гистидин (гис)

Белоктардың физикалық және химиялық қасиеттері
Белоктар үлкен молекулалы зат, ол жартылай өткізгіш мембранадан өте алмайды. Белоктарды басқа қоспалардан диализ арқылы тазарту осындай қасиетіне негізделген.
Дальтон дегеніміз- берілген зат молекуласының сутегі атомынан қанша есе ауыр екенін көрсететін шама
Мысалы: 16000 Д белоктың молекулалық массасы да 16000 болады.
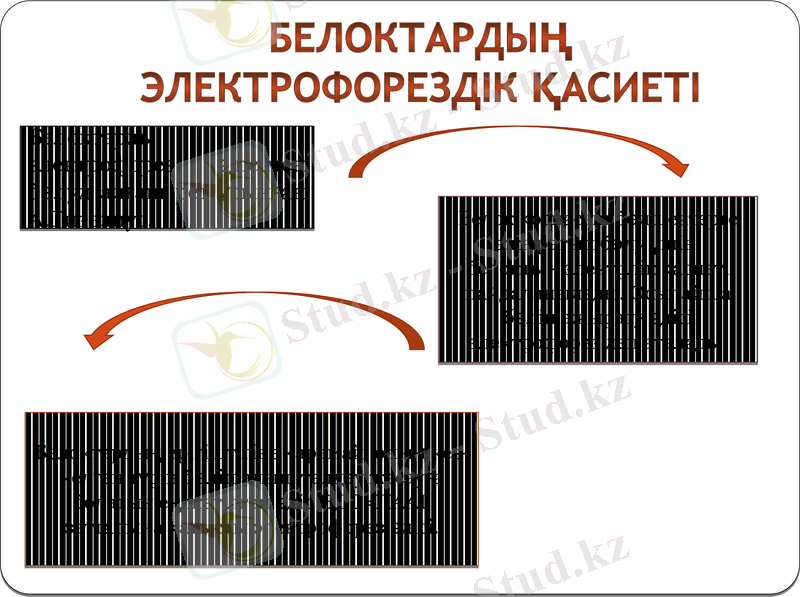
Белоктардың электрофорездік қасиеті
Белоктарды электрофорез әдісімен бөлуд алғаш рет ұсынған А. Тизелиус.
Белоктардың ерігіштігіне қарамай, оның кез-келген түрін бөліп алып, талдау жасауға болатын ең жетілген әдіс НДС=ПААГ заттарына қатысты электрофорез әдісі.
Белок қоспасын бөлшектерге ажыратып бөлу үшін, белоктың электрлік қасиеті пайдаланылады. Осылайша бөліп ажырату әдісі электрофорез деп аталады.

Белоктарға сапалық реакциялар
1. Биурет реакциясы. Бұл реакция арқылы белоктардың құрамындағы пептидті байланысты ашады. Пептидтер сілтілі ортада мыс иондарымен күрделі иондарымен күрделі комплексті қосылыстар түзіге қаблетті келеді.
NH2
NH2 C=O
C=O+HNH CO NH+NH3
NH2 NH2 CO
NH2
Несеп нәрі биурет

2. Ксантропротеин реакциясы. Белок ертітіндісіне концентрациялы азот қышқылымен әсер еткен кезде ерітінді сары түске боялады. Осыған аммиак қосса, қызғылт қоңыр түске боялады. Мысалы: тирозин, фенилаланин, триптофан сияқтылар.
ОН
NH2 NH2
СН СH2 СН СООН СH2 СН СООН
Тирозин
Фенилаланин
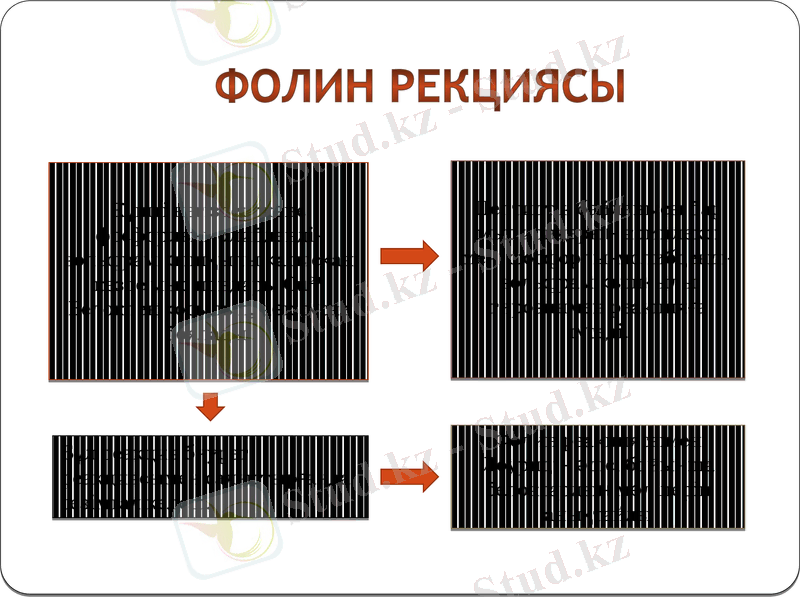
Фолин рекциясы
Күшті негіздер және фосфорлы-молибденді-вольфрам қышқылы қатысқан кезде мыс иондары Cu2+
Белокпен қосылып, көк түске боялады.
Пептидтік байланысы бар мыс иондарың комплексі мен фосфорлы-молибденді-вольфрам қышқылы тирозинмен реакцияға түседі.
Бұл реакция биурет реакциясымен салыстырғанда сезімтал келеді.
Фолин реакциясымен Лоуридің әдісі бойынша белоктардың мөлшерін анықтайды
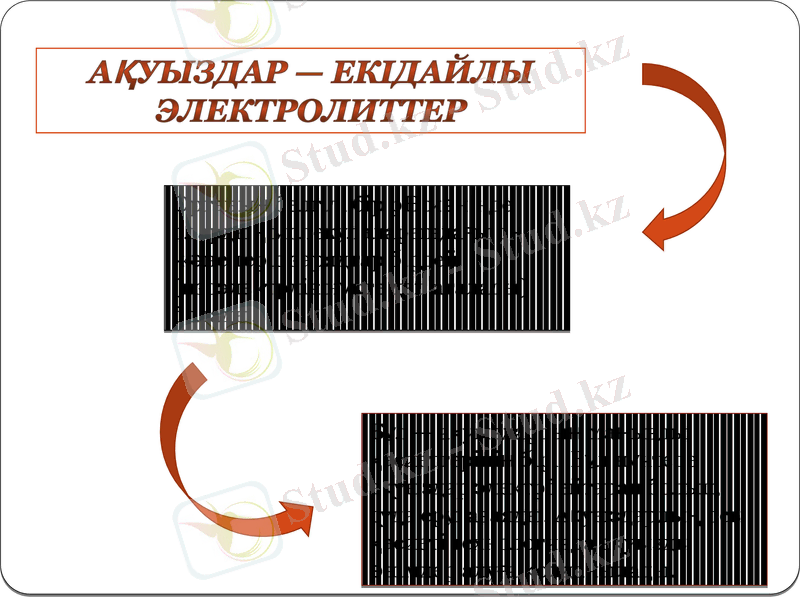
Ортаның белгілі бір рН мәнінде олардың молекулаларындағы оң және теріс зарядтар бірдей (изоэлектрлік нүкте деп аталады) болады.
Ақуыздар - екідайлы электролиттер
Бұл - ақуыздардың маңызды қасиеттерінің бірі. Бұл нүктеде ақуыздар электрбейтарап болып, суда еруі азаяды. Ақуыздардың осы қасиеті технологияда ақуызды өнімдер алуға қолданылады.

Пайдаланылған әдебиеттер:
1. Билогиялық химия оқу құралы З. Сейітов
Биологиялық химия К. С. Сағатов
2. www. wikipedia. com
- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz