Карбон қышқылдары: анықтамасы, құрылымы, жіктелуі және қасиеттері



Қазақ Ұлттық Аграрлық Университеті
2015 жыл

Карбон қышқылдары

Карбон қышқылдары
Карбон қышқылдары - молекула құрамында бір немесе бірнеше сутек атомдары карбоксил тобына - СООН алмасқан көмірсутектердің туындылары.
О
Карбоксил тобы С карбонил ( С О) және
ОН
гидроксил ( ОН) топтарынан тұрады. Карбон қышқылдарының жалпы формуласы: R(СООН) х.
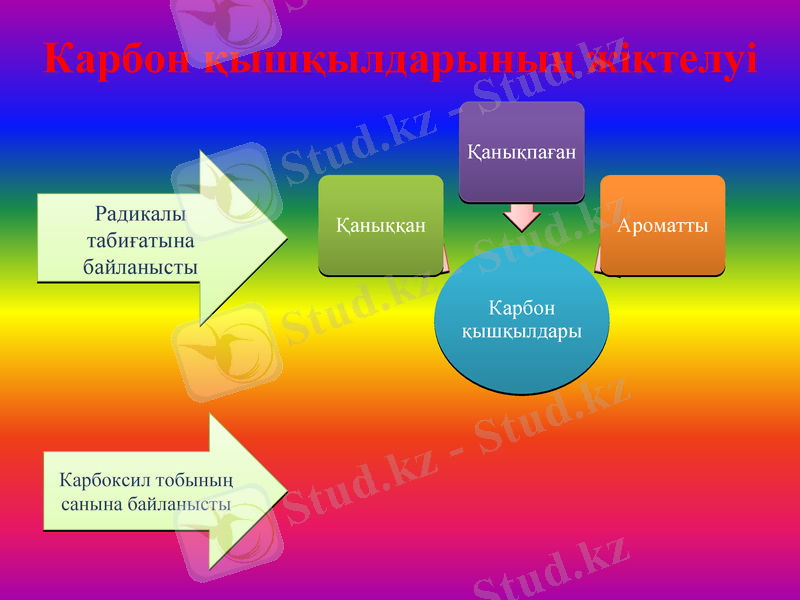
Карбон қышқылдарының жіктелуі
Радикалы табиғатына байланысты
Карбоксил тобының санына байланысты
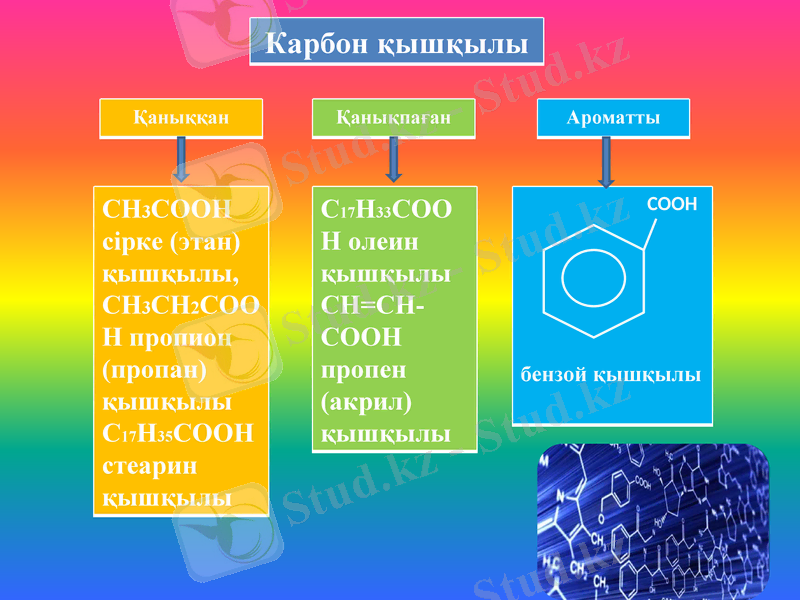
Карбон қышқылы
Қанықпаған
Ароматты
СН3CООН сірке (этан) қышқылы, СН3СН2СООН пропион (пропан) қышқылы С17Н35СООН стеарин қышқылы
СООН
бензой қышқылы
С17Н33СООН олеин қышқылы
СН=СН-СООН пропен (акрил) қышқылы
Қаныққан

Қаныққан бірнегізді карбон қышқылдары
Карбон қышқылдарымен танысуды бірнегізді қаныққан қышқылдан бастаймыз, жалпы формуласы: СnH2n+1COOH. Бұларды құрамындағы бір сутек атомы карбоксил тобына алмасқан алкандардың туындысы ретінде қарастыруға болады.
СН3 СН СООН
СН3
2-метилпропан қышқылы
СН3
СН3 С СООН
СН3
2, 2-диметилпропан қышқылы
Мысалы:

Химиялық қасиеттері
Карбон қышқылдарының химиялық қасиеттері олардың құрылысына байланысты. Карбон қышқылдарына, негізінен, бірнеше реакцяға тән:
Карбоксил тобының О - Н байланысы үзілу арқылы жүретін реакциялар, мысалы, диссоциациялану, тұз түзу реакциялары:
Карбоксил тобынан ОН тобы үзілуі арқылы жүретін реакциялар, мысалы, күрделі эфир, ацилгалогенид түзу, тотықсыздану реакциялары:
Радикалдық α-көміртек атомында жүретін реакциялар, мысалы, α-галоген карбон қышқылдарының түзілуі:

Физикалық қасиеттері
Қаныққан карбон қышқылдарының ағашқы үш мүшесі: құмырсқа, сірке және пропион қышқылдары - өткір иісті, сұйық заттар, суда ериді. Май қышқылдарның жағымсыз иісі бар, суда нашар ериді. Жоғарғы карбон қышқылдары С10 -нан бастап қатты заттар. Гомологтік қатарда молекулалық массаларының өсуіне қарай суда ерігіштігі кемиді, қайнау температуралары өседі.
Құрамында бірдей көміртек атомдары бар спирттер мен карбон қышқылдарының қайнау температураларын салыстырайық. Спирттерге қарағанда сәйкес карбон қышқылдарының қайнау температуралары едәуір жоғары. Олардың қайнау температураларының жоғары болу себебі, екі карбон қышқылы арасында молекулааралық сутектік байланы түзіліп, диерленеді. Молекулалары арасында біреуінің карбонилдегі оттек атомы мен екіншісінің гидроксил тобындағы сутек атомының арасында екі сутектік байланыс түзіледі:
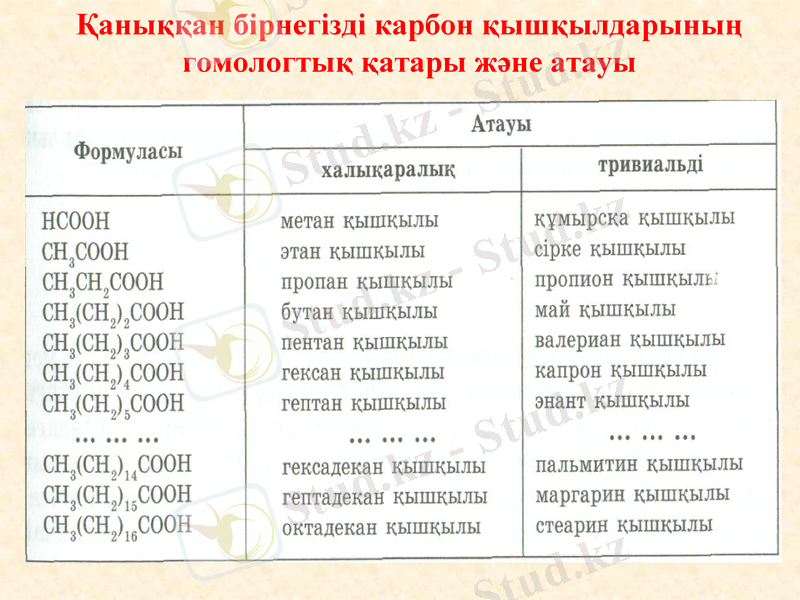
Қаныққан бірнегізді карбон қышқылдарының гомологтық қатары және атауы
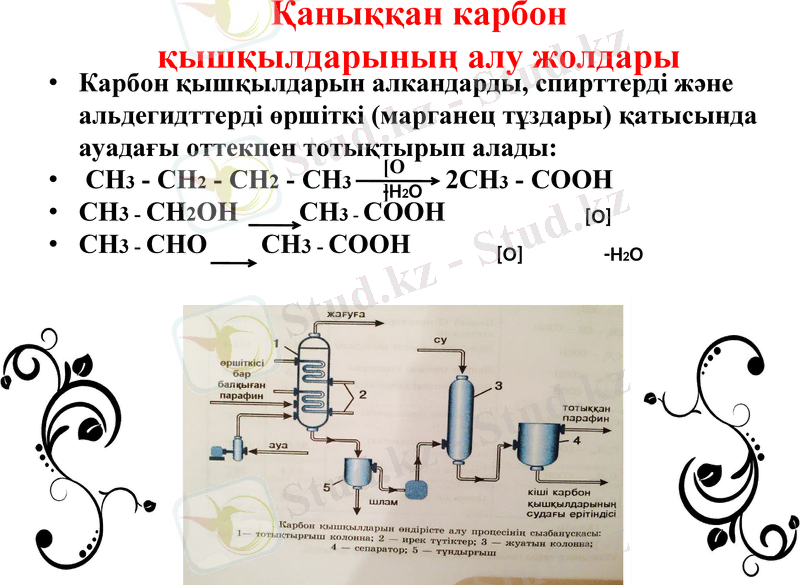
Қаныққан карбон қышқылдарының алу жолдары
Карбон қышқылдарын алкандарды, спирттерді және альдегидттерді өршіткі (марганец тұздары) қатысында ауадағы оттекпен тотықтырып алады:
СH3 - СН2 - СН2 - СН3 2СН3 - СООН
СН3 - СН2ОН СН3 - СООН
СН3 - СНО СН3 - СООН
[О]
[О]
[О]
-Н2О
-Н2О

Қанықпаған бірнегізді карбон қышқылдары
Қанықпаған карбон қышқылдары
қанықпаған көмірсутек радикалы карбоксил тобымен
байланысқан қосылыстар.
Құрамында бір қос байланысы бар қанықпаған карбон
қышқылдарының жалпы формуласы: СnH2n-1COOH.
Мысалы:
СН2 СН СООН
СН2 С СООН
СН3
2- метилпропен қышқылы (метакрил қышқылы)

Қанықпаған карбон қышқылдарды алу жолы
Қанықпаған қышқылдарды α-галоген қышқылдарына сілтінің спирттегі ерітіндісімен әсер етіп алады:
СН3 СН СООН СН2 СООН+Н2О+КCl
Cl
α- хлорпропан қышқылы

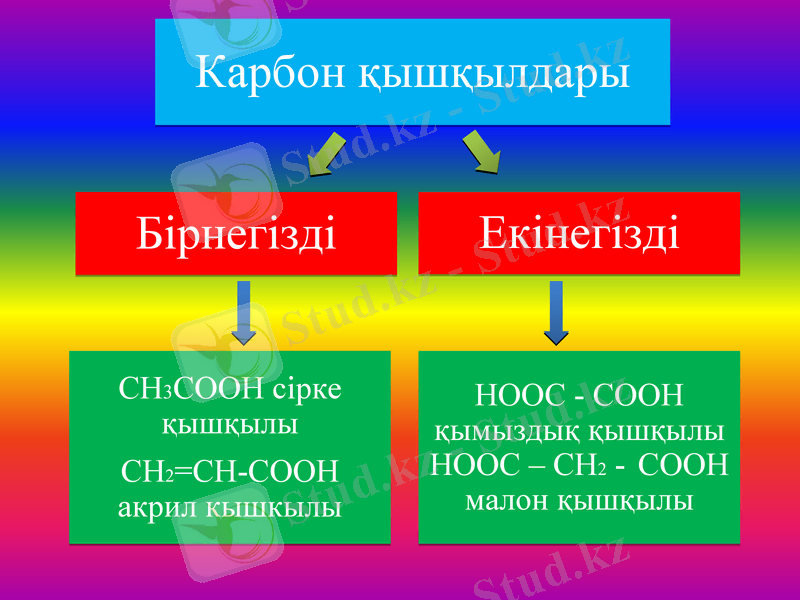
Екінегізді карбон қышқылдары
Суда жақсы еритін кристалды заттар. Молекуладағы карбоксил топтарының өзара әсерінен екінегізді қышқылдар бірнегізділерден қарағнда күштрек болады. Мысалы, қымыздық қышқылы сірке қышқылынан 200 еседей күшті. Дикарбон қышқылдарының диссоциациясы сатылап жүреді:
НООС СООН НООС СОО¯ +Н
НООС СОО¯ ¯ООС СОО¯ +Н
+
+

Химиялық қасиеттері
Екінегізді карбон қышқылдарының химиялық қасиеттері бірнегізді бірнегізді карбон қышқылдарына ұқсас, айырмашылығы - құрамында екі карбоксил тобы болуына байланысты. Карбоксил тобының біреуі немесе екеуі де реакцияға түсіп, бір немесе екі алмасқан туындылар түзе алады.
СООNa СООNa
және
COOH СООН
қышқылорта_
тұздар
СООС2Н5 СООС2Н5
және
СООН СООН
қышқыл орта_
эфирлер
Карбон қышқылдарының табиғатта кездесуі
Карбон қышқылдары табиғатта кең тараған. Құрмысқа қышқылы құмырқада, қалақайда, шырша жапырағында кездеседі. Оның тітіркендіргіштік қасиеті қалақай шаққанда сезіледі. Сірке қышқылы зат алмасу процесінде маңызды рөл атқарады. Адам организімінде тәулігіне 400 грамдай сірке қышқылы түзіледі. Май қышқылы майдың құрамында болады. Валериан қышқылы валериан өсімдігінің тамырында, лаурин қышқылы (С11Н23СООН) лавр өсімдігінде, кокос майында болады. Ешкі сүтінің құрамында алты, сегіз және он көміртек атомдары бар қышқылдар болады.

Карбон қышқылдары қалдықтарының атаулары
Қышқыл қалдығы
Атаулары
Ацил тобы
атауы
ацилат
Н - СО¯
СН3 -СО¯
СН2СН3 - СО¯
СН3СН2СН - СО¯
СН3СН - СО¯
СН3
СН3СН2СН2СН2 - СО¯
СО¯
Формил
Ацетил
Пропионол
Бутирил
Избутирил
Валерил
Бензоил
Н - СОО¯
СН3 -СОО¯
СН2СН3 - СОО¯
СН3СН2СН - СОО¯
СН3СН - СОО¯
СН3
СН3СН2СН2СН2 - СОО¯
СОО¯
Формиат
Ацетат
Пропионат
Бутират
Изобутират
Валерат
Бензоат
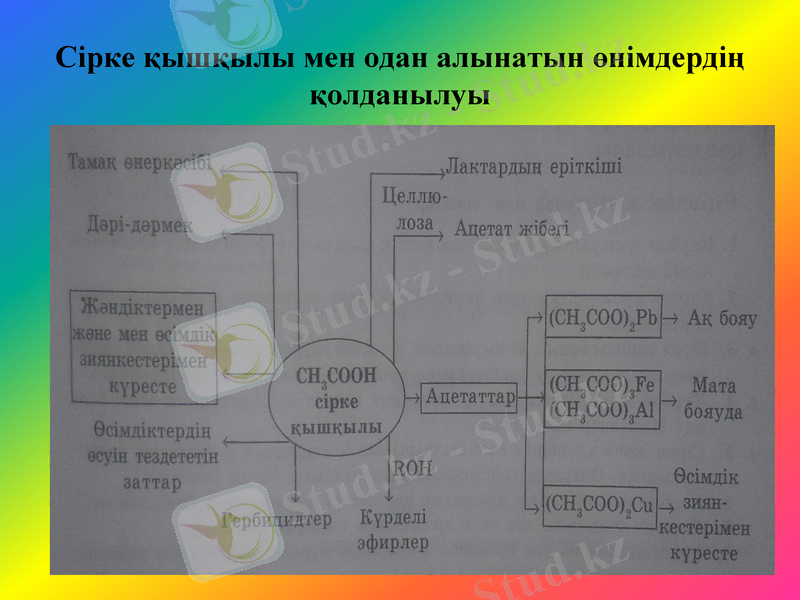
Сірке қышқылы мен одан алынатын өнімдердің қолданылуы

НАЗАРЛАРЫҢЫЗҒА РАХМЕТ!!!
- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz