Атомдық физика: элементар бөлшектер, ядролық процестер және атомдық теориялар



8. Атомдық физика
протон
нейтрон
электрон
позитрон
фотон(квант)
нейтрино немесе антинейтрино
π-мезондар
мюондар
- + 0
π
- +
μ

Элементарлы бөлшектердің қасиеттері
Электрон - теріс зарядталған, массасы ≈ 0, 511 МэВ элементар бөлшек, спины 0, 5 ћ.
Протон - оң зарядталған, массасы ≈ 938, 3 МэВ(≈ 1 а. б), спины 0, 5 ћ.
Позитрон - электронның антибөлшегі. Заряды 1, массасы электронның массасымен бірдей, спины-0, 5 ћ.
Нейтрон - нейтралды элементарлы бөлшек, массасы ≈ 939, 6 МэВ, спины 0, 5 ћ.
Еркін жағдайда нейтрон тұрақты емес және аз уақыт шамасында әсер етеді.
Протондармен бірге нейтрон атомдық ядро құрайды, ядродағы нейтрон тұрақты.

Сутегі және оның изотроптары
Сутегінің 3 изотоптары бар:
протий, дейтерий және тритий.
H
D
T
Массасы 1ге тең жеңіл сутегі немесе протий деп атайды және Н әрпімен белгіленеді, ал ядросы болса, протон деп атап, Р әрпімен белгілейді.

Дейтерий және тритий
Массасы 2-ге тең ауыр сутегі, оны дейтерий деп атайды. Оны 2Н символымен белгілейді немесе D (оқылуы «де») әрпімен белгілейді.
Ядро d - дейтрон.
Массасы 3-ке тең радиоактивті изотопты өте ауыр сутегі немесе оны тритий деп атайды, 3Н символымен немесе Т әрпімен (оқылуы «те») белгіленеді, ядро t - тритон.
Тритийдің радиоактивті схемасы:
T
3He
e-
ν
p+

Микроәлемнің заңдары
Нейтрондар еркін кезде протон, электрон және антинейтриноға тарайды. Неге лептондардың жұптары туындайды? Сонда антинейтрино тарататын энергияны электрон тарата алмайды ма?
Барлық реакциялар сақталу заңдары бойынша жүруі керек. Бұл заңдарға энергияның сақталу заңы жатады, лептонның, электр тогының, барионды зарядының сақталу заңы т. б…

Күннің көзіндегі ядролық реакциялар
Күннің көзі, жұлдыздар сияқты термоядролық реакциялар арқылы жарық береді.
H
H
D
3He
H
H
4He
e+
ν
γ

Жоғары энергиясы бар протондар жақындағанда, олардың біреуі протон, екіншісі позитрон және нейтриноға айналуы мүмкін. Сол кезде дейтерия ядросы пайда болады.
Дейтерия ядросы өзіне протонды қосып алады және қуатты гамма-квант таратады да, жеңіл геллийдің ядросы болып қалады
Ядролар бір-біріне жақындаған кезде, екі протонды «еркіндікке жіберіп», гелийдің ядросына айналуы мүмкін. Қорытынды жасайтын болсақ, айналымдардың нәтижесінде Гелийдің ядросы пайда болады. Геллийдің ядросының массасы 4 сутегінің ядросының массасынан төмен болғандықтан, қалған масса энергияға ауысады.
Қорытынды жасайтын болсақ, айналымдардың нәтижесінде Гелийдің ядросы пайда болады. Геллийдің ядросының массасы 4 сутегінің ядросының массасынан төмен болғандықтан, қалған масса энергияға ауысады.
.

π-мезон
Ядродағы протондар мен нейтрондар көп әсер ететін бөліктермен - шамамен электроннан 270 рет ауыр π-мезондармен ауысып отырады.
Зарядталған кезде мюон және антинейтриноға тарайды:
π -
Мюонды антинейтрино
μ-
Нейтралды түрде бір сәтте-ақ, екі γ-фотонға тарайды:
π 0
γ
γ

Мюон және ауыр лептон
Мюон электронға қатты ұқсайды, бірақ 200 есе ауыр болып келеді. Сонымен қатар мюон радиоактивті, ол электрон мен антинейтриноға тарайды:
μ-
ν
e-
Ауыр лептонға да осы қасиеттермен сипатталады.
«Лепто» - грек тілінен «жеңіл» деген мағына бередң, бірақ мюон мен лептонның ашылуынан кейін, «лептон» және «адрон» сөздері тек шартты болып қалды.

Ядронның құрылымы
Элементарлы бөлшектердің кестесін құру кезінде барлық топтастардың негізінде, кварк топтастары ретінде - (-⅓, -⅔, +⅔) электронына қарағанда, заряды аз бөлшектер шартты түрде алынды. Нуклондар 3 кварктерден тұрады: мезондардан, кварктен және антикварктен.
Зондтаушы электрон арқылы кварктер глюондармен айырбас жүргізіп отыратыны белгілі. Бір глюоннан басқа глюондар туындайтын болғандықтан, әсер етуші күш арақашықтыққа байланысты өсіп отырады.
Глюондарды бір-бірінен үзу кезінде жаңа мезондар пайда болады:
e-
π 0
π 0
Атом моделі
9.
9. 1.

Томсон атомының моделі
Атом - зарядталған бөлшектерден тұрады және олар тұрақты конфигурацияны сақтау үшін олар әрқашанда қозғалыста болады. Томсон моделінің негізгі идеясы да осы болатын.

Нагаоке атомның моделі
Нагаоке атомның моделі - «сатурнтәрізді». Мұндағы электрондар оң зарядталған денені айналатын шеңбер. Нагаоке атомның моделіндегі ортаңғы дененің атомының өлшемі Томсон моделіндегідей.

Планеталық атом моделі
Ескі атом моделі - планеталық болған. Көптеген оқымыстылар осы атом моделі жайлы айтқан болатын, бірақ оның ешқандай физикалық негізі болған жоқ.

Атомның құрылымы.
Радиоактивтіліктің ашылуы.
9.
9. 2.

Радиоактивтіліктің ашылуы
1 март 1896 ж.
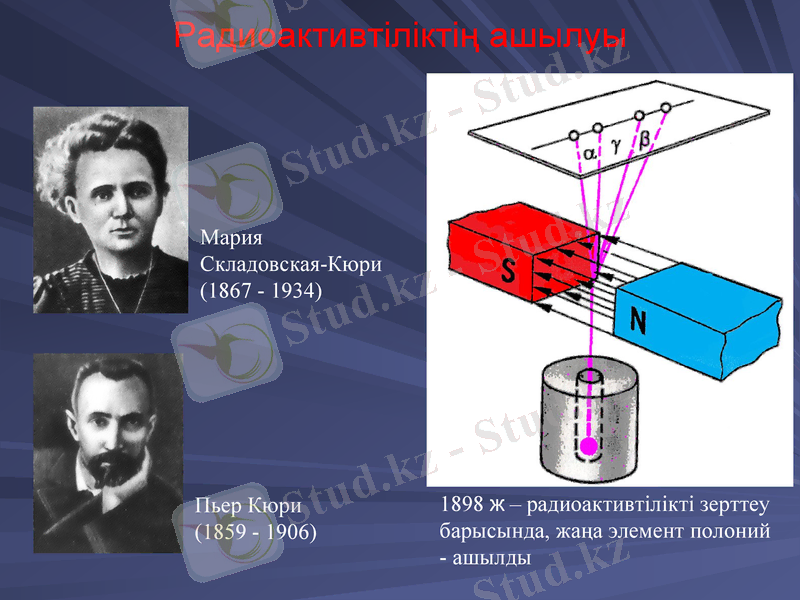
Радиоактивтіліктің ашылуы
1898 ж - радиоактивтілікті зерттеу барысында, жаңа элемент полоний - ашылды

Резерфордтың a-бөлшектердің таралуы жайлы тәжірибелері
9. 3.

Эрнест Резерфорд
Жаңа Зеландияда фермер жанұясында 1871 жылы өмірге келген. 1885 жылдан бастап ол Кавендиш лабораториясында жұмыс істей бастады. Сол жылдары Резерфорд бірінші докторант болатын. Резерфорд Дж. Дж. Томсон жетекшілігімен рентген сәулелерін және катодты зерттеу жұмыстарын жүргізді. Сол жылдары ол «Электромагниттік толқындардың магниттік детекторын» жасап шығарды.
Сонымен бірге, 1898 жылдан бастап радиоактивтілікті зерттеумен сондай-ақ, заряд және a-бөлшектің массасын ұсынды. Ал Ф. Соддимен біріге отырып радиоактивтіліктің жойылу процессінде басқа элементтің атомы пайда болатындығын және радиоактивтіліктің жоюлу заңын ашты.
1898 - 1907 жылдары ол Монреалда (Канада), 1907-1919 жылдары Манчестер университететінде (Великобритания) және 1919-1937 жылдары Кавендиш лабораториясының директоры болып қызмет атқарды.
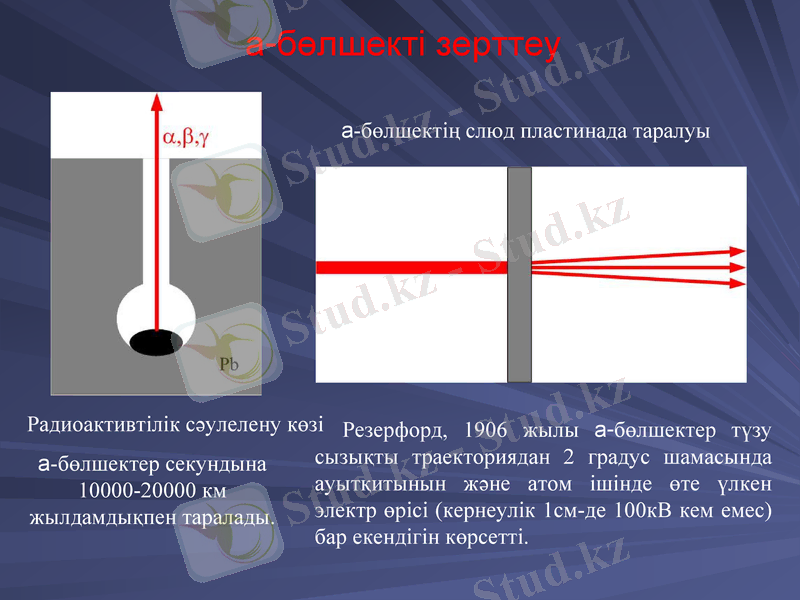
a-бөлшекті зерттеу
a-бөлшектер секундына 1-2 км жылдамдықпен таралады.
a-бөлшектің слюд пластинада таралуы
Резерфорд, 1906 жылы a-бөлшектер түзу сызықты траекториядан 2 градус шамасында ауытқитынын және атом ішінде өте үлкен электр өрісі (кернеулік 1см-де 100кВ кем емес) бар екендігін көрсетті.

a-бөлшектердің алтын фольгада таралуы
1909 ж., Резерфорд, Марсден, Гейгер.
8000 a-бөлшектен бірі 180° жуық бұрышпен таралатындығы байқалды.
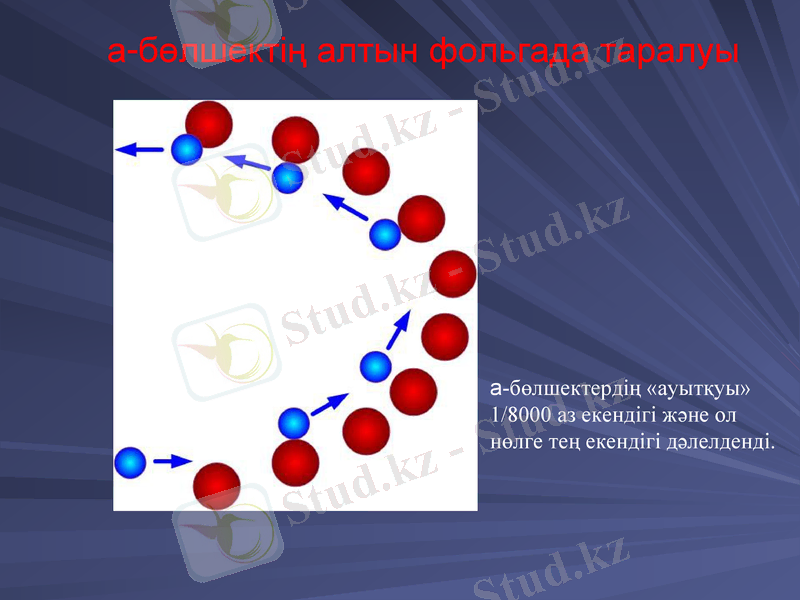
a-бөлшектің алтын фольгада таралуы
a-бөлшектердің «ауытқуы» 1/8000 аз екендігі және ол нөлге тең екендігі дәлелденді.
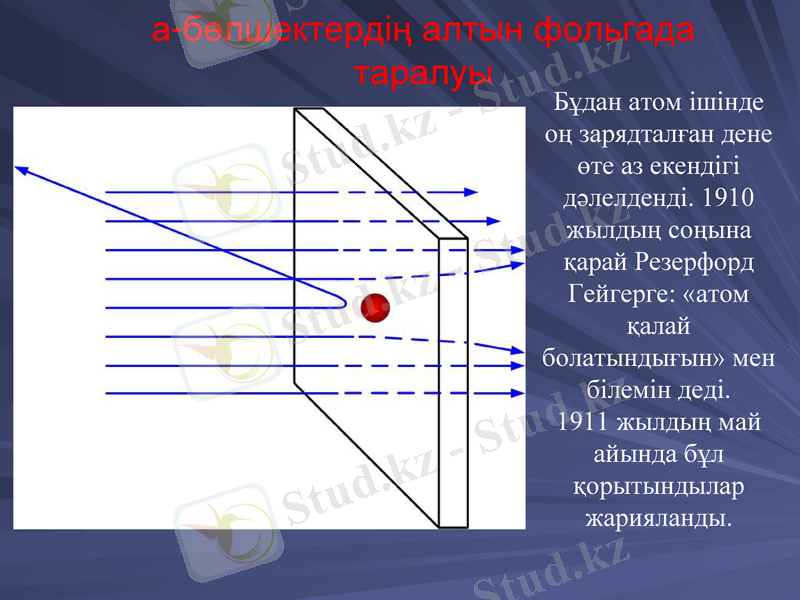
a-бөлшектердің алтын фольгада таралуы
Бұдан атом ішінде оң зарядталған дене өте аз екендігі дәлелденді. 1910 жылдың соңына қарай Резерфорд Гейгерге: «атом қалай болатындығын» мен білемін деді.
1911 жылдың май айында бұл қорытындылар жарияланды.
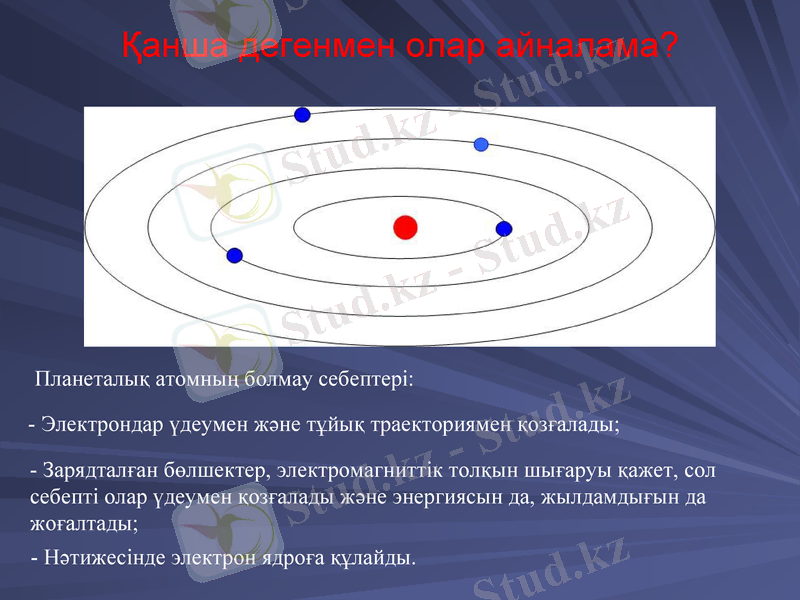
Қанша дегенмен олар айналама?
Планеталық атомның болмау себептері:
- Электрондар үдеумен және тұйық траекториямен қозғалады;
- Зарядталған бөлшектер, электромагниттік толқын шығаруы қажет, сол себепті олар үдеумен қозғалады және энергиясын да, жылдамдығын да жоғалтады;
- Нәтижесінде электрон ядроға құлайды.

Бор-Зоммерфельдтің квантталу туралы ережелері
9. 4.

Атом және квантың ұқсастығы неде?
1. Резерфордтың планеталық атомының бар екендігін дәлелдеу үшін, Бор квант қасиеттерін, жарықтың кванты - фотонның терең маңызы жоқ деген ұсынысты айтты.
2. Ол h Планк тұрақтысының өлшемі жоқ екендігіне көңіл аударды. Ол кезде (СИ жүйесінде Дж·с) болмаған еді.
3. Бор h Планк тұрақтысы, кез-келген процессте физикалық шама тұрақты нақты сан болу керек екендігін және ол өзгермеу қажет екендігін айтты.
4. Квантталу барысында осындай ұсыныстарға сүйене отырып, Бор электрон оң зарядталған ядроны айнала орбита бойымен қозғалатындығын және мынадай шарт бойынша орындалатындығын 2p RmV=nh, сонымен бірге
яғни электрон квантталадығын дәлелдеген болатын

Бор - Зоммерфельдтың квантталу ережелері
Планкқа сәйкес жарықтың сәулеленуі порция порциямен, яғни квантпен шығады және энергия тең болады:
Тұратын толқын энергиясының өзгерісі, сондай-ақ абсолют қара денеде пайда болатын энергияда тең болады:
Тұратын толқындарды сызықтық гармониялық осциллятор ретінде қарастыруға болады. Планкқа сәйкес, барлық сызықтық гармониялық осцилляторда мынадай энергия болады.
мұндағы n - бүтін сан
Сонда, соңғы шартты былай жазуға болады

Бордың сутегі атомы жайлы теориясы
6. 5.

Бордың сутегі ұқсас атомдарының теориясы
Электрон ядроны айнала дөңгелек орбита бойымен қозғалады. Оған ядро жағынан кулондық тартылу күші әсер етеді.
Электронның толық энергиясын табу керек және оның импульс моменті дискретті түрде өзгеретіндігін ескеруіміз қажет яғни ол мынадай түрде болады.
Толық энергия дегеніміз электронның механикалық энергиясы ол электронның кинетикалық және потенциалдық энергияларының қосындысы
Электронның потенциалдық энергиясы кулондық өрісте

мұндағы V - электронның жылдамдығы, R - орбита радиусы
мұнда Z - ядро заряды.
Ньютонның екінші заңын жазайық. Центрге тартқыш үдеу тең болады
Бордың сутегі ұқсас атомдарының теориясы

Бордың ұсынысына сүйене отырып, классикалық механикадағы барлық мүмкін болатын электрондардың тек орбиталық импульс моменті бар электрондар ғана орбита құра алады.
Бордың сутегі ұқсас атомдарының теориясы
бұдан
Алдында көрсетілгендей
Мұнда жылдамдық өрнегін қоямыз V:
сонда
Орбита радиусы өрнегін R -ді электрон энергиясы теңдеуіне қоямыз:

Бордың сутегі ұқсас атомдарының теориясы
Сонда, сутегі ұқсас атомдардың электрондарының энергиясы көптеген дискретті мәндер алуы мүмкін
Сонымен бірге, Бордың теориясына сәйкес сутегі ұқсас атомдардың электрондары орбитада мынадай радиуспен болады
мұнда n - бүтін сан.
- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz