s-, p- және d-элементтердің биологиялық маңызы және медицинадағы қолданылуы



Қ. А. Ясауи атындағы Халықаралық қазақ-түрік университеті
s-, p-, d- элементтерінің медициналық-биологиялық маңызы. Медицинада олардың қосылыстарының қолданылуы
Қабылдаған: Тулешова Эльмира
Орындаған: Базарбай Бақнұр
Тобы: ЖМ-004

Химиялық элементтер тірі ағзаның негізгі жасушаларын және биологиялық сұйықтықты құрайды. Адам мен жануарлар ағзасына әртүрлі химиялық элементтердің әсерін оқып-үйрену ХIХ ғасырдың екінші жартысынан басталды. Вернадскийдің анықтамасы бойынша ағзада жинақталып, әртүрлі биологиялық қызмет атқаратын элементтерді биогенді деп атайды. Академик Вернадский мен оның шәкірті Фесенков адам ағзасындағы барлық биогенді элементтерді олардың денедегі шама - мөлшеріне орай үш типке бөлді:
Бірінші тип - адам ағзасындағы шамасы оның массасынан 10% асатын макроэлемент. Оларға 13 химиялық элементтер жатады: O, C, H, N, Ca, P, K, N, S, Cl, Mg, F, Fе.
Бұл элементтердің қосындысы адам денесі массасының 99, 99% құрайды.
негізінен жасушалар құрылысында, ортаның рН және иондық не қышқылдық негіздік тепе-теңдікті қалыпты деңгейде ұстап тұруда, коллоидтар үшін т. б. маңызы зор.
Биологиялық активті заттармен алмасу жэне көбею процестеріне қатысады.
Үшінші типке әрқайсысының мөлшері 10 %-дан аспайтын, ультрамикроэлементтер. Мысалы, оларға Zn, Mn, Cu, Si, Br, Ag, As, Co жатады.
Адам денесі массасының 0, 001% соңғы екі тип, яғни олиго- және ультрамикро-элементтер құрайды. Олигоэлементтер және де ультрамикроэлементтер барлығы 21 элементтен тұрады.

Элементтер электрондық орбитальдардың толуына байланыста s-, p-, d- деп жіктеледі
периодтық жүйенің IA және IIA негізгі топшасында орналасқан. Сыртқы электрон қабатында бір (s1-элементтер) немесе екі (s2 элементтер) электроны бар. Оларды сілтілік және сілтілік-жер металдары деп атайды. Топтарда s-элементтері гидроксидтерінің негіздігі жоғардан төмен қарай артады (мысалы, LiOH тан CsOH қарай) ал период бойынша (s1- ден s2 элементке өткенде) артады.
Д. И Менделеевтің жүйесінің III A-VIII А топтарында орналасқан элементтер жатады. Олардың ішінде практикалық маңызы бар катиондар Al, Pb, As жатады. Олар ауыспалы валенттілік көрсетеді, сондықтан әр түрлі қышқылдар түзеді. Элементтің тотығу дәрежесі өскен сайын қышқылдың күші артады. Көбісі оттекті қышқылдар және топ элементтері ғана оттексіз қышқылдар түзеді.
Д. И. Менделеевтің периодтық жүйесінде 33 d-элемент бар: олар төртінші, бесінші және алтыншы периодтарда 10 d элементтен орналасқан. Олар s және p- элементтердің арасында орналасқан. d- элеметтерге тән ерекшелік, олардың атомдарының орбитальдары электронмен толтырылуы сыртқы қабаттан емес одан одан кейінгі ішкі қабаттан басталады.
s-элементтер
p-элементтер
d-элементтер
H, He, Li, Be, Na, Mg, K, Ca, Rb, Sr, Cs, Ba, Fr, Ra
B, C, N, O, F, Ne, Al, Si, P, Cl, Ar, Ga, Ge, As, Se, Br Kr, In, Sn, Sb, Te, I, Xe, Tl, Pb, Bi, Po, At, Rn, Nh, Fl, Mc, Lv, Ts, Og
Sc, Ti, V, Cr, Mn, Fe, Co, Ni, Cu, Zn, Y, Zr, Nb, Mo, Tc, Ru, Rh, Pd, Ag, Cd, La, Hf, Ta, W, Re, Os, Ir, Pt, Au, Hg, Ac, Rf, Db, Sg, Bh, Hs, Mt, Ds, Rg, Cn

Биосферада сутек бос күйінде кездеспейді. Биосферада ол табиғи су, газдар және органикалық заттардың құрамында болады. Сутек ағзадағы көмірсутек ақсылдар, майлар және нуклеин қышқылдарының құрамына кіреді. Сутек органикалық қосылыстардың құрылысын түзуге қатыспайды. Тірі жасушалар массасының 90% құрайтын суда сутегі атомдарының негізгі мөлшері болады. Су жасушалар жүйесінде еріткіш қызметін атқарады.
Бұл микроэлемент. Ол тірі ағзалардың тұрақты кұрамды бөлігі. Литий ионы сілтілік металдардың ішінде ең радиусы кішісі, сулы ерітінділерде күшті гидратталған, осы гидратталған түрінің радиусы Na+ және K+ радиусынан жоғары болады. Li+ иондары, кейбір ферменттер активтілігіне әсер ете отырып, бас миы қатпарлары жасушаларында Na+- К+ иондық теңдігін реттейді. Сондықтан құрамында литий ионы бар дәрілер жүйке ауруларын емдеуде қолданылады.
Бұл адам ағзасында (1, 5%) көптеу таралған элементтердің (О, С, Н, N, Са) бірі. Кальций қан ұю механизмдеріне қатысады, ағзадан ауыр металдардың бөлініп шығуына жағдай тудырады, антиоксиданттық қызмет атқарады. Ағзада болатын негізгі массасы сүйектер мен тісте болады. Кальций тапшылығы гипертоникалық кризиске, жүктілік токсикозына шалдықтыруы мүмкін, холестериннің қандағы деңгейін жоғарлатады, сүйектердің мықтылығын төмендететін остеопорозды дамытуы, жүйке жүйесінің қозуын жоғарлатуы, шашты түсіруі мүмкін.
Барийдің биогенді маңызы аз зерттелген. Суда және қышқылдарда еріген барий тұздары улы болады. Қышқылдар мен суда ерімейтін күкіртқышқылды барий рентген сәулелерін жақсы жұтады, сондықтан оны асқазан мен ішекті зерттеуде қолданады. BaS04 барий сульфаты; рентген айқындауда қолданылады.
S - элементтерінің биологиялық маңызы және олардың қосылыстарының медицинада қолданылуы
H
Li
Ca
Ba
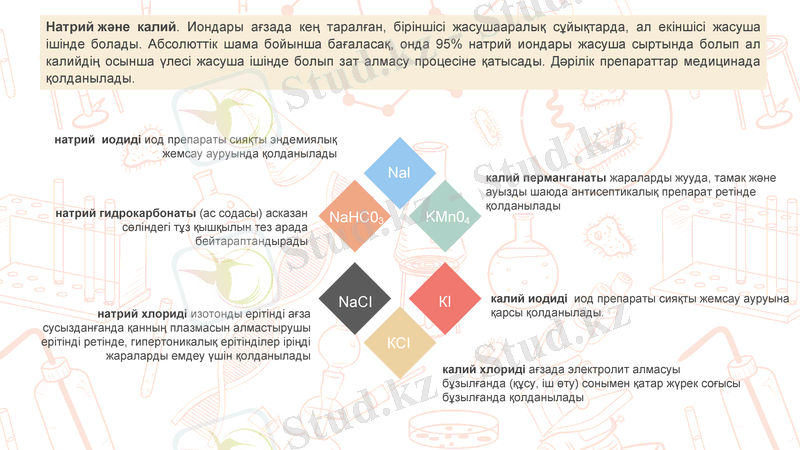
Натрий және калий. Иондары ағзада кең таралған, біріншісі жасушааралық сұйықтарда, ал екіншісі жасуша ішінде болады. Абсолюттік шама бойынша бағаласақ, онда 95% натрий иондары жасуша сыртында болып ал калийдің осынша үлесі жасуша ішінде болып зат алмасу процесіне қатысады. Дәрілік препараттар медицинада қолданылады.
натрий иодиді иод препараты сияқты эндемиялық жемсау ауруында қолданылады
натрий гидрокарбонаты (ас содасы) асказан сөліндегі тұз қышқылын тез арада бейтараптандырады
натрий хлориді изотонды ерітінді ағза сусызданғанда қанның плазмасын алмастырушы ерітінді ретінде, гипертоникалық ерітінділер іріңді жараларды емдеу үшін қолданылады
калий перманганаты жараларды жууда, тамак және ауызды шаюда антисептикалық препарат ретінде қолданылады
калий иодиді иод препараты сияқты жемсау ауруына қарсы қолданылады.
калий хлориді ағзада электролит алмасуы бұзылғанда (құсу, іш өту) сонымен қатар жүрек соғысы бұзылғанда қолданылады

С
O
F
Br
Р - элементтерінің биологиялық маңызы және олардың қосылыстарының медицинада қолданылуы
Көміртегі оксидінің (II) адам ағзасына зиянды әсері бар, оны «пеш газы» деп те атайды. Дем алғанда көміртегі оксиді (II) қанға өтеді және гемоглобинмен - карбоксигемоглобин түзеді. Пеш газымен улану өлімге себепші болады. Медицинада қолданылады: 1. Активтелген көмір (карболен) ; ауыр металдар тұздарымен, алкалоидтармен т. б уланғанда қолданылады. 2. NaHC03 натрий гидрокарбонаты; асқазан сөлінің кышқылдығын кемітеді; ол сулы ерітінділерді шаюда, жууда қолданылады.
Ауадағы оттектің мөлшеріне көптеген өмірлік процестер байланысты. Оттектің негізгі қызметі тірі ағзадағы зат алмасу процестеріндегі тотығу-тотықсыздану реакцияларын реттеу. Медицинада оттек көміртек оксидімен (II), НСN уланғанда және оттек жетіспейтін ауруларды емдеуде қолданылады. Емдеу мақсатында оттекті тері астына жіберуге асқазанға оттегі коктейлі түрінде пайдалануға болады. Кейінгі кезде жоғарғы қысымда оттегімен емдеу оны гипербаралык медицина деп атайды.
Фтордың биологиялық маңызы аз зерттелген. Tic және сүйектін негізгі қатты бөліктерінің түзілуіндегі минералды зат алмасу процесіне қатысады. Tic және сүйекте фтор фторапатит (Са5(Р04) 3Ғ) түрінде болады. Адам фторды ішетін судан қабылдайды, негізінде Iл суда 1 мг- фтор болуы тиіс. Егер ішетін суда фтор жеткіліксіз болса, онда тіс эмалдары бұзыла бастайды. Tic кариесінің негізгі емі-суды фторлау. Бос күйіндегі газ тәрізді фтор өте улы келеді. Медицинада натрий фториді NaҒ қолданылады; ол тіс пастасы құрамына ендіріледі, (кариесті емдеу үшін) .
Биогенді элементтерге жатады. Медицинада (NaН4Вг) аммоний, (КВг) калий және натрий NaВг) бромидтері қолданылады.
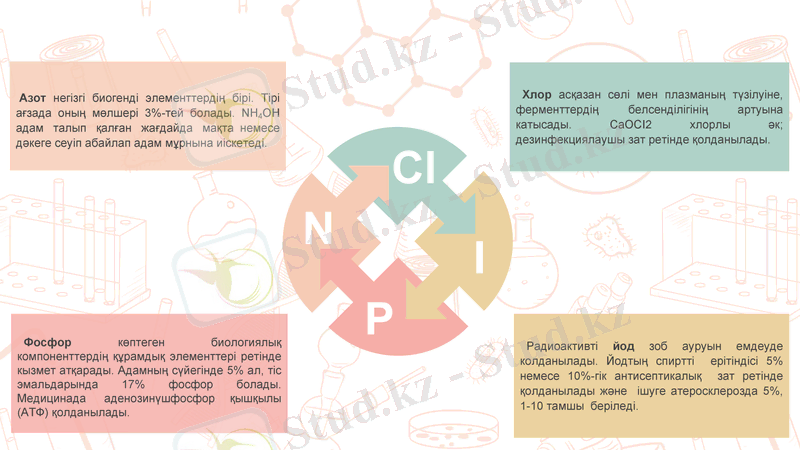
Азот негізгі биогенді элементтердің бірі. Тірі ағзада оның мөлшері 3%-тей болады. NH4OH адам талып қалған жағдайда мақта немесе дәкеге сеуіп абайлап адам мұрнына иіскетеді.
Фосфор көптеген биологиялық компоненттердің құрамдық элементтері ретінде кызмет атқарады. Адамның сүйегінде 5% ал, тіс эмальдарында 17% фосфор болады. Медицинада аденозинүшфосфор қышқылы (АТФ) қолданылады.
Хлор асқазан сөлі мен плазманың түзілуіне, ферменттердің белсенділігінің артуына катысады. СаОСІ2 хлорлы әк; дезинфекциялаушы зат ретінде қолданылады.
Радиоактивті йод зоб ауруын емдеуде колданылады. Йодтың спиртті ерітіндісі 5% немесе 10%-гік антисептикалық зат ретінде қолданылады және ішуге атеросклерозда 5%, 1-10 тамшы беріледі.

Ag
Cu
Mn
Mo
d - элементтерінің биологиялық маңызы және олардың қосылыстарының медицинада қолданылуы
Тірі ағзада күмістің физиологиялық рөлі жеткіліксіз зерттелген. Күміс - ультрамикроэлемент. АgNO3 (ляпис) күміс нитраты; жұмсартушы және күйдіруші зат ретінде қолданылады. Стоматологияда тісті бүтіндеу, алдын-ала тіс каналдарын күмістейді. Бірінші күміс нитратынан күміс оксидінің аммиакты ерітіндісін және 10%-тік формалинді алады. Бұл процестің өтуін былай жазамыз:
2AgNО3 + 2NН4ОН -Аg20 + 2NН4NО, + Н20 Аg0 + Н-СНО -Аg + Н-СООН
- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz