Аниондардың сапалық реакциялары мен аналитикалық жіктелуі



АНИОНДАРДЫҢ САПАЛЫҚ РЕАКЦИЯЛАРЫ
қалған реакцияларды кітаптан жазыңыз!!!
"Файловый менеджер" арқылы жібердім
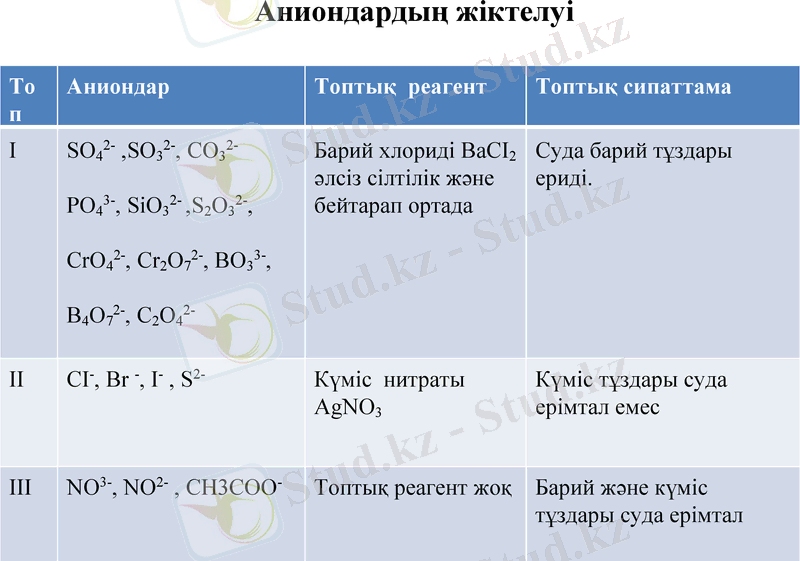
Аниондардың жіктелуі
Топ
Аниондар
Топтық реагент
Топтық сипаттама
I
SO42-, SO32-, CO32- PO43-, SiO32-, S2O32-, CrO42-, Cr2O72-, BO33-, B4O72-, C2O42-
Барий хлориді ВаСІ2 әлсіз сілтілік және бейтарап ортада
Суда барий тұздары ериді.
II
CI-, Br -, I-, S2-
Күміс нитраты AgNO3
Күміс тұздары суда ерімтал емес
III
NO3-, NO2-, CH3COO-
Топтық реагент жоқ
Барий және күміс тұздары суда ерімтал

І аналитикалық топ аниондарына сапалық реакциялар
1-ші аналитикалық топ катиондарында
SO42- сульфат ионы,
SO32- сульфит ионы,
СО32- карбонат ионы,
РО43- фосфат ионы,
SіО32- силикат ионы жатады.
Бұл аниондар Ва2+ катионымен тұздар түзеді, ол тұздар суда аз ериді, тек қана барий сульфаты сұйытылған минерал қышқылдарда жақсы ериді. Сол себептен бұл топтың катиондарын топтық реагент арқылы бөліп алуға, әлсіз сілтілік және бейтарап ортада болады. Бірінші топтың аниондары катион Аg+ мен тұз түзеді, ол тұз сұйылтылған азот қышқылында ериді, ал күміс сульфаты суда да ериді.

Сульфит - анионына SО32- сапалық реакция
Барий хлориді ВаСl2 сульфит-анионымен ақ тұнба барий сульфитін ВаSΟ3 түзеді
ВаСl2 + Nа2SО3 → ВаSО3↓+ 2ΝаСl

тұнба қышқылдарда ериді

РО43- фосфат ионына жеке реакциялар
1. Магнезиальды қоспа (МgСl2, NH4OH және NH4CI) - қоспасы РО43- аниондарымен ақ кристалды тұнба түседі.
Na2HPO4 + NH4OH + МgСl2 → МgNH4PO4 ↓ + 2NaСІ + H2O

Тәжірибе.
5-6 тамшы МgСl2 магний хлориді ерітіндісіне бірнеше тамшы аммиак ерітіндісін қосса, магний гидроксидінің тұнбасы түзіледі.
Ол тұнбаны аммоний хлоридін қосып ерітеді, сонан соң үстіне бірнеше тамшы натрий гидрофосфатының ерітіндісін қосып, пайда болған ақ тұнба МgNH4PO4, фосфат анионының бар екендігін көрсетеді.

2. Күміс нитраты AgNO3 фосфат-ионымен сары түсті күміс фосфаты тұнбасын береді
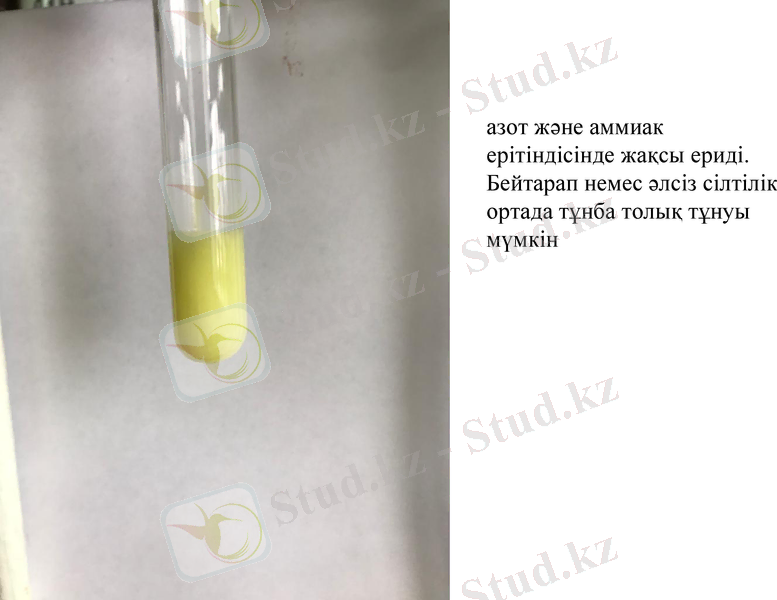
азот және аммиак ерітіндісінде жақсы ериді. Бейтарап немес әлсіз сілтілік ортада тұнба толық тұнуы мүмкін

Көмір қышқылдарының тұздары қышқылдарда көміртек оксидін (ІV) бөле жүреді
Na2CO3 + 2HCI → NaCI + H2CO3
H2CO3 → H2O + CO2↑
Көміртек оксидінің бар екендігін ізбес суы арқылы білуге болады.
Са(ОН) 2 + СО2 → СаСО3 ↓ + Н2О
СО32- карбонат анионына жеке реакциялар

Видео
H2CO3 → H2O + CO2↑
Суретке басыңыз

S2O32- тиосульфат-иондарының реакциялары
S2O32- тиокүкірт қышқылының Н2S2O3 анионы. Тиокүкірт қышқылы тұрақсыз және бос күйінде кездеспейді. Бұл қышқылдың сілтілік металдарының тұздары тұрақты болғанмен, сулы ерітінділерінде гидролизге ұшырайды. Тиосульфаттар күшті тотықсыздандырғыштар.
Минералды қышқылдар тиокүкірт қышқылын өзінің тұздарынан ығыстырып шығарады:
Na2S2O3+2HCl=H2S2O3+2NaCl
Күкірт түзу нәтижесінде ерітінді лайланады. Бұл реакция сульфиттердің катысында тиосульфаттарды анықтауға болады, себебі күкіртті қышқыл ыдырау кезінде тек SO2 газы бөлінеді, ал күкірт түзілмейді.
https://www. youtube. com/watch?v=I6QbHIYzc3M
Видео!!!
Тиокүкірт қышқылы түзілген сәтте ыдырайды:
H2S2O3=S↓+SO2↑+H2O

CrO42- хромат-иондарының реакциялары
Хромат - ионы H2CrO4 хром қышқылының анионына жатады. Қышқылдық ортада ол дихромат-ионына Cr2O72- ауысады:
CrO42-+2H↔Cr2O72-+H2O
BaCl2 барий хлориді хроматтармен барий хроматының сары тұнбасы түзіледі

Тұнба минералды қышқылдарда ериді, ал сірке қышқылында ерімейді. Cr2O72- ионы барий хлоридімен Ba CrO4 тұнбасы түзеді тек натрий ацетаты қатысында.
қалған реакцияларды кітаптан жазыңыз!!!
"Файловый менеджер" арқылы жібердім
- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz