Витаминдер мен органикалық қышқылдарды биотехнологиялық өндіру әдістері мен технологиясы



Витаминдер алу биотехнологиясы

2. Витаминдер әртүрлі химиялық табиғаттағы алмастырылмайтын органикалық қосылыстар тобы. Олар кез-келген организмге каталитикалық және реттеуші функцияларды орындау үшін аз концентрацияда қажет.
Витаминдер негізгі көзі - өсімдіктер.
Витаминдер адам ағзасына тағам өнімдерімен бірге келеді.
Дәрумендердің жетіспеушілігі әртүрлі ауруларға әкелуі мүмкін (бұл цинга, әртүрлі анемия және т. б. ) .
Витаминдерді қолдану:
1. бұл дәрі-дәрмектер
2. бұл теңдестірілген тамақтану компоненттері
3. бұл парфюмерлік өнімдердің компоненттері
4. бұл биологиялық белсенді қоспалар
5. бұл өндірістің биотехнологиялық процестерін қарқындатуға арналған компоненттер.

Әдетте, витаминдердің өздері емес, олардың туындылары - коферменттер жоғары биологиялық белсенділікке ие екендігі белгілі. Витаминдік аналогтары табылмаған коферменттер де ашылған.
Әр түрлі витаминдерге негізделген коферменттік формалар кең әсер ету спектріне ие және медициналық практикада тиімді қолданылады.
Көптеген витаминдерді табиғи көздерден бөліп алады немесе химиялық жолмен синтездейді. Алайда, биотехнологияның көмегімен бүгінде құрылымы жағынан өте күрделі В2, В12 витаминдері, β-каротин (А провитамині), РР және Д витаминінің ізашарлары (эргостерин) өндіріледі.
Сонымен қатар, С дәрумені (аскорбин қышқылы) синтезінде микроорганизмдер d-сорбитті L-сорбозаға селективті тотықтырғыштары ретінде қолданылады.

В2 витаминін (рибофлавин) алу.
Бастапқыда бұл витаминді табиғи шикізаттан бөліп алды (максималды концентрацияда ол сәбіз мен бауырда болады) . Содан кейін өнеркәсіптік синтездің химиялық және микробиологиялық әдістері жасалды. Рибофлавин коэнзим формаларында жұмыс істеуімен сипатталады:
- флавиномононуклеотид (ФМН)
- (ФАД) .
Рибофлавин көздеріне мыналар жатады:
-жоғары өсімдіктер
-ашытқылар
- мицелиалды саңырауқұлақтар.
Олардың барлығы рибофлавинді синтездей алады.
Рибофлавиннің белсенді продуценті - Eremothecium ashbyii және Ashbya gossipii ашытқы тәрізді саңырауқұлақ культурасы. Рибофлавиннің жоғары синтезін жабайы штаммдарға В2 витамині синтезінің ретроингибирлеу механизмін бұзатын мутагендер, флавин нуклеотидтері, сондай-ақ культуралық ортаның құрамын өзгерту арқылы алуға болады. Рибофлавин продуценттерінің өсуіне арналған орта құрамына мыналар кіреді:
- соя ұны
- жүгері сығындысы
сахароза
кальций карбонаты
натрий хлориді
Витаминдер
техникалық май.

Ферментерге берер алдында ортаның инфицирленуін болдырмау үшін антибиотиктер мен антисептиктердің көмегімен стерильдейді. Ферментация процесі аяқталғаннан кейін культуралық сұйықтықты концентрлейді, кептіреді және толтырғыштармен араластырады.
1983 жылы генетика институтында Bacillus subtilis продуцентінің рекомбинантты штаммы жасалды, ол Eremothecium ashbyii-ге қарағанда үш есе көп синтездеуге қабілетті және бұл продуцент экзогендік кантаминацияға төзімдірек.
Витаминдер ағзаға тамақпен бірге беріледі немесе белгілі бір патологиялық процестерге арналған дәрі-дәрмектер түрінде тағайындалады.

Аскорбин қышқылын (С витамині) биотехнологиялық өндіру
Қазіргі уақытта L-аскорбин қышқылын (С витамині) кең көлемде өндіру үшін негізінен бір микробиологиялық кезең мен бірнеше химиялық процесті қамтитын көп еңбекті қажет ететін процесс қолданылады. Ол үшін бастапқы субстрат D-глюкоза болып табылады (16 сурет) .
Бұл процестің соңғы кезеңінде 2-кето-L-гулон қышқылы (2-KLG) қышқыл жағдайда L-аскорбин қышқылына айналады.
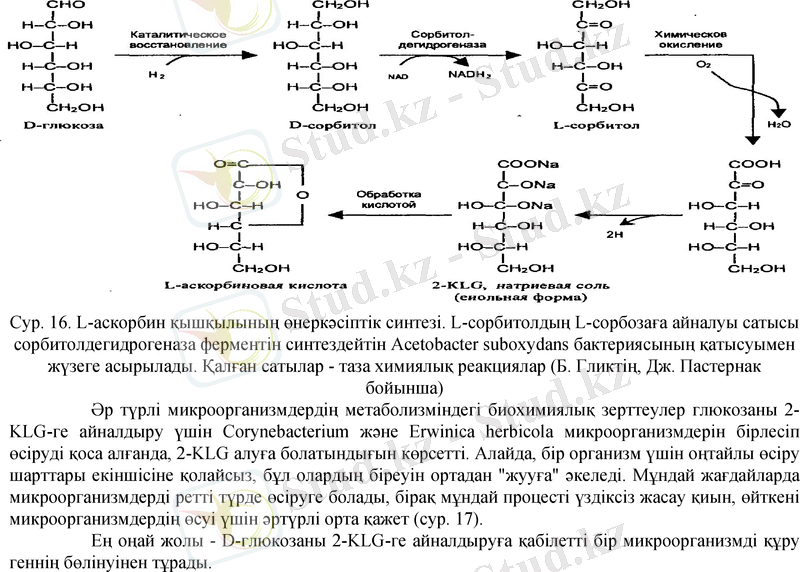
Сур. 16. L-аскорбин қышқылының өнеркәсіптік синтезі. L-сорбитолдың L-сорбозаға айналуы cатысы сорбитолдегидрогеназа ферментін синтездейтін Acetobacter suboxydans бактериясының қатысуымен жүзеге асырылады. Қалған сатылар - таза химиялық реакциялар (Б. Гликтің, Дж. Пастернак бойынша)
Әр түрлі микроорганизмдердің метаболизміндегі биохимиялық зерттеулер глюкозаны 2-KLG-ге айналдыру үшін Corynebacterium және Erwinica herbicola микроорганизмдерін бірлесіп өсіруді қоса алғанда, 2-KLG алуға болатындығын көрсетті. Алайда, бір организм үшін оңтайлы өсіру шарттары екіншісіне қолайсыз, бұл олардың біреуін ортадан "жууға" әкеледі. Мұндай жағдайларда микроорганизмдерді ретті түрде өсіруге болады, бірақ мұндай процесті үздіксіз жасау қиын, өйткені микроорганизмдердің өсуі үшін әртүрлі орта қажет (сур. 17) .
Ең оңай жолы - D-глюкозаны 2-KLG-ге айналдыруға қабілетті бір микроорганизмді құру геннің бөлінуінен тұрады.
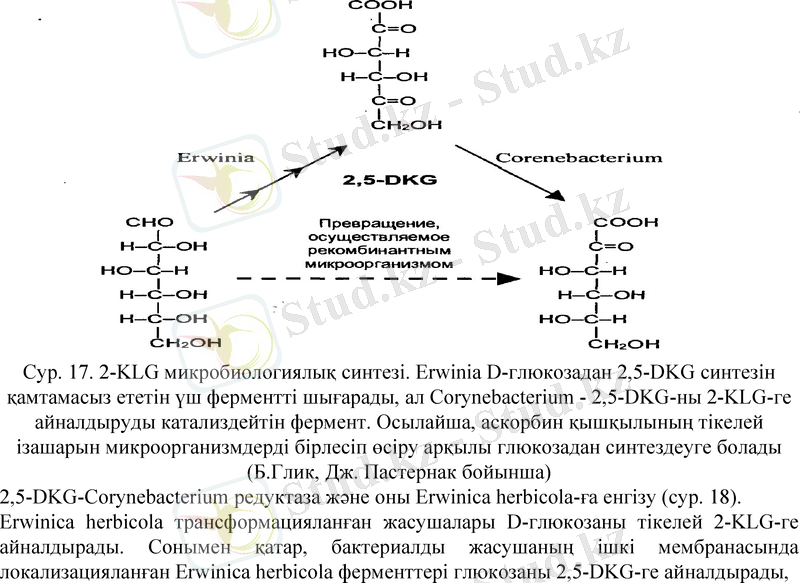
Сур. 17. 2-KLG микробиологиялық синтезі. Erwinia D-глюкозадан 2, 5-DKG синтезін қамтамасыз ететін үш ферментті шығарады, ал Corynebacterium - 2, 5-DKG-ны 2-KLG-ге айналдыруды катализдейтін фермент. Осылайша, аскорбин қышқылының тікелей ізашарын микроорганизмдерді бірлесіп өсіру арқылы глюкозадан синтездеуге болады (Б. Глик, Дж. Пастернак бойынша)
2, 5-DKG-Corynebacterium редуктаза және оны Erwinica herbicola-ға енгізу (сур. 18) .
Erwinica herbicola трансформацияланған жасушалары D-глюкозаны тікелей 2-KLG-ге айналдырады. Сонымен қатар, бактериалды жасушаның ішкі мембранасында локализацияланған Erwinica herbicola ферменттері глюкозаны 2, 5-DKG-ге айналдырады,
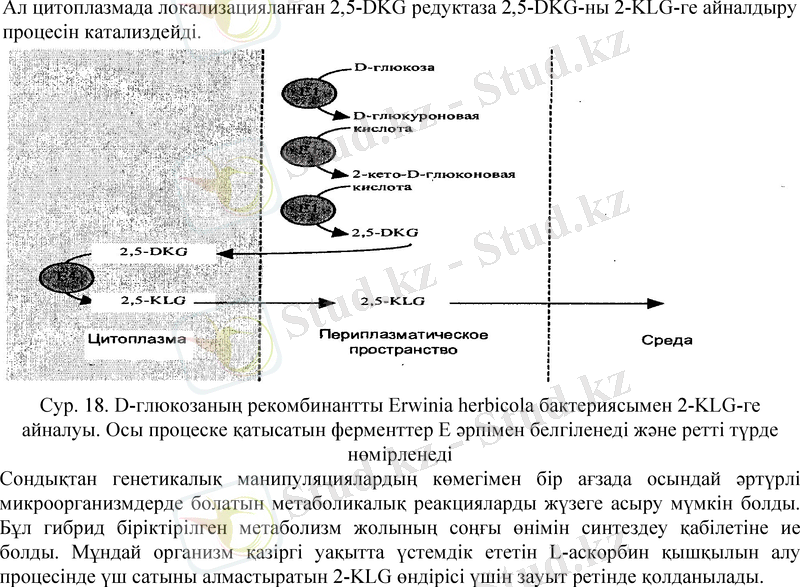
Ал цитоплазмада локализацияланған 2, 5-DKG редуктаза 2, 5-DKG-ны 2-KLG-ге айналдыру процесін катализдейді.
Сур. 18. D-глюкозаның рекомбинантты Erwinia herbicola бактериясымен 2-KLG-ге айналуы. Осы процеске қатысатын ферменттер Е әрпімен белгіленеді және ретті түрде нөмірленеді
Сондықтан генетикалық манипуляциялардың көмегімен бір ағзада осындай әртүрлі микроорганизмдерде болатын метаболикалық реакцияларды жүзеге асыру мүмкін болды. Бұл гибрид біріктірілген метаболизм жолының соңғы өнімін синтездеу қабілетіне ие болды. Мұндай организм қазіргі уақытта үстемдік ететін L-аскорбин қышқылын алу процесінде үш сатыны алмастыратын 2-KLG өндірісі үшін зауыт ретінде қолданылады.

В12 витаминін алу
Бұл витамин АҚШ пен Англияда бір уақытта ашылды. 1972 жылы Гарвард университетінде В12 витаминінің химиялық синтезі жүзеге асырылды, оның оны алудың 37 кезеңі бар, бұл осы витаминнің өнеркәсіптік өндірісін ұйымдастыру мүмкіндігінен айырды. Екінші жағынан, бұл өндіріс қажет болды, өйткені В12 витамині адам мен жануарлар ағзасындағы белгілі бір бұзылуларды түзетуде өте маңызды. Ол көмірсулар мен липидтер алмасуын реттейді, маңызды аминқышқылдарының, пурин мен пиримидин негіздерінің метаболизміне қатысады, гемоглобиннің түзілуін ынталандырады, қатерлі анемияны, радиациялық ауруды, бауыр ауруларын және басқа жағдайларда емдеу үшін қолданылады.
Алдымен В12 витамині тек табиғи шикізаттан алынды (бауырдың 1 тоннасы - витаминнің 15 миллиграммы) .
Қазіргі уақытта оны алудың жалғыз жолы - өнеркәсіптік масштабтағы микробиологиялық синтез. Бір қызығы, В12 витамині антибиотиктерді өндіруде жанама өнім ретінде осы витамин продуценттерін іздеуге түрткі болды.
В12 витамині продуценттері - пропион бактериялары, олар табиғи жағдайда да осы витаминді түзеді. Адам ағзасындағы витаминнің маңызды функциясын ескере отырып (бұл антианемиялық фактор), оның әлемдік өндірісі жылына 10 тоннаға жетті, оның 6, 5 тоннасы медициналық қажеттіліктерге, ал 3, 5 тоннасы мал шаруашылығына жұмсалады.

Цианкобаламиннің отандық өндірісі оттегісіз мерзімді режимде өсірілетін P. freudenreichii var. shermanii культурасын қолдануға негізделген.
Ферментациялық ортада әдетте глюкоза, жүгері сығындысы, аммоний және кобальт тұздары бар, рН шамамен 7, 0, ол NH4OH (аммоний гидроксиді) қосу арқылы сақталады; ферментация ұзақтығы - 6 күн; үш күннен кейін В12 витаминінің ізашары болып табылатын 5, 6-диметилбензимидазол ортаға қосылып, тағы үш күн ферментацияны жалғастырады.
Цианкобаламин бактериялардың жасушаларында жиналады, сондықтан витаминді шығару операциялары келесідей: жасушаларды сепарирлеу, рН 4, 5-5, 0 және 85-90 ° C температурада стабилизатордың қатысуымен сумен экстрагирлеу (натрий нитритінің 0, 25% ерітіндісі) . Экстракция бір сағат ішінде жүреді, содан кейін су ерітіндісі салқындатылады, ащы натр ерітіндісімен бейтараптандырылады, ақуыз коагулянттары (темір (III) хлориді және алюминий сульфаты) қосылады, содан кейін фильтрацияланады. Фильтрат буланып, ион алмасу және хроматография әдістерін қолдана отырып қосымша тазартылады, содан кейін витамин 3-4°C температурада су-ацетон ерітіндісінен кристалданады. Витаминді бөліп алу бойынша барлық операциялар В12 витаминінің жоғары сезімталдығына байланысты қараңғыланған жағдайларда (немесе қызыл жарықта) жүргізілуі керек.

В3 витамині (пантотен қышқылы)
Алу әдісі - бактериялардың иммобилизденген жасушаларын, актиномицеттерді (негізгі әдіс) қолдана отырып, органикалық синтезбен және микробиологиялық синтезбен алу.
РР витамині
РР витаминін алу үшін биотехнологиялық әдіс қолданылады, микроорганизмдерден экстракция әдісі, әдетте ізашарлар қосылған наубайханалық ашытқылардан алады. Brevibacterium ammoniagenes штамы қолданылады.

D витаминін алу
D витамині - эукариоттардың жасушалық мембраналарында табылған эргостеринге негізделген байланысты туыстас қосылыстар тобы.
Денедегі D витаминінің ізашары болып табылатын 1, 25- гормонының жетіспеушілігінен балаларда рахит, ал ересектерде остеомаляция дамиды.
Эргостериннің D2 витаминіне (кальциферол) айналуы ультракүлгін сәуленің әсерінен болады. Бұл жағдайда сақинадағы байланыс үзіледі (9, 10 позиция) және бүйір тізбекте қос байланыс пайда болады (22, 23 позициялар) . Бұл D3 витаминінде гидрирленген. Бұл витаминдердің физиологиялық белсенділігі тең.
Ашытқыдан басқа, эргостерин продуценттері мицелиалды саңырауқұлақтар - аспергилдер мен пенициллдер болуы мүмкін, олардың құрамында 1, 2-2, 2% эргостерин бар, әсіресе Saccharomyces cerevisiae.

Өндірістік жағдайда эргостерин алуды келесі кезеңдерге бөлуге болады: бастапқы культураның көбеюі және инокуляттың жиналуы, ферментация, жасушалардың бөлінуі, ультракүлгін сәулелермен сәулелену, мақсатты өнімді кептіру және орау.
Сонымен, ашытқыларға қатысты инокулят жасушалардың толық дамуын қамтамасыз ететін ортада алынады, содан кейін көміртегі көзімен байытылған және құрамында азоттың мөлшері аз ацетаты бар негізгі орта салыстырмалы түрде көп мөлшерде егіледі. Ашытқыны ферментациялау белгілі бір штамм үшін максималды температурада және айқын аэрация кезінде жүзеге асырылады (газ фазасында 2% О2) . Үш-төрт күннен кейін жасушалар бөлініп, вакуумды кептіріледі.
Содан кейін құрғақ ашытқы ультракүлгін сәулелермен сәулеленеді (толқын ұзындығы 280-300 нм) . Сәулелендірілген құрғақ ашытқы мал шаруашылығында қолданылады; өнеркәсіпте олар "D2 витаминімен байытылған жемшөп гидролизі ашытқысы« деген атпен шығарылады.
D2 кристалды витамині алынған жағдайда продуценттің жасушалары тұз қышқылымен 110 ° C температурада гидролизденеді, содан кейін температура 75-78 ° C дейін төмендейді және этанол қосылады. Қоспа 10-15°C температурада сүзіледі, сүзгіленгеннен кейін қалған масса сумен жуылады, кептіріледі, ұсақталады, 78°C дейін қыздырылады және үш есе этанол көлемімен екі рет өңделеді. Алкоголь экстракттары құрғақ заттардың 70 %-на дейін біріктіріліп, буланады. Алынған "липидті концентрат" ащы натр ерітіндісімен өңделеді. Эргостерин 0°С кезінде концентраттың сабынданбаған фракциясынан кристалданады. Оны қайта кристалдану арқылы тазартуға болады. Кристалдар кептіріліп, этил эфирінде ерітіледі, ультракүлгін сәулеленеді, эфир шығарылады, D2 витамині ерітіндісі концентрленеді және кристалданады.

β-каротин.
Каротиноидтар (политерпендер) - табиғи пигмент. Изопрен бірліктерінен биосинтездің жалпы жолы. Көзі - жоғары өсімдіктер, балдырлар, микроорганизмдер.
Алу - бұл жұқа органикалық синтез (химиялық әдіс) және биотехнология (мицелиалды саңырауқұлақтарды қолдану)
- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz