2 (ІІА) топ элементтері: қасиеттері, реакциялары және қолданылуы



2(IIА) топ элементтері

Сабақтың мақсаты:
2 (ІІ А) топ элементтерінің физикалық, химиялық қасиеттерінің өзгеру заңдылықтарын, олардың маңызды қосылыстарының қолданылуын үйрену;
Кальций мен магний қосылыстарының биологиялық ролін және олардың маңызды қосылыстарының негізгі қасиеттерін сипаттап, судың кермектігін анықтау әдістерімен танысып оны жою жолдарының реакция теңдеулерін жазу.

Бағалау критерилері
2 (ІІ А) топ элементтерінің физикалық қасиеттерінің өзгеру заңдылықтарын түсіндіреді;
Судың кермектігі теңдеулерін құрастырады және оны жою тәсілдерін атайды;
Сілтілік-жер металдардың маңызды қосылыстарының қолданылу аясын ашады;
Кальций мен магний қосылыстарының биологиялық ролін түсіндіреді;
Кальций, магний және олардың маңызды қосылыстарының негізгі қасиеттерін сипаттайтын реакциялар теңдеулерін құрастырады.
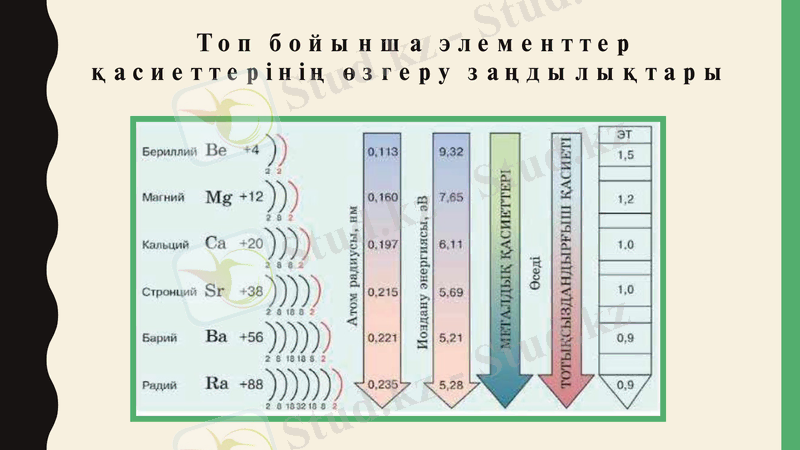
Топ бойынша элементтер қасиеттерінің өзгеру заңдылықтары

Оксидтер мен гидроксидтерінің сипаттамалары
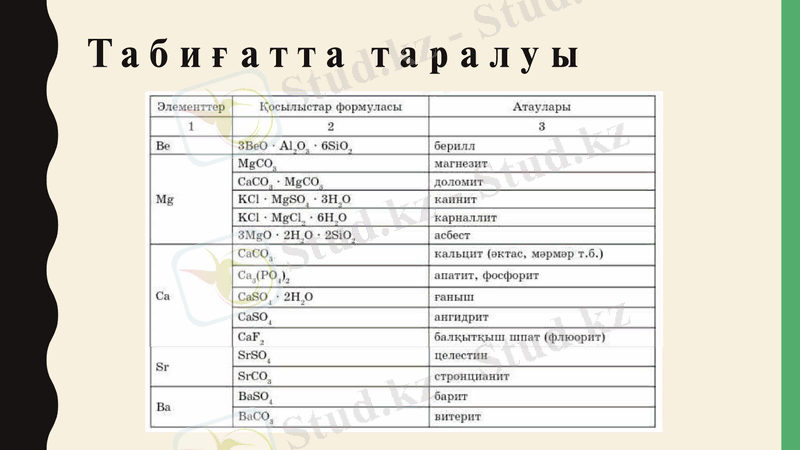
Табиғатта таралуы

Физикалық қасиеттері
Барлық сілтілік жер металдары сұр, бөлме температурасында қатты зат болып табылады. Сілтілік металдармен салыстырғанда сілтілік жер металдары қаттырақ және пышақпен кесіле қоймайды (стронцийдан басқасы) . Сілтілік жер металдарының тығыздығының өсуі тек кальцийдан басталады. Ең ауыры - радий.

Алынуы
CaCl2 →Ca+Cl2
ЭО +2Al =Al2O3 +3Э (Э − Ca, Sr, Ba)
BeF2 + Mg = MgF2 + Be
MgO + C = CO + Mg

ХИМИЯЛЫҚ ҚАСИЕТТЕРІ
Бейметалдармен әрекеттесуі
Оттегімен
2Mе+O2=2MO (оксид)
Галогенмен
Mе+Cl2=MCl2 (хлорид)
Күкіртпен
Mе+S=MS (сульфид)
Азотпен
3Mе+N2=M3N2 (нитрид)
Сутегімен
Mе+H2=MH2 (гидрид)
фосформен
Mе+2Р = M3P2(фасфид)

2. Сумен әрекеттесуі
Mе+2H2O=Mе(OH) 2+H2
3. Қышқылдармен әрекеттесуі

4. Сілтілермен әрекеттесуі
5. Оксидтермен әрекеттесуі
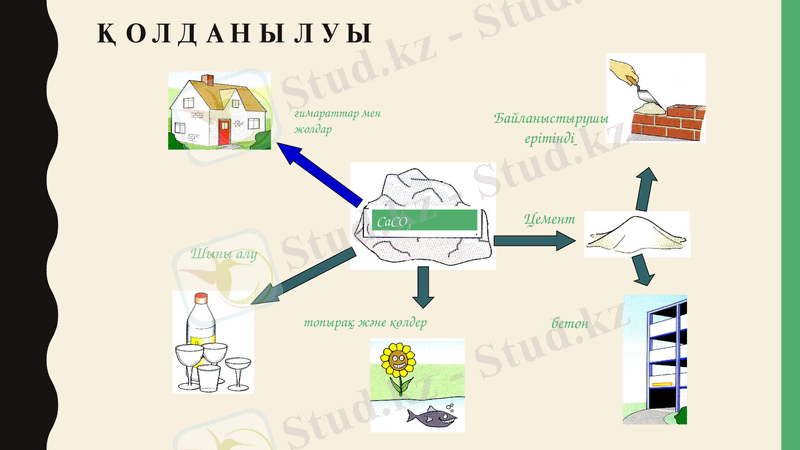
Қолданылуы

Кальциттің мөлдір кристалды (исланд шпаты) түрлері оптикада, құлпырма «ақтана» түрлері зергерлік-көркемдік істерде, мрамор мүсін ісінде, электротехникада т. Б., Бор жазуға, бояуға, құрылысқа, ізбестастар түрлі құрылыс ісінде, металлургияда, химиялық өндірістерде қолданылады. Кендері. Кальцит кеңес одағында орта азияда (заревшан-гиссар аудандарында), уралда, белгород ауданында, қырымда, кавказда т. Б. Кездеседі. Шет елдерде ол исландияда, италияда (каррара кені), грекияда т. Б. Бар.
Мәрмәр, әктас, бор - СаСО3
Мәрмәр
Әктас
Бор
Аналық кальцит
Исландиялық шпат

Үй тапсырмасы
2(IIА) топ элементтері тақырыбы бойынша конспекті жасау.
Чек парағына жауап беру.
Суретке түсіріп edupage-жіберу.
- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz