Биологиялық жүйелердегі осмостық қысымның рөлі



ПРЕЗЕНТАЦИЯ
Тақырыбы: Биологиялық жүйедегі осмос қысымының рөлі.
Орындаған: Пухарбаев. Е
Тобы: ФӨТҚА-02-20
Қабылдаған: Серимбетова. Қ
Шымкент 2021ж.
ҚАЗАҚСТАН РЕСПУБЛИКАСЫНЫҢ ДЕНСАУЛЫҚ САҚТАУ МИНИСТРЛІГІ
ОҢТҮСТІК ҚАЗАҚСТАН МЕМЛЕКЕТТІК
ФАРМАЦЕВТИКА АКАДЕМИЯСЫ
Фармакогнозия және химия кафедрасы

Жоспар
Кіріспе
Негізгі бөлім
Ерітінділердің коллигативтік қасиеттері
Вант-Гофф теңдеуі
Рауль заңы
Осмостың биологиялық маңызы
Гипо-, изо-, және гипертонды ерітінділер
Плазмолиз, гемолиз, тургор
Қорытынды
Қолданылған әдебиеттер

Жартылай өткізгіш мембрана арқылы төмен концентрациялы ерітіндіден жоғары ерітіндіге еріткіш молекулаларының біржақты өздігінен жүретін диффузиясы осмос деп аталады. Осмос процесі өте күрделі және оның табиғаты осы күнге дейін жеткілікті зерттелмеген, осмос құбылысын арнаулы аспаптарда осмометрлерде бақылауға болады. Осмосты тоқтату үшін ерітіндіге таңуға қажетті гидростатикалық қысымды осмос қысымы деп атайды.

Коллоидты ерітінділерге нағыз ерітіндідегідей осмостық қысым тән. Ол да газ қысымы секілді ерітіндінің коллигативті (біріккен, орташа) қасиеті екен, яғни ол тек еркін қозғалатын коллоидты бөлшектерге ғана тәуелді. Егер коллоидты бөлшектердің көлемі мен массасының нағыз ерітінділердегі молекула көлемі мен масса-сынан үлкен екенін ескерсе, онда бірдей көлемдік концентрацияда-ғы коллоидты және нағыз ерітінділерді алып, белгілі бір көлемін-дегі коллоидты бөлшекті және молекуланы салыстырғанда, колло-идты бөлшектер аз болады.

Осмос қысымын П немесе p деп белгілейді. Осмос қысымы еріген зат табиғатына тәуелсіз, ал ерітіндінің концентрациясына және температураға тура пропорционал екендігін Голландия ғалымы Вант-Гофф 1887 жылы (газдарға қолданылған Бойль-Мариот пен Гей-Люссак заңдарына ұқсас екендігін анықтады) мына формуламен есептеуге болатынын тапты: p = cRT, мұндағы с - ерітіндінің молярлы концентрациясы, моль/л; R - константа, сандық мәні газдар тұрақтысына тең, 0, 082л-атом/град, Т - абсолют температура.
Вант-Гофф, Якоб Хендрик

Ерітіндінің осмос қысымы(өлшемі - атм. ), сол еріген зат газ күйінде болып, осы температурада, ерітіндінің көлеміндей көлем алып тұрғандағы туғызытын қысымына тең (Вант-Гофф заңы) . с = n/V болғандықтан Вант-Гофф теңдеуі идеал газ күйі теңдеуіне ұқсас, оны мына күйге келтіруге болады: π = n/VRT немесе π×V = nRT бұл теңдеу газ күйінің теңдеуіне (PV = nRT) ұқсас. Концентрациясы с(Х) = 1моль/л болатын барлық бейэлектролиттер ерітінділерінің осмос қысымы бірдей, яғни 0°С температурада 22, 69×105Па.


Коллоидты ерітінділер нағыз ерітінділерге өте ұқсас болғандықтан, оған Вант-Гофф формуласын қолдануға болады:
мұндағы П - зольдің осмостық қысымы; n- колоидты бөлшектердің мольдік өлшемі; V- зольдің көлемі. Коллоидты бөлшектің мольдік өлшемі деп Авогадро саны қабылданады.
ПV = nRT немесе П = nRT/V

Егер берілген зольде ν коллоидты бөлшек болса, онда 1 мольде NA бөлшек бар. n=ν/ NA ескерсек, (39) теңдеу:
болады.
ПV = (ν / NA) RT, П = ν / V· RT/ NA

1887 жылы француз физигі Рауль көптеген ерітінділермен жұмыс істеп, мына заңдарды ашқан:
1. Еріткіш бу қысымының салыстырмалы төмендеуі еріген заттың моль сандарының ерітіндідегі жалпы моль сандарын (еріген зат пен еріткіштің) қатынасына тең.
2. Ерітіндінің қату температурасының төмендеуі не қайнау температурасының жоғарлауы, еріткіштің сол салмақ мөлшерінде еріген заттың мөлшеріне (ерітіндінің моляльдығына) пропорционал.
3. Түрлі заттардың эквимолекулалық мөлшерлері бір еріткіштің бірдей етіп алынған мөлшерінде ерітілген болса, ол ерітінділердің қату температурасы (қайнау температурасы) бірдей градус санына төмендейді (жоғарылайды) .
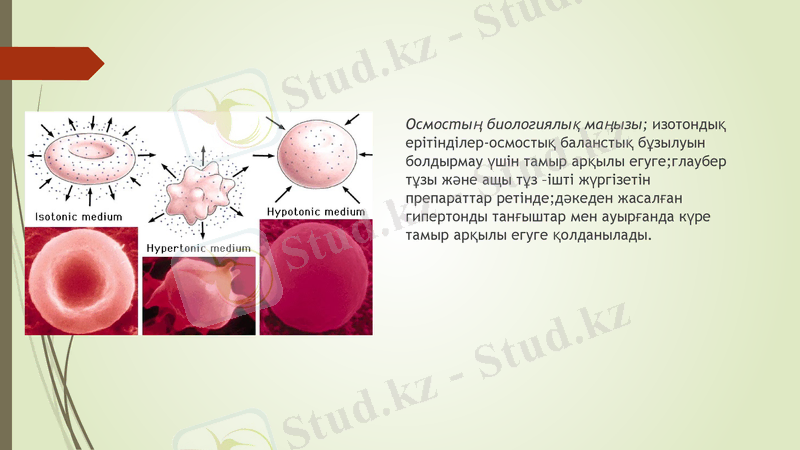
Осмостың биологиялық маңызы; изотондық ерітінділер-осмостық баланстық бұзылуын болдырмау үшін тамыр арқылы егуге; глаубер тұзы және ащы тұз -ішті жүргізетін препараттар ретінде; дәкеден жасалған гипертонды танғыштар мен ауырғанда күре тамыр арқылы егуге қолданылады.
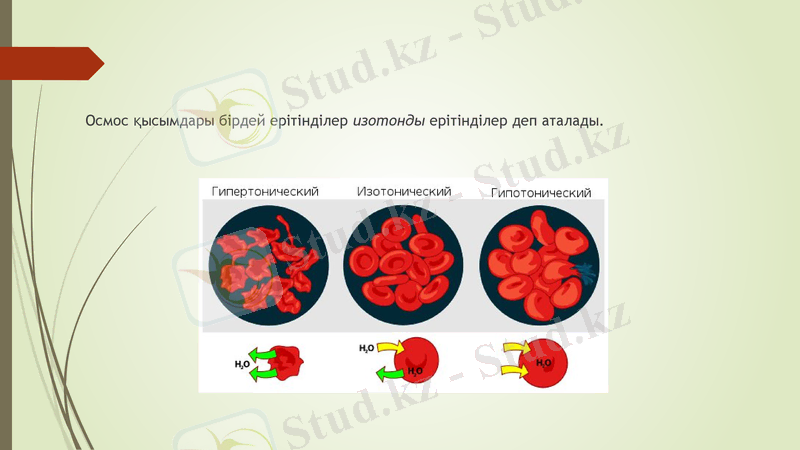
Осмос қысымдары бірдей ерітінділер изотонды ерітінділер деп аталады.

Басқа ерітіндіге қарағанда осмос қысымы жоғары болса гипертонды
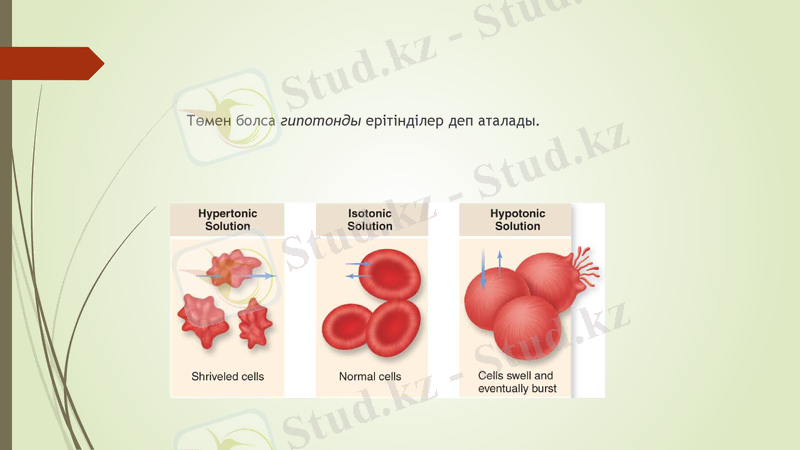
Төмен болса гипотонды ерітінділер деп аталады.

Осмос қысымын П немесе p деп белгілейді. Осмос қысымы еріген зат табиғатына тәуелсіз, ал ерітіндінің концентрациясына және температураға тура пропорционал екендігін Голландия ғалымы Вант-Гофф 1887 жылы (газдарға қолданылған Бойль-Мариот пен Гей-Люссак заңдарына ұқсас екендігін анықтады) мына формуламен есептеуге болатынын тапты: p = cRT, мұндағы с - ерітіндінің молярлы концентрациясы, моль/л; R - константа, сандық мәні газдар тұрақтысына тең, 0, 082л-атом/град, Т - абсолют температура.
- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz