VII A (галогендер) топ элементтерінің химиялық және физикалық қасиеттері



Тақырып:VII A топ элементтері

Жоспар:
Кіріспе
1. Химиялық элеметтер анықтама
II. Негізгі бөлім
VII A топ элементтері
III. Қорытынды

Кіріспе
Химиялық элементтер - ядродағы зарядтары бірдей болып келетін атомдар тобы. Табиғатта кездесетін барлық жай және күрделі заттар химиялық элементтерден түзіледі.

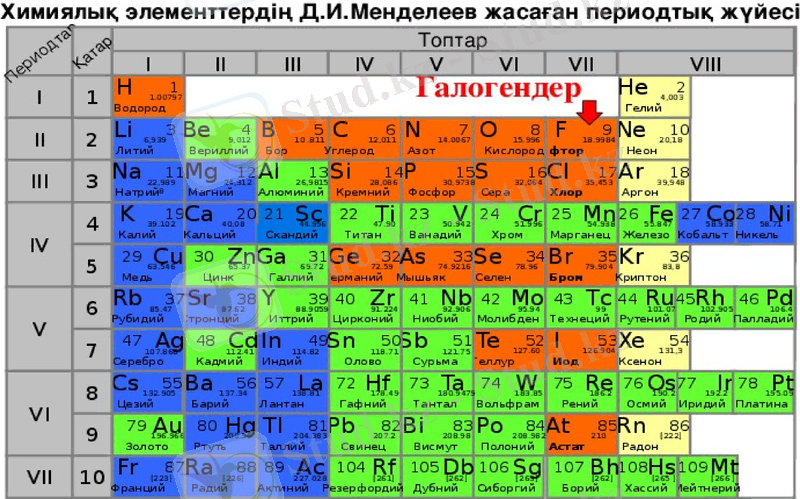
Д. И. МЕНДЕЛЕЕВ 1869 ЖЫЛЫ ПЕРИОДТЫҚ КЕСТЕНІ АШҚАН БОЛАТЫН. КЕСТЕДЕ 7 ПЕРИОДТАН, 8 ТОПТАН, НЕГІЗГІ ЖӘНЕ ҚОСЫМША ТОПШАЛАРДАН, ЛАНТАНОИДТАР МЕН АКТИНОИДТАРДАН ТҰРАДЫ.
Галогендер периодтық жүйеде әрбір периодтың соңына қарай VII A топшада бейметалдық қасиеті айқын білінетін элементтер орналасқан.

VII A топ элеметтері(Галогендер)

Фторды алғаш рет 1886 жылы А. Муассан алған. Грек тілінен алынған «фторос» - бүлдіргіш деген сөзді білдіреді. 1810 ж. А. Ампер, балқытқыш қышқыл, тұз қышқылына ұқсас екенін байқап, хлорға ұқсас элемент бар екенін сеніммен айтқан, ол оны басында флюорий деп атаған. 1816 ж. А. Ампер болжамдағы элементті фтор деп атады. Батыс елдерінің көбі фторды флюор деп атайды
Фтор

Фтор (Fluorum), F - элементтердің периодтық жүйесінің VII тобының негізгі топшасында орналасқан 9 - шы элемент Табиғатта тұрақты бір изотопы және жасанды жолмен алынған 5 радиоактивті изотоптары бар. Оның улылығы сондай - Фторды алумен айналысқан көптеген химик-ғалымдар (Г. Дэви, Т. Нокс, Д. Никлес, П. Луйэ) қаза тауып, ал А. Муассан мен Г. Нокс мүгедек болып қалған. Фтормен жұмыс істеу өте үлкен ұқыптылықты керек етеді, сәл салақтық болса фтор ең кемі адамның тісін күйретіп, тырнақтарына зақым келтіреді.

ФТОР әсер еткенде сілемейлі қабықша қабынады, ал теріні қатты күйдіреді. Сұйық галогендермен күйген жағдайда ұзақ уақыт жазылмайды. Фтор қосылыстарында тек бір валенттілік қана көрсетеді, тотығу дәрежесі үнемі -1, 0 -ге тең, себебі ол электртерістіктілігі ең жоғары элемент; Ғ 0 + е Ғ оның екінші энергетикалық деңгейінде екі ғана деңгейшесі бар, электрондардың дараланып көшетін орны болмағандықтан топ нөміріне сәйкес валенттілік көрсете алмайды.
Фтордың Жер қыртысындағы салмақ мөлшелері 6, 25° 10- 2%, әр түрлі тау жыныстары мен тұзды құмдар құрамында шашыраңқы түрде кездеседі. Қалыпты жағдайда Фтор солғын сары түсті, өткір иісті, улы газ, балқу t - 219, 61°С, қайнау t 188°С. Фтор молекуласы екі атомнан тұрады (F 2) .

Химиялық қасиеттер
Фтор қалыпты температураның өзінде көптеген элементтермен, оның ішінде азот және ауыр инертті газдармен (гелий, неон, аргоннан басқа) әрекеттесіп, фторидтер түзеді. Галогендер металдармен жылу бөле шабытты әрекеттеседі, нәтижесінде тұз түзіледі. 2 Na + F 2 = 2 Na. F (суықта) 2 Fe + 3 Cl 2 = 2 Fe. Cl 3 (қыздырғанда) Электр терістілігі жоғары элементтердің бірі оттек (3, 5) фтормен қосылысында оң тотығу дәрежесін көрсетеді. (оттектің фториді) Фтор сутегімен тіпті қараңғыда да шабытты әрекеттеседі F 2+H 2=2 HF↑ фторлы сутек. Кейбір металдардың бетінде (қалыпты температурада) жұқа берік фторид қабықшасы түзілетін болғандықтан су болмаса үрдіс бірден тоқтап қалады. Fe (Cu, Ni, AI, Zn) + F 2 ≠ Ме. F 2↓ • Хлорда темір ұнтақтары қыздырмай -ақ жана бастайды.

Хлор
Хлорлы тұз қышқылының ерітіндісіне марганец диоксидімен әсер етіп 1774 жылы Карл Шееле алған. Г. Деви оның химиялық элемент екенін тапты. Хлор атауы оның сарғыш - жасыл түсіне қарай 1812 жылы ұсынылды.

Молекуласы екі атомнан (Cl 2) тұрады; өткір иісті сарғылт - жасыл түсті улы газ; тығыздығы 0, 3214 г/см 3. Балқу t - 101°С; Табиғатта екі тұрақты изотоптары (35 CI және 37 CI) бар.
Хлор (лат. Clorum), Cl- элементтердің •периодтық жүйесінің VІІ тобындағы химиялық элемент, атомдық номері 17, атомдық массасы 35, 45; галогендер тобына жатады.

Жер қыртысындағы салмақ мөлшері 4, 5102%. Хлор өте белсенді элемент, бос күйінде жанартау лавасында ғана, ал байланысқан түрінде тау жыныстарында, теңіз, мұхит, өзен суларында, өсімдік және жануарлар организмдерінде кездеседі. Байланыстағы хлор көптеген минералдардың құрам бөлігі. Қалыпты жағдайда хлор сарғыш - жасыл, ерекше өткір иісті газ, тығыздығы 3, 214 г/л, ауадан 2, 5 есе ауыр, қайнау t - 33, 6 С, балқу t - 100, 98 С. Суда жақсы ериді. Тотығу дәрежелері +1, +3, +5, +7.

Бром
Бромды 1826 жылы француз ғалымы А. Ж. Балар теңіз балдырының күлінен алған. «Бром» атауы гректің «бромос» деген сөзінен шыққан, «сасық» деген мағынаны білдіреді және ол бромның тұншықтырғыш, өткір иісімен байланысты.

- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz