Атом құрылысының кванттық-химиялық сипаттамасы: электрон бұлты, квант сандары және ядро моделі



Атом құрылысының кванттық-химиялық сипаттамасы
Орындаған: Бейсенбай Э. С.
Тексерген: Мусина А. С.

Ашылуы:
Ашқан :Нильс Бор
Резерфорд пен Планктың теориясын қолданып, атом моделінің құрылысын жасады.

Атом құрылысы квант - механикалық теориясының ережелері
1. Электронның екі жақты табиғаты ( бөлшектік-корпускулалық және толқындық ) болады. Ол өзін бөлшек ретінде де, толқын ретінде де ұстай алады:бөлшек ретінде, электронның белгілі массасы мен заряды бар; мұнымен қатар қозғалыстағы электрон толқындық та қасиет көрсетеді, мәселен дифракцияға қабілеттілігімен сипатталады.
2. Электрон үшін координат пен жылдамдықты бірден, бір сәтте дәл өлшеу мүмкін емес. Жылдамдықты неғұрлым дәл өлшенген сайын, соғұрлым координатта белгісіздік болады және керісінше.
3. Атомдағы электрон белгілі траектория бойынша қозғалмайды, ядро маңындағы кеңістіктің кез келген бөлігінде бола алады, алайда оның атом кеңістігінің әртүрлі бөлігінде болу ықтималдылығы бірдей емес.

Электрондық бұлт
Электронда теріс заряд болатындықтан, оның орбиталі зарядтың белгілі бір таралуын электрондық бұлт деп атайды.
Электрон бұлты─атомдағы электронның кванттық механика тұрғысынан қарағандағы моделі. Орбиталь электрондық бұлттың формасын сипаттайды. Ядроның маңайындағы электрон бұлтының тығыздығы әртүрлі болады
. Электрон бұлттары бір-бірінен өздерінің энергия мөлшері, пішіндері және кеңістікте орналасу бағыты арқылы ажыратылады. Э. Шредингер теңдеуі арқылы электрон қозғалысының ең маңызды сипаттамаларының бірі-оның толқындық функциясы анықталады

Квант сандары
Бас квант саны (n) -электронның энергиясы мен орбитальдың өлшемін анықтап, энергетикалық деңгейді сипаттайтын шама. n=1, 2, 3, 4, 5. Оның мәні жоғары болса, энергиясыда жоғары болады. Энергетикалық деңгей-бас квант санының бірдей мәні бар орбитальдардың жиынтығы.
Орбитальдық квант саны (l) -энергетикалық деңгеидің деңгейшесінде орналасқан электронның энергиясын сипаттайтын ж\е электрондық бұлт пішінін анықтайтын шама. Энергетикалық деңгейше-бір энергетикалық деңгейде болатын ж\е бірдей формадағы орбитальдардың жиынтығы. l=0 шар тәрізді(s-деңгей), l=1гантель формалы(p-деңгей) .
Магнит квант саны (Ml) -сыртқы магнит өрісінің әсерінен орбитальдардың кеңістікте орналасуын және деңгейдегі орбиталдардың санын анықтайтын шама. -1, 0, +1 бүтін сандар мәнін қабылдайды.
Спин квант саны (Ms) -электронның өз өсінің айналасында айналуын сипаттап, тек қана екі мәнді қабылдай алатын шама. (+1/2және1/2)

Атом ядросының құрылысы
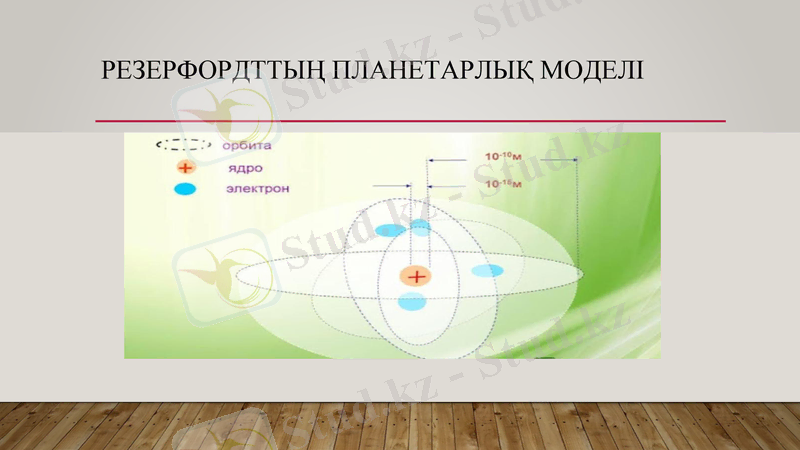
Резерфордттың планетарлық моделі

- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz