Фосфор қышқылы өндірісінің технологиясы: экстракциялық және электротермиялық әдістер



Фосфор қышқылы өндірісі
Қабылдаған: Шахабаев Е. Дайындаған: Минаварова Х.
Тобы: ЖХМ - 812
Түркістан - 2021

Жоспар:
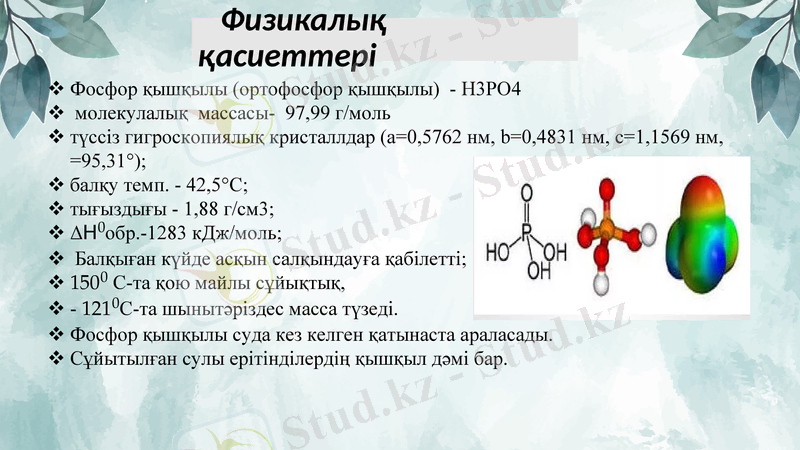
Физикалық қасиеттері

Алынуы

Химиялық қасиеттері
Фосфор қышқылы тотықтырғыш қасиет көрсетпейді, қышқылдарға тән барлық реакцияларға түседі.
1) активті металдармен сутек бөле әрекеттеседі:
2Н3РО4 + ЗСа = Са3(РО4) 2+ ЗН2↑
2) негіздік оксидтермен тұз бен су түзеді:
2Н3РО4 + 3MgO = Mg3(PО4) 2+ ЗН2О
3) негіздермен тұз бен су түзе әрекеттеседі:
Н3РО4 + 3NaOH = Na3PО4 + 3H2О
4) әлсіз қышқылдардың тұздарымен әрекеттеседі;
2H3PО4 + 3Na2S = 2Na3PО4 + 3H2S↑
жаңа тұз және жаңа қышқыл түзеді.
Фосфор қышқылының қалдығына (РО43-) сапалық реакция жасау үшін күміс ионы (Ag+) қолданылады.
Н3РО4+ 3AgNО3 = Ag3PО4↓+ 3HNО3
(РО43-+ 3Ag+→ Ag3PО4↓
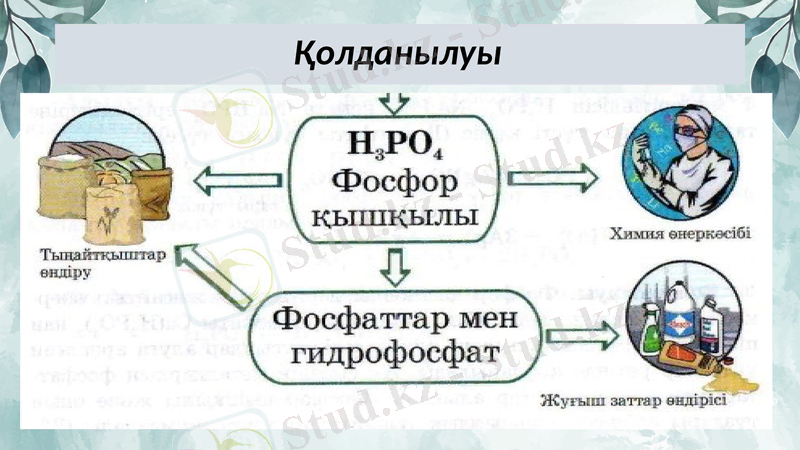
Қолданылуы

Термиялық фосфор қышқылы балқытылған фосфорды немесе фосфорды электроайдау кезінде түзілетін фосфорқұрамды газдарды күйдіру арқылы алынады. Фосфор қышқылы өндірісінің электропеш газдарын тура күйдірудегіден қарағанда екі сатылы әдісі кезінде, яғни электропеш газдарынан конденсациялау кезінде және тазалау фосфор қышқылы шығады. Одан басқа, екісатылы әдістің артықшылығы газдан фосфорды конденсациялаудан кейінгі қалатын жоғары пайызды көміртек тотығын қолдану мүмкіндігі болып табылады
Бірсатылы әдіс кезінде көміртек тотығы фосформен бірге күйдіріледі, ал фосфор қышқылын үлкен көлемде түзіліп жатқан газдан ұстап қалу ауқымдырақ аппарат қажет етеді; электроэнергия, су және шығыны бұл әдісте айтарлықтай көп.
Ауада бу тәрізді немесе сұйық фосфорды күйдіру кезінде фосфор ангидридін құрайтын газ түзіледі, оның фосфор қышқылына айналуы газды сумен шаймалау кезінде іске асады. Газдың жоғары температурасы салдарынан (800-1000°С) фосфор ангидриді гидратациясы кезінде бастапқыда кейінгі суыту және гидратацияда тұман тәрізді ортофосфор қышқылына айналатын бу тәрізді метафосфор қышқылы түзіледі. Фосфордың гидратация кезінде фосфорлау және фосфорлылау қышқылдарына өтетін төмен тотықтарын болдырмау үшін фосфорды күйдіру ауаның екі еселік артығында орындалады
Термиялық фосфор қышқылын алу

Процестің физика-химиялық негіздері
Фосфор қышқылын өндірудің экстракциялық әдісі табиғи фосфаттардың күкірт қышқылымен ыдырау реакциясына негізделген. Процесс екі кезеңнен тұрады: фосфаттардың ыдырауы және түзілген фосфор қышқылын сүзу және кальций сульфатын сумен жуу.
Кальций фосфатының күкірт қышқылының ыдырауы "қатты - сұйық" жүйесінде жүретін және теңдеумен сипатталатын гетерогенді қайтымсыз процесті білдіреді:
Ca5(PO4) 3F + 5H2SO4 + nH3PO4 + 5mH2O = (n + 3) Н3РО4 + 5CaSO4 · mH2O + HF

Қазіргі аналитикалық құралдардың әр түрлі обьектілеріндегі элементтер ізін анықтауда концентірлеу яғни экстракция әдісі қолданылады. Бұл әдіс көптеген белгілі әдістердің ішінен ең көп дамығаны және көптеп таралғаны болып табылады
Экстракция бұл өзара араласпайтын екі фаза арасында заттың үлестірілуіне негізделген физика және химиялық процесс. Бұл тәсіл заттарды бөлу үшін жиі пайдаланылатын ең күрделі және ең көп дамыған, кең тараған әдіс

Экстракцияда екі еріткіш пайдаланылады
Экстракция екі заңға бағынады
Нернсттің таралу заңына Әрекеттесуші массалар заңына

Экстракцияны сипаттау үшін таралу коэффициентін қолданған жөн:
D = CAорг/САсу
Мұндағы, D- таралу коэффициенті;
С- жалпы концентрация.
Экстракция тиімділігі экстракциялау дәрежесі немесе бөліп шығару формуласы сипаттайды:
R= (QAорг /(QAорг+QAсу) ) *100%
QAорг= САорг*Vорг
QAсу= САсу* Vсу
V- фазалар көлемі. .
Егер фазалар көлемі бірдей болса, Vорг =Vсу онда мынандай тәуелділік пайда болады:
R= 100 D/ D+1; D=R/100-R
толық болу үшін R>99%.
Егер, бұған жетпесе, экстракцияны бірнеше сатыда қайталайды.
Бөлу дәрежесі: αA/B= DA/DB
Экстракциялау константасы Кэкс- бұл таралу реакциясының тепе-теңдік константасы.

Экстракция толық жүруі үшін мына шарттарды орындау керек

Экстракцияның қолданылуы
Экстракцияны қоспаларды бөлу үшін пайдаланады. Ол үшін талғамды экстрагенттер пайдаланады. Себебі:
1. Эффективтілігі жоғары. Қосарласа тұндыру кезінде фазалардың бөліну беті үлкен болады, қосарласа тұну жүреді. Экстракция кезінде бөліну беті үлкен емес, алайда, сирек кездеседі, өте аз мөлшерде жүреді.
2. Универсалды қарапайым және жылдам, кез-келген зат үшін экстракция жағдайын табуға болады. Экстракциялау үшін бөлгіш воронка болса жеткілікті, 3-5 минут ішінде жүреді;
3. Экстракцияны сандық анализ үшін пайдалануға болады;
4. Таралу коэффициентін рН-қа, концентрацияға тәуелді өлшеу арқылы түзілетін компонент құрамын және тұрақтылық константасын есептеуге болады.

Экстракциялау механизмінің түрлері
I. Физикалық улестірудің механизмі.
II. Сольваттық механизм
III. Гидрат-сольваттық механизм
IV. Иондық ассоциаттарды экстракциялау

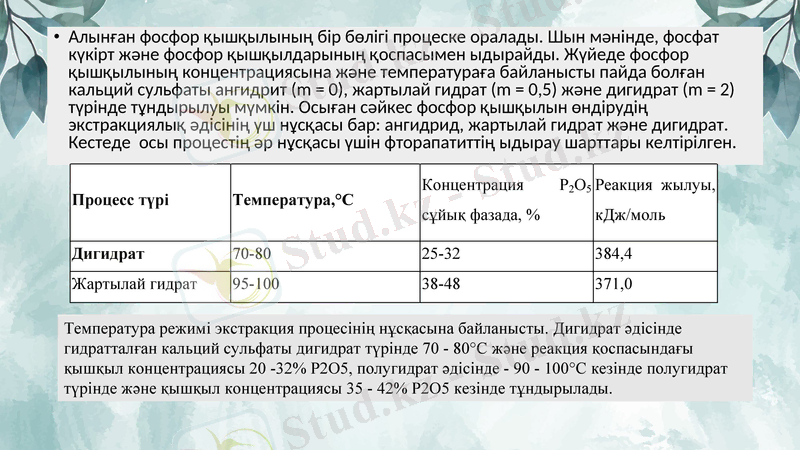
Алынған фосфор қышқылының бір бөлігі процеске оралады. Шын мәнінде, фосфат күкірт және фосфор қышқылдарының қоспасымен ыдырайды. Жүйеде фосфор қышқылының концентрациясына және температураға байланысты пайда болған кальций сульфаты ангидрит (m = 0), жартылай гидрат (m = 0, 5) және дигидрат (m = 2) түрінде тұндырылуы мүмкін. Осыған сәйкес фосфор қышқылын өндірудің экстракциялық әдісінің үш нұсқасы бар: ангидрид, жартылай гидрат және дигидрат. Кестеде осы процестің әр нұсқасы үшін фторапатиттің ыдырау шарттары келтірілген.
Процесс түрі
Температура, °С
Концентрация Р2О5 сұйық фазада, %
Реакция жылуы, кДж/моль
Дигидрат
70-80
25-32
384, 4
Жартылай гидрат
95-100
38-48
371, 0
Температура режимі экстракция процесінің нұсқасына байланысты. Дигидрат әдісінде гидратталған кальций сульфаты дигидрат түрінде 70 - 80°С және реакция қоспасындағы қышқыл концентрациясы 20 -32% Р2О5, полугидрат әдісінде - 90 - 100°С кезінде полугидрат түрінде және қышқыл концентрациясы 35 - 42% Р2О5 кезінде тұндырылады.

Технологиялық схемаға сипаттама
Балқыған фосфордан термиялық фосфор қышқылын алудың технологиялық нобайы бейнеленген. Шығыс резервардан ыстық су қысымы астында фосфор құбырөткізгіш арқылы 6-7 форсункаға (1) мұнара-күйдіру камерасын жауып тұратын горизонтальді торда құрылған қышқылға төзімді хром-никельді шойыннан немесе хромды қазандықтан беріледі. Мұнара корпусы шойыннан жасалған, ішкі жағы гуммирленген және резеңке қабаты бойынша қышқылға төзімді кірпіштермен қаланған. Биіктігі 10м, үстіңгідиаметрі 2, 75м, астыңғы диаметрі 2, 35м мұнарада тәулігіне 12 т фосфор өңдеуге болады, бұнда 37, 5 т/тәулік 100% фосфор қышқылына сәйкес келеді. Фосфор қысылған ауаболып түсетін форсункаға шашыратылады және төменге қаратылған факел түзіп күйдіріледі. Күйдіруге қажет қосымша ауа форсунка бекітілген тор арқылы келеді. Мұнараның үстіңгі аумағында ‘воротник’ - салқын фосфор қышқылы және күйдірілетін фосфордан фосфор қышқылы түзілуі үшін керек су түсетін (30-40°С) [3] сақиналы науа бар. Су, сонымен бірге, мұнараның ортаңғы бөліктерінде орналасқан бірнеше тесік арқылы беріледі; кірпішке су ағыны пәрменімен шашырайды және газбен араласады. Су мөлшері мұнарадан ағатын қышқыл концентрациясы 88% Н3РО4 болатындай ретке келтіріледі
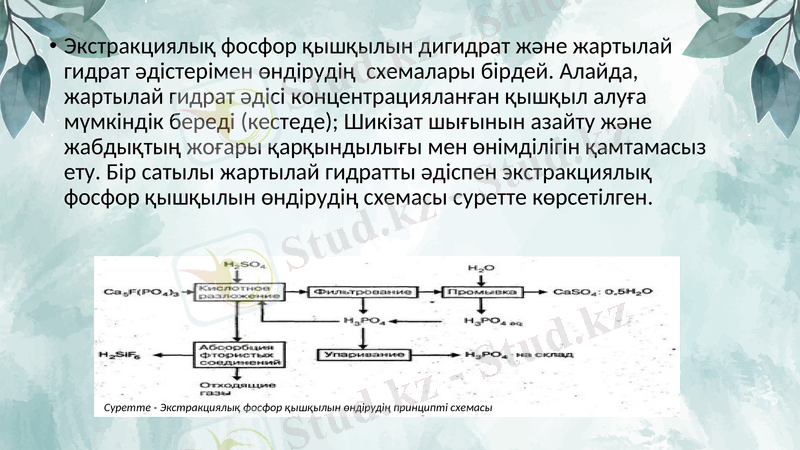
Экстракциялық фосфор қышқылын дигидрат және жартылай гидрат әдістерімен өндірудің схемалары бірдей. Алайда, жартылай гидрат әдісі концентрацияланған қышқыл алуға мүмкіндік береді (кестеде) ; Шикізат шығынын азайту және жабдықтың жоғары қарқындылығы мен өнімділігін қамтамасыз ету. Бір сатылы жартылай гидратты әдіспен экстракциялық фосфор қышқылын өндірудің схемасы суретте көрсетілген.
Суретте - Экстракциялық фосфор қышқылын өндірудің принципті схемасы
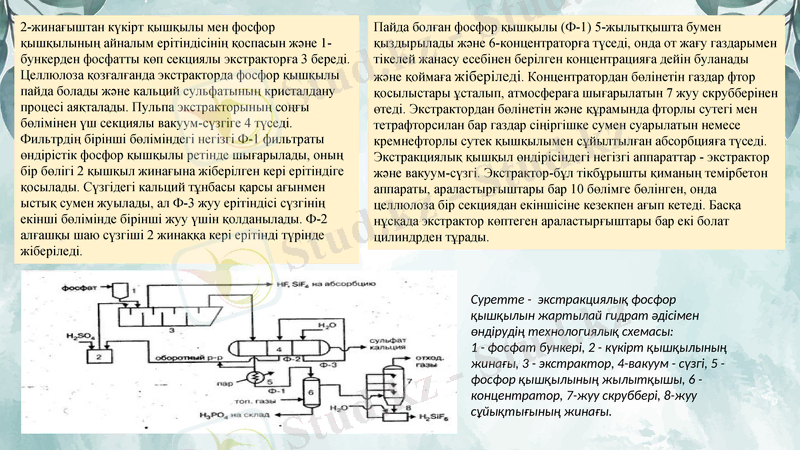
2-жинағыштан күкірт қышқылы мен фосфор қышқылының айналым ерітіндісінің қоспасын және 1-бункерден фосфатты көп секциялы экстракторға 3 береді. Целлюлоза қозғалғанда экстракторда фосфор қышқылы пайда болады және кальций сульфатының кристалдану процесі аяқталады. Пульпа экстракторының соңғы бөлімінен үш секциялы вакуум-сүзгіге 4 түседі. Фильтрдің бірінші бөліміндегі негізгі Ф-1 фильтраты өндірістік фосфор қышқылы ретінде шығарылады, оның бір бөлігі 2 қышқыл жинағына жіберілген кері ерітіндіге қосылады. Сүзгідегі кальций тұнбасы қарсы ағынмен ыстық сумен жуылады, ал Ф-3 жуу ерітіндісі сүзгінің екінші бөлімінде бірінші жуу үшін қолданылады. Ф-2 алғашқы шаю сүзгіші 2 жинаққа кері ерітінді түрінде жіберіледі.
Суретте - экстракциялық фосфор қышқылын жартылай гидрат әдісімен өндірудің технологиялық схемасы:
1 - фосфат бункері, 2 - күкірт қышқылының жинағы, 3 - экстрактор, 4-вакуум - сүзгі, 5 - фосфор қышқылының жылытқышы, 6 - концентратор, 7-жуу скруббері, 8-жуу сұйықтығының жинағы.
Пайда болған фосфор қышқылы (Ф-1) 5-жылытқышта бумен қыздырылады және 6-концентраторға түседі, онда от жағу газдарымен тікелей жанасу есебінен берілген концентрацияға дейін буланады және қоймаға жіберіледі. Концентратордан бөлінетін газдар фтор қосылыстары ұсталып, атмосфераға шығарылатын 7 жуу скрубберінен өтеді. Экстрактордан бөлінетін және құрамында фторлы сутегі мен тетрафторсилан бар газдар сіңіргішке сумен суарылатын немесе кремнефторлы сутек қышқылымен сұйылтылған абсорбцияға түседі. Экстракциялық қышқыл өндірісіндегі негізгі аппараттар - экстрактор және вакуум-сүзгі. Экстрактор-бұл тікбұрышты қиманың темірбетон аппараты, араластырғыштары бар 10 бөлімге бөлінген, онда целлюлоза бір секциядан екіншісіне кезекпен ағып кетеді. Басқа нұсқада экстрактор көптеген араластырғыштары бар екі болат цилиндрден тұрады.

Фосфор қышқылын жартылай гидраттық әдіспен өндіру бойынша жұмыс істеп тұрған қондырғылардың өнімділігі жылына 350 мың тоннаға дейін жетеді және төмендегідей параметрлерімен сипатталады:
- процесс температурасы 80-100°С,
- сұйық фазаның қатты фазаға қатынасы 2, 5:1,
- күкірт қышқылының бастапқы концентрациясы 0, 75 масса. үлестер,
- экстракция дәрежесі 0, 98 дол. бірл.,
- өндірістік фосфор қышқылының концентрациясы 0, 45 дол. Р2О5 бойынша бірл. Фосфор қышқылын өндірудің экстракциялық әдісінің барлық нұсқалары жалпы кемшіліктермен сипатталады:
- алынған фосфор қышқылын минералды тыңайтқыштар өндірісінде қажетті концентрацияға дейін буландыру қажеттілігі,
- шоғырландыру сатысында аппаратураның қатты коррозиясы,
- аппаратура қабырғаларында кальций сульфаты мен кремний қышқылы гелі кристалдарының тұндырылуы.

Фосфор қышқылын электротермиялық әдіспен өндіру
Процестің физика-химиялық негіздері
Фосфор қышқылын өндірудің электротермиялық әдісі фосфаттарды Элементарлық фосфорға дейін, оны кейіннен фосфор (V) оксидіне дейін тотықтыруға және оксидті фосфор қышқылына дейін гидратациялауға негізделген:
Ca5(PO4) 3F→ Рn → Р2О5 → Н3РО4.

1. Фосфор алу.
Табиғи фосфаттардан фосфорды қалпына келтіру-бұл кезеңдерден өтетін күрделі көп сатылы гетерогенді процесс:
- шикіқұрам компоненттерін қыздыру,
- кальций фосфаты мен кремний оксидінің балқымаға түсуі,
- трикальцийфосфаттың диссоциациясы,
- диссоциация өнімдерінің көміртегі бөлшектерінің бетіне диффузиясы,
- трикальцийфосфаттың көміртегімен өзара әрекеттесуі және фосфордың, көміртек (II) оксиді мен кальций оксидінің түзілуі,
- кальций силикаттары түрінде реакция аймағынан кальций оксидін алып тастау.
Ағындар болмаған кезде қалпына келтіру реакциясы 20 минут ішінде 1400°C температурада жүреді. Процестің температурасын төмендету және реакцияның тепе-теңдігін оңға жылжыту үшін жүйеге кремний оксиді, алюминий оксиді немесе алюминий силикаттары енгізіліп, нәтижесінде пайда болған кальций оксидін оңай алынатын шлак түрінде байланыстырады:
2Ca5(PO4) 3F + 15С + 6SiO2 ↔ЗР2 + 15СО + 3(3CaO·2SiO2) + CaF2 + Н
Н = 1730 кДж.

2. Фосфорды жағу
Гетерогенді экзотермиялық процесс, мына теңдеу арқылы жүреді:
Р4 жидк. + 5О2 газ = Р4О10 тв - Н
Н = 753кДж
Фосфордың тотығу дәрежесі температураға тәуелді. Жанудың толықтығын қамтамасыз ету және төменгі фосфор оксидтерінің пайда болу мүмкіндігін болдырмау үшін процесс 1000 - 1400°C температурада және екі есе артық ауада жүргізіледі.

3. Фосфор оксидінің гидратациясы
Процестің бірінші кезеңінде жүйеде жоғары температураның әсерінен фосфор оксиді буларының сумен әрекеттесуі метафосфор қышқылын береді.
Р4Н10 + 2Н2О = 4НРО3 - Н.
Температура төмендеген кезде метафосфор қышқылы полифосфор қышқылдары арқылы фосфор (ортофосфор) қышқылына айналады:
НРОз + Н2О = Н3РО4 - Н.
Фосфор (V) оксидінің димерін гидратациялау процесі экзотермиялық болып табылады және технологиялық процестің осы кезеңін ұйымдастыруда ескерілетін жылудың едәуір мөлшерін шығарумен бірге жүреді.
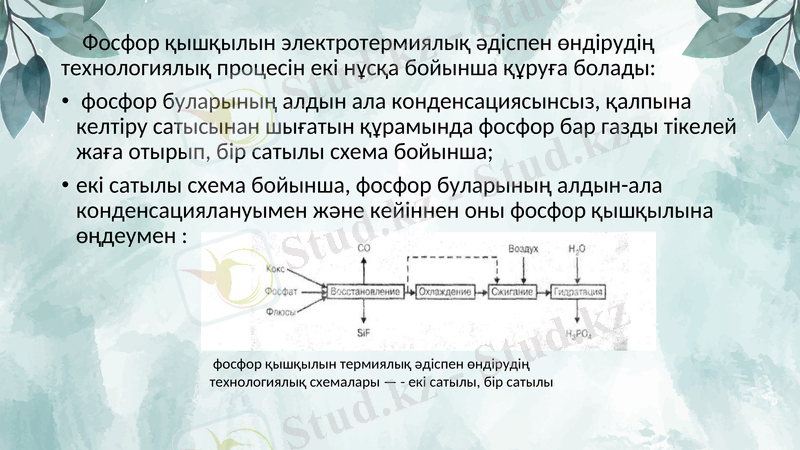
Фосфор қышқылын электротермиялық әдіспен өндірудің технологиялық процесін екі нұсқа бойынша құруға болады:
фосфор буларының алдын ала конденсациясынсыз, қалпына келтіру сатысынан шығатын құрамында фосфор бар газды тікелей жаға отырып, бір сатылы схема бойынша;
екі сатылы схема бойынша, фосфор буларының алдын-ала конденсациялануымен және кейіннен оны фосфор қышқылына өңдеумен :
фосфор қышқылын термиялық әдіспен өндірудің технологиялық схемалары - екі сатылы, бір сатылы
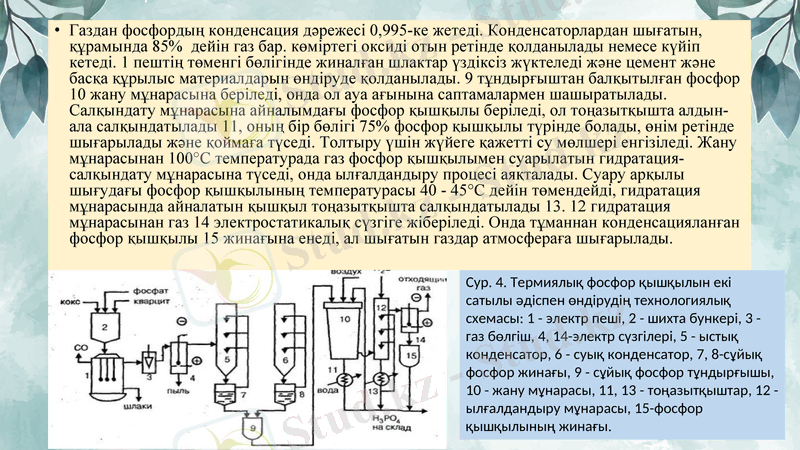
Газдан фосфордың конденсация дәрежесі 0, 995-ке жетеді. Конденсаторлардан шығатын, құрамында 85% дейін газ бар. көміртегі оксиді отын ретінде қолданылады немесе күйіп кетеді. 1 пештің төменгі бөлігінде жиналған шлактар үздіксіз жүктеледі және цемент және басқа құрылыс материалдарын өндіруде қолданылады. 9 тұндырғыштан балқытылған фосфор 10 жану мұнарасына беріледі, онда ол ауа ағынына саптамалармен шашыратылады. Салқындату мұнарасына айналымдағы фосфор қышқылы беріледі, ол тоңазытқышта алдын-ала салқындатылады 11, оның бір бөлігі 75% фосфор қышқылы түрінде болады, өнім ретінде шығарылады және қоймаға түседі. Толтыру үшін жүйеге қажетті су мөлшері енгізіледі. Жану мұнарасынан 100°C температурада газ фосфор қышқылымен суарылатын гидратация-салқындату мұнарасына түседі, онда ылғалдандыру процесі аяқталады. Суару арқылы шығудағы фосфор қышқылының температурасы 40 - 45°C дейін төмендейді, гидратация мұнарасында айналатын қышқыл тоңазытқышта салқындатылады 13. 12 гидратация мұнарасынан газ 14 электростатикалық сүзгіге жіберіледі. Онда тұманнан конденсацияланған фосфор қышқылы 15 жинағына енеді, ал шығатын газдар атмосфераға шығарылады.
Сур. 4. Термиялық фосфор қышқылын екі сатылы әдіспен өндірудің технологиялық схемасы: 1 - электр пеші, 2 - шихта бункері, 3 - газ бөлгіш, 4, 14-электр сүзгілері, 5 - ыстық конденсатор, 6 - суық конденсатор, 7, 8-сұйық фосфор жинағы, 9 - сұйық фосфор тұндырғышы, 10 - жану мұнарасы, 11, 13 - тоңазытқыштар, 12 - ылғалдандыру мұнарасы, 15-фосфор қышқылының жинағы.

Термиялық фосфор қышқылын өндірудегі негізгі құрылғылар-жану (жану) мұнарасы және ылғалдандыру мұнарасы. Жану мұнарасы қуыс, конустық пішінді, диаметрі шамамен 4 м және биіктігі шамамен 14 м. мұнараның қақпағы сумен салқындатылып, фосфорды шашырататын саптамаға ие. Гидратация мұнарасы биіктігі 15 м және диаметрі 3 м цилиндр түрінде жасалған және Рашиг сақиналарынан және қышқыл шашыратуға арналған үш саптамадан тұрады.
- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz