Сандық талдаудың міндеттері мен әдістерінің жалпы сипаттамасы: гравиметрия, титриметрия және физико-химиялық әдістердің жіктелуі



Сабақтың тақырыбы:
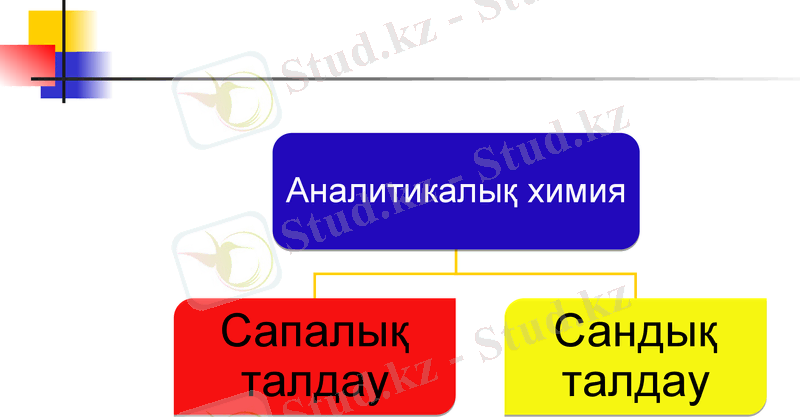
Сандық талдаудың міндеттері мен әдістерінің жалпы сипаттамасы.
Физикалық, физико-химиялық талдау әдістері, олардың жіктелуі.
«Аналитикалық химия» пәні
Оқытушы: Оспанова Айгуль Канатовна

Гравиметрия
Гравиметриялық анализ - құрамы оның белгілі қосылыс түріне немесе химиялық таза күйінде бөлінген анықталатын компоненттің массасын дәл өлшеуге негізделген мөлшерлік анализ әдісі.

Гравиметрия
әдіс
әдістің негізгі принципі
Бөлу
Анақталатын құрам бөлікті бос күйінде бөліп алып өлшейді немесе қалдықты өлшейді.
Тұндыру
Анықталатын құрам бөлікті анықталатын құрамның аз еритін қосылысы түрінде тұндырады. Қалдықты жуып, кептіреді немесе қатты қыздырып, өлшейді.
Айдау
Анықталатын құрам бөлікті ұшқыш қосылысқа айналдырып, қыздыру арқылы айдайды, оны гравиметриялық формаға келтіріп, өлшейді немесе қалдықты өлшейді.
Гравиметриялық анализ әдістері үш топқа бөлінеді:

Гравиметриялық анализ барысында барлық немесе кейбір операциялар тұндыру әдісімен өткізіледі. Тұндыру әдістері мына ретпен жасалады:
Орташа өлшендіні іріктеу;
Өлшендіні (татпаны) өлшеу;
Өлшендіні еріту;
Толық тұнуға сынама жасалған анықталатын құрамдас бөлікті тұндыру;
Тұнбаны сүзу немесе центрифугалау;
Толық жуылғандығы туралы татпасы бар тұнбаны жуу;
Тұнбаны кептіру және қатты қыздыру;
Гравиметриялық форманы өлшеу;
Анализдің нәтижелерін есептеп шығару.

Абсолютті қателік - талдау нәтижесінің өлшенетін шаманың ақиқат пәніне ауытқуы:
мұндағы хі - анықтау нәтижесі, - талданған компоненттің ақиқат мөлшері.
Салыстырмалы қателік - өлшеудің абсолютті қателігінің ақиқат мәнге қатынасы:
немесе Δ
салыстырмалы қателік көбінесе % арқылы өрнектеледі. Өлшеу қателігі көптеген факторларға байланысты, олар: реагенттердің, аналитикалық ыдыстың тазалығы; орындаушының өзіндік қабілеттілігі; өлшеу методикасы; химиялық және физикалық операциялар саны, пайдаланатын ыдыс пен жабдықтардың (аппаратураның) дәлдік класы және т. б.
Қателіктерді жіктеу.

Қателіктерді жіктеу.
Жүйелі қателік - өлшеудің әрдайым тұрақты болып қалатын немесе қайталанатын анализдерде заңдылық бойынша өзгеріп отыратын қателікті сипаттайды. Жүйелі қателік тұрақты таңбаға ие болады, яғни ол анализ нәтижесін тек арттырып немесе кемітіп отырады. Жүйелі қателіктер түзетулер енгізу, эталнмен салыстыру және басқа да мәселелер арқылы есептелсе және елеулі түрде азайтыла алады.
Өлшеудің кездейсоқ қателігі деп қайталанған өлшеулерде кездейсоқ сипатта өзгеретін қателік аталады. Оның таңбасы тұрақты емес, кездейсоқ түрде өзгеріп отырады.
Өрескел қателіктер тәжірибені қайталаған сайын елеулі түрде өзгеріп отырады. Олар аналитиктің оперативтік қателіктері нәтижесінен және пайдаланылатын жабдықтың (аппаратураның) кездейсоқ қателіктері салдарынан пайда болады. Тәжірибелік нәтижелерді өңдеу кезінде олар байқалуы және шығарылып тасталуы тиіс.

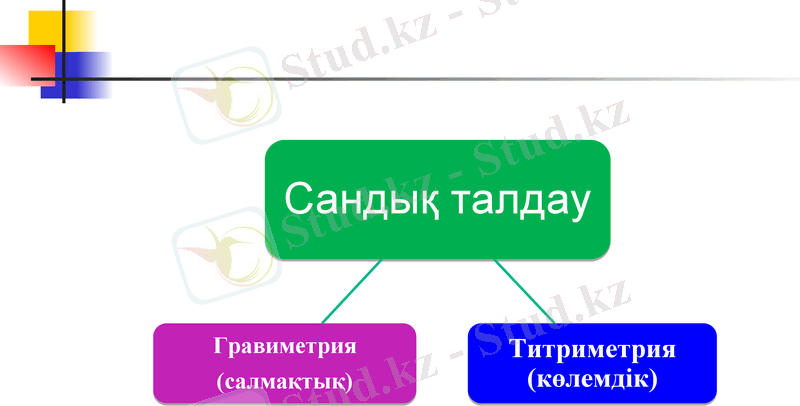
Титриметрия (көлемдік талдау)
Титиметриялық анализ - анықталатын заттың берілген мөлшерімен өткізуге жұмсалған нақты концентрациялы реактив ерітіндісінің көлемін өлшеуге негізделген мөлшерлік анализ әдісі.

Титриметриялық әдістерді жіктеу
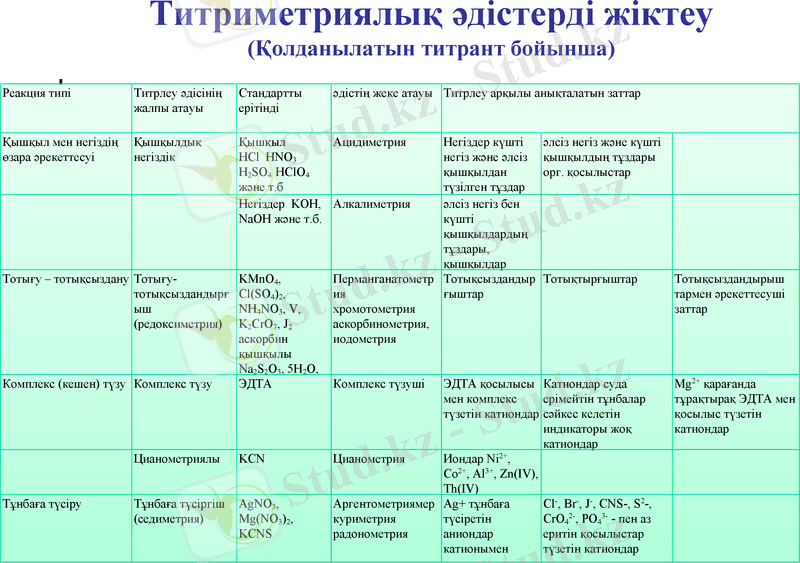
Титриметриялық әдістерді жіктеу
(Қолданылатын титрант бойынша)
Реакция типі
Титрлеу әдісінің жалпы атауы
Стандартты ерітінді
әдістің жеке атауы
Титрлеу арқылы анықталатын заттар
Қышқыл мен негіздің өзара әрекеттесуі
Қышқылдық негіздік
Қышқыл
HCl HNO3
H2SO4 HClO4
және т. б
Ацидиметрия
Негіздер күшті негіз және әлсіз қышқылдан түзілген тұздар
әлсіз негіз және күшті қышқылдың тұздары орг. қосылыстар
Негіздер KOH, NaOH және т. б.
Алкалиметрия
әлсіз негіз бен күшті қышқылдардың тұздары, қышқылдар
Тотығу - тотықсыздану
Тотығу-тотықсыздандырғыш (редоксиметрия)
KMnO4, Cl(SO4) 2, NH4NO3, V, K2CrO7, J2 аскорбин қышқылы Na2S2O3, 5H2O,
Перманганатометрия
хромотометрия
аскорбинометрия, иодометрия
Тотықсыздандырғыштар
Тотықтырғыштар
Тотықсыздандырыш тармен әрекеттесуші заттар
Комплекс (кешен) түзу
Комплекс түзу
ЭДТА
Комплекс түзуші
ЭДТА қосылысы мен комплекс түзетін катиондар
Катиондар суда ерімейтін тұнбалар сәйкес келетін индикаторы жоқ катиондар
Mg2+ қарағанда тұрақтырақ ЭДТА мен қосылыс түзетін катиондар
Цианометриялы
KCN
Цианометрия
Иондар Ni2+, Co2+, Al3+, Zn(IV), Th(IV)
Тұнбаға түсіру
Тұнбаға түсіргіш (седиметрия)
AgNO3, Mg(NO3) 2, KCNS
радонометрия
Ag+ тұнбаға түсіретін аниондар катионымен
Cl-, Br-, J-, CNS-, S2-, CrO42-, PO43- пен аз еритін қосылыстар түзетін катиондар

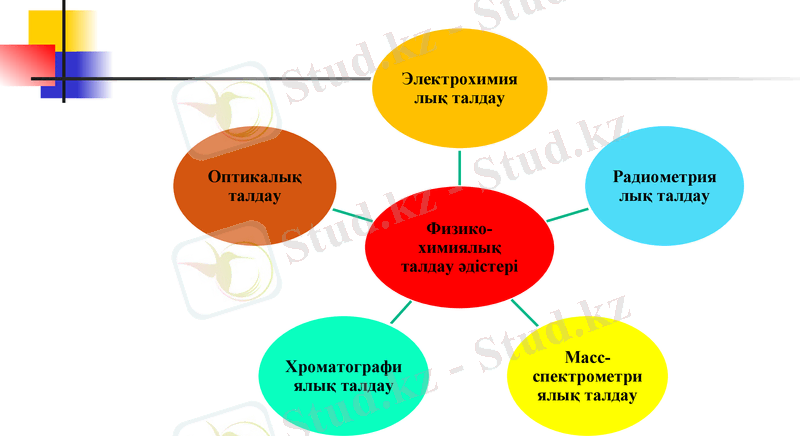
Физико-химиялық талдау әдістері, олардың жіктелуі.
Физика - химиялық әдістер қандай да болмасын химиялық әрекеттесу немесе айырылу реакциясын қатыстырып физикалық қасиетін өлшеуге негізделген.
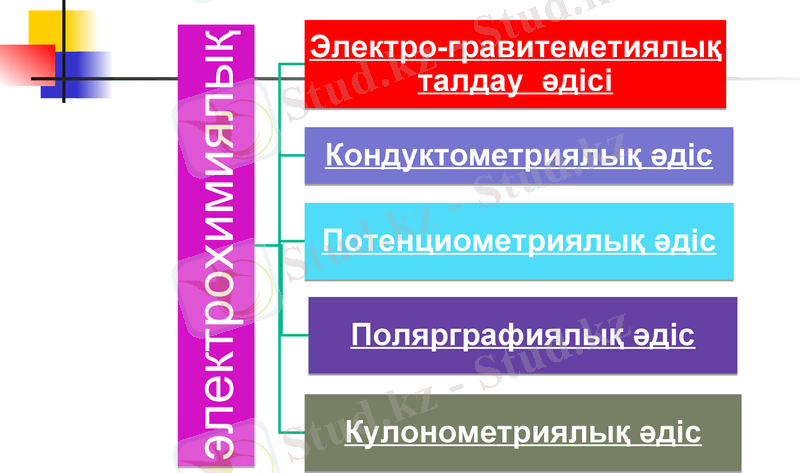
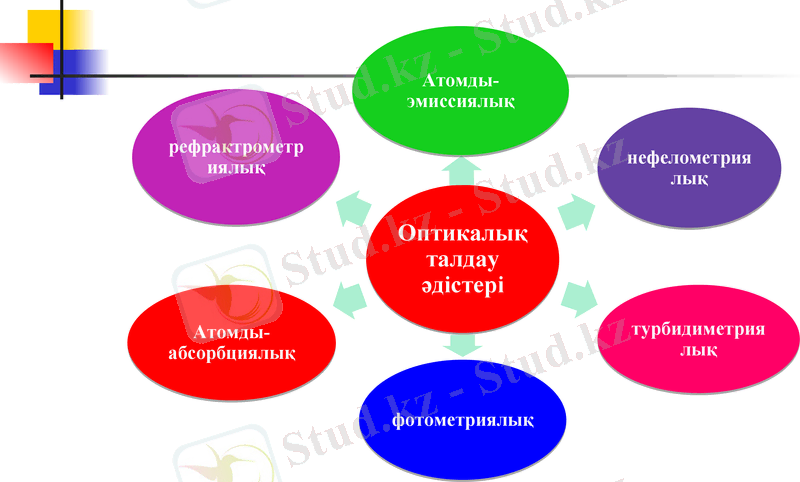
- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz