Металл коррозиясының жылдамдығы: теориялық және тәжірибелік аспектілері


Мазмұны
Кіріспе 3
I. Теориялық бөлім 3
1. 1. Коррозия жылдамдығы 4
1. 2. Коррозия жылдамдығына ішкі және сыртқы факторлардың әсері 5
1. 3. Коррозия жылдамдығының көрсеткіші және оны өрнектеу тәсілдері 12
1. 4. Металл коррозиясының жылдамдығы 20
1. 5. Металлдар коррозиясының көрсеткіші 22
II. Тәжірибелік бөлім 25
2. 1. Қолданылатын аспаптар, әдістемелер, реактивтер 25 2. 3. Нәтижелерді талдау 28
2. 4. Қосымша 29
III. Қорытынды 34
IV. Пайдаланған әдебиеттер тізімі 35
Кіріспе
Металдар және құймалар қоршаған ортадағы әртүрлі заттармен жанасып, олармен әрекеттесіп, түрлі қосылыстар түзе алады. Бұл кезде металл бұйымның қасиеттері өзгереді, көбінесе металдан жасалған конструкция түгелдей бұзылады. Бұл өте зиянды және қауіпті процесс жемірілу немесе коррозия деп аталады.
Жемірілу нәтижесінде металл бұйымдар пайдалануға жарамсыз болып қалады. Сондықтан жемірілу процесінің негізін түсініп және оның жағымсыз салдарын болдырмау үшін алдын алу керек [6] .
Барлық металдар жемірілуге бірдей үшырамайды. Кернеу қатарында күмістен кейін тұрған бекзат металдар деп аталатын металдар мүлдем жемірілуге ұшырамайды. Сондықтан бұл металдар мен олардың құймаларын жемірілуге тіптен жол берілмейтін жерлерде қолданады. Мысалы, алтынды ғарыштық техникада, электрондық өнеркәсіпте жанастыратын бұйымдар жасауда қолданады.
Кернеу қатарында магнийдің сол жағында тұрған металдар қарама-қарсы қасиеттерге ие. Олар кәдімгі жағдайларда қоршаған ортадағы көптеген заттармен оңай әрекеттеседі, сондықтан олар конструкциялар мен аппараттар дайындауда қолданылмайды. Кернеу қатарының орта бөлігінде баяу жемірілетін металдар орналасқан. Олардың кейбіреуі, мысалы, магний, мырыш, алюминий, хром, никель жемірілуге тұрақты. Олардың бетінде металды қоршаған заттармен жанасудан қорғайтын берік оксидті қабықшалар түзіледі.
Жемірілу жылдамдығына электролит ерітіндісінің құрамы да әсер етеді. Оның қышқылдығы неғұрлым жоғары болса, сондай-ақ оның құрамында тотықтырғыштар көп болса, жемірілу соғұрлым жылдам жүреді. Температура өскен сайын жемірілу жылдамдығы да артады [1] .
1. Негізгі бөлім
1. 1. Коррозия жылдамдығы
Коррозия жылдамдығы - уақыт бірлігі ішінде коррозияның металға әсерінің нәтижесі. Коррозия жылдамдығы туралы берілген анықтама техникалық жүйеге және коррозия түріне байланысты. Коррозия жылдамдығы уақыт бірлігі ішіндегі коррозия тереңдігінің жоғарылауымен (ену жылдамдығы) де сипатталуы мүмкін. Мысалы, мм/жыл немесе уақыт бірлігінде аудан бетінің бірлігінде коррозиялық өнімге айналған металл массасы (салмақ жоғалту, мысалы, г/м 2 /жыл) [10] .
Коррозия эффекті уақыт өте келе өзгеруі мүмкін және коррозияланушы кеңістіктің барлық нүктелерінде бірдей болуы мүмкін. Сәйкесінше, коррозия жылдамдығы туралы есеп уақытқа тәуелділік типі және коррозия әрекетінің нәтижесін ауыздықтау жайлы анықтамамен қатар жүру керек. Коррозия жылдамдығын, басқа процесстер сияқты, процесстің қозғаушы күші мен процесс кедергісі шамаларының қатынасымен анықтауға болады. Металлдардың термодинамикалық потенциалының мәнін процесстің қозғаушы күшін бағалау мақсатында қолдануға болады, яғни
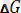
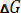 мәнін білсе коррозияның өту ықтималдығын табуға болады [6] .
мәнін білсе коррозияның өту ықтималдығын табуға болады [6] .
Шешуші мәнге ие коррозия процессінің жылдамдығы бір уақытта әрекет ететін факторлардың көбіне тәуелді болып келеді: ішкі, металл табиғатын сипаттайтын; оның дайындалу технологиясын, қоспа құрамын; құрылым типін; ішкі күш; агрессивті ортаның құрамын сипаттайтын ішкі және беткі жағдайлары және процесстің өту шарттары (температура, қысым, гидродинамикалық шарттар) . Мүмкін процесстің жылдамдығы туралы мәліметті және процесс нәтижесіне әр түрлі факторлардың әсер ету сипатын кинетикалық зерттеулер береді.
Көптеген металлдардың коррозия жылдамдығы мықты дәрежеде түзілген қорғаныс қабықшаларының қасиеттеріне немесе олардың бүліну жылдамдығына байланысты, егер олар тәжірибеге дейін металл бетінде болса. Табиғи жағдайда қорғаныс қабаттары түзілуі немесе олардың бүлінуі үшін ұзақ уақыт керек. Агрессивті ортаны көбейту себепті сынақ уақытын көп қысқартып жіберу көбінесе, процесс сипатының, коррозия өнімі қасиетінің және оларды беттер бойынша бөлудің өзгеруіне әкеледі; жабынның қорғаныш қасиеттері және коррозия интенсивтілігі өзгереді. Коррозиялық тұрақтылығы бойынша аз ажыратылатын материалдар үшін тексеру ұзақтығын осы айырмашылықты ажырата алатындай есеппен таңдалу керек [12] .
1. 2. Коррозия жылдамдығына ішкі және сыртқы факторлардың әсері
Коррозиялық процестердің жүру жылдамдығы ішкі және сыртқы факторларға тәуелді.
Ішкі факторлар материал күйін сипаттайды. Оларға: Д. И. Менделеевтің периодтық жүйесіндегі орны, термодинамикалық тұрақтылық, химиялық құрамы және материал құрылымы, ішкі кернеудің болуы және материал бетін өңдеу сипаты.
Металдың периодтық жүйедегі орны оның тек коррозиялық әрекетін жалпы бағалауға мүмкіндік береді, бірақ коррозиялық процесті дәл сипаттауға мүмкіндік бермейді.
Коррозияға периодтық жүйенің 1 және 2 топтардың сол жақ топшасының металдары неғұрлым тұрақты. 1 және 2 топтардың оң жақ топшасында және абсқа топтарда коррозиялық тұрақтылық реттік нөмірдің артуымен өседі. 4 және 6 топтардың сол жақ топшасындағы, және 8 топта оңай пассивтенетін металдар орналасқан, олардың пассивацияға бейімділігі реттік нөмірдің артуымен кемиді.
Элементтің периодтық жүйедегі орны барлық жағдайда металдың коррозияға тұрақтылығын сипаттауға мүмкіндік бермейді. Коррозиялық әрекетіне қатысты химиялық қасиеттер заңдылықтарына ұқсас белгілі бір заңдылықтар байқалады. Коррозияға тұрақсыз металдар І және ІІ топтардың сол жақ топшаларында орналасқан.
І және ІІ топтардың оң жақ топшаларында және басқа топтарда коррозиялық тұрақтылық атомдық нөмір артуымен артады ( Cu -Ag -Au, Zn - Cd -Hg, Ni-Pd-Pt) .
ІV, VІ топтардың сол жақ топшаларында және VІІІ топта оңай пассивтенетін металдар орналасқан, сонымен қатар атомдық нөмір артқан сайын пассивацияға бейімділік бірінші жуықтауда кемиді (Ti-Zr-Hf; Cr-Mo-W) .
Металдың термодинамикалық тұрақтылығы.
Металдардың термодинамикалық тұрақтылығы олардың тепе-теңдік потенциалдарына тәуелді, бірақ бұл тәуелділік олардың коррозия жылдамдығын анықтамайды. Бұл коррозияның реалды және идеалды процестерінің жүрудегі айырмашылықтарымен түсіндіріледі.
Металдар тұрақтылығының неғұрлым дәл сипаттамасын Пурбэ диаграммалары береді, олар коррозиялық ортаның концентрациясы мен рН белгілі бір мәндерінде металдың термодинамикалық тұрақтылығын көрсетеді.
белгілі бір коррозиялық ортада коррозиялық әрекетті термодинамикалық болжауға ластаушы қоспалар мен кинетикалық факторлар әсері кедергі келтіреді.
Металдың термодинамикалық тұрақтылығы оның стандартты потенциал шамасымен сипатталады. Сонымен сұйытылған күкірт қышқылында алюминий (φ0=- 1, 67 в) тұрақты, ал темір (φ0=-0, 44в) тұрақсыз. Балқытқыш қышқылда магний (φ0=-2, 34 в) коррозияланбайды, ал қалайы (φ0=-0, 13в) коррозяға ұшырайды.
Сәйкесінше, металдардың стандартты потенциалдар қатынасы олардың коррозиялық қасиеттерін бағалай алмайды.
Бұл, біріншіден, реалды процесс жүру жағдайлары әрқашан стандартты жағдайлардан айрықша болуымен байланысты, екіншіден, коррозиялық тұрақтылығын деңгейін болжау мүмкіндігі болмауы коррозия жылдамдығына қатты әсер ете алатын көптеген кинетикалық факторлардың болуында, үшіншіден таза металдар техникада сирек қолданылады.
Балқыманың химиялық құрамы коррозия жылдамдығына әсер етеді. Металл неғұрлым таза болса, яғни оларда қоспа неғұрлым аз болса, коррозия жылдамдығы соғұрлым төмен. Коррозиялық тұрақтылығын арттыратын легирлеуші элекменттері бар балқымаларда коррозия жылдамдығы осы элементтердің үлестік мөлшері артуымен кемиді. Құрылымына байланысты балқымаларды көп фазалы және бір фазалы деп бөледі.
Механикалық қоспа типіндегі көп фазалы балқымаларда коррозия жылдамдығы салмақтық қатынаспен де, катод пен анод ролін атқаратын фазалардың өзара орналасуымен анықталады. Егер фазалар біркелкі таралса және анодты құраушы үлесі аз болса, коррозия тұтас және қысқа болады. Анодтық фаза біркелкі емес таралса коррозия меншікті және ұзақ болады, ал коррозия ошағы тереңге таралады, ол өте қауіпті. Қатты ерітінді типті бір фазалы балқымаларда коррозия жылдамдығы балқыма құрамына тура тәуелділікте емес, Тамман жасаған тұрақтылық шегі ережесіне сай секірме тәрізді өзгереді. Сондай-ақ n/8 ереже деп аталатын бұл ереже электроңдығы төмен металл электроңдығы жоғары (асыл металмен) металмен легирленгенде коррозия жылдамдығы неғұрлым асыл металдың атомдық үлесін қысқа n/8 мөлшерін қосу мөлшеріне қарай секірме түрінде төмендейді. Сонымен қатар балқыманың тепе-теңдік потенциалы таза неғұрлым асыл металл потенциалына жуықтап сатылы артады. Бірақ бұл кез келген бір фазалы балқыма оның құрамы өзгергенде тұрақтылықтың барлық 8 шегін иеленеді дегенді білдірмейді. Тұрақты шек саны мен олардың мәні металдар табиғатына және орта агрессивтігінің дәрежесіне тәуелді. Тұрақтылық шегі пайда болу себептерін түсіндіре отырып Тамман неғұрлым асыл металдар атомдары коррозиялаушы металл атомдарын шектейді деген болжам айтты.
Ішкі кернеуліктер материалда термиялық өңдеу жасау салдарынан және детальдар дайындау процесінде пайда болуы мүмкін. Осы кернеуліктердің саны неғұрлым көп болса, коррозия жылдамдығы соғұрлым жоғары.
Бұйымдар бетін өңдеу сипаты коррозия жылдамдығына әсер етеді.
Беттікті өрескел және жұқа өңдеуді ажыратады.
Өрескел өңдеуге кварцтеу (металл щеткалар көмегімен өңдеу), егеумен өңдеу кіреді.
Жұқа өңдеу бетті тегістеуден тұрады. Өңдеудің тазалық дәрежесі неғұрлым жоғары болса, бұйымның коррозиялық тұрақтылығы агрессивті орта шоғырланатын бұдырлықтың жойылу есебінен соғұрлым жоғары [4; 1] .
Сыртқы факторлар коррозиялық орта күйін сипаттайды. Оларға коррозиялық ортан рН, температура, қысым, еріген оттегі концентрациясы, бейтарап ерітінділердің құрамы мен концентрациясы, салыстырмалы металл ортасының қозғалыс жылдамдығы жатады.
Коррозиялық орта рН әсері. Әрбір нақты жағдайда қандай да бір металдың мүмкін болатын коррозиялық әрекетінде ортаның рН-на тәуелді қалыпты температурада тепе-теңдік потенциал - рН координаттарында тұрғызылған сәйкес диаграммасы (Пурбэ диаграммалары) бар. Пурбэ диаграммасы коррозиялық тұрақтылықтың (немесе иммунитет) металл тотығуы термодинамикалық мүмкін болмайтын аймағын анықтауға және оның пассивті және коррозиялық-активті аймақтардын болжауға мүмкіндік береді.
Диаграмма әрқашан металдың коррозиялық әрекеті жайлы нақты жауап бере алмайды, себебі ол оның тепе-теңдік күйін сипаттайды, ал коррозиялық процесс әрқашан тепе-теңсіздікте болады және көптеген кинетикалық факторлар әсеріне ұшырайды.
Коррозия жылдамдығына рН әсері металл табиғатына тәуелді. Қалыпты температура үшін осыған байланысты металдарды бес топқа бөлуге болады.
Топ I - асыл металдар және белгілі бір дәрежеде Ti, олардың коррозиясына рН әсер етпейді. Бұл топқа Pt, Au, Ag және т. б. кіреді.
Топ II - бейтарап ортада тұрақты, бірақ қышқылдық және сілтілік орталарда тұрақсыз атмосфералық металдар. Оларға Zn, Al, Pb, Sn жатады.
Топ III - қышқылдық және бейтарап орталарда толық тұрақты, бірақ сілтілік ортада күшті коррозияланатын металдар. Мұндай металдар болып Mo, W және Та табылады.
Топ IV - бейтарап және сілтілік ортада әлсіз коррозияланатын, бірақ олардың коррозия жылдамдығы қышқылдық ортада артатын металдар. Бұл топқа Ni, Co, Cd кіреді.
Топ V - қышқылдық ортада тұрақсыз және бейтарап ортада аздап коррозияланатын металдар; сілтілік ортада олардың тұрақтылығы рН 12-14 болғанда максимумға дейін жоғарылайды. Бұл топқа Мn, Mg, Cr, Cu және Fe жатады [8] .
Ерітіндінің рН кемігенде Н иондарының активтігі артады, және ережеге сай, коррозия жылдамдығы да артады. Бірақ бұл агрессивті орта пассивтеуші әсер көрсетпеген жағдайда ғана және металл бетінде қорғаушы жабын түзілуіне әкелмесе ғана мүмкін болады. рН-ң коррозия жылдамдығына әсерінде металл табиғаты анық байқалады. Осы сипаты бойынша бөлме температурасында металдарды топқа бөлуге болады.
Бірінші топқа асыл металдар (Ag, Au, Pt и др. ) және белгілі бір мөлшерде титан жатады, олардың коррозиясына рН әсер етпейді.
Екінші топқа - қышқылдық және сілтілік ортада тұрақсыз, бейтарап ортада тұрақты металдар (Al, Zn, Sn, Pb) .
Үшінші топқа - қышқылдық ортада тұрақсыз және сілтілік ортада тұрақты металдар (Ni, Co, Cd) .
Төртінші топқа - сілтілік ортада тұрақсыз, қышқылдық ортада тұрақты металдар (Mo, W, Ta) .
Бесінші топқа - қышқылдық ортада тұрақсыз, бейтарап ортада әлсіз тұрақты, сілтілік ортада тұрақты металдар (Fe, Cr, Cu, Mn, Mg) .
Тұздардың бейтарап ерітінділерінің құрамы мен концентрациясының әсері.
Бейтарап ортада коррозия оттектік деполяризациямен жүреді. Коррозия жылдамдығына тұздардың бейтарап ерітінділерінің әсер ету дәрежесі коррозияның түзілген өнімдері қасиеттеріне тәуелді. Қиын еритін қосылыстар металл бетін бүркемелейді, нәтижесінде коррозия жылдамдығы кемиді.
Нитраттар, хлоридтер, кейде сульфаттар да металдармен еритін қосылыстар түзеді, олар металл бетін экрандамайды, ол коррозия жылдамдығының артуына әсер етеді. Активтендіру әсері мына қатар бойынша артады: иодидтер, бромидтер, хлоридтер, фторидтер.
Аммоний хлориді, натрий ацетаты сияқты гидролизге бейім тұздардың әсері гидролизден кейін орта рН-ы қаншалықты өзгергендігіне тәуелді.
бейтарап тұздар концентрациясын белгілі бір мәндерге дейін арттырғанда ерітіндінің электр өткізгіштігінің артуынан, ал хлоридтер жағдайында - хлор иондарының активтеуші әсері салдарынан коррозия жылдамдығы да артады. Концентрацияны ары қарай арттырғанда катодты реакцияға қатысатын оттек ерігіштігі төмендейді және коррозия жылдамдығы кемиді.
Бейтарап тұздардың коррозия жылдамдығына әсері коррозияда түзілген өнім қасиеті арқылы байқалады.
Қиын еритін қосылыстар түзілгенде жартылай немесе толық металл бетінің бүркемеленуі жүреді және коррозия жылдамдығы түседі. Тұздар металда беттікті пассивтейтін окисьтік жабындар түзе алады. Көбінесе бейтарап ерітінділерде коррозия оттек деполяризациясымен жүреді. Бейтарап тұздар концентрациясын белгілі бір мәнге дейін арттырғанда ерітінді электр өткізгіштігінің артуынан коррозия артуы байқалады, кейін катодты реакцияға қатысатын оттек ерігіштігінің төмендеуінен коррозия кемиді.
Оттектің әсері. Бейтарап ортада металдар коррозиясының жылдамдығы коррозиялық ортада катодты реакцияның жүруін қамтамасыз ететін еріген оттек концентрациясына тәуелді. Көп жағдайларда оттек атмосферадан түседі және коррозия жылдамдығы электрохимиялық процестің диффузиялық кинетика механизміне сәйкес оның концентрациясына тура пропорционал. Сызықтық тәуелділік оттектің жоғары концентрациясына жеткенге дейін байқалады, бұл кезде металл беті пассивтене бастайды. Коррозиялық ортадағы оттек мөлшері тұздардың құрамы мен концентрациясына, температураға, араластыру жағдайларына және берілген ортада оның ерігіштігін анықтайтын басқа факторларға да тәуелді.
Металл бетіне оттектің біркелкі емес тасымалдануы меншік коррозияны тудырады, оның жылдамдығы аэрацияның біркелкі емес дәрежесіне тәуелді. Коррозия жылдамдығына оттек ортадағы еріген оттек концентрациясы едәуір әсер етеді. Оттек не пассиватор ролін не деполяризатор ролін атқарады.
егер оттек пассиватор ролінде болса, онда алғашында коррозия жылдамдығы окисьтік жабынның түзілуімен болған металл жоғалтудан артады, барлық беттік окисьтік жабынмен қапталғандағы оттектің кейбір концентрацияларында коррозия жылдамдығы түседі.
Егер оттек деполяризатор ретінде болса, онда коррозия жылдамдығы еріген оттек мөлшерінің өсуімен сызықты тәуелділікте артады.
Температура әсері. Егер коррозиялық процесс сутектік деполяризациямен жүрсе, ондатемпература артқан сайын бір уақытта коррозия жылдамдығы да артады. Бұның негізгі себебі болып катодтық процестің аса кернеуінің төмендеуі, диффузияның жылдамдауы және ортаның электрлік кедергісінің кемуі табылады.
Оттектік деполяризациямен жүретін коррозиялық процестер жылдамдығы температура артқанда оттек ерігіштігінің кемуі салдарынан төмендейді. Температураның артуы кейде металл пассивтенуіне әкеледі.
Егер коррозия сутектік деполяризациямен жүрсе, онда температураның артуы коррозия жылдамдығын арттырады. Бұл сутек бөлінуінің аса кернеуінің кемуімен, диффузияның жылдамдауы және ортаның электрлік кедергісінің кемуімен түсіндіріледі.
Оттектік деполяризациямен коррозияда температура артуымен коррозия жылдамдығы баяулайды, себебі ол оттек концентрациясына тәуелді. Температура артқанда ерітіндіде оттек ерігіштігі төмендейді. Бірақ егер жүйе жабық болса, онда коррозия жылдамдығы артады.
Қысымның артуы коррозиялық ортада газдар ерігіштігінің артуы және металда ішкі кернеулер туындау салдарынан коррозия жылдамдығы артады.
Коррозиялық ортаның салыстырмалы қозғалыс жылдамдығының әсері. Коррозия жылдамдығы металл немесе коррозиялық орта қозғалыста болуына тәуелді емес. Салыстырмалы қозғалыс жылдамдығы оттектік деполяризациямен жүретін коррозиялық процестерге едәуір әсер етеді, себебі қозғалыстан электродтық қабатта оттек концентрациясы артады. Металл бетін пассивтейтін коррозия өнімдері қозғалыс кезінде қатпарланады, ол коррозия жылдамдығының артуына әкеледі. Салыстырмалы қозғалыстың жоғары жылдамдықтарында оттек концентрациясы металл бетінің пассивтенуіне әкеледі. Өте жоғары жылдамдықта коррозиялық эрозия, яғни металдың аралас электрохимиялық және эрозиялық бұзылуы байқалады.
Металл бұзылуының жылдамдығына ерітінді қозғалысы жылдамдығының әсері оттектік деполяризациямен коррозия кезінде байқалады. Ерітінді қозғалысы электродтық қабатта оттек концентрациясының артуына және беттікті пассивтеуге қабілетті коррозияның өнімдерін жоюға әсер етеді. Мұның бәрі коррозия жылдамдығын арттырады. Едәуір жылдамдықтарда беттіктің оттектің аса жоғары концентрациясы есебінен пассивтенуі мүмкін. Сонымен, орта қозғалысының жылдамдығын одан ары арттырғанда коррозиялық эрозия ошағы металдың электрохимиялық және механикалық бұзылуы процестерінің аралас әсері ретінде байқалады [9; 7] .
1. 3. Коррозия жылдамдығының көрсеткіші және өрнектеу тәсілдері
Берілген ортада металл коррозиясы жылдамдығын анықтау үшін металл қасиетінің өзгергенін объективті көрсететін қандай да бір сипаттамасының уақыт бойынша өзгеру бақылауын жүргізеді.
Коррозиялық практикада келесі көрсеткіштер жиі қолданылады:
1) Масса өзгеру көрсеткіші - уақыт бірлігіне және металл беттігі бірлігіне S қатысты коррозия нәтижесінде үлгі массасының өзгеруі (мысалы, г/м сағ) . Коррозия жағдайына байланысты ажыратады:
а) масса өзгеруінің теріс көрсеткіші
К
-
m
=
 m / S
m / S




мұндағы m - коррозия уақытында коррозия өнімдері жойылғаннан кейін металл массасының азаюы;
б) масса өзгеруінің оң көрсеткіші
К
+
m
=
 m / S
m / S




мұндағы m - коррозия өнімдері жабынының өсуі салдары уақытында металл массасының артуы.
Егер коррозия өнімдерінің құрамы белгілі болса, онда К - -тан К + -қа және керісінше қайта есептеуге болады:
К - m =К + m (n ok A Me / n Me A ok )
мұндағы А және М - Ме мен тотықтырғыштың сәйкесінше атомдық және молекулалық массалары; n және n тотықтырғыш ортада металл мен тотықтырғыш валенттіліктері.
2) Коррозияның көлемдік көрсеткіштері
К - процесте уақыт бірлігіне және металл беттігі бірлігіне қатысты сіңірілген немесе бөлінген газ көлемі V (мысалы, см/см сағ. ) .
К= көлем
 V/ S
V/ S

Газ көлемін әдетте қалыпты жағдайларға келтіреді.
Катодтық деполяризация процесі сутек иондары разрядталу, мысалы, 2Н + 2е = Н схемасы бойынша, немесе оттек молекулаларының ионизациясы О + 4е +2НО = 4ОН есебінен жүзеге асырылғанда электрохимиялық коррозияға қолданылады; сәйкесінше оттектік (К) және сутектік (К) көрсеткіштер енгізіледі.
Коррозияның сутектік көрсеткіші - бұл Su қатысты коррозия процесінде бөлінген Н көлемі.
Коррозияның оттектік көрсеткіші - Su қатысты процесте сіңірілген О көлемі.
3) Кедергі көрсеткіші.
Зерттеудің белгілі бір уақытында металл үлгісінің электрлік кернеуінің өзгеруі де коррозия көрсеткіші (К) ретінде қолданылады.
К
R
= (
 R/R
o
) 100% t уақыт ішінде
R/R
o
) 100% t уақыт ішінде
мұндағы R
o
және
 R үлгінің сәйкесінше коррозияға дейінгі және кейінгі электрлік кедергісі.
R үлгінің сәйкесінше коррозияға дейінгі және кейінгі электрлік кедергісі.
Бұл тәсілдің кейбір кемшіліктері бар, металл қалыңдығы зерттеудің барлық уақытында бірдей болу керек, сол себепті көбінесе меншікті кедергіні, яғни бірге тең ұзындықта үлгі ауданы бірлігіне (см, мм) электрлік кедергінің өзгеруін анықтайды. Бұл әдіс қолданылуы шектеулі. Анағұрлым дәл мәліметтерді сымдық үлгілер үшін алады. Бұл әдіс пісіру қосылыстарына жарамсыз.
4) Коррозияның механикалық көрсеткіштері.
Коррозия уақытында металдың қандай да бір қасиетінің өзгеруі. Беріктік шек өзгеруін салыстырмалы түрде жиі пайдаланады. Беріктік көрсеткіш бұл кезде былай өрнектеледі:
К
o
= (
 в
/
в
/
 во
) 100% t уақыт ішінде
во
) 100% t уақыт ішінде
мұндағы
 o
уақыт аралығында үлгінің коррозиядан кейінгі созылу кезіндегі беріктік шегінің өзгеруі;
o
уақыт аралығында үлгінің коррозиядан кейінгі созылу кезіндегі беріктік шегінің өзгеруі;
 во
коррозиядан кейінгі беріктік шегі.
во
коррозиядан кейінгі беріктік шегі.
5) Коррозияның тереңдік көрсеткіші.
К - уақыт бірлігінде металл бұзылуының тереңдігі П (мысалы, мм/жыл)
К
П
= п/

Коррозиялық бұзылу тереңдігі П орташа немесе максималды болуы мүмкін. Коррозияның тереңдік көрсеткішін металдардың біркелкі де, біркелкі емес те коррозия үшін қолдануға болады. Ол әртүрлі тығыздықты металдардың коррозия жылдамдығын салыстыруға қолайлы. Массалық, токтык және көлемдіктен тереңдікке ауысу біркелкі коррозияда мүмкін болады [3] .
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz