Халькогендер (O, S, Se, Te, Po): периодтық жүйедегі орны, физико-химиялық қасиеттері, қосылыстары және қолданылуы


Жоспар:
- Кіріспе.
- Халькогендерге сипаттама
- Негізгі бөлім.
- Д. И. Менделеевтің периодтық жүйесіндегі халькогендердің орналасу ерекшеліктері.
- Халькогендердің физикалық және химиялық қасиеттері
- Халькогендердің табиғатта таралуы, алынуы және қолданылуы
- Халькогендердің қосылыстары
- Зерттеулер
- Қорытынды.
- Пайдаланылған әдебиеттер

Халькогендер -VI A-тобы элементтерініңтоптық атауы. Топқа оттегі О, күкірт S, селен Se, теллур Te, полоний Po элементтері жатады. Оттегі қосылыстарда көбінесе теріс жирек - 2, сирек - 1 тотығу дәрежелерін көрсетеді. Басқа халькогендерге +4 және +6, сонымен бірге -2 тотығу дәрежелері тән. Электртерістіктері бойынша О және S -бейметалдар, ал Se, Te және Po - амфотерлі элементтер; Se мен Te бейметалдық, ал Po металдық қасиеттерді басымырақ көрсетеді. Бос күйінде оттегі O 2 - газ, ал күкірт және оның аналогтары- қатты заттар. Оттегіден полонийға қарай жай заттардың тотықтыру мүмкіндіктері азаяды.
6А топша элементтеріне - оттек, күкірт, селен, теллур және радиоактивті полоний жатады. Бірінші төртеуінде бейметалдық сипаттар бар және олар халъкогендер “кен түзуші ’’деген мағыныны білдіретін жалпы атаумен біріктіріледі.
6А топша элементтері атомдарының сыртқы деңгейлерінде 6 электроннан бар: екеуі s -орбиталъда, төртеуі р- орбиталъда орналасқан: ns 2 np 4 . Олардың орбиталъдағы екі р-электроны жұптаспаған . Бұл олардың валенттігі қозбаған күйде 2-ге тең екенін көрсетеді. Оттек атомы құрылысының ерекшілігі- оның сыртқы денгейдегі электрондары орналасқан d- денгейшесі жоқ. Сондықтан оттектің валенттігі 2- тең.
Қалған халькогендердің атомдарының сыртқы электрондық қабатында d-деңгейшесі бар. Атом қозған кезде р- және s - электронының d- орбиталъға ауысуы болады. Сондықтан олар 2 ғана емес, 4 және 6 валенттік көрсетеді.
Полонийден басқа 6А топша элементтері 7А топша элементтеріне қарағанда белсенділігі төмен болғанымен- типтік бейметалдар.
Халькогенидтерде, яғни олардың электр оң элементтермен қосылыстарында, сонымен бірге халкогендер сутекпен қосылыстарында -2 тотығу дәрежесін көрсетеді. Оттекпен және басқа бейметалдармен, мысалы, күкірт, селен және теллурмен қосылыстарында +4 немесе +6 тотығу дәрежелерін көрсетеді.
Реттік нөмері артқан сайын бейтарап атомдардың тотықтырғыштық белсенділігі төмендейді де, теріс иондардың тотықсыздандырғыштық қасиеті өседі. Халькогендің бейметалдық қасиеттері оттекте айқын білінеді де, теллурға өткенде әлсірейді.
6А топша элементтерінің сутекті қосылыстарын (гидриттерін) Н 2 Э жай заттардан (немесе күшті қышқылдармен халькогениттерге әсер етіп) синтездеп алады. Олардың формулалары H 2 O, H 2 S, H 2 Se, H 2 Te, H 2 Po. Сутекті қосылыстарды суда еріткенде сәйкес қышқылдар түзіледі. Бұл қышқылдардың күші элементтердің реттік нөмерлердің өсуіне қарай артады.
Күкірт, селен, теллур, полоний оотегімен ЭО 2 , ЭО 3 типтес окситтер түзеді. Бұл оксидтерге Н 2 ЭО 3 және Н 2 ЭО 4 қышқылдары сәкес келеді. Бұл қышқылдардың күші элементтердің, реттік нөмерлерінің өсуіне қарай кемиді. Элементтердің, реттік, нөмерлерінің өсуіне байланысты бейметалдық кеміп, металдық қасиеті артады. Мысалы, оттегі бейметал, күкірт пен селеннің бейметалдық қасиеті оттегінен төмен, ал теллур бейметалл қатарына жатқанмен металдық жарқылы бар, электр тогын өткізеді.
 Халькогендердің физико- химиялық қасиеттері
Халькогендердің физико- химиялық қасиеттері
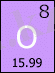
Оттегі - екінші периодтың, VI- топтың элементі. Электртерістілігі жоғары, типтік бейметалдық қасиеттерді көрсетеді. He, Ne, Ar элементтерден басқа элементтермен қосылыстар береді, көптеген оксидтер, гидроксидтер, оттекті қышқылдар тұздарының құрамына енеді. Жер қабатында 55% және табиғи суларда ең көп таралған элемент, бос және байланысқан түрде кездеседі. Минералдар мен тау жыныстары (алюмосиликаттар, құм, балшыққұмдақтар т. б. ) құрамына енеді. Бос оттегі ауа құрамында болады. Барлық организмдердің тіршілігіне өте қажетті элемент, органикалық заттар көбінің құрамында болады, сан алуан биохимиялық процестерге қатынасады, тіршілікті қамтамасыз етеді. Оттегін 1769-1771 жылдары швед химигіК. В. Шееле ашты және одан тәуелсіз 1774 жылы ағылшын химигі Дж. Пристли қоса ашты. Олар оттегін HgO мен KNO 3 -ті қақтау арқылы алды.
Табиғатта кездесу. Табиғатта оттегісі бар 1400 минерал кездеседі (кварц, слюда, дала шпаты, саз, ізбес, т. б. ) . Оттегінің өте көп мөлшері химиялық байланысқан, еріген күйінде суда болады. Адам организмінде 65%. Оттекті 1772 жылы швеция ғалымы Карл Шееле ашты. Оттек табиғатта ең көп тараған элемент. Жер қыртысы массасының 47, 2% оттектің үлесіне келеді. Оттек табиғатта бос күйінде де, қосылыс күйінде де кездеседі. Табиғаттағы оттек үш түрлі изотоптан тұрады: 16 8 О, 17 8 О, 18 8 О.
Оттегіні алу әдістері: 1. Сұйық ауаны фракционды айдап;
2. Судың электролизі арқылы: 2H 2 O → электролиз 2H 2 + O 2 .
Зертханада:
1. Оксидтерді термиялық айыру арқылы : 2CrO 3 → t0 2Cr+3O 2 ;
2. Пероксидтерді айыру арқылы: BaO 2 (пероксид) → t0 Ba+O 2 ;
3. Оксоқышқылдар тұздарын айыру арқылы:
2KNO 3 → t0 2KNO 2 +O 2 ;
2KClO 3 → t0 2KCl+3O 2 ;
2KMnO 4 → t0 K 2 MnO 4 +O 2 +MnO 2 ;
Өнеркәсіпте оттекті ауадан алады. Ол үшін ауаны сұйық күйге айналдырады, одан соң буландырады. Өнеркәсіпте таза оттекті суды электролиздеу арқылы алады. Зертханада оттекті кейбір оксидтерді, тұздарды қыздырып ыдырату арқылы алады:
2KClO 3 → 2KCl + 3O 2
2KMnO 4 →K 2 MnO 4 +MnO 2 +O 2
2HgO→2Hg + O 2
Физикалық қасиеттері: O 2 суда аз ериді 100:3. Жер бетінен 100 км жоғары атом күйінде болады, УФ-сәулесі әсерінен айрылады О 2 → фотолиз О+O. О 3 - озон оттегінің аллотропиялық түр өзгерісі, молекуласы диамагнитті. O 2 -түссіз, О 3 - көк түсті газ, полярлығы және полярлануы O 2 -ге қарағанда жоғары. Оттек молекуласы (О 2 ) екі атомнан тұрады. Оттек атмосфералық қысымда және -183 0 С-та сұйыққа айналады. Сұйық оттек көкшіл түсті болады. -219 0 С-та оттек қар тәрізді қатты күйге көшеді.
Химиялық қасиеттері: Оттектің химиялық активтігі тек галогендерден ғана төмен. He+O 2 → жүрмейді; Ne+O 2 → жүрмейді; Ar+O 2 → жүрмейді, басқа барлық элементермен қосылыс түзеді. 3O 2 → эл. разряд 2О 3 . Атмосферада 3O 2 найзағай әсерінен 2О 3 . Озонның химиялық активтігі оттекке қарағанда жоғары.
О 3 +2H + +2e - → O 2 +H 2 O E 0 =+2, 07в
O 2 +4H + +4e - →2 H 2 O E 0 =+1, 23в, соңдықтан О 3 өте күшті тотықтырғыш. Химиялық активтігі бойынша O 2 тек F 2 кейін тұр. Инертті газдар, Pt, Au +O 2 → жүрмейді. Қалған бейметалдар оттегімен әрекеттеседі. Оттегі және бейметалдар айырмашылығы аз болғандықтан, оксидтері ковалентті байланыс түзеді. Соңдықтан бейметалл оксидтері - газдар, ұшқыш сұйықтар, тез еритін қатты заттар. Бейметаллдар оксидтері суда еріп, қышқыл түзеді. СО, NO, N 2 O, SiO тұз түзбейтін оксидтер, суда ерімейді, себебі ол молекулалар өте берік. Бейметаллдар оксидтері қышқылдық қасиет көрсетеді: P 4 O 10 (к) + 6H 2 O(су) = 4H 3 PO 4 ;
SO 3 (г) + H 2 O(с) = H 2 SO 4 ; Cl 2 O 7 (г) + H 2 O(с) = 2HClO 4 . Элементтердің тотығу дәрежесі өскен сайын, олардың қышқылдық қасиеті артады: FeO 3 , CrO 3 , Mn 2 O 7 тағы сол сияқты.
Металдардың оксидтері: негіздік, қышқылдық, амфотерлік болып бөлінеді. Сілтілік және сілтілік - жер металдар оксидтері суда ериді, бұл оксидтерде иондық байланы с болады. Металдардың тотығу дәрежесі өскен сайын оксидтерде коваленті байланыс болады. Егер элемент бірнеше оксид түзетін болса, оның тотығу дәрежесі артқан сайын оксидтердің қышқылдық қасиеті артады.
Оксидтердің жіктелуі . Күрделі қосылыстардың үлкен бір тобы (класы) - оксидтер. Оксидтер үшке бөлінеді: қышқылдық, негіздік, екідайлы (амфотерлі) .
Бейметалдардың оксидтері - қышқылдық оксидтер, ал белсенді металдардың оксидтері - негіздік болып келеді.
Оксидтердің аталуы
Кейбір оксидтер үшін қарапайым (үйреншікті) атаулары бар, олар ертеден қолданылып келеді.
АІ 2 О 3 - глинозем,
SiО 2 - кремнезем.
Оксидтердің алынуы
Оксидтердің алынуының екі үлкен тәсілі бар.
Жай және күрделі заттарды жағу аркылы:
бейметалдарды:
C+O 2 =CO 2
S+O2=SO 2
металдарды:
2Cu+O 2 =CuO
2Mg+O 2 =MgO
күрделізаттарды:
CH 4 +2O 2 =CO 2 +2H 2 O
2H 2 S+3O 2 =2H 2 O+2SO 2
Ерімейтіннегіздер, тұздар, қышқылдарды айыруаркылы:
2Fe(OH) 3 →Fe 2 O 3 +3H 2 O
CaCO 3 →CaO+CO 2
H2SiO 3 →H 2 O+SiO 2
Оксидтерді әрі карай тотыктыру аркылы:
2SO 2 +O 2 =2SO 3
4FeO+O 2 =2Fe 2 O 3
Оксидтердің физикалық қасиеттері
Оксидтер , мысалы:
CuO, CaO, Fe 2 O 3 , P 2 O 5 - қатты заттар;
CO 2 , SO 2 , NO 2 - газдар;
H 2 O, N 2 O 3 (t<0) - сұйық.
:
- Ғе2О3- қызыл-қоңыр,
- CuO - кара,
- Сr2O3- жасыл,
- ZnO, MgO - ақ,
- МnO2- кою қоңыр,
- SnO - кою көк түсті, т. б.
Иістері де әр алуан түрлі болып келеді.
- SО2, SО3, NО2, Р2О5- тұншықтырғыш иісті.
- CO, NO, СО2- иіссіз.
Оксидтердің химиялық қасиеттері
, .
Қышқылдықоксидтердің қасиеттері
Кейбір қышқылдық оксидтерсумен әрекеттесіп қышқылдар түзеді:
Р 2 O 5 +ЗН 2 O=2Н 3 РO 4 ;
SO 2 +H 2 O=H 2 SO 3 ;
СO 2 +Н 2 O=Н 2 СO 3
Мысалы, күлгін лакмус ерітіндісі тамызылған суға көмірқышқыл газын жіберсек, оның түсі күлгіннен біртіндеп қызыл түске өзгереді. Нәтижесінде әлсіз, тұрақсыз көмір қышқылы түзіледі.
Қышкылдық оксидтер негіздік оксидтермен әрекеттесіп тұз түзеді
CO 2 +CaO=CaCO 3
P 2 O 5 =2Na 3 PO 4
Қышқылдық оксидтер сілтілермен әрекеттесіп тұз және су береді
SO 3 +2NaOH=Na 2 +H 2 O
Cr 3 +Ca(OH) 2 =CaCrO 4 +H 2 O
Негіздік оксидтердің қасиеттері
Белсенді металдардың оксидтері сумен әрекеттесіп сілті түзеді
Na 2 O+H 2 O=2NaOH
CaO+H 2 O=Ca(OH) 2
Осы реакциялардың ішінен екіншісін тәжірибе жасап көрсек, яғни, сөндірілмеген әкке су құйып, үстіне бір тамшы фенолфталеин тамызсақ, оның түсі таңкурай түске өзгереді. Ол әрине сілтінің ерітіндісі түзілгендігіне дәлел болады.
Негіздік оксидтер қышқылдармен әрекеттесіп тұз және су түзеді
CaO+2HCl=CaCl 2 +H 2 O
CuO+H 2 SO 4 +H 2 O
Екідайлы оксидтердің қасиеттері
Олар негізінен қатты күйде кездеседі.
1) Қышқылдармен әрекеттескенде негіздік оксидтің қасиетін көрсетеді:
ZnO+2HCl=ZnCl 2 +Н 2 O
2) Сілтілермен . , . (ZnО+H2О=H2ZnО) . Олардың қолданылу аясы өте кең:
ZnО+2NaОH=Na 2 ZnО 2 +H 2 О
cy + тұз = сілті + екідайлыоксид
Оксидтердің қолдануы:
- CO2- тамақөнеркәсібінде (копсытқышретінде) ; өртсөндіруде;
- CaO - сөндірілмеген әк, құрылыста
- ZnO - мырышбояуларыналуда
- Н2О - негізгіәмбебаперіткіш
- Сr2O3- жасылбояуалуда
- SiO2- шыныөндірісінде
Пероксидтер, супероксидтер, озонидтер: Пероксидтер сілтілік, сілтілік-жер металдар оттегіде жанғанда түзіледі:
2K+O 2 → K 2 O 2 , құрамында О 2 2- - анионы бар, тұрақсыз, суда гидролизге ұшырайды, сутек пероксидін түзеді. Сондықтан олар сутек пероксидтерінің тұздары деп саналады.
Супероксидтер сілтілік металдар жоғары қысымда, оттек атмосферасында жанған кезде түзіледі:
К + О 2 → KO 2 , олар тұз тәріздес иондық құрылысты кристалдық заттар. Күшті тотықтырғыштар, сумен қуатты әрекеттесіп, оттек бөліп, ыдырайды. 2КО 2 + 2 H 2 O = H 2 O 2 + 2КОН + О 2 .
Озонның электронтартқыштығы жоғары, сондықтан ол сілтілік металдармен немесе олардың гидроксидтерімен оңай әрекеттесіп озонидтер түзеді:
K + O 3 → KO 3 oзонидтер қызыл түсті, гидролизге түседі.
K+O 2 →KO 2 супероксидтер.
K 2 +O 2 →K 2 O 2 пероксид.
Озон.
Озо́н- химиялық формуласы О 3 болып келетін оттегінің аллотропиялық түр өзгерісі. Түсі қою көк, өткір иісті газ, ал сұйық озон күлгін көк. Озонды 1785 жылы голландия физигі
М. Ван Марумашқан.
Озон тұрақсыз, өздігінен жылу бөліп, оттекке айналады. Күшті тотықтырғыш, алтын мен платинадан басқа барлық металдарды тотықтырып, кейбір органикалық және бейорганикалық қосылыстарға әсеретіп, озонидтертүзеді. Озонды иод-крахмал қағазының түсінің өзгеруі бойынша анықтайды:
O 3 + 2KІ+H 2 O=І 2 (көк) +O 2 +2KOH.
“Кәдімгі оттек КІ-мен реакцияға түспейді. Табиғатта озон найзағай жарқылдаған кезде және кейбір органикалық заттар тотыққанда түзіледі (Озоно сферақабаты) . Таза озон - күштітотықтырғыш, микроорганизмдерді өлтіреді, сол себепті суды, ауаны дезинфекциялауда, күшті тотықтырғыш болғандықтан қағаз ағартуда, т. б. қолданылады.
Физикалыққасиеттері
Молекулалықмассасы - 47, 998 м. а. б.
183 °C-- 1, 71 г/см³
Қайнаутемпературасы−111, 9 °C.
Балқутемпературасы- 197, 2 ± 0, 2 °С .
Озонның газ күйі - диамагнитті, ал сұйықкүйі - әлсіз парамагнитті.
Озон оттектің аллотропиялық түр өзгерісі. Ол табиғатта нажағай ойнағанда, ал зертханада оттекке баяу электр разрядын жіберу арқылы түзіледі:
3О 2 →2О 3
Оттекпен салыстырғанда озонның тотықтырғыштық қасиеті өте күшті, өйткені ол өте активті атом күйдегі оттекті бөле ыдырайды:
О 3 →О 2 + О
Озон оттек әрекеттеспейтін көптеген заттарды тотықтырады. Озонның орагникалық заттарды тотықтыру қасиетін судағы, ауадағы бактерияларды жоюға қолданады.
Сутегі пероксиді.
Сутегі оттегімен судан бөлек пероксид деп аталатын қосылыс түзеді - Н 2 О 2 . Жаратылыста ауадағы оттек түрлі заттарды тотықтырып оксид түзгенде, соған қосалқы зат ретінде сутек пероксиді түзіліп, артынша айырылып жатады. О-О арасындағы байланыс энергия (210 кДж), екі есеге жуық кем. Сутек пероксиді молекуласындағы оттек атомдары полюссіз байланыс арқылы, ал оттек пен сутек атомдары полюсті байланыспен қосылысқан.
Н-О арасындағы байланыстар молекула ішінде симметриясыз орналасқандықтан, сутек пероксиді молекуласы өте полюсті молекула. Н 2 О 2 молекулалары арасында туатын сутектік байланыс берік болып, молекулалар ассоциацияланып жүреді. Сондықтан сутек перексоді қалыпты жағдайда - түссіз, қою сұйықтық (S=1, 44) қайнау температурасы да едәуір жоғары (150, 2 °С) қатуы -0, 43 °С. Н2О2 су сияқты сутектік байланыс түзетіндіктен, сумен кез-келген мөлшерде араласып ериді, ертіндіден кристаллогидрат Н 2 О 2 ·2Н 2 О түрінде (тұрақсыз, T=-52, 0 °С) бөлінеді. Алғаш сутегі пероксидін барий пероксидіне қышқылмен әсер етіп алған:
ВаО 2 +H 2 SO 4 →H 2 O 2 +BaSO 4
Қазір оны алудың бірнеше тәсілі бар:
- Персульфат ионның гидролизі:
H 2 S 2 O 8 +2H 2 O→2H 2 SO 4 +H 2 O 2
- Сутегі жанған кезде қосымша өнім ретінде түзіледі:
H 2 +O 2 →H 2 O 2
- Металдар су қатысып тотыққан кезде:
Zn+O 2 +2H 2 O→H 2 O 2 +Zn(OH) 2
Пероксид молекуласында екі оттегі бірімен-бірі ковалентті байланысқан:
Н - О - О - Н. Ол - түссіз қоймалжын сұйық зат, - 1, 7 0 С-та ине тәрізді кристалл түзіп қатады, сумен, спиртпен кез келген қатынаста араласады. Концентрлі сутегі пероксиді әсерінен қағаз жанып кетеді, ал теріні күйдіреді. Сутегі пероксиді тұрақсыз:
2Н 2 О 2 →О 2 +2Н 2 О
Сутегі пероксидінің судағы ерітіндісі әлсіз екі негізді қышқыл болып табылады, ол екі сатыда диссоциацияланады:
Н 2 О 2 ↔︎Н + +НО 2 - ↔︎2Н + +О 2 2-
Сутегі пероксидінде оттегінің тотығу дәрежесі -1, яғни аралық тотығу дәрежесі. Осыған орай сутегі пероксиді тотықсыздандырғыш та, тотықтырғыш та бола алады.
 Күкірт
- пероидтық жүйенің үшінші периоды және VIA-тобының элементі. Күкірттің электртерістілігі 2, 60-қа тең, оған бейметалдық қасиеттер тән. Сутекті және оттекті қосылыстарында, әр түрлі аниондар құрамында кездеседі, оттекті қышқылдар мен олардың тұздарын, бинарлы қосылыстарды түзеді. Табиғатта химиялық таралуы бойынша он бесінші орында, (бейметалдар арасында жетінші) . Бос күйінде, байланысқан түрлерде кездеседі. Әр түрлі минералдардың, кендер мен тау жыныстары (сульфидтер, сульфаттар), мұнай, көмір құрамына енеді. Табиғи сулар құрамында алтыншы элемент. Жоғары дамыған организмдер тіршілігі үшін маңызды элемент, көп белоктардың құрамы бөлігі, шаштарда шоғырланады. Күкірт көне заманнан белгілі, оны бос күйінде тапқан. Алхимиктерде барлық металдар "тегінің" бірі болып саналған, ол атақты ортағасырлық ғалым Р. Бэконның (XIII ғасыр) еңбектерінде толық жазылған.
Күкірт
- пероидтық жүйенің үшінші периоды және VIA-тобының элементі. Күкірттің электртерістілігі 2, 60-қа тең, оған бейметалдық қасиеттер тән. Сутекті және оттекті қосылыстарында, әр түрлі аниондар құрамында кездеседі, оттекті қышқылдар мен олардың тұздарын, бинарлы қосылыстарды түзеді. Табиғатта химиялық таралуы бойынша он бесінші орында, (бейметалдар арасында жетінші) . Бос күйінде, байланысқан түрлерде кездеседі. Әр түрлі минералдардың, кендер мен тау жыныстары (сульфидтер, сульфаттар), мұнай, көмір құрамына енеді. Табиғи сулар құрамында алтыншы элемент. Жоғары дамыған организмдер тіршілігі үшін маңызды элемент, көп белоктардың құрамы бөлігі, шаштарда шоғырланады. Күкірт көне заманнан белгілі, оны бос күйінде тапқан. Алхимиктерде барлық металдар "тегінің" бірі болып саналған, ол атақты ортағасырлық ғалым Р. Бэконның (XIII ғасыр) еңбектерінде толық жазылған.
Табиғатта таралуы.
Табиғатта күкірт бос күйінде де, қосылыс күйінде де кездеседі. Қосылыс түрінде күкірт сульфидтер және сульфаттар түрінде таралған. Күкірт белокты заттардың құрамына кіретіндіктен өсімдіктер және жануарлар организмдерінде болады. Күкірт мұнайдың да құрамында кездеседі.
Физикалық қасиеттері. Күкірт сары түсті қатты зат. Суда іс жүзінде ерімейді. Ол күкіртті көміртекте, анилинде жақсы ериді, ал спиртте нашар ериді. Күкірт бос күйінде бірнеше аллотропиялық түр өзгерістерін түзеді: ромба тәрізді, моноклинді, пластикалық. Бұлардың ішіндегі кәдімгі температурада ең тұрақтысы ромбалық күкірт. Ромбалық күкіртке табиғи күкірт жатады.
Кәдімгі жағдайда күкірттің молекуласы сегіз атомнан тұрады-S 8 . Қыздырғанда 160 0 С -тан бастап S 6 айналып, 900 0 С-қа дейін S 8 → S 6 → S 4 → S 2 айнала береді, 1500-2000 0 С-та жеке атомдарға айналады.
Химиялық қасиеттері. Химиялық қосылыстарында күкірт -2, +2, +4, +6 тотығу дәрежелерін көрсетеді. Күкірттің тотықтырғыштық қасиеттері оттекке қарағанда төмен. Сондықтан күкірттің басқа заттармен реакцияласу қабілеті қыздырғанда артады. Күкірт көптеген металдармен, металеместермен тікелей әрекеттесіп, оларды тотықтырады. Активтігі өзінен басым металеместермен күкірт тотықсыздандырғыш ретінде әрекеттеседі:
S+Cl 2 →SCl 2
S+O 2 →SO 2
Күшті тотықтырғыштар болып есептелетін күрделі заттармен әрекеттескенде күкірт тотықсыздандырғыш қызметін атқарады:
3S+2KClO 3 →3SO 2 +2KCl
S+2HNO 3 →H 2 SO 4 +2NO
Алынуы. Таза күкіртті бос күйіндегі күкірттен алады. Күкіртті бөгде қоспалардан тазарту үшін оның оңай балқығыштығын пайдаланады. Арнаулы пеште балқыған күкіртті қыздырып қайнатады. Буға айналған күкіртті камерада суытады. Суыған күкірт камераның қабырғасына күкірт түсі деп аталатын ақшыл сарғылт ұнтақ түрінде жиналады. Егер камераны 120 0 С-қа дейін қыздырса, күкірт буы сұйыққа айналады. Оны ағаш қалыптарға құйып таяқша тәрізді күкірт алады.
Күкіртті пиритті ауа қатыстырмай 600 0 С - та қыздыру арқылы шахта пештерінде алады:
FeS 2 → FeS + S
Күкірт қосылыстары
Табиғаттағы күкірт айналымьна физикалық, химиялық факторлармен қатар биологиялық процестерде әсер етеді.
Әдетте күкірт тірі организмдер цитоплазмасында кездеседі. Өсімдік қалдықтары мен жануарлар өлекселері ыдыраған кезде, олардан күкірт бөлінеді. Көбінесе күкірт күкіртті сутек түрінде бөлінеді. Бұл қосылыстың түзілуі құрамында күкірті бар белок заттарының ыдырауына байланысты.
Белокты осындай өзгеріске ұшырататын - шіріту бактериялары. Сонымен қатар күкірттің әр түрлі қосылыстары (50 2 , 50 3 , Н 2 ) түрлі вулкандардың атқылауы кезінде газ күйін-де бөлініп атмосфераға таралады. Топырақта түрлі биологиялық процестер әсерінен пайда болған сутегі құрамында күкірті бар амин қышқылдарын тотықсыздандырады да күкірт сутегін түзеді. Сонымен қатар күкірт сутегі күкірт және күкіртті қышқылдар түздарының сутегі ионының тотықсыздандырғыш әрекеті нәтижесінде пайда болады.
Мұндай тотықсыздану қабілеті, әсіресе күкірт бактерияларынан байқалады. Олардың негізгі өкілдерінің біріне Спириллум десульфуриканс жатады. Ол ұсақ спираль тәрізді таяқша бактерия. Соңғы жылдары жүргізілген зерттеулер күкірт бактерияларының негізінен екі түрі болатындығын анықтады. Оның біріншісі - вибрио, екіншісі - слоровибрио. Олар құрамында органикалық қышқылдар мен спирттер бар ортада жақсы өніп-өседі де күкірт қышқылының тұздары - сульфаттарды оңай тотықсыздандырады. Бұл процесс ауасыз жерде өте қарқынды жүреді.
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz