Уран өндірісінде жұмыс істейтін адамдардағы XRCC1 (Arg194Trp) генінің полиморфизмі мен таралу жиілігі


ҚАЗАҚСТАН РЕСПУБЛИКАСЫ БІЛІМ ЖӘНЕ ҒЫЛЫМ МИНИСТРЛІГІ
ӘЛ-ФАРАБИ АТЫНДАҒЫ ҚАЗАҚ ҰЛТТЫҚ УНИВЕРСИТЕТІ
Биология факультеті
Генетика және молекулалық биология кафедрасы
БІТІРУ ЖҰМЫСЫ
Уран өндірісінде жұмыс істейтін адамдардағы ДНҚ репарациясы
генінің полиморфизмі
Орындаған
4 курс студенті: Манат Есбол
(қолы, күні)
Ғылыми жетекшісі
б. ғ. к. Бекманов Б. О.
(қолы, күні)
Норма бақылаушы: Сатылған И. Ә.
(қолы, күні)
Кафедра меңгерушісінің
рұқсатымен қорғауға
жіберілді, б. ғ. д Айташева З. Ғ.
(қолы, күні)
Алматы, 2010
РЕФЕРАТ
Бітіру жұмысы 24 беттен, 6 сурет, 2 кестеден және 25 әдебиеттер тізімінен тұрады.
Кілтті сөздер: Радиациялық сәулелердің адам организіміне әсері, радиацияның әсерінен ДНҚ молекуласының бұзылыстары, ДНҚ молекуласының репарациясы, репарация процесіне қатысатын генінің полиморфизімі.
Өзектілігі: Уран өндірісінде жұмыс істейтін адамдардағы ДНҚ молекуласының репарация процесіне катысатын гендерінің полиморфизмін зерттеу нәтижесінде, адам организміндегі репарациялық процестердің механизмдерін қарастыру.
Зерттеу объектісі: Уран өндірісінде ұзақ уақыт жұмыс істеген адамдардың қан үлгілері алынды. Бұл қан үлгілері Жалпы генетика және цитология институты молекулалық генетика лабораториясында мұздатқыштарда (-20 0 С) сақталған.
Қолданылған әдістер: Қан үлгілерінен ДНҚ молекуласын бөліп алу, агароздық электрофорез, полимеразды тізбекті реакция және рестрикциялық талдау әдістері.
Жұмыстың мақсаты: Уран өндірісінде жұмыс істейтін адамдардағы ДНҚ молекуласының репарциясына қатысатын XRCC1 геннің таралу жиілігін және полиморфты жағдайын анықтау.
Жұмыстың міндеті: Осы жұмыс барысында қан үлгілерінен ДНҚ-ны бөліп алу, агароздық электрофорез, полимеразды тізбекті реакция және рестрикциялық талдау әдістерін игеру.
Қортынды: Әдебиетке шолу мен зерттеу нәтижелерінен төмендегідей қортынды жасалынды: Зерттеуге алынған уран өндірісінде жұмыс істейтін адамдардың ДНҚ молекуласының репарациясы процесіне қатысатын XRCC1 Arg194Trp генінің адам популяциясында қалыпты варианттарының таралу жиілігі басым, ал мутантты аллелінің таралу жиілігі аз шамада болады. Осылайша уран өндірісінде жұмыс істейтін адамдардағы ДНҚ молекуласының репарациясына қатысатын генінің полиморфизімі анықталды деп қорытынды жасауға болады.
Глоссарий
Радиация - Электромагниттік немесе корпускулалық сәуле, заттарға тікелей немесе жанама әсер ететін, табиғаты жағынан иондар, фотондар, атом бөлшектері немесе нейрондар тәрізді, жоғары энергияға ие иондаушы сәулелер.
ДНҚ - дезоксирибонуклеин қышқылы. Тірі организімнің белгілерінің тұқым қуалу және өзгергіштігі туралы негізгі ақпарат жазылған хромосоманың бір бөлігі.
Репарация - ДНҚ молекуласының әртүрлі себептермен пайда болған бұзылыстардың қалпына келу барысы.
Полиморфизім - белгілі бір геннің ДНҚ молекуласындағы орналасу (полиморфты) жағдайы.
Ген- белгілі бір белгі туралы ақпарат жазылған ДНҚ-молекуласының бір бөлігі.
Мазмұны
10
1. 2. 3 ДНҚ молекуласының репарациясына қатысатын гендерге
сипаттама
12
15
3. 1Уран өндірісінде жұмыс істейтін адамдардағы ДНҚ-репарация
генінің полиморфизмі
Кіріспе
Әлемде адамзат пайдаланатын энергияның белгілі мөлшері атомэлектр станцияларынан келетіні белгілі. Онда негізгі шикізат ретінде уран қолданылады, уранның аз мөлшердегі көлемі жоғары қуатты энергия берумен ерекшеленеді. Сол үшін уран өндірісі соңғы жылдары жоғары қарқынмен дамуда.
Қазақстанда уранның жоғары мөлшерде индустриалды мөлшері жинақталған. Онда уранның 2 миллион тонна табиғи қоры жинақталған. Осы күнге дейін оның 925 мың тоннасы игерілген, бұл дүние жүзі бойынша сақталған уран запас қорының 25% құрайды.
Бірақ in vitro жағдайында өсірілген адам және жануарлар клеткаларына жасалған көптеген зерттеулер уранның токсикалық қасиетеке ие екендігін дәлелдеген. Демек, уран өндірісінде жұмыс істейтін адамдардың денсаулығына кері әсерін тигізеді.
Тікелей иондаушы сәулелер әсерінен ДНҚ молеклуласының атомдары арасындағы байланыс бұзылады. Бұзылыс көбінесе қант пен фосфат арасындағы байланыста байқалады, сөйтіп ДНҚ молекуласының біртұтастығы бұзылады. Сонымен бірге ДНҚ молекуласында радиацияның әсерінен үнемі өзін-өзі реттей алмайтын атомдарының аралық байланыстарының үзілісі болып тұрады. Бұл бұзылыстарды тек күрделі ферменттік жүйенің көмегімен ғана реттеуге болады. ДНҚ бұзылысын реттейтін осы ферменттік жүйенің ашылуы радиобиологияның басталуы болып табылады. Белокты кодтайтын құрылымдық гендердің репарациялануында бұл жүйенің атқаратын рөлі өте жоғары.
Осыған байланысты менің бітіру жұмысымдағы негізгі мақсат уран өндірісінде жұмыс істейтін адамдардың қан үлгісінен ДНҚ молекулысын бөліп алып, агароздық электрофорез арқылы сапасын анықтау, полимеразды тізбекті реакция және рестрикциялық талдау әдістерін пайдаланып уран өндірісінде жұмыс істейтін адамдардағы ДНҚ молекуласының репарация процесіне қатысатын XRCC1 генінің таралу жиілігін және полморфты жағдайын анықтау болып табылады.
1 Негізігі бөлім
1. 1 Қазақстандағы уран өндірісі
Қазақстанда уранның жоғары мөлшерде индустрияльды мөлшері жинақталған. Онда уранның 2 миллион тонна табиғи қоры жинақталған. Осы күнге дейін оның 925 мың тоннасы игерілген, бұл дүние жүзі бойынша сақталған уран запас қорының 25% құрайды (1-кесте) . Ақмола облысында және Солтүстік Қазақстан облыстарында 40 жылдан бері тау - кен байыту өнеркәсібі мен уранды қайта өңдеу өнеркәсібі жұмыс істейді. Ең үлкен уран қазу комплексі Степнагор қаласында (Ақмола облысы) орналасқан. Осы өндіріс ошақтарының маңайына әртүрлі радиоактивті зиянды қалдықтар жинақталған. Осындай ашық сақталған қалдықтар қоршаған ортаны ластауда (1 кесте) [1] .
1 Кесте
(А) 2007-жылдағы әлемдегі сақталған уран қоры, World Nuclear Association[WNA] және European Nuclear Society[ENS] санағы. (Б) 2006-жылғы уран өндірісі(тонна) British Geological Survey. [Б] санағы [2] .
(тонна)
(Б) Кестеден 2006-жылғы әлемде өнділген уранның мөлшерін және (А) кестеден 2007-жылғы әлем еледерінде сақталған уранның қалдық қорын көруге болады. Қазақстан Республикасы әлем бойынша уранның қоры бойынша Австралиядан кейінгі екінші орынды алады. Сонымен бірге кестеден Қазақстандағы уран өндірісінің жоғары дәрежеде дамығандығын және оның мөлшерін салыстырмалы түрде білуге болады.
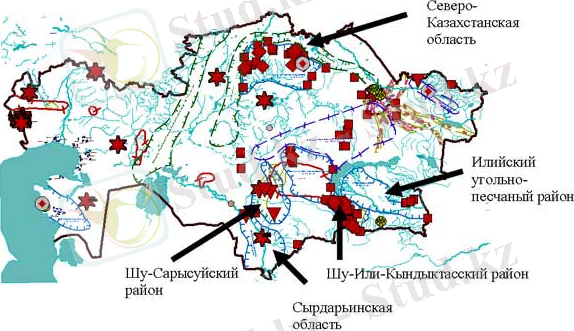
1 Cурет. Қазақстандағы уран өндіріс ошақтары мен уранға бай өңірлер және атом бомбасы жарылған өңірлер [2] .
1- cуреттен Қазақстандағы уранның негізгі таралған өңірін және өндіріс ошақтарын көруге боады. Ең көп уранның қалдық қоры Солтүстік Қазақстанда және Шу-Іле-Кіндіктас аудандарында жинақталған. Қазақстандағы уран өндірісімен шұғылданатын компания ол - Ұлттық Атом компаниясы (Казатомпром) . Аталған компания өз жұмысын ең алғаш Қырғызстанда бастаған, кейін Қазақстанда уран өндіре бастады [2] .
- Уран элементінің адам организміне тигізетін зияны
In vitro жағдайында өсірілген адам және жануарлар клеткаларына жасалған көптеген зерттеулер уранның токсикалық қасиетеке ие екендігін дәлелдеген. Уран өндірісінде жұмыс істеген, сол облыста тіпті көрші облыстарда тұрып жатқан тұрғындардың барлығы әртүрлі мөлшерде токсикалық бөлшектер әсеріне ұшырауы әбден мүмкін.
Уран өндірісінде жұмыс ісетеген адамдардың қанының лимфоциттеріне жүргізілген зерттеулер мен маркерлік гендер көмегімен жасалған анализдер бұл мәлметті растайтындығы анықталған.
Хромосомалық аутқуларға анализ жасау популяцианы бақылауда биологиялық белгілер ретінде қолданылады. Бұл биологиялық белгілер хромосомалық аутқулардың денсаулыққа қандай әсері бар екендігін зерттеуде өте маңызды [3] .
Сонымен бірге уран элементінің адам организіміне әртүрлі дәрежеде кері әсерінің бар екендігі, соның нәтижесінде көптеген аурулардың пайда болатындығы: тері аурулар, қатерлі ісік, жүрек қантамыр аурулары, нерв әлсіздігі, т. б. Толығырақ уран элементінен бөлінетін радиацияның әсерінен туындайтын ауруларды төмендегі мәліметтен көруге болады.
- Радиация әсерінен туындайтын аурулар
Өте күшті сәулелі ауру. Ол жалпы органзизімнің бірнеше рет қатты сәулеге шалдығуынан болады. Ол бірнеше факторларға байланысты. Сәулеге шалдығудың түрі жалпы немесе нақты бір жерінің сәулеге шалдығуы деп бөлуге болады.
Сәулелі аурудың өзі: қатты сәулелі зақымдану және созылмалы сәулелі зақымдану болып екіге жіктеледі. Қатты сәулелі ауруды 3 кезеңге бөледі. Олар: қалыптасу кезеңі, қайта қалпына келу кезеңі, салдары және нәтижесі.
Иондаушы сәулелер әсерінен пайда болатын аурулар:
- Жіті және созылмалы сәулелік аурулар;
- Сәулелік катаракта;
- Сәулелік дерматит және күйіктер;
- Сәулелік гипотиреоз;
- Сәулелік аутоиммундық тиреодит.
2. Қатерлі жаңа өскіндер:
1) Жіті лейкоз;
2) Созылмалы лейкоздар және миелодиспластикалық синдром (созылмалы лимфолейкозды қоспағанда) ;
3) Қатерлі лимфомдар;
4) Қомақты қатерлі жаңа өскіндер (өкпе, қалқанша безі, сүт безі обыры, несеп-жыныс жүйесінің, асқазан-ішек жолдары мен гепатобиллиарлық жүйенің қатерлі ісіктері және т. б. )
3. Жалпы соматикалық аурулар:
1) Қалқанша безі аурулары (аутоиммундық тиреоидит, диффуздық түйнді зрб) ;
2) Қан және қан өндіу жүйесі аурулары (агралоцтрз, гипопластикалық және апластикалық анемия ) ;
3) Жүрек қан тамыры жүйесі аурулары (жүректің ишемиялық ауруы, гипертрниялық ауру) ;
4) Жүрек-бұлшық ет жүйесінің дегенерацялық-дистрофиялық зақымдануы (инфекфиялық және жарақаттану генезінен басқа) ;
4. Туа біткен аурулар даму кемістіктері:
1) Олигофрения;
2) микроцефалия;
3) Алдыңғы бас сүйектің және сүйек-бұлшық ет жүйесінің даму кемістіктері [4] .
1. 2 ДНҚ молекуласының радиация әсерінен бұзылулары
Тікелей иондаушы сәулелер әсерінен ДНҚ молекуасының атомдары арасындағы байланыс бұзылады. Бұзылыс көбінесе қант пен фосфат арасындағы байланыста байқалады, сөйтіп ДНҚ молекуласының біртұтастығы бұзылады. Егер бұзылыс ДНҚ молекуласының бір тізбегінде болса онда ондай бұзылысты бір тізбекті бұзылыс деп, ал бұзылыс бір нүктеде қарама-қарсы екі тізбекте бірдей болса оны қос тізбекті бұзылыс деп атаймыз. Әдетте бір тізбекті бұзылыстар тек иондаушы сәулелер әсерінде ғана емес, сонымен бірге ДНҚ молекуласының жылулық тұрақсыздығы салдарынан да, кейбір тотықтырғыштар мен ферментативтік процестер салдарынан да болуы мүмкін. Сонымен бірге иондаушы сәулелер әсерінен пайда болған бір тізбекті бұзылыстар кейбір ішкі себептер әсерінен өзінің екінші тізбегінде бүлдіруі мүмкін. Осылайша ДНҚ тізбегінде көптеген үзілген аймақтар пайда болуы мүмкін. Мұндай жағдайда олардың реттелуі тіпті де қиындай түседі [5] .
Екі тізбекті бұзылыстар бір тізбекті бұзылыстың қарама-қарсы тізбегін бүлдіруіне ұқсайды. Сол себепті бір уақтта екі тізбектің бұзылысы салдарынан клетканың кішкентай көлемінде көп мөлшерде энергия жиналады. Тіпті сирек иондаушы сәулелердің өзіде клеткаға әртүрлі мөлшерде энергия бөледі. Атомның әртүрлі көлемде бөлінуіне байланысты оларда бірнеше электрон-вольттан бірнеше жүздеген электрон-вольт энергия болады. Көп жағдайда иондаушы сәулелердің үлкен мөлшерімен әсер еткенде атом не молекула әртүрлі көлемде бөлінсе, кей жағдайда ДНҚ молекуласы бірдей ұзындыққа бөлінуі мүмкін. Зақымдау көзі азайған сайын олардың атомдарды микрокөлемге бөлу қабілеті арта түседі. Сол себепті екі тізбекті бұзылысқа иондаушы сәуленің дозасы көбірек болады.
Қантты-фосфт байланысындағы атомдардың арасындағы байланыстың бұзылыуы ДНҚ молекуласының біртұтастығын, ондағы генетикалық ақпараттың сақталуына және ДНҚ - ның қалыпты репликациясына кедергі келтіреді. ДНҚ молекуласының қаңқасының бұзылуы дезоксирибозаның қаңқасын құруға қатыспайтын атомдарының бұзылуымен қатар келуі мүмкін. Егер бұзылыс дезоксирибозаның ДНҚ қаңқасына қатыспайтын бөлігінде болса онда ондай бұзылысты нуклеотидтағы бұзылыс деуге болады. Егер пурин немесе пиримидин негіздері арасында болса оны негіздің бұзылуы деп атаймыз. Негіздің немесе нуклеотидтың бұзылуы химиялық өзгерісті тудырады. Мысалы гуаниннің тотығуы нәтижесінде 8-гуанин тотығы түзіледі. ДНҚ молекуласын атқылайтын судың жоғары активті радикалы негіздердің өзгеруін тудырады. Мысалы: OH * радикалы мен тимин қосылып тимингликол түзіледі.
Кей жағдайда ДНҚ бұзылысы өздігінен қалпына клесе, көп жағдайда репарациялық ферменттер көмегімен реттеледі. Бірақ репарация барлық бұзылыстарды қалпына келтіруге қабылеті жоқ. Өйткені бұзылыс өте көп болған жағдайда бұзылыс аймағындағы бос ұштардың, қарама-қарсы тізбектің бос ұштары арасында, әр жерде пайда болаған бұзылыстардың бос ұштары арсында тіпті басқа ДНҚ молекуласының бұзылысы салдарынан пайда болған бос ұштары арасында өзара ретсіз байланысуы мүмкін. Бұндай дұрыс болмаған ретсіз байланыстар салдарынан ДНҚ молекуласының ширатылуы қатая түседі. Кейде бұзылыс болғаннан кейін пайда болған бос ұштары маңайындағы белоктармен «тігіледі», соның салдарына тіпті хромосомалардың да құрылысында өзгеріс болады.
Негіздердің дұрыс емес репарациясы және олардың химиялық өзгерістері жұптаспайтын негіздер деп аталатын ДНҚ молекуласының тағы бір бұзылысын пайда қылады. ДНҚ молекуласында тек комплементарлы негіздер аденин-тимин және гуанин-цитозин жұптасады. Олардың біреуінің орнының алмасуы генетикалық кодтың өзгеруін пайда қылады. Жоғарыда гуаниннің тотығуы салдарынан 8-гуанин тотығы түзілуін айттық, ДНҚ репликациясы кезінде синтезделіп жатқан тізбектің гуанинге комплементарлы цитозин болса, ал 8- гуанин тотығына аденин келіп жалғанады. Кейін иРНҚ синтезі барысында генетикалық кодтың жеткізілуінде жаңылыс болады, сөйтіп ең соңында белок синтезі барысында аминқышқылдар қатарында жаңылыс пайда болады. Сонымен бірге қате жұптасқан негізде ДНҚ молекуласының кеңістік құрылымында өзгертеді.
Сирек иондаушы сәулелердің 2 гр дозасында адамның әртүрлі ткандарының 10-90% клеткасы бұзылысқа ұшырайды. Бір клетканың ДНҚ молекуласында 2000 ға жуық бір тізбекті, 80 ге жуық екі тізбекті бұзылыс пайда болса, 1000 ға жуық негіздің бұзылуымен қатар 300 дей құрылымы өзгерген негіздің белоктармен байланысуы байқалады. Оның үстіне дәл осы бұзылыстардың радиоактивтілігі ұзақ уақыт сақталады . Әрі клетка бөлінуі арқылы ұрпаққа беріліп, өзінің зияндаушы әсерін ұрпақтан-ұрпаққа беріп отырады [5, 6] .
1. 2. 1 Эксцизионды репарация
Эксцизионды репарация бірнеше ферменттің көмегімен іске асады. Бірінші кезеңде эндонуклеаза ферменттері ДНҚ молекуласындағы қателікті тауып оны үзеді. Мұның нәтижесінде ДНҚ тізбегінде тесік пайда болады. Осыдан кейін ДНҚ ның бос ұштарын экзонуклеаза ферменттері таниды да тізбекті ары қарай үзіп тесікті кеңейтеді. Мысалы, тимин димерлерінен басқа жүзге жуық басқа нуклеотидтер үзіледі. Полимераза ферменті мутациялық өзгерісі жоқ екінші тізбекті матрица ретінде пайдаланып, жалаң тізбектің синтезін немесе үзілген фрагменттің екінші синтезін іске асырады. Соңында лигаза ферменті жаңа синтезделген тізбекті басқа тізбекпен жалғайды [7] .
Эксцизионға негізделген жолымен BER репарация. BER системасы бұзылған нуклеотид бірлігін бұзылмаған нуклеотидпен алмастырады. Түрлі ішкі және сыртқы факторлардың, ионданушы радиацияның, алкилдеуші және қышқылданудың нәтижесінде ДНҚ-ның бұзылуы жүзеге асады. Бұл бұзылған ДНҚ репарациясына BER жолы қолданылады. Эксцизионді негізге ала отырып репарация жолы ДНҚ-ның аз бұзылған бөлігіне қолданатын негізгі жүйе. Мысалы, тотығу немесе тотықсыздану және ірі емес ДНҚ-аддукты. BER ДНҚ құрылымын бұзуға спецификалық гликозилазаны қолданып, ДНҚ-ның бүлінген аймағын таниды, сол бүлінген аймағымен байланысып, соңында осы бүлінген негізді жояды. Азоттық негізден айрылған аймақ эндонуклеазамен танылып, қант қалдығын жояды. Бос аймақ ДНҚ-лигазаның көмегімен толтырылады. BER-дің келесі репарациялық фазасында пуриндеуші және пиримидиндеуші эндонуклеаза, полинуклеотид киназа, ДНҚ- полимераза ферменттері және XRCC1, XRCC3, т. б. гендерінің аймақтары қатысады.
XRCC1 және XRCC3, ИС және алкилдеуші агенттердің көмегімен түзілген ДНҚ үзілімдерінің репарациясына қатысады. XRCC1, XRCC3 гендері полиморфты болып есептелінеді және полиморфты генотиптердің активтілігі кеңінен зерттелуде [8] .
1. 2. 2 ДНҚ молекуласының біртізбекті және қостізбектегі үзілісінің репарациясы
ДНҚ молекуласында радиацияның әсерінде үнемі өзін-өзі реттей алмайтын атомдар аралық байланыстарының үзілісі болып тұрады. Бұл бұзылыстарды тек күрделі ферменттік жүйенің көмегімен ғана реттеуге болады. ДНҚ бұзылысын реттейтін осы ферменттік жүйенің ашылуы радиобиологиялық зерттеудің басталуы болып табылады. Белокты кодтайтын құрылымдық гендердің репарациялануында бұл жүйенің атқаратын рөлі өте жоғары [9] .
ДНҚ молекуласының қарапайым бір бізбекті бұзылыстары ДНҚ лигазамен аласталады. Ол қантты-фосфаттық қаңқадағы атомдар арасындағы байланысты қалпына келтіреді. Сәуленің әсері кезінде бір тізбекті бұзылыс болумен қатар дезоксирибозаның құрамында да күрделі бұзылыс болады немесе негізде жоғалуы мүмкін. Бұндай жағдайда ДНҚ тізбегінің қалпына келуі ДНҚ лигазаның көмегімен емес, одан күрделірек процесс нуклеотидттердің эксцизиондық репарациясы көмегімен жүреді [10] .
ДНҚ-ның бір тізбектік бұзылыстарының репарациясы әрі тез, әрі нәтижелі өтетін процес. Ал екі тізбекті бұзылыстарының репарациясы күрделі және төмен нәтижелі болумен қатар қателіктері де кездеседі. Қос тізбектің репарациясы гомолокты емес соңдарының жұптасуының гомолокты рекомбинациясы арқылы жүреді (сурет 2) . Репарацияның бұл түрі циклдің барлық стадиясыда жүреді. Бірақ тізбектің үздіксіздігінің қалпына келуіне бұл жеткіліксіз болады. Өйткені тізбектің дұрыс болмаған құрылымы салдарынан хромосоманың да құрылымында өзгеріс пайда болады.
Гомолокты рекомбинация жолымен репарациялануы сәулелену кезінде клетканың S-периодының соңы мен G 2 -периодында жүреді. Демек осы период ішінде бұзылысқа ұшыраған ДНҚ тізбегі қалпына келіп үлгіреді. әрі бұл процеске гомолокты негіздер қатары бар басқа ДНҚ молекуласы да қатысады. Қайта құрылатын ДНҚ бөлшегіндегі екі бұзылыстың ортасында кемінде 200 жұп нулеотид болу керек. ДНҚ -ның бұзылысы бар соңы қайта құрылуы үшін бұзылысы жоқ гомологымен байланысып оны матрица ретінде пайдалана отырып жеткіліксіз ДНҚ бөлімшесін синтездейді. Осыдан кейін жаңа тізбек лигазаның көмегімен негізгі тізбекке «тігіледі».
ДНҚ молекуласының жоғары дәрежеде ширатылуы мен ДНҚ молекуласы репарация қателіктері үзіліске ұшыраған ДНҚ фрагменттерінің қайта қалпына келуіне кедергілік жасайды. Тіпті ДНҚ молекуласының ұзына бойына қайта құрылуында екі түрлі ДНҚ молекулаларының немесе жақын
жатқан басқа хромотиндер мен хромосомалардың кейбір бөліктері бірігуі мүмкін.
Гликозилазамен жойылуы Геликазамен тарқатылуы
Эндонуклеазамен кесілуі Эндонуклеазамен кесілуі
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz