Биологиялық химия: оқу лекциялары жинағы


Ф. 7. 11-19

УРМАШЕВ Б. А., ЕРМАХАНОВ М. Н., САБДЕНОВА Ұ. Ө.
БИОЛОГИЯЛЫҚ ХИМИЯ
Лекция жинағы

Шымкент, 2017 ж.
ҚАЗАҚСТАН РЕСПУБЛИКАСЫНЫҢ БІЛІМ ЖӘНЕ ҒЫЛЫМ МИНИСТРЛІГІМ. ӘУЕЗОВ атындағы ОҢТҮСТІК ҚАЗАҚСТАН МЕМЛЕКЕТТІК УНИВЕРСИТЕТІ
«Химия» кафедрасы
УРМАШЕВ Б. А., ЕРМАХАНОВ М. Н., САБДЕНОВА Ұ. Ө.
БИОЛОГИЯЛЫҚ ХИМИЯ
Лекция жинағы
Шымкент-2017жӘОЖ546. (083. 13)
Құрастырушылар: Урмашев Б. А., Ермаханов М. Н., Сабденова Ұ. Ө.
«Биологиялық химиядан» пәнінен лекция жинағы. - Шымкент: М. Әуезов атындағы ОҚМУ, 2016. - 67 бет.
Лекция жинағы оқу жоспарының және «Биологиялық химия» пән бағдарламасының талаптарына сәйкес құрастырылған және студенттер үшін қажетті жүйеленген мәліметтерді қамтиды.
050112 - Химия мамандығы бойынша оқитын студенттерге арналған.
Лекция жинағында Биологиялық химия курсының бағарламасында қарастырылғын материалдың оқу жүйесі берілген.
Пікір жазғандар:
Жатқанбаев Е. Т. - т. ғ. к., М. Әуезов атындағы ОҚМУ
“Химия”кафедрасы
Шағраева Б. -х. ғ. к., ОҚМПИ «Химия» кафедрасының доценті
«Химия» кафедра мәжілісінде № 6 хаттама, 18. 05. 2017 және Жаратылыстану педагогикалық факультетінің әдістемелік комиссиясында қарастырылған және баспаға ұсынылған
№ 11 хаттама «_25_»__05_2017 ж.
Баспаға М. Ауезов атындағы ОҚМУ-нің оқу-әдістемелік кеңесі ұсынған
№ хаттама «» 201 ж.
© М. Әуезов атындағы Оңтүстік Казахстан мемлекеттік университеті, 2017 ж.
Шығаруға жауапты: Урмашев Б. А.
№ 1-ші дәріс
Дәрістің тақырыбы: Кіріспе. Биохимия пәні.
Жоспар:
1. Биологиялық химия тірі ағзадағы заттардың химиялық табиғатын зерттейтін ғылым.
2. Биохимияның зерттейтін нысандары және зерттеу әдістері.
3. Заманауи биохимияның өз бетінше ғылым ретінде негізгі қалыптасу кезеңдері.
1. Биологиялық химия тірі ағзадағы заттардың химиялық табиғатын зерттейтін ғылым.
Биологиялық химия - тiрiағзаның құрамына кiретiн химиялық табиғи заттардың құрылысын, өзгерiсiн және тiрi материяда болатын химиялық реакцияларды зерттейтiн ғылым.
Тiрi ағза жасушаларында барлық биохимиялық құбылыстар физикалық және химиялық заңдылықтарға сәйкес жүредi. Сондықтан да биохимия физикалық және химиялық заңдылықтарға сүйене отырып, тiрi ағза жасушасының сапалық өзгерiстерiн, құрылыстарын, сыртқы ортамен байланысын, яғни зат және қуат алмасу ерекшелiгiн зерттейдi. Сонымен қатар биохимия тiрi ағзадағы химиялық құбылыстарды басқару, игеру жолдарын табуға көмектеседi.
Биохимия үш бөлiмнен тұрады:
1. Статистикалық биохимия - ағзаның химиялық құрамымен шұғылданады.
2. Динамикалық биохимия - ағзадағы заттар мен энергия алмасудың өз ара байланысын зерттейдi
3. Функционалдық биохимия - ағзаның құрамындағы мүшелердің қызметiн қамтамасыз ететiн химиялық өзгерiстердi зерттейдi. Осы бөлiмге спорттық биохимия да жатады.
2. Биохимияның зерттейтін нысандары және зерттеу әдістері.
Зерттеу нысандарына байланысты биохимия адам биохимиясы, жануарлардың биохимиясы, өсімдіктер биохимиясы және микробтардың (микроағзалардың) биохимиясы болып жіктеледі. Себебі барлық тіршліктің биохимиясының бірдей болуына қарамастан, тірі жануарлардың және өсімдіктердің ағзаларында зат алмасулар ерекшеленеді. Зат алмасу немесе метаболизм - ағзада жүретін барлық химиялық реакциялардың жиынтығы. Бұл реакциялар тірі жүйелердің сақталып және өздігінен байта өсуі үшін бағытталған. Бұл үрдіс миллиондаған жылдар бойында қалыптасқан. Өсімдіктердің өздерінің денелеріндегі күрделі заттарын (көмірсулар, майлар, ақ уыздар) су, көмірқышқыл газы, минералдық заттар сияқты қарапайым заттардан түзетіндігі белгілі. Ал осы синтез үшін қажет энергия жарықты сіңіру есесінен жүреді ( фотосинтез үрдісі) . Ал, тірі ағзалар болса, керісінше, олар су мен минералдық заттардан басқа, күрделі заттарды да - ақуыздар, майлар, көмірсулардан құралған коректі қажет етеді. Тірі жануарлардың ағзаларында тіршілік үшін және олардың денесіндегі заттардың синтезі үшін белгілі мөлшерде энергия қажет. Бұл энергия күрделі органикалық заттардың ыдырауы немесе тотығуы кезінде бөлінген химиялық энергияның (химиосинтез) есесінен қамтамасыз етіледі. Мысалы:
С 6 Н 12 О 6 → 2С 3 Н 6 О 3 + 210 кДж/моль
Глюкоза сүт қышқылы
Осы энергияның шамамен 126 кДж жылу түрінде таралады, ал 84 кДж АТФ молекуласында фосфаттық байланыстарда энергия түрінде жиналады.
Органикалық заттарды қорек ретінде пайдаланбайтын өсімдіктер аутотрофты ағзалар болып табылады. Ал, жануарлар гетеротрофтық ағзалар болып табылады. Микробтардың арасында аутотрофтық та, гетеротрофтық та зат алмасу түрлері кездеседі. Сонымен бірге микробтар олардағы заттардың және реакциялардың кең шеңберімен сипатталады. Бұл реакциялар және заттар жануарларда және өсімдіктерде кездеспейді.
Зерттеу әдістері:
-экстракциялау; диализ; кристалдау;
-гомогенизациялау; Фракциялау; хроматографиялау;
-электрофорез; фильтрациялау; гель-электрофорез.
-изотоптық; аналитикалық-дезинтеграциялық;
3. Заманауи биохимияның өз бетінше ғылым ретінде негізгі қалыптасу кезеңдері.
Заманауи биохимияның өз бетінше ғылым ретінде негізгі қалыптасу кезеңдері ХІХ-шы және ХХ-шы ғасырларға жақын. Осы көрсетілген уақытқа дейін қазіргі кездегі биохимияның қарастыратын сұрақтарын органикалық химия және физиология әр тұстан зерттеді. Орта ғасырларда (ҮІІІ - Х) Европада алхимияның дамуына байланысты анағұрлым күрделі органикалық заттардың құрамы туралы нақты материал бірте-бірте жинақтала басталды. Алайда, орта ғасырдағы алхимиктердің жинаған мәліметтері сол кездегі ғылымда үстемдік алған ой-тұжырымдармен сәйкестік таппады.
ХҮІ - ХҮІІ ғасырларда алхимиктердің жинақтаған білімдерін ятрохимиктер ( iatros - дәрігер , грек тілінен аударғанда) өз еңбектерімен жалғастырды және ары қарай дамытты. Осы ятрохимияның көрнекті өкілдерінің бірі Парацельс болды. Парацельс - неміс дәрігері және жаратылыстанушысы. Ол химияның және медицинаның арасындағы тығыз байланыстың бар екендігі туралы батыл әрі прогрессивтік қағиданы айтты. Ол адамның тіршілік етуінің негізінде химиялық реакциялар жатыр, адам ауырған кезде әр түрлі реакциялар бұзылатындығын, ауруладың түрлерін емдеу үшін химиялық заттарды дәрі ретінде пайдалану керектігін айтты.
ХҮІІ-ші ғасырдың ятрохимигі И. Ван-Гельмонт ең алғашқылардың бірі болып, тірі денедегі «сөлдердің» құрамында ерекше заттардың - «ферменттердің» болатындығын, осы заттардың химиялық өзгерістерге қатысатындығы туралы қағиданы айтты.
Алайда, химиялық және ферментативтік реакциялардың заңдылықтарын түсіну ятрохимиктер үшін шешімі жоқ жұмбақтардың бірі болып қала берді. Оның себептері:
-физиканың және химияның негізгі заңдарының болмауы;
-органикалық заттардың және қосылыстардың элементтік құрамын анықтайтын әдістер мен тәсілдердің дамымауы;
-сонымен бірге, ятрохимиктер алхимиктер сияқты дүние танымы бойынша метафизиктер болды және олардың басым көпшілігінде виталистік көзқарас басым болды.
ХҮІІ - ХҮІІІ -шы ғасырлардың аралығында ғалымдардың арасында жану негізінің теориясы - флогистон кең қолданысқа ие болды. Оны негіздеген немістің химигі және дәрігері Шталь болды. Бұл теорияның негізгі қағидалары қате болды. Алайда, ғылымның дамуында оның қосқан үлесі болды. Яғни, эксперименттік бағыттағы жұмсытарға бастау болды. Бұл теорияға сәйкес зат жанған кезде белгісіз бір ерекше салмағы жоқ зат бөлінеді екен. Бұл теорияның кемшілігін Ломоносов пен Лавуазье өздерінің еңбектерінде көрсетті. Олар материяның (массаның) сақталу заңын ашты және бекітті. Сонымен бірге, Лавуазье тыныс алғанда оттегінің жұтылатыны, ал тыныс шығарғанда көмір қышқыл газының бөлінетіндігін көрсетті.
ХҮІІІ-шы ғасырдың екінші жартысынан бастап көптеген жаңа органикалық заттар табылып, бөлініп алына бастады. Оларды өсімдіктерден және жануарлардан бөліп алды. ХҮІІІ-ші ғасырдың екінші жартысындағы ең ірі жаңалықтардың бірі - Реомюрдің және Спалланцанидің асты қорыту физиологиясы бойынша зерттеулері. Бұл зерттеулер ас қорыту сөлдерінің ферменттерін зерттеуге бастама болды. Орыстың химигі К. С. Кирхгоф 1814 жылы крахмалдың өнген арпаның сығындысының (амилазаның) әсерінен қантқа айналуын сипаттады. ХІХ-шы ғасырдың ортасына таман басқа да ферменттер сипатталды: ауыз қуысының сөлі амилаза, асзан сөлінің пепсині, асқазан асты безінің сөлі трипсин. Берцелиус химияға катализ және катализаторлар ұғымдарын енгізді. Соңғылардың қатарына сол кездегі белгілі болған ферменттердің барлығы жатқызылды. 1839 жылы Либих тағамның құрамына ақуыздардың, майлардың және көмірсулардың кіретіндігін және олар жануарлардың және өсімдіктердің басты құрама бөліктері болып табылатындығын анықтады.
Витализммен күресте мықты соққыны Велер жасады. 1828 жылы Велер химиялық жолмен мочевинаны алды. Мочевина - адамның және жануарлардың ағзасындағы азоттық зат алмасудың соңғы өнімдерінң бірі. Өзінің ұстазы Берцелиусқа жазған хатында Велер былай деді: «мен енді мочевинаны жасай аламын. Ол үшін маған бүйректің, тіпті еш қандай да жануардың, адамның немесе иттің қажеті жоқ. Міне мен осыны сізге мәлімдегім келеді». Көп ұзамастан соңынан басқа тамаша жұмыстар жасалды. Олар: Кольбенің сірке қышқылын (1844 ж. ), Бертлоның майларды (1844 ж. ), Бутлеровтың көмірсуларды синтездеуі.
Витализммен күресу жолында ашу үрдісінің табиғаты туралы зерттеулер маңызды орын алды. Ашу үрдісін зерттеген ғалымдардың ішінде Ю. Либих және Л. Пастер болды. Пастер ашу - тірі ашытқы клеткаларының қатысуымен жүретін биологилық үрдіс деп қорытындылады. Либих ашу үрдісінің таза химиялық теориясына қатысты сұрақтармен айналысты. Алайда бұл теорияның кемшіліктері болды. Яғни, теория толық жетілмеген еді. Эксперименттің барысындағы алынған мәліметтерді түсіндіре алмады. Негізгі мәселерді орыс химигі М. М Манассеина (1871 ж. ) және немістің ғалымы Бухнер (1897 ж. ) дәлелдеді. Олар клеткасыз ашытқы шырынының спирттік ашуға қабілетті екендігін дәлелдеді.
Өсімдік және жануарлардың ағзаларындағы химиялық заттар, ағзалардағы жүретін химиялық үрдістер туралы салыстырмалы түрде айтқанда сол уақыттардағы жинақталған көп материалдар мен мәліметтер оқу құралдарында жүйелене бастады. Осыған әрекет жасалды: Зимонның (1842 ж. ) және Либихтің (1847 ж. ) оқулықтары. Ресейде алғашқы оқулық - физиологиялық химия баспадан шықты (А. И. Ходнев, 1847 ж. ) .
ХІХ-шы ғасырдың екінші жартысында көптеген орыс және шет елдік университеттердің медицина факультеттерінде арнайы медициналық, немесе физиологиялық химияның кафедралары бекітілді. Ресейде медициналық химия кафедрасы бірінші рет 1863 жылы Қазан университетінде А. Я. Данилевскийдің көмегімен ашылды. 1864 жылы А. Д. Булыгинский Мәскеу университетінде медициналық химия кафедрасының негізін қалады. 1892 жылы Петерборда Әскери-медициналық (Медицина-хирургиялық) академиясында физиологиялық химия кафедрасы жұмысын бастады. Бұл кафедраны А. Я. Данилевский басқарды. Жоғарғы оқу орындарында физиологиялық химияның кафедраларының құрылуына себеп - биологиялық химия түбіне келгенде органикалық химиямен және физиологиямен байланысты болғанына қарамастан өз алдына жаңа ғылым болды, оның өзінің зерттеу нысаны және зерттеу әдістері бар.
Биохимияның шын мәнінде гүлденуі ХХ ғасырда болды. Биохимияның салаларындағы жаңалықтар бірінен соң бірі ашылды. Қазіргі уақытта классикалық биохимияның қамтитын сұрақтары әлде қайда кеңейді. Ал енді келешекте биохимияда тағы да жаңалықтар ашылып биологияға және химияға қатысты бөлімдерді қамтуы мүмкін.
Бақылау сұрақтары:
1. Биологиялық химия нені зерттейді ?
2. Биологиялық химияның бөлімдері қалай аталады ?
3. Заманауи биохимияның пайда болуы және даму кезеңдері.
4. Биохимияның дамуына үлес қосқан ғалымдардың қандай еңбектерін білесіздер ?
5. Биохимияның келешегі қандай болады ?
№ 2-ші дәріс
Тақырыбы: Ақуыздардың химиясы
Жоспар:
1. Ақуыздардың маңызы.
2. Ақуыздардың жіктелуі.
3. Ақуыздардың құрамы және құрылысы.
4. Ақуыздардың физикалық және химиялық қасиеттері.
Белоктар өзарат пептидтік байланыспен қосылған аминоқышқылдарынан құралған өте күрделi жоғары молекулалы органикалық заттар. Табиғатта шамамен 10 10 -10 12 әртүрлi белоктар кездеседi. Оның бес миллионға жуықтауы адам денесiнде кездеседi. Белоктар адам денесiнiң 18-21 % құрайды. Ал кейбiр мүшелерде (көкбауыр, өкпе, бұлшық етте бүйректе т. б. ) белоктың мүшелерi 70-80 %. Қорыта айтқанда белоктар жасушаның ең негiзгi құрылыс материалы.
Белоктар-ферменттер жасушада жүретiн химиялық реакциялардың жылдамдығын тездетедi. Белоктар тасымалдау, тыныс алу қызметiн атқарады. Қызыл қан түиiршiгiнiң белогы гемоглобин оттегiн қосып алып, барлық үлпаға, жасушаға таратады да, олардан көмiрқышқыл газын өкпеге тасымалдайды.
Белоктар қозғалыс қызметiн атқарады. Мысалы, бұлшық еттердiң, жүректің, өкпенiң, iшекқарынның қабырғасындағы еттердiң жиырылуы арқылы қозғалыстың бiрнеше түрi iске асып, сол мүшелердiң қызметi қамтамасыз етiлуiнде белоктардың маңызы зор. Белоктар қуат көзi, 1 г белок толық ыдырағанда 4, 1 ккал (17, 6 кДж) қуат босап шығады. Тәулiгiне жұмсалған қуаттың 10-15 % -ға жуығы белоктар арқылы өтеледi.
Ағзада ферменттер, гормондар т. б. заттар үздiксiз жұмсалып: ескiрген белок молекулалары ыдырап, үлпалар мен жасушалар жаңарып отырады. Осының бәрiне белок қажет. Мысалы, тiршiлiк барысында организмдегi көптеген жасушалар бiрнеше рет жаңарады; қандағы қызыл қан түйiршiктерi эритроциттер 100-200 күн аралығында толық жаңарып алмастырылса, бауыр жасушаларындағы белоктар 10 күн аралығында жартылай жаңарады. Салмағы 70 кг-дай ересек адам ағзасында тәулiгiне шамасы 400 гр-дай белоктар ыдырап және қайта құрылады. Сондықтан да осы жұмсалған белоктардың орнын толтыру үшiн тамақпен енгiзiлген белоктың мөлшерi жеткiлiктi болуы қажет.
Қалыпты жағдайда тәулiгiне адам ағзасына 80-100 г белок керек болса, дене еңбегiмен айналысқанда оның мөшелерi 120-150 г дейiн өседi. Белок жеткiлiксiз болған жағдайда бүйрек, қалқанша, жыныс бездерiнiң қызметi бұзылады. Орталық жүйке жүйесi белоктың жеткiлiксiздiгiн өте тез сезедi. Ашыққанда ми мен жүрек өзiнiң салмағын көп уақытқа дейiн жоғалтпайды, себебi олар өзiнiң белоктарын бұлшық ет пен бауырдың белоктарының есебiнен толықтырады.
2. Ақуыздардың жіктелуі.
Биологиялық маңызы жағынан белоктарды құнды және құнсыз деп екi топқа бөледi. Құнды белоктар дегенiмiз - құрамында ауыстыруға болмайтын аминқышқылдары бар белоктар. Организмде түзiлмейтiн аминқышқылдарын ауыстыруға болмайды деп санайды. Бұларға: валин, лейцин, изолейцин, метионин, треонин, лизин, триптофан, фенил-аланин сияқты сегiз аминқышқылдары жатады. Жартылай ауыстырылмайтын аминқышқылдары төртеу - аргинин, гистидин, цистейн мен тирозин. Ауыстыруға болатын амин қышқылдары организмнiң өзiнде кетоқышқылдардан, май қышқылдарынан түзiледi. Олар аланин, аргинин аспарагин, глицин, глотамин, пролин, серин қышқылдары.
Биологиялық құнды белоктардың құрамында белок молекуласын құруға қажеттi барлық аминқышқылдары болады. Оған жануарлардан алынатын белоктар жатады. (жұмыртқа, ет, сүт, балық белоктары), құнсыз белоктардың құрамында ауыстыруға болмайтын аминқышқылдары кездеспейдi. Мысалы, жүгерiнiң, бидайдың, белоктары, желатин - құнсыз белоктар.
Ағзадағы белок тепе-теңдiгiн қамтамасыз ететiн тағамдағы белоктың ең аз мөлшерiн - белоктыңминимумы деп атайды. Белоктар көмiрсулар мен майлар тәрiздi коректiк зат болып жинақталмайды. Тағамдағы белоктың мөлшерi көп болған жағдайда ағзадағы белок тепе-теңдiгiн сақтау үшiн, олардың катаболизмi күрт өсiп, соңғы өнiмдерi сыртқа шығарылады.
Барлық белоктар құрамы бойынша екi топқа бөлiнедi. Тек қана аминқышқылдарының қалдығынан тұратын қарапайым белок - протеиндеп аталады. Қарапайым белокқа бөтен зат байланысқан болса, оны күрделi белок протеиддеп атайды.
3. Ақуыздардың құрамы және құрылысы.
Белоктың құрамында жиырма түрлі амин қышқылдары болады. Әр түрлі белоктардың амин қышқылы құрамы жағынан да, олардың тізбектегі орналасу тәртібі жағынан да бір-бірінен айырмашылығы зор. Табиғатта белок түрлерінің көп болуы да осыған байланысты. Мысалы, үш амин қышқылының қосылуынан алты түрлі, төрт қышкылдан жиырма төрт түрлі белок изомерлері пайда болады. Белок молекуласы амин қышқылдарының өзара моншақтай тізіле байланысқан полипептидтік тізбегінен құралады. Белок молекуласының сыртқы пішіні екі түрлі болады. Біріншісі - шар тәрізді домалақ - глобулярлы белоктар. Бұларға альбуминдер, глобулиндер, гемоглобин және т. с. с белоктары жатады. Екіншісі фибриллярлық (талшық тәріздес) белоктар. Бұларға бұлшық ет белогы - миозин, актин және т. с. с. жатады. Белок молекуласының өзіне тән ерекшеліктері мен құрылымдылық дәрежелері көптеген сутектік байланыстар, электростатикалық қуаттар, күкірттен құралатын дисульфидтік байланыстар арқылы қамтамасыз етіледі.
Белоктардың қасиеттерін олардың құрамы мен құрылымы анықтайды. Белок молекуласындағы а-аминқышқылдары қалдықтарының саны әр түрлі болады, кейде бірнеше мыңға дейін жетеді. Әр белокта α-аминқышқылдары тек осы белокқа ғана тән ретімен орналасады. Олардың молекулалық массалары бірнеше мыңнан миллионға дейін жетеді. Мысалы, жұмыртқа белогының молекулалық массасы 36000, бұлшық ет белогының молекулалық массасы - 15 шамасында. Белоктар, негізінен, көміртек (50-55%), оттек (20-24%), азот (15-19%), сутектен (6-7%) тұрады. Кейбір белоктардың құрамына бұлардан басқа күкірт, фосфор, темір кіреді. Белоктар гидролизденгенде α-аминқышқылдарының қоспасы түзіледі. α-аминқышқылдарының жалпы формуласы:
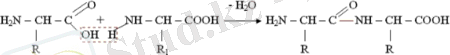
Пептидті байланыс бір аминқышқылының карбоксил тобымен екінші аминқышқылының амин тобының байланысынан түзіледі. Пептидтік байланыс табиғатын зерттеген ғалым Э. Фишер.
Нәруыздың бірінші ретті құрылымы. Полипептидтік тізбектегі әр түрлі аминқышқылдары қалдықтарының бір-бірімен кезектесіп байланысу ретін нәруыздың бірінші реттік құрылымы дейді.
…- ала - лиз - вал - вал - иле - …
Нәруыздардың бірінші реттік құрылымы жүйелік номенклатураға қолданылу мүмкін.
Нәруыздың екінші ретті құрылымы. Нәруыз молекулалары полипептидтік тізбектерінің кеңістіктегі оралма тәрізді болып келген пішінін нәруыздың екінші реттік құрылымы дейді. Мұнда оралманың көрші оралмадағы -NH- және -CO-топтарының арасында түзілген сутектік байланыстар түзіледі.
Нәруыздың үшінші ретті құрылымы. Полипептидтік байланыс оралымға айналғанда ондағы радикалдар сырттап қалады. Сол радикалдардан нәруыз молекуласының үшінші реттік құрылымы түзіледі.
Нәруыздың төртінші ретті құрылымы. Нәруыздың төртінші ретті құрылымы бірнеше шумақталған оралымнан тұрады, яғни бірнеше нәруыз молекулаларының қосындысы.
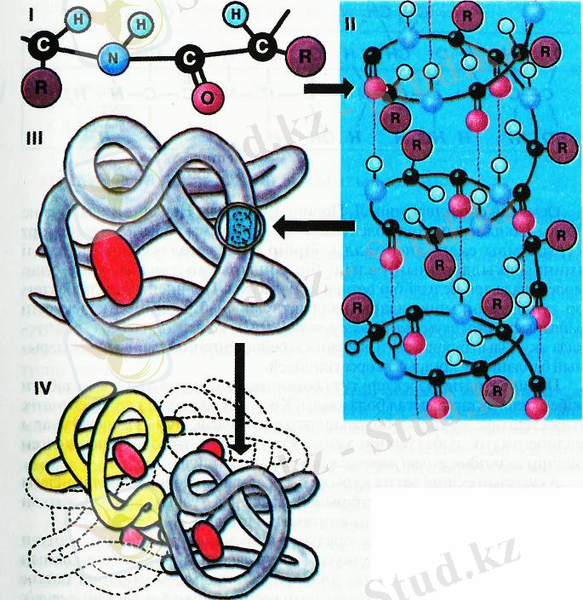
4. Химиялық қасиеттері
Белок ерітіндісін қыздырса немесе оған күшті кышқылмен әсер етсе, ол өзінің табиғи қасиеттерін (ферменттік, гормондық) жояды, кейде ұйып та қалады. Мұндай құбылысты денатурация деп атайды.
Құрамы мен құрылысы күрделі болғандықтан, белоктардың қасиеттері де алуан түрлі. Олардың құрамында әр түрлі химиялық реакцияларға түсетін функционалдық топтар бар.
Белоктар - екідайлы электролиттер. Ортаның белгілі бір рН мәнінде олардың молекулаларындағы оң және теріс зарядтар бірдей (изоэлектрлік нүкте деп аталады) болады.
Белоктардың гидролизі. Сілті немесе қышқыл ерітінділерін қосып қыздырғанда, белоктар гидролизденіп, аминқышқылдарын түзеді:
Белоктардыц түсті реакциялары. Белоктарды сапалық анықтау үшін түсті реакциялар қолданылады.
а) , ә) Биурет реакциясы. б) құрамында күкірті бар белоктарға қорғасын ацетатын және сілті қосып қыздырғанда, қорғасын сульфидінің қара түнбасы түзіледі.
Бақылау сұрақтары:
1. Ақуыздардың маңызы қандай ?
2. Ақуыздар қалай жіктеледі ?
3. Ақуыздардың құрылымдары қандай болады ?
4. Ақуыздардың физикалық және химиялық қасиеттері қандай ?
№ 3-ші дәріс
Дәрістің тақырыбы: Көмірсулардың химиясы
Жоспар:
1. Көмірсулардың химиясы.
2. Көмірсулардың жіктелуі.
3. Көмірсулардың маңызы.
1. Көмірсулардың химиясы.
Көмірсулар - химиялық құрамы С m (H 2 O) n яғни көмірсутек + су, аты осыдан шыққын) формуласымен өрнектелетін табиғи органикалық қосылыстар класы. Көмірсулар химиялық құрамына қарай үлкен 3 топқа бөлінеді:
-мономерлік көмірсулар немесе моносахаридтер;
-олигосахаридтер;
-полисахаридтер.
Соңғы екі топтың өкілдері моносахаридтердің конденсация өнімдері болып табылады.
Ашық түрдегі моносахаридтердің типтік формалары: альдоза үшін СН 2 ОН(СНОН) n СНО; кетоза үшін СН 2 ОН(СНОН) n СОСН 2 ОН, мұндағы n>1. Моносахаридтердің көп бөлігінде тармақталмаған көміртектік тізбекпен бір альдегидтік (альдозалық) немесе кетондық (кетозалық) топ болады.
Тізбектегі көміртек атомының санына орай моносахаридтер:
-тетрозаға (С 4 ),
-пентозаға (С 5 ),
-гексозаға (С 6 ), т. б. бөлінеді.
Кейде кетоза атауына "ул" жұрнағы жалғанады (мысалы, пентулоза, гептулоза, нонулоза, т. б. ) . Моносахаридтерде көміртектің асимметриялық атомдары болады және оптикалық белсенді стереоизомерлер түзіледі. Көмірсулар мысалдарына құрамы (С 6 Н 10 О 5 ) n формуласымен өрнектелетін глюкоза немесе жүзім қанты (С 6 Н 12 О 6 ), қамыс немесе қызылша канты (С 12 Н 22 О 11 ) және крахмал немесе целлюлозаны келтіруге болады. «Көмірсулар» деген атауды 1844 жылы К. Шмидт ұсынған. Бұл атау осы қосылыстар тобының алғашқы белгілі өкілдерін анализдеу негізінде пайда болды. Зерттеу нәтижесінде осы топ заттарының көміртектен, сутектен, оттектен тұратыны және сутек пен оттек атомдарының сандық қатынасы су молекуласындағыдай, яғни сутектің екі атомына оттектің бір атомы келетіні анықталған. Осы айтылғандарға сәйкес көмірсулардың жалпы формуласы: Жақша сыртына n-ді шығарсақ С m (Н 2 О) n деген «көмірсулар» атауына дәл келетін формуланы аламыз. Алайда, кейінірек кейбір көмірсулардың құрамындағы сутек пен оттектің сандық қатынасы судағыдай емес екені анықталды, мысалы, рамноза С 6 Н 10 О 4 мен дезоксирибоза С 5 Н 10 О 4 .
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz