Орта мектепте атом құрылысын оқытуда ұжымдық оқыту технологиясының тиімділігі және педагогикалық шарттары


МАЗМҰНЫ
КІРІСПЕ . . . 3
1. 1 Ғылыми педагогика іліміндегі оқытуды ұйымдастырудың негізгі түрлері . . . 5
1. 2 Ұжымдық оқыту технологиясы . . . 5
1. 3 Ұжымдық оқыту тәсілінің негізінде оқу үдерісін ұйымдастыру . . . 16
2 . 1«Атом құрылысын» ұжымдық оқыту . . . 20
2. 2 Атом құрылысына Д. И. Менделеевтің периодтық заң және химиялық элементтердің периодтық жүйесі тұрғысынан сипаттама . . . 20
- «Атом құрылысын» ұжымдық оқыту технологиясымен сабақты жүргізу үдерісін тәжірибелік-эксперименттік негіздеу; . . . 26 2. 4«Атом құрылысын» ұжымдық оқыту технологиясымен сабақты жүргізу үдерісін тәжірибелік-эксперименттік негіздеу;
- Атом құрылысын оқыту кезінде ұжымдық оқыту әдісінің дидактикалық және тәжірибелік-эксперименттік меңгеру нәтижелерін қорытындылау.
3 ЭКСПЕРИМЕНТТІК БӨЛІМ . . . 29
ҚОРЫТЫНДЫ . . . 43
ӘДЕБИЕТТЕР ТІЗІМІ . . . 45
Кіріспе
Жұмыстың жалпы сипаттамасы. Орыстың педагогтерінің бірі К. Д. Ушинскийдің айтқанындай қазіргі заман талабына сай әрбір мұғалім, өз білімдерін жетілдіріп, ескі бір сарынды сабақтардан гөрі, жаңа талапқа сәйкес инновациялық технологияларды өз сабақтарында күнделікті пайдаланса сабақ тартымды да, мәнді, мағыналы, тиімді болары сөзсіз. Бұл туралы Қазақстан Республикасының «Білім туралы» Заңының 8-бабында: «Білім беру жүйесінің басты міндеттерінің бірі - оқытудың жаңа технологияларын енгізу, білім беруді ақпараттандыру, халықаралық ғаламдық коммуникациялық желілерге шығу» - деп, атап көрсеткен. Елбасымыз Н. Ә. Назарбаев Жолдауында айтқандай: «Болашақта өркениетті дамыған елдердің қатарына ену үшін заман талабына сай білім қажет. Қазақстанды дамыған 50 елдің қатарына жеткізетін, терезесін тең ететін - білім». Сондықтан да қазіргі даму кезеңі білім беру жүйесінің алдында оқыту үдерістерінің технологияландыру мәселесі қойылып отыр. Оқытудың әртүрлі технологиялары сарапталынып, жаңашыл мұғалімдердің іс-тәжірибесі зерттелініп, мектептің өміріне енуде.
Әдебиеттерде оқығанда көретініміздей, педагогикада оқу - тәрбие процесінде оқушылардың белсенділігін жоғарылатудың жолдары үздіксіз түрде жүргізілетіндігі көрсетіледі. Оқу үдерісінде оқушылардың өз бетінше және белсенділік принципі атақты дидакт М. Н. Скаткиннің жұмыстарында ұсынылды. Кейін ол М. И. Махмутова, Т. И. Шамова, Н. А. Половникова, Д. В. Вилькеева, И. Я. Лернер зерттеулерінде дамыды. Бірақтан да алдыңғы ғасырдың 80 - жылдарына дейін бұл бағытты зерттеу оқытуды ұйымдастырудың бір түрі - тек сабақта ғана жүргізілді. Сабақтың әр кезеңдерінде оқушыларды белсенділігін арттырудың тәсілдері қарастырылды. Зерттеушілер оқу процесінде әрбір оқушының белсенділігін арттыруда оқу әрекетін жекешелендіру мүмкіндіктерін қарастырды. Басқалары бұл міндетті шешуде оқытудың ұжымдық формасын қарастырды. 80 - жылдардың басынан бастап педагогикада педагогикалық технологиялармен байланысты зерттеудің жаңа бағыттары пайда болды. Бұл бағыт аумағында әр түрлі оқытудың инновациялық технологиялары қарқынды түрде бастау ала бастады және олардың қатарында оқытудың ұжымдық әдісі де рөл атқарды. Педагогикада бұл технология В. К. Дьяченко атымен байланысты. Ол бұл форманың негізін, мазмұнын және мақсатын құрды. Ол өзінің зерттеулерінде ұжымдық оқыту технологиясының әрбір оқушының белсенділік әрекетінің міндеттерін шешуде, оқушылардың ынтасын жоғарылатуда, коммуникативті дағдыларын қалыптастыруда үлкен мүмкіндікке ие екендігін айтты. Сол уақыттарда оның қарқынды түрде жүзеге асуына жұмыстар жүргізілмеді.
Ұжымдық оқытудың тарихы М. А. Брейтерман., З. А. Вихман., З. Чаганның жұмыстарында көрсетілді. Оқытудың ұжымдық әдісінің технологиясының теориялық және әдістемелік негіздері А. Г. Ривин., В. К. Дьяченко., М. А. Мкртчян еңбектерінде қарастырылды. Ал бұл технологияның жүйелік талдауын Г. К. Селевко ұсынды.
Оқытудағы ұжымдық проблемасының көп ғасырлық тарихы бар. 16-17 ғасырлардың өзінде мұғалімнің бір уақытта сыныптағы барлық оқушылармен жұмыс жасауын ұжымдық деп атаған.
Бірақ ұжымдық жұмысты әртүрлі зерттеушілер әрқалай түсінеді. Бір жағдайда бұл мұғалінің барлық сыныппен бір уақыттағы жұмысы
(Е. Н. Медынский, А. А. Бударный) . Басқасында - ауызша немесе жалпы сыныптық әрекет жағдайы (бірігіп іздену, талқылау, бір-біріне көмек беру) . Үшіншіден - егер жұмыс нәтижесі өзара талқыланып, талданса, онда ауызша немесе топтық болады. Төртіншіден - дифференциалды топтық жұмыс, мұнда әрбір топ өздерінің жеке тапсырмаларын алады, одан кейін топ мүшелері арасында жеке тапсырмаларға және тақырыптарға бөліп алады. Бесіншіден - алмаспалы құрамды жұппен жұмыс.
Ұжымдық оқыту тәсілінің негізінде оқу үдерісін ұйымдастыру Ресейде кең қолданыс тапқан. Сонымен қатар Ресеймен көршілес мемлекеттерде де әдіс негізінде жұмыстар жүргізілуде. Алдағы уақытта да әдістің Қазақстанда дамуы үшін педагогикалық мүмкіндіктерін жүзеге асыратын жаңа деңгейде әрекеттер жасау керек.
Зерттеудің мақсаты: орта мектепте атом құрылысын оқыту кезінде ұжымдық оқыту әдісін қолданудың тиімділігі мен педагогикалық шарттарын анықтау.
Зерттеудің нысаны: орта мектепте бейорганикалық химия курсын оқыту үрдісінде ұжымдық оқыту технологиясын пайдалану әдістемесі.
Зерттеу пәні: бейорганикалық химияны оқыту үрдісінде ұжымдық оқыту технологиясы арқылы оқыту.
Зерттеу міндеттері:
- Негізгі оқытуды ұйымдастырудың ұжымдық формасы болатын ұжымдық оқыту сабақтарын дидактикалық негіздеу;
- Орта мектепте бейорганикалық химия курсында ұжымдық оқыту технологиясымен сабақты жүргізу үдерісін тәжірибелік-эксперименттік негіздеу;
- Атом құрылысын оқыту кезінде ұжымдық оқыту әдісінің дидактикалық және тәжірибелік-эксперименттік меңгеру нәтижелерін қорытындылау.
Зерттеудің ғылыми болжамы:
Орта мектепте бейорганикалық химияны оқыту үрдісінде ұжымдық оқыту әдісі пайдаланылса, онда оқушылардың білім көрсеткіштері жоғарылап, химия пәніне деген қызығушылықтары оянып, танымдық белсенділіктері артады және сабаққа деген ынтасы жақсарады.
Зерттеудің жетекші идеясы: оқу үдерісінде ұжымдық оқыту технологиясын пайдалану - оқушылардың қазіргі кезде заман талабына сай жеке тұлға ретінде қалыптасуына жағдай жасайды.
Зерттеудің теориялық-әдіснамалық негізіне: ғылыми таным теориясы, тұтас педагогикалық процестегі тұлғаның қалыптасу теориясы, іс-әрекеттер теориясы, Қ. Р. Білім беру заңы, Қ. Р. 2015 жылға дейінгі білім беруді дамыту тұжырымдамасы, жас ұрпақты оқыту, тәрбиелеу және дамыту туралы директивалық нұсқаулар, Қ. Р. ресми материалдары /Қ. Р. білім беруді дамытудың 2010-2020 жылдарға арналған Мемлекеттік бағдарламасы, ақпараттандыру саласындағы құжаттар жатады. Зерттеу міндетін шешуде келесі әдістер қолданылады:
- философиялық, психологиялық-педагогикалық және әдістемелік әдебиеттерді теориялық талдау;
- мұғалімнің педагогикалық тәжрибесін талдау және игеру;
- бақылау, әңгімелесу;
- оқу үдерісін ұйымдастыруды құру;
- тәжірибелік-эксперименттік жұмыс.
Қойылған міндеттерді шешу үшін түрлі зерттеу әдістері қолданылды:
Мемлекеттік деректік құралдарды, заңдарды зерделеу; зерттеу бағыты бойынша ғылыми-әдістемелік, психологиялық, педагогикалық әдебиеттерді талдау; оқушылармен, мұғалімдермен, мектеп басшыларымен, ата-аналарымен әңгімелесу, олардың арасында сауалнамалар жүргізу; оқу үрдісіне енгізу жолдарын ұсыну.
Зерттеу процесі бірнеше кезеңдерде жүргізілді:
Зерттеуде 3 кезең қарастырылады:
1 - кезең. Зерттеу тақырыбын таңдау және негіздеу. Бірінші кезеңде философиялық, психологиялық-педагогикалық және әдістемелік әдебиеттердің теориялық талдау әдістері: педагогикалық тәжірибені талдау; бақылау, әңгімелесу, сауалнама қолданылды; зерттеу тақырыбына сәйкес ғылыми әдебиеттер қаралды, инновациялық педагогикалық технология аумағында педагогикалық тәжірибе талдау жүргілді.
2 - кезең. Зерттеу жүргізу. Егер оқу үрдісіне ұжымдық оқытуды енгізсе, онда оқыту сапасы жоғарылайды. Мектептерде тәжірибелік-экспериметті қолдану және ұйымдастыру. Бұл кезеңде экспериментті қалыптастырушы әдіс, құрастыру, талдау, қорытындылауға мүмкіндік туды. Орта мектепте бейорганикалық химияны оқытуда ұжымдық оқыту әдісінің қарқындылығын қамтамасыз ететін, ұйымдастырушы-педагогикалық шарт негізіне бағытталған тәжрибелік-эксперименттік жұмыстар жүргізілді.
3 - кезең. Зерттеу нәтижелерін мақалалар, педагогикалық семинарларда таныстыру.
Зерттеу базасы: зерттеудің эксперименттік базасы кафедра
Зерттеулердің ғылыми жаңалығы мен теориялық мәні:
Ұжымдық оқыту технологиясы бойынша ұжымдық сабақтардың моделін құруға негізделеді. Жүргізілген зерттеулер ұжымдық оқыту технологиясының түсінігін нақтылауға және толықтыруға мүмкіндік берді:
- ұжымдық оқыту оқытуды ұйымдастырудың бірнеше формасынан тұрады;
- ұжымдық оқыту сабақтарының маңыздылығы әлеуметік-психологиялық жағдай туғызу;
- ұжымдық оқыту сабақтары жеке, жұптық және топтықпен қатар оқыту сабақтарының жүйесі болып табылады;
- орта мектепте бейорганикалық химияны оқытуда ұжымдық оқыту әдісінің қарқынды жүзеге асыруында ұйымдастырушылық-педагогикалық шарттар ұсынылды;
- оқушылардың мүмкіндіктерін (коммуникативті дағды, танымдық әрекетіндегі өз бетінше әрекеті, оқудағы білігі) қалыптастыруда ұжымдық оқыту технологиясының педагогикалық мүмкіндіктері анықталды
Зерттеу нәтижелері ұжымдық оқыту сабақтарын бейорганикалық химияны оқыту үдерісінде қолдануда оқытудың қарқындылығын жоғарылатудың мүмкіндіктерін негіздейді.
Зерттеудің практикалық құндылығы:
- ұжымдық оқыту әдісін қолдануда оқытудың қарқындылығын жоғарылату;
- оқушы ұжымын барлығын және әрбір оқушыны оқытуға үйрету;
- ұжымдық сабақтарды құрастыру.
Ұжымдық оқыту тәсілін қолдану жеке оқушылардың тәрбиесін және дамуының жүзеге асуында нәтижелі болуына негіз болады.
Қорғауға зерттеудің төмендегі қорытындылары ұсынылады:
- оқушыларға білім беруде жалпы білім беретін орта мектепке оқытудың ұжымдық әдісін енгізілуі;
- ұжымдық оқыту әдісі арқылы орта мектепте бейорганикалық химияны оқытуда оқушылардың білім көрсеткіштерінің жоғарылауы.
Жұмыстың апробациясы. Жұмыстың нәтижелері көрсетілген және баяндалған.
Жарияланған басылымдар. Жұмыстың нәтижелеріне байланысты л ғылыми басылым жарияланды.
Диплом құрылымы:
Кіріспеден, екі тараудан, зерттеудің тұжырымдамасы келтірілген қорытындыдан, пайдаланған әдебиеттер тізімі және қосымшадан тұрады.
“Атом - молекулалық ілімнің тарихы. Химияның негізгі ұғымдары мен заңдарың тақырыбының мақсаты - ғылыми атоммистиканың шығу мен дамуы жөніндегі оқушылардың білімін кеңейту. Осы мақсатты орындау үшін ежелгі атомистика, М. В. Ломоносов және Дж. Дальтон атомистикасы туралы кең түсінік беріледі. «Атом» және «Химиялық элемент» ұғымдарының байланысы ашылады. «Элемент» ұғымы дамуының кезеңдері сараланады. Тақырып периодтық заңның химия ғылымын, ғылымның дамудағы мәнін баяндаумен аяқталады. Келесі «Атомдармен молекулалардың құрылысы» тақырыбында «химиялық элемент» ұғымы дамытылып, бұрынғыдан гөрі дәләрек анықтама беріледі, элементтердің бір-біріне айналуы жөнінде түсінік қалыптастырылды.
Атомның құрылысы негізгі курстағыдан гөрі толығырақ айтылып, s - және p - деңгейшелерінен басқа f және d деңгейшелердің электрондармен толу ерекшеліктері түсіндіріледі. Электрондардың орналасу ретін көрсететін формулалар жазылады. Химиялық байланыстардың түрлері, түзілу механизмдері тереңірек сипатталады. Жиынтық қосылыстардаға химиялық байланыстың табиғаты қарастырылады.
“Химиялық кинетика және тепе-теңдік” тақырыбы химиялық реакциялардың жүру заңдылықтарын баяндауға арналған. Жаңадан әрекеттесуші массалар заңы және Ле - Шателье принципі өтіледі. Осылардың тұрғысынан химиялық реакцияларды жылдамдығына әсерін тигізетін жағдайлар және химиялық тепе-теңдіктің ұғысу жағдайлары қарастырылады. Катализ туралы ұғым кеңінен талданады. Активті малекулалар және активтендіру энергиясы туралы жаңа ұғым беріледі.
Дисперстік жүйелерге арналған. Мұнда коллоидты ерітінділердің құрамы, оның бөлшектерінің құрылысы, қасиеттері және түрлері (лиофильді, лиофобты) ғылыми сарамандық маңызы коллоидты жүйелердің тұрақтылығы жөніндегі мәселелер толық қарастырылады. кәдімгі ерітінділердің қасиеттері Рауль заңы, эбуллиоскопия; криоскопия және осмос бойынша түсіндіріледі. Электролит ерітінділерінің қасиеттерін түсіндіру үшін С. Аррениус теоремасымен біріге қазіргі заманның теорялары пайдаланылады.
“Химиялық энергетикаң тақырыбында оқушылардың термохимия негіздерінен алған білімдері кеңейтіледі. Реакцияның жылу эфектісі, заттардың түзілу жылуы, химиялық реакция кезінде бөлінетін жылу ұғымдарын пайдаланып есептеулер жасалады.
Атом құрамы, ядро және электрон
Күнделікті тұрмыста көріп жүргеніміздей, көптеген химиялық реакциялардың жүруі әр түрлі физикалық құбылыстармен тікелей байланысты. Мысалы жану кезінде жылу мен жарық бөлінеді. Күн сәулесі жарықтың әсерінен өсімдіктер дүниесінде өте күрделі химиялық реакция - фотосинтез жүреді. Өмірде толып жатқан өзгерістер физикалық және химиялық құбылыстардың өзара өте тығыз байланыста екендігін айғақтайды. Міне осындай физика және химия ілімдерінің тоғысуынан туындаған жаратылыстану ғылымының жаңа саласы - физикалық химия деп аталады. Ол табиғатта орын алатын заңдылықтарды негізге ала отырып, химиялық реакциялардың жүру жағдайлары мен жылдамдығы және әрекеттесуші заттарға сыртқы күштердің әсерлерін зерттейді. Сыртқы күш ретінде жылу, қысым және т. б. физикалық шамалар қабылданып, олардың жүйе күйінің өзгерісіне тигізер әсері қарастырылады.
Физикалық химияның мақсаты - белгілі бағытта химиялық реакцияның жүру мүмкіндігін айқындайтын заңдылықтарды тұжырымдап, олардың реакция жылдамдығына, әрекеттесуші заттар мен түзілген өнімдердің қасиеттеріне тәуелділігін ашу.
Физикалық химия шартты түрде мына бөлімдерден тұрады.
- зат құрылысы
- химиялық термодинамика
- ерітінділер
- физика-химиялық сараптау
- электр химиясы
- катализ және химиялық кинетика
Физика-химиялық және химиялық құбылыстардың өту заңдылықтарын зерттеу барысында оларды сандық, яғни мөлшер шамасын білу қажеттілігі туындайды. Бұл орайда іс-тәжірибе жүзінде алынған мәліметтерді ғылыми түрде сараптап жинақтауда негізінен үш тәсіл қолданылады.
- Статистикалық физика - заттардың молекула элементар бөлшектерден тұратындығын және де осы бөлшектер дене бойында ықтималдық ілімге сәйкес орналасқандығын ескере отырып, жүйе қасиетін әрбір және бөлшек қозғалу заңдылықтары тұрғысынан қарастырады.
- Термодинамика - энергия түрленуі мен берілісінің нақты бір жүйелерде термодинамикалық қасиеттерінің өзара байланысын анықтау арқылы болжам жасайды.
Осы екі тәсілді пайдалану нәтижесінде статистикалық термодинамика ілімі дүниеге келді.
- Кванты - механика - денелерді құрайтын элементар бөлшектерге тән қостүрлі, яғни “ толқындық” және “сызықтық” қозғалыс құбылыстарына сүйене отырып, атом-молекула құрылысын, олардың өзара әрекеттесу бейімділігн және химиялық байланыс табиғатын түсіндіруді негізге алады.
Кез-келген физика-химиялық құбылысты зат құрылысы квантты химия, термодинамика және кинетикалық тұрғыдан қарастырған жөн.
2) Зат құрылысын анықтау заттардың бөлшектер ағыны (электрон, протон, нейтрон, α-бөлшек, иондар ағыны т. б. ) немесе өріспен (гравитациялық, электрлік магнит, ядролық өрістер т. б. ) әрекеттесулеріне негізделген.
Жарықты (фотондар) бөлшектер ағыны деп қарастыруға болады. Протонның орташа өмір сүру уақыты - 13 мин. Осы уақыттан кейін протон нейтронға позиронға түрленеді.
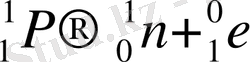 (позитрон)
(позитрон)
Нейтрон атом ядросында болады. Ядролық түрленулер негізінде немесе нейтрон дербес жағдайда болғанда (орташа өмір сүру уақыты шамамен 13 мин.
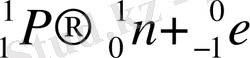
Жарық кванты (фотондар)
Жарық ағымының заттармен әрекеттесуін заттардың құрылысын, қасиеттерін анықтауға пайдалануға болады. Бұл жерде жарық ұғымын кең ауқымда түсіну қажет (инфрақызыл сәулелер, көзге көрінетін сәулелеріне ультракүлгін сәулелер, ренген сәулелер, гамма сәулелер) . Жарық сәулесіндегі энергияның шығуы үздіксіз ағын түрінде емес, кесімді порция (бөлшек) яғни квант түрінде болады деп, заттың құрылысындағы атом жайындағы түсінікті энергияға қолданған. Жарықтың осындай порция-порция энергиясы бар бөлшегі фотон деп аталады.
Жарық кванты энергиямен, импульсімен, массасымен, толқын ұзындығымен, жиілігімен сипатталады. Түрлі сәуле шығаруда кванттың Е мөлшері әртүрлі әрі ол жарықтың сәулесінің тербеліс жиілігіне пропорционал. Бұл шамалар мына теңдеумен анықталады.
E = h ⋅ v = hc/λ (1)
P = m ⋅ c = E/c (2)
M = E/c 2 = P/c (3)
v = c/λ (4)
Атом құрылысын зерттеу
Атом құрылысын зерттеу бірден басталмады, себебі ХІХ ғасырдың аяғына дейін химияда да, физика да атом материяның бөлініп болған ең кіші бөлігі, одан да әрі бөлінбейді деген метафизикалық жалған пікір үстем болды. Бұл пікірдің қате екеніне ертеден-ақ түсінік берді. 1819 ж. М. Г. Павлов (Москва университеті профессоры) барлық зат материядан тұрады, материяда электр зарядтары болады, ең кіші бөлшек атом оң және теріс зарядтан түзілген, элементтердің атомдары планетарлық құрылыста болады деген. Бұл атомның күрделі жүйе екендігі жөнінде айтылған ең алғашқы пікір еді. Осы жайында А. М. Бутлеров (1886) былай деді: “Атомдар . . . жаратылысы бойынша бөлінбейді емес, қазіргі біздің қолымызда бар тәсілдермен ғана бөлінбейді . . . кейін ашылатын жаңа процестерде бөлінуі мүмкін”. Сондай-ақ бірнеше ғалымдар осындай түсінікте болды.
ХІХ - ХХ ғасыр аралығында физика мен химия саласында атомның ыдырайтындығын, атомдарда ұсақ бөлшектер бар екені дәлелдейтін жаңалықтар ашылды.
Д. Ж. Томсон катод сәулелерін зерттеу нәтижесінде электронды және атом изотоптарын ашты. Релтген кейінірек өз есімімен аталған сәулелерді зерттеді. Ерлі-зайыпты Кюрилер (1898 ж) радиоактивтілікті ашты. Э. Резерфорд (1911) α-бөлшектердің металл қаңылтырында шашырауларын зерттей келе атом ядродан және оны айнала қозғалатын электрондардан тұрады деген шешімге келді. Резерфордың моделі бойынша атом өте кішкентай, бірақ массивті ядродан (мөлшері
 10
-14
м) тұрады, ядроның заряды q=z⋅e (1)
10
-14
м) тұрады, ядроның заряды q=z⋅e (1)
Мұндағы: z- элементтің реттік номері
е = 1, 6 ⋅ 10 -19 Кл, протонның заряды.
Ядроның айналасында бейтарап атомда z электрон қозғалыста болады. Атомның диаметрі 10 -10 м шамасында әрі ядро мөлшерінен ∼ 10 +4 есе үлкен.
Ең қарапайым сутегі атомы бар протон (ядро) мен айналасында дөңгелек орбита бойынша қозғалған бір электроннан тұрады. Протонның массасы электрондікінен 1836 есе артық болғандықтан, электрон өте үлкен жылдамдықпен қозғалады деп протонның қозғалысын елемеуге болады. Электронды орбиталда ұстап тұратын, әрі оған центрге тартқыш үдеу беретін Кулон күші:
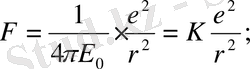 (2)
(2)
Механикадан белгілі, дене шеңбер бойымен қозғалғанда оның нормаль үдеуі (жылдамдықтың тек бағыт бойынша өзгереді)
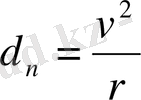 (3)
(3)
Сонда Ньютонның ІІ заңы бойынша электронның қозғалыс теңдеуін келесі түрде жазуға болады.
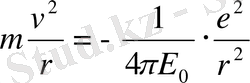 (4)
(4)
Бұл теңдеудегі минус таңбасы протон мен электрон арасындағы күш - тартылу күш екендігін білдіреді.
Дат ғалымы Нильс Бор өзінің сутегі атомының спектрін түсіндіретін жұмысы да осы. Резерфордтың планетарлық атом моделін қолданады.
Атом ядролық моделі
Атомның құрамын және құрылысын зерттеу жөніндегі тәжірибені ХХ ғасыр басында ағылшын физигі Резерфорд жасады. Ол өлшемдері жағынан атоммен салыстырарлықтай өте кішкентай, ал жылдамдығы үлкен зарядталған бөлшектерді металл пластина арқылы өткізген. Осы бөлшектердің “снарядтардың” металл атомдары арқылы қалай ұшып өтетіне қарап, атом ішінде басқа бір зарядталған бөлшектердің бар-жоғын білуге болады. Табиғатта кездесетін кейбір заттардың (мысалы, уранның, родийдің т. б. ) атомдарынан оң зарядпен зарядталған кішкентай бөлшектер үздіксіз ұшып шығып тұрады екен. Мұндай бөлшектер альфа α-бөлшектер деп аталады. Бұл бөлшектердің жылдамдығы өте үлкен 15. 000 км/сек шамасында. Яғни Резерфорд тәжірибиесінде табиғаттың өзінде кездесетін осындай кішкентай снарядтарды пайдаланды.
4
3
1 2
0 0 0
0 0 0
0
- қорғасын қорап ішіне α бөлшектерін шығаратын зат қояды.
- Бөлшектер қораптан шоқ түрінде ұшып шығады.
- өте жұқа пластина қойылған (қалыңдығы 0, 001 мм) (алтын фольга) осы пластина арқылы α-бөлшектердің көпшілігі еш нәрсе жоқтай кедергісіз ұшып өтеді, біразы аздап ауытқыған.
- Яғни тәжірибеге қарағанда атом ішінде зат бөлшектерімен толықтырылмаған бос жерлер (бостықтар) бар. Атомның едәуір үлесін осы бостықтар алып тұрады. Әйтпесе көптеген α-бөлшектер пластина арқылы тура бағытпен ұшып өте алмас.
Ал аздап ауытқуына Резерфорд тәжірибесі атомның ішінде зарядталған бөлшектер бар екенін көрсетті, яғни Резерфорд жорамалдауынша: атомның құрылысы күрделі. Атомның ортасында оң зарядпен зарядталған бөлшек атом ядросы бар. Шанына таяп барған аздаған α-бөлшектерді кейін итеріп тастаған міне осы ядро, ядродан едәуір қашықтықта теріс зарядталған ұсақ бөлшектер - электрондар бар.
Атомның күрделілігін зерттейтін тәжірибелер
Барлық заттар бөлiнбейтiн аса ұсақ бөлшектерден - атомдардан тұрады деген ұғым ерте қалыптасқан болатын. Егер атом шындығында заттың бөлiнбейтiн алғашқы кiрпiштерi болса табиғаттағы кездесетiн сан алуан заттарға сан алуан атомдар сәйкес қойылуы тиiс. Бұлай болуы бiр жағынан күмән туғызады.
Физика ғылымының дамуы барысында ХIХ ғасырдың аяғына қарата атомның қасиеттерiне байланысты жаңа тәжiрибелiк деректер жинала бастады. Мысалы М. Фарадей 1833 жылы электролиз құбылысын зерттеу барысында электролит ертiндiлерiндегi ток иондардың реттелген қозғалысы екенiн анықтады. Ал 1897 жылы Дж. Томсон сиретiлген газдардағы электр разрядын зерттеу барысында қыздырылған немесе ультракүлгiн жарықпен сәулелендiрiлген кез-келген химиялық элементтiң атомы өзiнен терiс зарядталған бөлшектердi шығатынын анықтады. Осылай алғашқы элементар бөлшек - электрон ашылды. Атом құрылысының күрделiлiгiне нұсқайтын тағы бiр бұлтартпас факт 1869 жылы орыс ғалымы Д. И. Менделеев ашқан химиялық элементтердiң периодтылық заңы. Атомдық масса өскен кезде элементтердiң қасиеттерiнiң қайталануын атомның құрамына кiретiн бөлшектердiң саны өскен кезде оның iшкi құрылымының қандай да бiр ерекшелiгiнiң қайталануымен түсiндiруге болатындай.
- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz