Құрылыс байланыстырғыш заттардың классификациясы, шикізаттары және физико-химиялық қасиеттері


КІРІСПЕ
Құрылыста көпшілігінде толтырғышы ортақ монолитке цементтелген жасанды құрылыс конгломераттары (ЖҚК) кеңінен қолданылады. Жасанды және табиғи конгломераттардың пайда болу ерекшелігі, оларда полигранулярлы немесе басқа типтегі дискретті толтырғыштарды (талшықты, пластинкалы, т. б. ) міндетті түрде цементтеу кезінде екінші реттік (байланыстырушы) заттар немесе алғашқы байланыстар ( химиялық, электрлік, т. б. ) көмегімен жүреді. ЖҚК көмегімен кез-келген формада және көлемде, қажетті беріктікте құрылымдар құрастырылып жасалады, сонымен қатар оларға сенімділік пен ұзақ мерзімділігін қамтамасыз ететін өзге де қасиеттер беріледі. Бұл материалдар құрылыс мақсаттарына байланысты құрамы мен қасиеттерін реттеуге мүмкіндік береді. Болжалды есептеулер көрсеткендей, құрылыс материалдарының жалпы көлемінің 90 Ғ немесе одан да көп бөлігі ЖҚК-ны және олардың компоненттері - байланыстырғыштар мен толтырғыштарды құрайды. Жалпы материалдардың қалған 10 : немесе одан аз бөлігін металл және ағаш материалдары құрайды . Бұл материалдар ЖҚК-ға ұқсас құрылымға ие. Олар кристаллдар жиынтығы түріндегі /толтырғыштар/ мен аморфты зат саналатын /байланыстырушылардан\ тұрады. Бүгінгі күнге дейін барлық белгілі және белгісіз ЖҚК-ларды екі түрге біріктіруге болады: байланыстырғыштың химиялық және физико-химиялық түрлендірулерінің әсерінен құрылымның түзілуі нәтижесінде салыстырмалы түрде төмен температурада пайда болатын күйдірілмеген, әсіресе ерітінділер күйінде (молекулалық және коллоидты, сұйық және қатты, сұйытылған және концентрацияланған) ; қатаюы негізінен конгломераттардағы байланыстырушы қызметін атқаратын отты -сұйық балқымаларды салқындату кезінде пайда болатын күйдірілген . Бұл екі түрдің бөлінуі шартты болып табылады, өйткені олардың арасында ерітінділер мен балқымалардай нақты шекараны қою қиынға соғады. Сондай-ақ, екі типке де тән процесстердің тізбекті немесе параллельді біріктірулер кезінде қатаятын конгломераттар типі болуы мүмкін. Күйдірілмеген ЖҚК-лер басым жағдайға ие. Олардағы цементтейтін бөлік келесі байланыстырғыштарға бөлінеді: бейорганикалық, органикалық ( полимерді қосқанда), комплексті . ЖҚК массасы бойынша бөлуге болады (аса ауыр, ауыр, жеңіл, ұялы) ; өндірістік мақсаттары бойынша (құрылыымдық, жылу оқшаулағыш, гидротехникалық, химиялық төзімді, т. б. ) және т. б. Құрылыс материалдарын өндіру мен пайдалануға байланысты процесстердің басым көпшілігі химиялық сипатта болады. Тұрғын үйлерді кірпіштен немесе бетоннан жасалған бұйымдардан тұрғызу үшін 1 м2 тұрғын үйге орта есеппен 300 кг байланыстырғыш материалдар жұмсалады. Байланыстырғыш материалдар қосылыстарының әр түрлі химиялық қасиеттерін қамтитынына байланыстыолардың көптеген жіктелімдері бар. Мысалға, оларды топқа бөлуге болады:
- Гетерогенді жүйелердің дисперсия дәрежесі бойынша (Н. Ф. Федоров)
- Кристаллды-химиялық принципке сәйкес (Э. А. Эванс)
- Қатаю кезіндегі химиялық және физикалық процесстердің айырмашылығы бойынша (В. Ф. Журавлев )
Бұл оқулықта біз қатаю жағдайына және қолдану саласына байланысты байланыстырғыш заттардың жалпы қабылданған бөлінуін қолданамыз.
- Байланыстырғыш заттар туралы негізгі ақпараттар
Байланыстырғыш заттар туралы түсінік
Құрылыстық байланыстырғыш заттар - сумен араластырғанда пластикалық, жеңіл өңделетін масса түзетін, ұнтақ тәрізді материал, ол уақыт өте қатты тас тәрізді денеге айналады.
Құрылыс байланыстырғыштары шығу тегіне байланысты екі топқа бөлінеді:
- Бейорганикалық (минералды) байланыстырғыш заттар;
- Органикалық байланыстырғыш заттар, негізінде мұнай айдау мен таскөмір өнімдері (битумдар, шайырлар)
Ары қарай бейорганикалық байланыстырушы заттар қарастырылады.
Байланыстырғыш заттар негізінде құрылыста қолданылатын жасанды материалдар жасалынады. Құрылыста құрамына байланысты әр түрлі қоспалар қолданылады:
Цементті қамыр - байланыстырушы зат пен судың қоспасы;
Цемент тасы - қатқан цемент пастасы;
Ерітінді қоспасы -байланыстырғыш зат пен судың, майда толтырғыштың (құм) қоспасы;
Құрылыс ерітіндісі - қатқан ерітінді қоспасы;
Бетон қоспасы -байланыстырғыш зат пен судың, ұсақ және ірі толтырғыштардың (құм, қиыршық тас) қоспасы;
Бетон -қатайтылған бетон қоспасы;
Темірбетон - болат арматурамен біріктірілген бетон.
Байланыстырғыш заттардың классификациясы
Минералды байланыстырғыш заттар құрамына, қатаю жағдайына, қолдану аймағына байланысты жіктеледі.
Ең ауқымды тобын гидравликалық байланыстырғыш заттар құрайды, олар сумен араластырылғаннан кейін ауада аз уақыт қатайғаннан кейін судың астында беріктігі артады береді. Осы қасиетінің арқасында гидравликалық байланыстырғыш заттарды сулы ортада жер үсті және жер асты құрылыстарда қолданады.
Гидравликалық байланыстырғыш заттарға жатады:
- Әкті: әлсіз гидравликалық, күшті гидравликалық;
- Роман-цемент;
- Портландцемент және оның түрлері (тез қататын ПЦ, пластифицирленген, гидрофобты, сульфатқа төзімді, экзотермиясы бар, декоративті және т. б. ) ;
- Пуцолланды (пуцолландыПЦ, әкті-пуцолланды ПЦ) ;
- Қожды цемент (қожды ПЦ, әк-шлакты цементтер) ;
- Глиноземді цемент;
- Арнайы цементтер ( кеңейетін, қысылмайтын, ыстыққа және қышқылға төзімді цементтер, т. б. ) .
Ауалық байланыстырғыш заттарды сумен араластырғанда алынатын қамыр тек ауада ғана қатайтып, қатаю салдарынан пайда болған беріктігін сақтайды.
Бұл топқа жатады:
- Әкті (сөндірілмеген әк, сөндірілген (гидратты) әк, әк қамыры) ;
- Гипсті (аз күйдірілген: құрылысты, қалыпталған, жоғары беріктікті гипс; жоғары күйдірілген: ангидридті байланыстырғыш, эстрих-гипс) ;
- Магнезиалды байланыстырғыш заттар (каустикалық магнезит, каустикалық доломит) ;
- Сұйық шыны. 2. Байланыстырғыш материалдарды өндіруге арналған шикізаттар
Байланыстырғыш материалдарды өндірудің негізгі материалы әр түрлі тау жыныстары мен қосымша шикізаттар болып табылады. Табиғи материалдарға жатады: негізінен сусыз кальций сульфатынан CaSO 4 тұратын дигидрат кальций сульфатына CaS0 4 •2H 2 0 немесе ангидридке бай гипс тасы, карбонатты әктас, бор CaCO 3 , магнезит MgCO 3 , доломит MgCO 3 •CaCO 3 ; сазды- СаСОз мен MgСО 3 аз мөлшердегі саздар мен мергельдер. Оған құрамында алюминий оксидінің 70% және одан да көп болатын боксит жатады; кремнеземді-негізінен кремний оксидінен тұратын кварц құмы, диатомит, трепел және т. б. жатады.
Байланыстырғыш материалдарды өндіруге арналған шикізаттар диірмендерде ұнтақталады. Ұнтақтауды күшейту физико-химиялық әдістермен жүзеге асырылады, атап айтқанда ұнталған материал бөлшектерінің бір-біріне жабысып, диірмендердің қабырғаларына жабысып қалуына жол бермейтін ББЗ (беттік белсенді заттар) қолданады.
Екінші реттік шикізатты қолдану экономикалық тұрғыдан тиімді. Екінші реттік шикізат кейбір салалардың қосалқы өнімдері болып табылады (металлургия, энергетика, химия, т. б. ) . Оларға қож, күл, белсенді кремний және басқалары кіреді. Құрамы бойынша байланыстырғыш заттарға жақын және табиғи заттармен салыстырғанда химиялық белсенділігі жоғары болады. Олардың химиялық белсенділігі термиялық өңдеумен байланысты, осының нәтижесінде өндірістік қалдықтар шыны тәрізді (аморфты) күйге ауысады және артық энергия алады.
Минералды байланыстырғыш заттар өндірісінің дамуы туралы қысқаша ақпарат
Күйдірілмеген саз - адамдар қолданған алғашқы байланыстырғыш зат. Жасанды байланыстырушы құрылымдар - гипс пен әк, біздің дәуірімізге дейінгі 2000-3000 жылдары тау жыныстарын жағу нәтижесінде алынған. Ресейде байланыстырғыш заттар ежелгі уақытта қолданылған, ал Киевте әк 990 жылы қолданылған. XVIII ғасырдың соңы -XIX ғасыр басында байланыстырғыш заттардың өндірістік және қолдану тәжірибесі қарқынды жүйеленген.
Академик В. М. Севергиннің 1807 жылы жарық көрген еңбектерінде, кейбір байланыстырушы заттардың қасиеттері сипатталған. Шарлевилдің 1822 ж. шыққан еңбегі бір топ орыс ғалымдары жүргізген арнайы эксперименттердің нәтижелеріне арналған. Е. Челиеваның 1820 ж. шыққан кітабында әк пен саздың қоспасынан байланыстырғыш зат алу әдісі қарастырылған.
Бірінші дүниежүзілік соғысқа дейін Ресейде жылдық қуаты 1, 6 миллион тонна цемент өндіретін 60 цемент зауыты болған. Әк пен гипстің көптеген кәсіпорындары салынды.
XIX ғ мен XX ғ басында Д. И. Менделеев бастаған орыс ғалымдары байланыстырғыштардың қасиеттерін зерттеуді жалғастырды. А. Р. Шуляченко (1841-1903) байланыстырғыштардың қатаю процесстерін зерттеп, 1901 жылы «Цемент, оны өндіру және» журналын құрды.
Н. Н. Лямин (1870-1912) цементтің теңіз суынан бұзылуы мен қатаюы аумағында физико-химиялық зерттеу жүргізді.
А. А. Байков, С. И. Дружинин, В. А. Кинд, В. Н. Юнг және т. б. ғалымдар байланыстырушы заттарды өндіру ғылымы мен тәжірибесіне көптеген үлестерін қосты. А. А. Байков байланыстырғыш заттардың қатаюы теориясын жасап, цемент бұзылуының себептерін зерттеді. С. А. Дружинин (1872-1935) цемент беріктігіне қоспалардың әсерін зерттеді.
В. А. Кинд портландцементтің минералдық құрамын есептеу әдісін ұсынды. В. Н. Юнг өз әріптестерімен бірге бірқатар цементтерді өндіру технологиясын жасады.
В. Ф. Журавлев силикаттардың, алюминаттардың, ферриттердің және Д. И. Менделеев жүйесінің II тобы металлдарының басқа қосылыстарының байланыс қасиеттерінің жұп және тақ қатарларында орналасуына байланысты периодтылығын белгілеген. П. П. Будниковтың гипсті байланыстырғыш заттарға арналған еңбектері белгілі.
Қазіргі уақытта ғалымдар цемент өнеркәсібінің дамуына ықпал ететін байланыстырғыш заттар саласындағы зерттеулерін жалғастыруда.
Болашақтың материалы болып компоненттері еш кемшіліктерсіз, бірқатар артықшылықтары бар біріктірілген конструкциялар саналады.
Құрылыс алаңдарында кейбір мәселелер тікелей шешіледі, мысалға, полимет-цемент композицияларын өндіруге және бетонды монолиттеу мәселелерін қарастыруға болады.
Бақылау сұрақтары
- Қандай заттарды байланыстырғыш заттар деп атайды ?
- Құрамына байланысты құрылыс ерітінділерін қалай атайды ?
- Қатаю жағдайына байланысты байланыстырғыштар қалай жіктеледі?
- Ауалық байланыстырушыларға қандай құрылыс материалдары жатқызамыз? Мысал келтіріңіз.
- Гидравликалық байланыстырушыларға қандай құрылыс материалдары жатады? Мысал келтіріңіз . .
- Байланыстырғыш заттар алуда қандай шикізаттар қолданылады?
- Өндірістік қалдықтардың табиғи шикізатпен салыстырғанда қандай айырмашылықтары бар?
- Қазіргі таңда қандай ЖҚК колданылады?
- БАЙЛАНЫСТЫРҒЫШ ЗАТТАРДЫҢ ФИЗИКО-ХИМИЯЛЫҚ ҚАСИЕТТЕРІ
БАЙЛАНЫСТЫРҒЫШ ЗАТТАРДЫҢ НЕГІЗГІ ФИЗИКО-ХИМИЯЛЫҚ ҚАСИЕТТЕРІНЕ ЖАТАДЫ: дисперсия, икемділік, қатаю қабілеті.
- Дисперсиялылығы
Құрылыс материалдарын өндіру үшін қолданылатын байланыстырғыш заттардың белсенділігі жоғары болуы, яғни сумен белсенді әрекеттесуі керек. Гидравликалық белсенділік гетерогенді жүйелерге қолданылатын массаның әсер ету заңына сәйкес, бөлшектерінің мөлшері 1-ден 40 мк -ға дейін аралықта болатын байланыстырғыштардың дисперсия дәрежесінің жоғарылауымен өседі. Байланыстырғыш заттар химиясының негізін қалаушылардың бірі В. К. Дементьев 20 ғ. Басында дисперсия дәрежесінің артуымен құрылыс материалдарының беріктігінің өсетінін тәжірибе жүзінде растады. Оның айтуынша, ұсақ ұнтақталған цементтен алынған сынамалардың сығылу беріктігі үш жылдан кейін 420 кг/см 2 , ал ірі цементтен небәрі 175 кг/см 2 -ге жеткен. Заманауи зерттеулер байланыстырғыштардың меншікті бетін 500-1000 см /г -ге ұлғайтудың жеткілікті екендігін көрсетті, әсерінен бір күндік бетонның беріктігі екі еселенеді, бірақ жиырылуы күшейіп панельдерде жарықтар пайда болады.
- Икемділік
Икемділік дегеніміз- сыртқы механикалық күш әсерінен деформациялану қабілеті және сыртқы әсер болмаған жағдайда берілген пішінін сақтау.
Байланыстырғыш заттардың сумен араласуы кезінде пайда болатын байланыстырушы қамырдың иілгіштігі судың беткі қабаттарының ерекшк қасиеттеріне байланысты. Байланыстырушы бөлшектерге тікелей жақын орналасқан судың қасиеттері кристалды күйдегісіне ұқсас.
Қабатының қалыңдығы микронның бірнеше фракциясына ие байланысты күйдегі су 1 см 2 -та бірнеше грамм қысымға төзеді. Жартылай қатты сулы қабықтар әрі байланыстырғыш, әрі жағар май болып табылады. Бұл қатты денелердің сырғып кетуіне және деформациялануына мүмкіндік береді. Пластикалық және жақсы қалыптасқан қоспаларды алу үшін байланыстырғышты араластыруға керек су мөлшерін көбейту керек. Алайда, байланыспаған су буланып, бос тесіктер түзеді, бұл материалдың беріктігі мен төзімділігін төмендетеді. Беттік белсенді заттардың көмегімен кристаллдардың пішіні мен өлшемін, меншікті бетінің ауданын және т. б. өзгерте отырып, қажетті судың мөлшері мен байланыстырғыш заттардың шығынын азайтуға және икемділігін сақтап қалуға болады.
- Қатаю қабілеті
Байланыстырғыш заттарды қатайту процесі күрделі мәселелердің бірі болып табылады. Физика-химиялық процестердің нәтижесінде пластикалық байланыстырғыш қамыр қатты тас тәрізді денеге айналады. Қатаю процесі екі кезеңге бөлінеді: ұстасуы (қамырдың икемділігін жоғалту) және қатаю (беріктік жиынтығы) . Бетон қоспаларын төсеу және тығыздау қоспасы әлі икемділігін жоғалтпаған кезде жасалады, сондықтан ұстасудың басталу және аяқталу уақытын ескеру қажет. Ұстасу ұзақтығы байланыстырғыш қамырдың құрылымын сипаттайды. Бірте-бірте материал қатайып, оның беріктігі артады. Қатаюдың үш түрі бар: гидратациялық, карбонатты, гидросиликатты.
Байланыстырғыш зат сумен әрекеттескенде пайда болатын гидратациялық қатаю механизмін қарастырыңыз. Сонымен, алғашқылардың бірі, Ле-Шательенің кристализациялық теориясы (1882 ж. ) қатаюды қаныққан ерітіндінің түзілуіне және одан ылғалданудың кристалды өнімдерінің бөлінуіне әсерінің нәтижесі деп түсіндіреді.
Михаэлистің коллоидтық теориясына сәйкес (1892) су молекулалары біртіндеп бастапқы байланыстырғыш минералдардың кристалдық торына енеді. Бұл жағдайда пайда болған гельдер қатаяды, өйткені олар суды байланыстыру нәтижесінде дегидратацияланады. А. А. Байков (1923) қатаю процесін мына кезеңдер бойынша қарастырды: қанықтыру (дайындық), коллоидация және кристалдану.
Қанықтыру кезеңінде су / қатты фазалардың шекарасында еритін байланыстырғыш бөлшектер қаныққан ерітінді түзеді және гидратацияланады.
Коллоидация кезеңінде бастапқы қосылыстарға қарағанда суда аз еритін гидраттық неоплазмалар қаныққан ерітінді түзеді. Қаныққан гель саналатын қаныққан ерітіндіден кристалды өскін баяу шығарылады. Сонымен қатар, гель сусызданады және босаған су бастапқы байланыстырғыштың бөлшектерін ылғалдандырады. Кристалдану кезеңінде түпкілікті қатаюмен қатты тас тәрізді дененің пайда болады. Үш кезең де бірінің артынан бірі жүрмейді, бірақ бірін-бірі қабаттастырады. Төменде әк-құм қоспаларын автоклавтау кезеңінде пайда болатын ауа гидратталған әк үшін карбонатты қатайту және гидросиликатты қатайту туралы айтылады.
Қазіргі уақытта рентгенография, электронды микроскопия және т. б. сияқты жаңа зерттеу әдістерінің пайда болуымен қатаю процесі күрделірек саналады. Алайда, осы уақытқа дейін қатаюдың бірыңғай теориясы жоқ. П. А. Ребиндер және оның қызметкерлерінің құрылымның физика - химиялық негіздеріне арналған жұмыстары маңызды саналады.
Термодинамикалық тұрғыдан алғанда, байланыстырғыштар артық бос энергияға ие және суда өздігінен энергияның аз қоры бар гидратациялық неоплазмаларға өтеді. Термодинамика реакция жолына қарамастан жүйенің бастапқы және соңғы күйін ескереді.
- Қатаю қатайған кезде судағы зат концентрациясының (иондар түрінде) өзгеру кинетикасы үлкен теориялық және практикалық қызығушылық тудырады, өйткені ол қатаю процесін қай кезеңде және қай уақытта анықталатындығына мүмкіндік береді. Осы кезеңді жеделдету арқылы қатаю процесін тездетуге болады.
Тұтқыр заттың гидратациялық қатаюымен бастапқы фазаның еруі және соңғы фазаның берілген ерітінділерінен кристалдануы келесі схема бойынша жүреді:
А→Б→В,
Мұнда А-бастапқы зат; Б - суда еритін заттың иондары; в - гидраттық неоплазмала /новообразования/. Байланыстырғыштың қатаюы кезінде талаптардың концентрациясының өзгеруінің кинетикалық қисықтары байланыстырғыштың түріне байланысты емес және ол 2. 1. суретте көрсетілген.
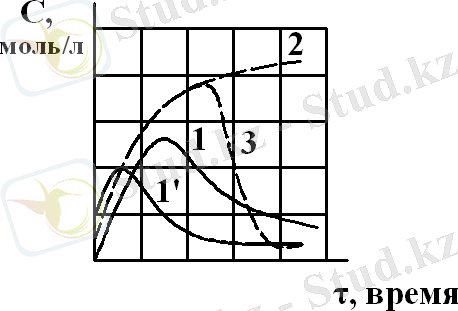
сурет 2. 1. . Мономинералды байланыстырғышты гидратациялау кезіндегі концентрацияның өзгеруінің кинетикалық қисықтарының сипаты (1 және 1'), оның неоплазмаларының кристалдануынсыз еруі (2), ерітіндіні толтырмай кристалдау (3)
Максималды қисық 1 ' температура жоғарылаған кезде солға, төмендеген кезде оңға қарай жылжиды. Кристалдану болмаған кезде процесс 2 қисығын білдіреді. Иондарды байланыстыру және кристалдану кезінде олардың кинетикасы 3 қисық сызықтан шығады 3. 2 Қисықтағы максимум байланыстырғыштың еруі жаңа фазаның пайда болуы үшін қажет болғаннан гөрі сұйық фазаға көбірек заттың енуін қамтамасыз ететіндігін көрсетеді.
3 қисығындағы максимумның оң жағында еритін байланыстырғыш кристалдануға кеткен заттың мөлшерін толығымен толтыра алмайды. Максимум 3 нүктесінде байланыстырғыштың еруіне байланысты заттың сұйық фазаға жалпы түсуі мен кристалдану кезінде шығаруы арасындағы теңдік байқалады.
Ерітілген байланыстырғыш заттың мөлшері мен ерітіндідегі және одан неоплазмалар түрінде түскен заттың мөлшері арасындағы теңгерім (сусыз заттарға қайта есептегенде) формуламен көрсетіледі:
•m 1 + • m 2 + c • = con st ,
мұндағы c τ - уақыт τ аралығындағы байланыстырғыштың концентрациясы,
∆mi=m 1 -m 1. 0 ; ∆m 2 =∆m 2 -m 2. 0 ; m 1 және m 2 - сәйкесінше гидраттың тұтқыр және жаңа фазаларының массасы ;
m 1. 0 , m 2. 0 - тәжірибенің басында бірдей.
Бастапқы және соңғы өнімдердің мазмұны, сондай-ақ ерітіндінің концентрациясы сәйкес өзгереді 2. 2. суретте
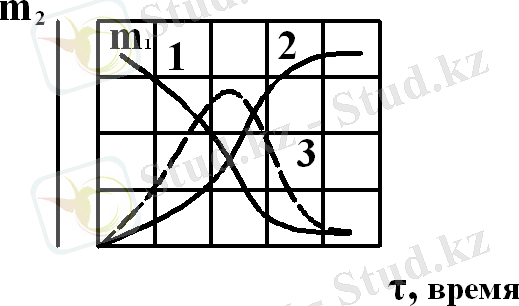
Сур. 2. 2. Типтік кинетикалық қисықтарда бастапқы заттың кемуі (1), Жаңа қосылыстың пайда болуы (2) және ерітіндідегі зат концентрациясының өзгеруі (3)
тұтқырдың гидратациясының дәйекті реакциясы үшін
3. Байланыстырғыштардың ерігіштігі
Гидратацияның қатаю процесі екі кезеңнен тұрады: бастапқы заттардың ерітіндісі және гидраттар түрінде қосылыстардың бөлінуі. Процесс қатты заттардың еруі сияқты, материалдың дисперсиясының жоғарылауымен, яғни, байланыстырғыштардың ұнтақталуының жоғарылығымен және температураның өсуімен жеделдетіледі.
Көптеген байланыстырғыштар аз ериді және ерітіндіде иондарға ыдырайды: Са 2+ , Al 3+ , SiO 2- , SO 2- , АlO және т. б., олар суда гидраттанады немесе бір уақытта гидратациямен гидролизденеді (Al 3+ , SiO 2- , А1О -2 иондары) .
Байланыстырғыштың ерігіштігі деп белгілі бір жағдайларда метастабильді қатты фазамен теңдікке сәйкес келетін ерітіндідегі заттың мүмкін болатын ең жоғары концентрациясымен түсіндіріледі.
Кейбір тұтқыр заттар мен олардың гидратация өнімдерінің ерігіштігінің экспериментті табылған мөлшері 1-кестеде келтірілген.
Байланыстырғыштар және олардың гидратация өнімдерінің ерігіштігі
Кесте 1
зат
Ерігіштігі, моль/л
Гипс CaS0 4 • 2Н 2 0
0. 0153
0. 0154
кальций сульфатының жартыгидраты
0. 06
CaSO 4 • 0. 5H 2 O
0. 05
0. 04
үшкальцийлі алюминат
0. 0071
ЗСаО • Аl 2 0 3
0. 0076
0. 0078
үшкальцийлі силикат ЗСаО Si0 2
0. 0015
0. 0015
Екікальцийлі силикат 2СаО Si0 2
0. 0011
0. 0012
Гиллебрандит 2CaO • Si0 2 •aq
0. 0001
Ксонотлит CaO • SiO 2 •aq
0. 0002
Тоберморит 5CaO • 6SiO 2 •aq
0. 0002
Кестеге сәйкес, байланыстырғыштардың ерігіштігі осы жағдайларда термодинамикалық тұрақты неоплазмалар ерігіштігінен асып түседі, сондықтан еріту процесі температураның жоғарылауымен өздігінен жүреді, ал жүйенің бос энергиясы төмендейді.
Кейбір байланыстырғыштарда, мысалы CaSO 4 • 0, 5H 2 O , ерігіштігі-
температураның жоғарылауымен төмендейді, бұл олардың гидратациялық қатаюының процестерін талдау кезінде ескерілуі керек. Ерітілген байланыстырғыштар кристалданып, жоғары дәрежелі гидратты неоплазмаларға айналады.
Неоплазмалардағы байланыс сипаты
Тұтқыр заттың қатаю процесінде жаңа құрылымдар пайда болады, оларды П. А. Ребиндер келесідей бөледі:
1) Коагуляциялық құрылымдар . Олар молекулааралық өзара әрекеттесу күштеріне байланысты пайда болады және тиксотропия мен жоғары майысатын қасиеттерге ие. Коагуляцияның беріктігі аз, сондықтан олардың қасиетін ББЗ-мен жақсартуға болады. Коагуляциялық құрылымдардың қалыптасу кезеңінде тығыздап жасау тиімді, өйткені бұл ең аз энергияны қажет етеді.
2) Шартты-коагуляциялық құрылымдар . Олар механикалық тоқудың арқасында "құйрық" немесе арасында сұйық қабат жоқ ұзартылған пішінді бөлшектердің "киізі" түрінде пайда болады. Бұл құрылымдардың беріктігі суланғанда төмендейді, содан кейін екінші рет кептіру арқылы қалпына келтіріледі. Гипске ұқсас құрылымға ие.
3) Кристалдану құрылымдары. Олар тиісті гидраттардың кристалдарының химиялық әрекеттесуі кезінде пайда болады, майыспайды және қайтымсыз жойылады.
Алдымен байланыстырғыш коагуляциялық құрылымға ие болады, содан кейін қатаю процесінде шартты коагуляциялық және кристалдану құрылымдары пайда болады. П. А. Ребиндер, Е. Е. Сегалова, а. ф. Полак және т. б. мәліметтері бойынша кристаллизациялық құрылымның беріктігі екі түрлі әсер ететін процестердің нәтижесі болып табылады: кристаллизациялық байланыстардың пайда болуына байланысты беріктіктің жоғарылауы және ішкі кернеулердің дамуына байланысты беріктіктің төмендеуі. Ішкі кернеулер үлгілердің тығыздығының жоғарылауымен, кернеудің жоғарылауымен және кристалдану байланыстардың санының өсуімен пайда болады.
... жалғасы1 Тиксотропия-құрылымды бірнеше рет қайтымды қалпына келтіру
Сонымен, тұтқыр материалдың беріктігі оның тығыздығына, химиялық-минералогиялық құрамына, Ішкі кернеулерге және неоплазмалардың кристалдану кинетикасына байланысты.
- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz