Калий бромидін өндірудің технологиясы, қасиеттері және материалдық баланстың есебі


ҚАЗАҚСТАН РЕСПУБЛИКАСЫ БІЛІМ ЖӘНЕ ҒЫЛЫМ
МИНИСТРЛІГІ
ҚАРАҒАНДЫ ИНДУСТРИЯЛЫҚ УНИВЕРСИТЕТІ
«ХимиЯЛЫҚ технология ЖӘНЕ экология» КАФЕДРАСЫ
«Жалпы химиялық технология» пәнінен
«Калий бромидін өндіру» тақырыбы бойынша
Курстық жұмысқа
Түсініктемелік жазба
КЖ. ЖХТ. 6В007204. 19. 14. 39. ТЖ
Орындаған:
ТФП-19К-1 топ студенті Жиен Аяулым
Жоба жетекшісі:
РhD. аға оқытушы
Орындау бағасы:
Комиссия мүшелері:
ТҒМ. Оқытушысы Жуманазарова ҒМ
х. ғ. к., кафедра
меңгерушісі қ. а. Кабиева С. К.
Теміртау, 2022 ж
МАЗМҰНЫ
I. кіріспе
1-бөлім Əдебиеттік шолу өндіріс бойынша, тарихы кезеңдері сипаттамасы
1-2-бөлім Калий бромидінің алынуы тарихы
1-3-бөлім Калий бромидінің бастапқы сипаттамасы
1-4-бөлім Калий бромидінің физикалық, химиялық қасиеттері
1-5-бөлім Алу химиясы реакция барысы (давлениясы катализаторы)
1-6-бөлім Калий бромидін өндіру процесінің технологиялық схемасы және оның сипаттамасы
ІІ. МАТЕРИАЛДЫҚ БАЛАНСЫН ЕСЕПТЕУ
ІІІ. ҚОРЫТЫНДЫ
Əдебиеттер тізімі
Кіріспе
Жалпы химиялық технология нені үйретеді?
Шикізатты тұтыну тауарлары мен өндіріс құралына айналдыру тәсілдері мен процестерін зерттейтін ғылым технология деп аталады. «Өңдеу әдістері мен процестері» ұғымы деп адамнан тікелей пайдаланылатын немесе өз кезегінде басқа өнімді немесе өндіріс құралдарын алу үшін шикізат ретінде қызмет ететін, берілген өнімді алу үшін әр түрлі машиналар мен аппараттарда шикізатпен жүргізілетін дәйекті операциялардың тізбегі түсініледі. Технология шартты түрде механикалық және химиялық болып бөлінеді. Металды өңдеу әдістері мен құралдары металл технологиясының пәні, ал машиналар мен аппараттарды жасау әдістері мен құралдары - машина жасау пәні. Механикалық технология процестері негізінен өңделген заттардың сыртқы түрін немесе физикалық қасиеттерін өзгертетін, бірақ олардың химиялық құрамына әсер етпейтін механикалық әрекетке негізделген. Химиялық технология процестеріне табиғаты күрделі химиялық және физикалық-химиялық құбылыстарға негізделген шикізатты химиялық өңдеу жатады.
Химиялық технологияның мазмұны
Химиялық технология бірінші кезекте физикалық химия, химиялық термодинамика және химиялық кинетика сияқты химиялық ғылымдарға негізделген, бірақ сонымен бірге ол жай қайталанбайды, сонымен қатар осы ғылымдардың заңдарын кең ауқымды өндірістік процестерге қатысты дамытады. технологиялар, академик Д. П. Коновалов химиялық технологияның негізгі міндеттерінің бірін оның пәнін таза химиядан бөліп қарастырып, «операцияның ең тиімді бағытын белгілеу және сәйкес қондырғылардың аспаптары мен қосалқы механикалық құрылғыларын жобалауды» қарастырды. Сондықтан химиялық технологияны экономика, физика, математика, кибернетика, қолданбалы механика және басқа да техникалық ғылымдармен тығыз байланыссыз ойлау мүмкін емес. Оның пайда болуының алғашқы кезеңінде химиялық технология негізінен сипаттама ғылымы болды.
Химия өнеркәсібінің маңызы
Химия өнеркәсібі негізгі жетекші салалардың бірі болып табылады. Ол шығаратын өнімдердің ассортименті өте үлкен және әр түрлі: қазіргі кезде отандық химия өнеркәсібі 50 мыңнан астам өнім шығарады. Химиялық өнімдердің ең маңыздысы - тыңайтқыштар, пестицидтер, қышқылдар мен сілтілер, лактар мен бояулар, синтетикалық талшықтар, пластмасса, синтетикалық каучук, көмірсутектердің көптеген туындылары және т. б. Көмірді, мұнайды, табиғи газды, ағашты және басқа көміртекті шикізатты химиялық өңдеудің маңызы өте зор. Химия кешені салаларының негізгі міндеттерінің бірі - химиялық материалтануды дамыту. Жаңа химиялық материалдарды құру және өндіру, оларды қайта өңдеу технологиясының дамуы машиналар мен жабдықтардың сенімділігі мен беріктігінің жоғарылауына, олардың материалды тұтынуының, энергия шығыны мен өндірістің еңбек сыйымдылығының төмендеуіне, сондай-ақ қара, түсті және сирек металдар экономикасына түбегейлі әсер етеді. Барлық химиялық-технологиялық процестердің материалдық негізін химиялық өндіріс машиналары мен құрылғылары құрайды.
Калий бромидінің өндірісі
Химиялық тұрғыдан тұзды екі белсенді зат түзеді: сілтілік металл және күшті қышқыл. Бромды тұздан босату үшін неғұрлым белсенді (бромға қарағанда) галогендермен әрекеттеседі. Жаңа тұздар түзу үшін басқа тұздармен әрекеттеседі. калий перманганатымен) . Басқа бромидтермен күрделі тұздар түзе алады. Органикалық химияда бромдау реакциясы жиі қолданылады - органикалық қосылысқа бром атомын енгізу. Бромды калий алкандарды, алкендерді, анилинді қосылыстарды бромдау үшін қолданылады.
Реагенттің концентрацияланған ерітінділері ауыз қуысының шырышты қабығына және асқазан-ішек жолына қатты тітіркендіргіш әсер етіп, жүрек айну, құсу, диарея тудырады. Кейбір адамдар затқа аллергиясы бар.
КБр негізіндегі препараттардың дозалануы «бромизм» деп аталатын ауруға әкеледі (броммен созылмалы улану) . Оның белгілері: препаратты қабылдағаннан кейін бірден жөтел, мұрыннан су ағу және бөртпе пайда болуы. Қатты дозаланғанда летаргиялық жағдай, апатия, ұйқышылдық, сөйлеудің артта қалуы, есте сақтау қабілетінің нашарлауы, көру және есту қабілетінің нашарлауы байқалады.
Өнеркәсіпте калий бромидін кино және фотопленкалар, фотопластинкалар, фотоқағаздар шығаруға сұранысқа ие күміс бромидін өндіруге арналған шикізат болып табылады және ол органикалық синтезде, нейлон өндірісінде, бояғыштарда, мұнай өндірісінде бұрғылау сұйықтығын дайындауда қолданылады. Инфрақызыл спектроскопияда KBr плиталары қолданылады, өйткені олар өздері ИҚ сәулесін сіңірмейді және ИҚ спектроскоптарының дәлдігіне әсер етпейді. Калий бромидінің ерітінділері мен таблеткалары емдік мақсатта седативті, эпилепсияға қарсы және антиконвульсант ретінде қолданылады.
1-бөлім
Əдебиеттік шолу өндіріс бойынша, тарихы кезеңдері сипаттамасы.
Химиялық технологияның тарихы химия өнеркәсібінің даму тарихымен бөлінбейді. Бастапқыда алғашқы химия салаларының пайда болуымен пайда болған химиялық технология қолданбалы химияның таза сипаттама бөлімі болды. Еуропада негізгі химиялық өнімдерді шығаруға арналған мануфактуралар мен өндірістердің пайда болуын әр түрлі фармацевтикалық және кейбір органикалық заттардың қышқылдары, сілтілері мен тұздарының кішігірім мамандандырылған өндірісі пайда бола бастағанда, XV ғасырға жатқызу керек. Ресейде 16-шы ғасырдың аяғы - 17-ші ғасырдың басында дамыған химиялық өнеркәсіптер бояулар, селитралар, порох жасау, сонымен қатар сода мен күкірт қышқылын өндіру болды. 18 ғасырдың екінші жартысында технологияны білімнің ерекше саласына бөлу басталды, ғылыми технология және ғылыми пән ретінде химиялық технологияның негізі қаланды. Бұл ұғымда алғаш рет «технология» терминін 1772 жылы Геттинген университетінің профессоры И. Бекманн қолданды, ол көптеген химиялық өндірістердің техникасын қамтитын алғашқы күрделі еңбектерді шығарды және бір уақытта химиялық технология бойынша алғашқы оқулықтар болды. 1795 жылы екі томдық курс И. Ф. Гмелин «Техникалық химияға басшылық», 1803 жылы В. М. Севергиннің орысша аудармасында «Қолөнер мен фабрикалардың химиялық негіздері» деген атпен жарық көрді. 18 ғасырдың аяғындағы химиялық технология Еуропадағы жоғары техникалық оқу орындарындағы университеттердегі, Ресейдегі коммерциялық және техникалық мектептердегі міндетті оқу пәніне айналды.
1803 жылы Ресей Ғылым академиясында химиялық технологиялар бөлімі құрылды. 1804 жылдан бастап Санкт-Петербургте «Технологиялық журнал немесе технологиямен байланысты шығармалар жинағы» шыға бастады. Сол жылдары Ресейдің жоғары оқу орындарында химиялық технологияны оқыту басталды. 1807 - 08 жылдары шыққан Мәскеу университетінің профессоры И. А. Двигубский. алғашқы химиялық технология бойынша орыс оқулығы «Технологияның бастапқы негіздері немесе өндірілген фабрикалар мен фабрикалардағы жұмыстың қысқаша нұсқауы», осы кітаптың алғысөзінде былай деп жазады: «Қазіргі кезде барлық дерлік қалыптасқан мектептерде технология немесе қолөнер туралы ғылым оқытылады, фабрикалар және өздерін ғылымға арнаған адамдар барлық технологияларды қарастыра отырып, өздерінің теориялық білімдерімен, қолөнерді, фабрикалар мен фабрикаларды қоғамдық доменді көбейтуге қажетті тарату мен жетілдіруге үлес қоса алады ». 1828 жылы профессор Ф. А. Денисов «Жалпы технологияға немесе әртүрлі техникалық өнерде қолданылатын барлық жұмыстарды, құралдарды, құралдар мен машиналарды білуге арналған кең көлемді нұсқаулық» оқулығын шығарды. Бұл оқулық жалпы химиялық технологияның, сондай-ақ химиялық технология процестері мен аппараттарының заманауи курстарының прототипі болды. Онда қолданыстағы химиялық өндірісті сипаттап қана қоймай, сонымен қатар технологияның типтік процестерін бөліп алуға тырысады. Химиялық технологияны дербес ғылыми пән ретінде дамытуға үлкен үлес қосты профессор П. А. Ильенков, ол 1851 жылы «Химиялық технология курсын» шығарды - сол уақытқа дейін болған барлық ірі химия салаларының энциклопедиясының бір түрі. ХІХ ғасырда пайда болуы. Батыс Еуропа мен Ресей елдерінде химиялық технология бойынша көптеген оқулықтар, оқу құралдары мен ғылыми зерттеулер химиялық өндірістің қарқынды өсуіне және сонымен бірге химиялық технологияның ғылыми негіздерінің дамуына ықпал етті. Химия өнеркәсібінің даму тарихындағы бірнеше ірі оқиғаларды ғана атауға болады. 1748 жылы Англияның Бирмингем қаласында алғашқы шағын күкірт зауыты салынды.
қорғасын камераларындағы қышқылдар (камералық әдістің басталуы) . 1805 жылы - 10 жыл. күкірт қышқылының камералық өндірісі Англияда және Францияда кең дамыды. 1804 жылы алғашқы күкірт қышқылы зауыты Ресейде, ал 1820 жылы Германияда жұмыс істей бастады. 1787 жылы - 89. Н. Лебланк сода өндірісінің алғашқы индустриялық әдісін жасады. Шыны өндірісі, каустикалық сода өндірісі және басқа салалардағы содаға деген сұраныстың үлкен болуына байланысты Лебланк әдісі өте кең таралды (Лебланк әдісімен алғашқы ірі сода зауыты 1823 жылы Англияда салынды) . 1861 жылы сода өндірудің аммиак әдісі (Сольвай әдісі) жасалды. ХІХ ғасырдың екінші жартысында. Катализ саласындағы зерттеулер кеңінен дамуда, бұл көптеген химиялық процестерді өнеркәсіптік ауқымда жүргізуге мүмкіндік берді. Сонымен, 70-ші жылдары. XIX ғасыр. күкірт қышқылын алудың байланыс әдісі жасалып, 1886 жылы осы әдісті қолдана отырып оның өнеркәсіптік өндірісі ұйымдастырылды. Органикалық синтезге гетерогенді катализді енгізу органикалық химия тарихында жаңа кезеңнің басталуын белгіледі. ХХ ғасырдың алғашқы онжылдықтарында. көмірсутектер мен көміртегі оксиді негізіндегі синтездер кең дамыды. Гетерогенді катализ саласындағы жұмыс С. В. Лебедевтің резеңке өндірістік синтезі.
1-2-бөлім
Калий бромидінің тарихы, дәстүрлі алынуы
KBr алудың дәстүрлі тарихи алыну тәсілі әдісі-калий карбонатының бром темірімен реакциясы(III, II) Fe 3 Br 8 , артық бромның су астындағы темір сынықтарын өңдеу арқылы алынады:
4K 2 CO 3 + Fe 3 Br 8 → 8KBr + Fe 3 O 4 + 4CO 2
Калий бромиді (KBr) -бұл 19-шы ғасырдың аяғы мен 20-шы ғасырдың басында антиконвульсант және седатив ретінде кеңінен қолданылатын тұз, 1975 жылға дейін АҚШ-қа қарсы қолдануға пайдаланды. Калий бромиді (KBr) кең мөлдірлігі арқасында спектроскопияда қолданылатын ең танымал материалдардың бірі. Бұл KCl және NaCl-мен бірге суда еритін тұздарға жатады, ал жылтыратылған бөлшектер эксикаторда немесе жылы бөлмеде кремнеземді гельмен дәнекерленген қаптамада сақтауды қажет етеді. Калий бромидінің антиконвульсант қасиеттерін алғаш рет Сэр Чарльз Локк 1857 жылы Корольдік Медициналық және хирургиялық қоғамның отырысында атап өтті. . 19 ғасырдың екінші жартысында калий бромиясы ұстамалар мен жүйке бұзылыстарын тыныштандыру үшін үлкен көлемде қолданылды, ал жеке ауруханаларды қолдану жылына бірнеше тоннаға жетті (белгілі бір адамға күніне бірнеше грамм болатын) . 20 ғасырдың басында жалпы сөз күш-қуатқа байланысты бола бастады. Осы уақытта АҚШ-та бромидтерді медициналық қолдану тоқтатылды, өйткені сол кезде көптеген жақсы және қысқа седативтер белгілі болды.
KBr-монокристалды материал, жұмсақ, жылу әсеріне төзімді, бірақ су және алкоголь ерітінділерімен, глицеринмен және қышқылдармен байланыста болмауы керек. Оның әсері бромид ионына байланысты (натрий бромиді де тиімді) . Калий бромиді иттерге арналған эпилепсияға қарсы дәрі ретінде ветеринарлық препарат ретінде қолданылады.
1-3 бөлім
КАЛИЙ БРОМИДНІҢ БАСТАПЫҚЫ СИПАТТАМАСЫ.
Бромды калий - бұл бейорганикалық қосылыс, калий тұзы КBr формуласы бар бромид калийі. Калидың бромиды типтi иондық болып табылады. Молярлық массасы: 119. 002 г / моль. Ол табиғатта кездеспейді, зертханалық қажеттіліктер үшін және өнеркәсіп үшін химиялық синтез арқылы алынады.
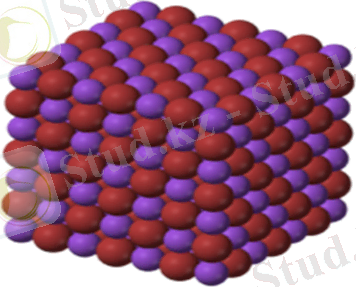
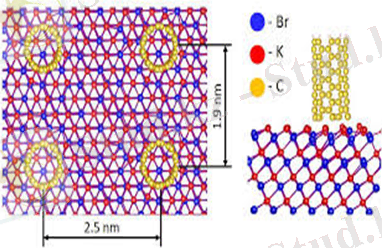
1-4 бөлім
КАЛИЙ БРОМИДІ НІҢ ФИЗИКАЛЫҚ ХИМИЯЛЫҚ ҚАСИЕТТЕРІ.
Физикалық қасиеттері
Жылтыр кристалдары бар, иісі жоқ, тұзды ақ түсті кристалды ұнтақ. Суда ериді, температура жоғарылаған сайын ерігіштік жоғарылайды. Глицерин, гидразин, этиленгликоль, сулы аммиакта ериді. Ол органикалық еріткіштерде өте аз ериді. Концентрацияланған гидробром қышқылында ерімейді. Кристалды гидрат түзбейді. Жанбайды, улы емес.
Химиялық тұрғыдан тұзды екі белсенді зат түзеді: сілтілік металл және күшті қышқыл. Бромды тұздан босату үшін неғұрлым белсенді (бромға қарағанда) галогендермен әрекеттеседі. Жаңа тұздар түзу үшін басқа тұздармен әрекеттеседі. Күшті тотықтырғыштармен жүретін химиялық реакцияларда ол қалпына келтіру қасиеттерін көрсетеді (мысалы, күкірт және басқа қышқылдармен, калий перманганатымен) . Басқа бромидтермен күрделі тұздар түзе алады. Органикалық химияда бромдау реакциясы жиі қолданылады - органикалық қосылысқа бром атомын енгізу. Бромды калий алкандарды, алкендерді, анилинді қосылыстарды бромдау үшін қолданылады.
Реагенттің концентрацияланған ерітінділері ауыз қуысының шырышты қабығына және асқазан-ішек жолына қатты тітіркендіргіш әсер етіп, жүрек айну, құсу, диарея тудырады. Кейбір адамдар затқа аллергиясы бар.
КBr негізіндегі препараттардың дозалануы «бромизм» деп аталатын ауруға әкеледі (броммен созылмалы улану) .
Оның белгілері: препаратты қабылдағаннан кейін бірден жөтел, мұрыннан су ағу және бөртпе пайда болуы. Қатты дозаланғанда летаргиялық жағдай, апатия, ұйқышылдық, сөйлеудің артта қалуы, есте сақтау қабілетінің нашарлауы, көру және есту қабілетінің нашарлауы байқалады.
Реагентті мөлдір емес ыдыста сақтаңыз және тасымалдаңыз. Жабық қоймаларда сақталады.
Бұл натрий хлоридіне ұқсас куб типті кристалды торы бар түссіз кристалдарға ұқсайды (a = 0, 6596 нм, z = 4, Fm3m кеңістік тобы) . 298 ° С-қа дейін қыздырғанда және 1, 7 ГПа қысыммен кристалдық тор хлорлы цезий сияқты басқа кубтық модификацияға айналады. Оның балқу температурасы 734 ° С және 1435 ° С-та қайнайды. Тығыздығы 2, 75 г / см3 . Молекуланың диполь моменті 9, 1 Дебай.
Термодинамикалық шамалар
Химиялық қасиеттері
Бромды калий - әдеттегі ионды тұз. Суда еріген кезде ол толық диссоциацияға ұшырайды, ал ол гидролизденбейді, өйткені ол күшті негізден (калий гидроксиді) және күшті қышқылдан (гидробром қышқылы) пайда болады. Кристалды гидрат түзбейді. Концентрлі гидробром қышқылында ерімейді.
Бромды неғұрлым белсенді галогендер ығыстырады:
2KBr + Cl 2 →2KCl + Br 2 ↑
Шешімдерде әдеттегі алмасу реакциялары пайда болуы мүмкін:
KBr + AgNO 3 →AgBr ↓ + KNO 3
Қалпына келтіру қасиеттерін көрсетеді:
2KBr + 3H 2 SO 4 →2KHSO 4 + Br 2 +SO 2 + Н 2 О
(конц. H 2 SO 4 , қай. )
5KBr + 3H 2 SO 4 + KbrO 3 →3Br 2 + 3Н 2 О + 3H 2 SO 4
(сұй. H2SO4)
2KBr + 2H 2 SO 4 + MnO 2 → Br 2 + K 2 SO 4 + 2Н 2 О
(конц. H 2 SO 4 , қай. )
10KBr + 2KMnO 4 + 8H 2 SO 4 →6K 2 SO 4 + 5Br 2 + 2MnSO 4 + 8Н 2 О
Концентрацияланған ерітінділерде кейбір бромидтермен күрделі қосылыстар түзілуі мүмкін:
2 KBr + CuBr 2 → K 2 [CuBr 4 ]
Ыстық ерітіндінің электролизі:
KBr+ Н 2 О→3Н 2 ↑+ KBrO 3
Калий бромиді бромид иондарының көзі ретінде қызмет етеді. Бұл реакция фотопленка үшін бромды күміс алу үшін маңызды:
KBr (водн. ) + AgNO 3 (водн. ) → AgBr (s) + KNO 3 (водн. )
Су бромиді Br-сонымен қатар мыс(II) бромиді сияқты кейбір металл галогенидтерімен әрекеттескенде кешендер түзеді:
2 KBr (водн. ) + CuBr 2 (водн. ) → K 2 [CuBr 4 ] (водн. )
Броматорлық агент
Ол дихенометан-су жүйесінде диацетокси йодобензол болған кезде алкендер мен алкиндердің көптеген байланыстарын селективті транс-бромдау үшін қолданылады. Цис-бромдау үшін церий-аммоний нитраты-калий бромиді жүйесі қолданылады. Деактивтелген анилин туындыларын моноброминациялау үшін бромды калиймен және натрий перборатымен тотықтырғыш бромдау қолданылады.
Қолдану
Олар бромды иондарының көзі ретінде күміс бромидін алу үшін қолданылады, ол фотографиялық және кинопленкалар жасау үшін қолданылады.
Бромид калийінің таблеткаларындағы сұйық заттардың спектрлерін зерттеуге арналған ИК-спектрофотометрге арналған қондырма. Фотографиялық өңдеушілерде тұманға қарсы зат ретінде қолданылады. Басқа антивалентті агенттермен салыстырғанда, ол іс жүзінде кескіннің контрастын көтермейді. Сұйық заттардың ИҚ спектрлерін зерттеу үшін калий бромидінің («таблетка» деп аталатын) тақталарының арасына затты орналастыру технологиясы қолданылады. Бромді калий толқын ұзындығының жеткілікті кең диапазонында (0, 25 мкм-ден 25 мкм-ге дейін) ИҚ сәулесін сіңірмейді, бұл оны осы мақсаттарда пайдалануға мүмкіндік береді.
Кино және фотопленкалар, фотопластинкалар, фотоқағаздар шығаруға сұранысқа ие күміс бромидін өндіруге арналған шикізат.
Фото әзірлеушілердің бөлігі. Бромды калий ол органикалық синтезде, нейлон өндірісінде, бояғыштарда, мұнай өндірісінде бұрғылау сұйықтығын дайындауда қолданылады. Инфрақызыл спектроскопияда KBr плиталары қолданылады, өйткені олар өздері ИҚ сәулесін сіңірмейді және ИҚ спектроскоптарының дәлдігіне әсер етпейді. Калий бромидінің ерітінділері мен таблеткалары емдік мақсатта седативті, эпилепсияға қарсы және антиконвульсант ретінде қолданылады. Олар ұйқысыздыққа, гипертонияға, вегетативті дистонияға, неврастенияға, эпилепсияға, мазасыздыққа, ашуланшақтыққа, хореяға және истерияға бейімділікке тағайындалады.
Ветеринарияда иттер мен мысықтардың ұстамаларын емдеу үшін қолданылады. Аналитикалық химияда, ядролық зерттеулерде қолданылады.
Бромид калийі әр түрлі жүйке жүйесі бар адамдарға әр түрлі әсер етуі мүмкін. Сондықтан өзін-өзі емдеуге жол берілмейді. Бұл дәрі-дәрмекті, оны қалай қабылдау керектігін және мөлшерін тек дәрігер тағайындай алады. Сонымен қатар, дәрі-дәрмектердің қарсы көрсетілімдері бар. Калий бромидін инъекция арқылы беруге болмайды, себебі жүрекке жағымсыз әсер ету қаупі бар.
Физиологиялық әрекеті
19 ғасырдың аяғы мен 20 ғасырдың басында антиконвульсант және седативті ретінде кеңінен қолданылады. Оның әрекеті бромид ионының физиологиялық әсеріне негізделген (бромды натрий аз тиімді) . KBr қазіргі кезде ветеринарлық препарат ретінде, ит пен мысыққа қарсы құрысуға қарсы препарат ретінде қолданылады
Сұйылтылған сулы ерітінділерде калий бромиді ерітіндіге тәтті дәм береді, жоғары концентрацияда ерітінді ащы дәмге ие (бұл әсерлер негізінен калий ионының әсерінен болады) . Бромды калий асқазанның ішкі қабатын қатты тітіркендіреді, нәтижесінде жүрек айну мен құсу пайда болады.
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz