Химиялық байланыстың ілімі: тарихи даму, теориялар мен құрылымдық-энергетикалық сипаттамалары


Химиялық байланыс туралы ілімнің дамуы
Химиялық байланыс туралы ілім − қазіргі химияның негізгі проблемаларының бірі. Өйткені не себепті атомдардың бір-бірімен әрекеттесіп заттар түзетінін және олардың түзілу механизмдерін білмей тұрып, заттардың құрамын, құрылысын, реакцияласқыштық қабілетін білуге болмайды.
Химиялық байланыстардың түзілу механизмін түсіндіру электрон ашылғаннан кейін ғана мүмкін болды.
1916 жылы неміс ғалымы В. Коссель бір элементтің электрон беруі, екінші элементтің осы электронды қосып алуынан түзілген иондардың арасындағы тартылыстың нәтижесінде химиялық байланыс түзіледі деген теориясын ұсынды.
В. Коссель идеясы байланыстың иондық теориясын жасауға негізгі тірек болды. Бірақ бұл теория да бірдей атомдардың арасындағы байланыстың табиғатын түсіндіре алмады.
Сол жылы американдық ғалым Г. Льюис әрекеттесетін атомдардың дара электрондарын ортақтастырудың нәтижесінде түзілген екі атомға да бірдей ортақ қос электрондар арқылы химиялық байланыс түзіледі деген теориясын ұсынды. Коссель мен Льюис теорияларын химиялық байланыс теориясының екі жағы деп қарастыруға болады. Өйткені Коссель теориясы бойынша химиялық байланыс (иондық) электрон беру, қосып алу нәтижесінде болған иондар арасында түзіледі, ал Льюис теориясы бойынша химиялық байланыс екі элементтің ортақтастырылған қос электрондары арқылы түзіледі. Қазіргі кезде қолданылатын химиялық байланыс туралы ілім Коссель мен Льюис теориялары негізінде дамыды.
Химиялық байланыстардың түзілуі
Химиялық байланыстар атомдардың әрекеттесуі нәтижесінде пайда болған екі атомдық немесе көп атомдық тұрақты жүйелерде (молекулаларда, кристалдарда) түзіледі. Ковалентті химиялық байланыс түзілу механизмін сутегі молекуласының пайда болу мысалы арқылы қарастырайық. Сутегі атомы бір протоннан, бір электроннан тұрады. Осындай екі атом жеткілікті мөлшерде бір-біріне жақындасқанда бір атомның ядросы мен екінші атомның электронының арасында тартылыс күші, ал екі атомның ядролары мен электрондарының арасында тебу күші пайда болады. Атомдардан молекула түзілуінің ең басты шарты − молекула түзілгенде энергияның бөлінуі, яғни атомдардың энергия қорынан молекуланың энергия қоры аз болуы керек. Молекулалардың, иондардың, радикалдардың, сондай-ақ кристалдардың түзілуіне әкелетін атомдардың әрекеттесу құбылысын химиялық байланыс деп атайды. Химиялық байланыстар түзілуі нәтижесінде атомдар инертті газдардағыдай электрондық конфигурацияны қабылдай алады, онда (гелийден басқасында) сыртқы қабатта сегіз (октет) электроннан бар. Мұндай тұрақты электрондық қабат жасауға ұмтылысты октет ережесі дейді. Бұл иондық байланыс үшін де, коваленттік байланыс үшін де әділ болып қалады.
Химиялық байланыстың сандық сипаттамалары . Химиялық байланыстар энергетикалық және геометриялық параметрлерімен (өлшемдерімен) сипатталады.
Байланыс энергиясы химиялық байланыс беріктігінің өлшемі. Бұл энергия байланысты бұзу (үзу) үшін қажет. Мұндай тұста молекула негізгі күйде және Т=0 Кельвин байланыс энергиясының шамасы 100-1000 кДж/моль аралығында болады.
Геометриялық параметрлерге химиялық байланыстың ұзындығы (молекуладағы, коплекстегі, кристалдағы және т. б. ) ; байланыстардың арасындағы бұрыштар жатады.
Байланыс ұзындығы - ол молекуладағы немесе кристалдағы атомдар ядросы ортасының (центрлерінің) арақашықтығы. Әдетте, байланыс ұзындығы азайған сайын байланыс энергиясы өседі және оған сәйкес молекуланың тұрақтылығы да арта түседі.
Коваленттік байланыс
Коваленттік байланыс теориясын түсіндіру үшін американдық ғалым Дж. Льюистің жұмыстары негізгі тірек болды. Атомдардан молекула түзілуінің ең басты шарты - молекула түзілгенде энергияның бөлінуі қажет, яғни атомдардың энергия қорынан молекуланың энергия қоры аз болуы керек.
Әрекеттесуші атомдардың жұптаспаған электрондарының қатысуымен жалпы электрон жұбы түзілуі үшін олардың антипараллельді спині болуы керек. Мұндайда электрондық бұлттардың қайта жабылуы жүреді.
Жалпы (екеуіне ортақ) электрондық жұптар арқылы іске асатын химиялық байланысты коваленттік деп атайды.
Осындағы “ковалентті” сөзі “біріккен” деген мағынаны дәл білдіреді. Ковалентті байланыстың екі түрі бар: полюсті (полярлы) және полюссіз (полярсыз) .
Ковалентті полюссіз байланысты симметриялы электрондық бұлт түзетін жалпы электрондық жұп іске асырады. Байланыстың бұл түрі электртерістілігі бірдей атомдардың арасында туындайды: H 2 , О 2 , N 2 , F 2 , Cl 2 , Br 2 , J 2 , C, P, As, PH 3 , CS 2 . Мысалы; хлор молекуласы түзілген кездегі электрондық жұп хлор атомдарының екеуіне бірдей қатысты.
Ковалентті полюсті байланыс - әртүрлі екі атом арасында түзіледі, осындағы электрондық бұлт электртерістілеу атомға қарай ығысқан: HCl, H 2 О, H 2 S, CО 2 және т. б. Мысалы; хлор мен сутек молекулаларының арасындағы реакция сатыларының біреуінде олардың атомдары әрекеттесіп, ковалентті байланыс түзеді:
Мұндай жағдайдағы түзілген электрондық жұп электртерістілеу хлордың ядросы жағынан күштілеу тартылыс күшіне кезігеді. Электрондық жұптың ығысуы салдарынан хлор атомындағы теріс зарядтың тығыздылығы жоғарылайды δ-; ал сутек атомында оң зарядтың тығыздылығы артады δ+. Атом алатын зарядты (δ+ немесе δ-) пәрменді (эффективті) заряд дейді.
Коваленттік байланыстың донорлық-акцепторлық механизмі деп бір атомның байланыс түзбеген жұп электроны мен екінші атомның бос орбиталі қосылуы нәтижесінде түзілген байланысты айтады. Жұп электронын беретін атом донор , ал оны қабылдаған атом акцептор деп аталады.
Молекуланың кеңістіктегі құрылысы
Молекулалардың кеңістіктегі құрылысын түсіндіру үшін химияға Л. Полинг енгізген атомдық орбитальдардың будандасуы туралы түсінікті пайдаланады. Будандасу (гибридтену) теориясы бойынша химиялық байланыс түзердің алдында атомның әр түрлі орбитальдарының формалары мен энергиялары өзгеріп, саны бастапқы орбитальдардың санына тең формалары және энергиялары бірдей, кеңістікте симметриялы түрде орналасқан жаңа гибридті орбитальдар пайда болады. Әрекеттесуші орбитальдардың сипатына тәуелді болатын будандасудың түрлі типтері бар (1- кесте) .
- кесте
Геометриялық түрпішіні
(формасы)
Айталық, қоздырылған күйдегі бериллий атомының 1s 2 2s 1 2р 1 конфигурациясы болады. Хлор атомдарымен бериллий атомы әрекеттескенде бір 2s- және бір 2р- орбитальдар бірдей екі будандық орбитальға айналады (sр - будандасу) , олар біріне бірі 180º бұрышта бағытталады. Сондықтан BeCl 2 молекуласы сызықты формада болады.
Химиялық байланыс түзілгенде BCl 3 молекуласындағы бор атомында (қоздырылған күйдегі электрондық құрылым 1s 2 2s 1 2р 2 ) будандасуға бір s-электронды және екі р-электронды орбитальдар қатысады (sр 2 - будандасу жүреді) . Бұл үш будандық орбитальдың түзілуіне әкеледі, олар бір жазықта 120º бұрышпен орналасады; молекула жазықтық құрылымда болады .
Метанның СН 4 молекуласындағы байланыс түзілгенде қозған күйдегі көміртек атомы (1s 2 2s 1 2р 3 ) сутектің төрт атомын қосып ала алады. Мұндайда көміртек атомында бір s- және үш р-орбитальдар будандасуға ( sр 3 - будандасу ) душар болады, бұл төрт будандық орбитальдың түзілуіне әкеледі. Олар кеңістікте симметриялы орналасады және тетраэдр төбесіне 109 0 28′ бұрышпен бағытталған.
Электрондық бұлттардың қайта жабылу сипаты бойынша мына байланыстарды ажыратады:
- σ (сигма) - байланыс , ол әрекеттесуші атомдардың центрін қосатын, ось бойымен электрондық бұлттардың қайта жабылуы кезінде түзіледі. Сигма - байланысы келесі орбитальдардың қайта жабылуы кезінде пайда болады: s-s; s-р; р-р; d-d; d-s; d-р; ƒ-ƒ және т. б. Бұл байланыс, әдетте, екі атомды қамтиды да олардың шегінен шықпайды, сондықтан екі центрлік локализденген байланыс болады. Сигма - байланыс жалқы және ол бір сызықшамен белгіленеді;
- π (пи) - байланыс , ол атомдардың перпендикулярлық центрін қосатын осьтің бойымен электрондық бұлттардың бүйірден қайта жабылуы тұсында түзіледі. Пи- байланыс келесі орбитальдық қайта жабылу кезінде түзіле алады: р-р; р-d; d-d; ƒ-р; ƒ-d; ƒ-ƒ;
- δ (дельта) - байланыс төрт жапырақшаның бәрімен де қайта жабылғанда түзіледі.
π - байланыстар σ - байланыспен түйіскенде қос байланыс түзіледі, мысалы: оттектің, этиленнің, көміртек диоксиді молекулаларында. Қанықпаған қос байланыс екі сызықшамен өрнектелінеді: О=О, О=С=О.
Екі π - байланыс бір σ - байланыспен түйіскенде үш байланыс түзіледі, мысалы: азоттың, ацетиленнің және көміртек (IV) оксидінің молекуласында. Үштік байланыстар үш сызықшамен өрнектелінеді: N≡N, -С≡С-, -С≡О. Жай және қос байланыстың ұзындығымен және энергиясымен салыстырғанда, үш байланыстың энергиясы жоғары, ал байланыстың ұзындығы қысқа. Қос және үш байланысты еселі байланыстар деп атайды.
Электрондардың таралуын көрсету молекуланың тек аз сандары үшін мүмкін. Әдетте, ковалентті байланысы бар екі атомдық және көп атомдық жүйелер үшін жуықтаған есептеу әдістерін: валенттік байланыстар әдісін (ВБӘ) және молекулалық орбитальдар әдісін (МОӘ) пайдаланады.
Валенттік байланыстар әдісі
1928 жылы неміс ғалымдары В. Гейтлер және Ф. Лондон валенттік байланыстар (ВБ) әдісін ұсынып, онымен сутек молекуласына кванттық - механикалық есептеулерін жүргізді. Кейінірек бұл әдіс Слейтер, Ван Флек, Л. Полинг еңбектерінде жетіле түсті.
ВБ әдісі келесі ережелерге негізделген:
1. Байланыстарды түзуге тек сыртқы электрон қабатындағы электрондар (валенттік электрондар) қатысады;
2. Химиялық байланыстарға түсуші атомдар өзара электрондарымен алмасады да, бұл электрондар байланыстырушы жұптарды түзеді;
3. Химиялық байланыс Паули қағидасына сәйкес, тек антипараллельді спиндегі электрондар арасында ғана түзіледі; мұндайда атом ядроларының арасында электрондық тығыздық жоғарылаған аймақ пайда болады ;
4. Химиялық байланыстың сипаттамалары (энергиясы, ұзындығы, үйектігі және т. б. ) атомдық орбитальдардың қайта жабылу типімен анықталады;
5. Молекулалар түзілген кезде электрондық құрылым (сыртқы қабаттан басқасы) және әрбір атомның химиялық өзінділігі сақталынады.
Валенттік байланыс теориясына сәйкес, коваленттік байланыстар әрекеттесуші атомдардың АО максималды қайта жабу жағына бағытталған.
Химиялық байланыстарды түзумен қатар атомның қосып алу және басқа атомдардың белгілі санының орнын басу қабілеттілігін валенттілік деп атайды. ВБ әдісінің алмасымдық механизміне орай ортақ электрондық жұп (коваленттік байланыс) түзуге әрбір атом жұптаспаған бір электроннан береді. ВБ әдісінде алмасымдық механизміндегі валенттіліктің сандық өлшемі ретінде атомның негізгі немесе қоздырылған күйде болатын жұптаспаған электрондар санын есептейді. Бұл сыртқы электрондық қабаттың жұптаспаған электрондары s- және р-элементте, d-элементтердің сыртқы және оның ішкері жағындағы қабатта, сол сияқты ƒ-элементтердің сыртқы үш қабаттарында болады (орналасады) .
Атомның қоздырылған күйге ауысуы элемент валенттілігінің артуына және ауыспалы валенттіліктің бар болуына мүмкіндік жасайды . Мысалы оттек пен фтор атомдарындағы электрондық жұптар бөліне (ажыраса) алмайды, өйткені екінші қабатта бос орбитальдар жоқ. Олардан өзгешілікте, күкірт пен хлор 3d-қабатшаның бос орбиталіне ажыраса алады, тиісінше күкірт 1 және 2 валенттіліктен (негізгі күйінде) басқа тағы да 4 және 6 валенттілікте (қоздырылған күйінде) болады, ал хлор 1 валенттіліктен (негізгі күйінде) басқа 3, 5 және 7 валенттілікте (қоздырылған күйінде) болады.
Молекулалық орбитальдар әдісі
Қарастырылған ВБ әдісі көрнекті және әртүрлі молекулалармен иондардың құрылымын, қасиетін (кеңістіктегі конфигурациясын, үйектілігін, байланыстың энергиясы мен ұзындығын және т. б. ) болжамдауға мүмкіндік береді. Бұған қарамастан бұл әдіс заттың магниттік қасиетін, жұптаспаған электрондары бар молекулалардың санын және де бірқатар басқа құбылыстарды түсіндіре алмайды.
Бұл деректер ғалымдарды ізденіске жетеледі. 1928 - 1930 жылдары ғалымдар Роберт Малликен және Фридрих Гунд молекулалық орбитальдар (МО) әдісін ойлап тапты. МО әдісінің негізгі ережелері:
1. Молекула өзінің дербестілігін (индивидуальділігін) сақтайтын атомдардың жиынтығы ретінде емес, ол ядро мен электрондардың біріккен жүйесі ретінде қарастырылады;
2. Молекулалардағы электрондар молекулалық орбитальдар бойынша таралады, олар атомдық орбитальдар (АО) сияқты белгілі энергиямен және түрпішінімен сипатталады;
3. Молекулалық орбитальдар екі - немесе көпцентрлік болады.
МО әдісінде атомдық орбитальдардың сызықты қиыстыруы (АОСҚ) барынша кеңінен пайдаланылады. Мұндайда бірнеше ереже сақталады:
- МО саны АО санына тең, АО жалпы санынан МО қиыстырылады;
- Берілген АО энергиясынан бір МО энергия жоғары болып келсе, басқасынікі (МО) - төмен. Түзілген МО энергиясы шамамен АО орташа энергиясымен бірдей, ал одан өздері (АО) түзіледі;
- Электрондар энергияның өсу ретімен АО толтырған сияқты, МО толтырады, мұндайда Паули тиым қағидасы және Гунд ережесі сақталады;
- МО түзілуіне тек энергия шамасы бойынша жақын болатын және байланыс осімен салыстырғанда шамамен бірдей симметриясы бар АО қатысады;
- Байланыстың беріктілігі атомдық орбитальдардың қайта жабылу дәрежесіне пропорционалды.
Байланыстырушы және қопсытушы орбитальдар . Егер А және В атомдарының АО ψА және ψВ арқылы, ал МО ψАВ арқылы белгіленсе, онда АОСҚ (ЛКАО) сәйкес
ψАВ = аψА ± bψВ
мұндағы ψАВ - молекуладағы (МО) электронның толқындық функциясы;
а және b - коэффициенттер, ол МО түзілуіндегі әрбір АО үлесін ескереді;
ψА және ψВ - А және В атомдарындағы электрондардың толқындық функциясы.
Таңба “плюс” кезінде байланыстырушы МО алынады.
Таңба “минус” болған кезде қопсытушы МО алынады. Қопсытушы МО жұлдызшамен (*) таңбалайды.
Байланыстырушы МО қалыптастырғанда электрондық тығыздық ядролар арасында жинақталады , сондықтан байланыстырушы МО түзілуі молекула энергиясын төмендетеді де оны орнықтыра түседі.
Ядролар арасындағы электрондық тығыздық қопсытушы МО-да төмендеу болады , сондықтан олар атомдарды молекулаға байланыстырмайды.
Атомдық орбитальдардан молекулалық орбитальдардың түзілуін энергетикалық диаграммалар түрінде өрнектейді, онда тік (вертикаль) сызық бойынша энергияның мәнін орналастырады. Диаграмманың оң және сол жағына атомдық орбитальдардың энергетикалық деңгейлерін, ал ортасында молекулалық орбитальдардың деңгейлерін келтіреді.
Байланыстардың реті мен энергиясы : МО әдісінде байланыс еселігінің орнына байланыстың реттілігі n түсінігін енгізеді, ол байланыстырушы N б және қопсытушы N к молекулалық орбитальдардағы электрондар айырымының жартысына тең:

Егер N б = N к болса, онда n = 0 және молекула түзілмейді.
МО әдісінің ВБ әдісінен айырмашылығы сол, онда химиялық байланыс бір электронмен де түзіле беріледі; тиісінше байланыс реті бүтін сан болуымен қатар бөлшекті сан да бола береді: n = ½, 1, 3/2, 2, 5/2, 3 . . .
Бірінші период элементтерінің екі атомды молекулалары мен молекулярлық иондары . Сутек молекуласындағы химиялық байланыстың түзілуін электрондық конфигурациямен беруге болады:
2Н [1s 1 ] → Н 2 [ (σ1s) 2 ] .
Байланыстың түзілуі кезінде энергетикалық диаграммамен сәйкестікте 1s - электрон σ1s-молекулярлық орбитальда табылады, ал σ ּ 1s-орбиталі толтырылмай қалады.
Байланыстың реті
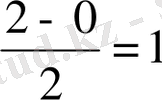 тең.
тең.
Сутек молекуласындағы электрондардың спиндері жұптасқан, және ол диамагнитті.
Сутектің атомы мен оң зарядталған сутек ионы әрекеттескенде молекулярлық Н 2 + түзіледі:
Н [1s 1 ] + Н + [1s 0 ] → Н 2 + [ (σ1s) 1 ] .
МО байланысының реті
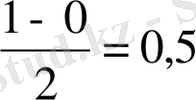 молекулярлық Н
2
+
ионына қарағанда Н
2
молекуласының байланыс ұзындығы аз, ал байланыс энергиясы үлкен. МО әдісі теріс зарядталған Н
2
-
ионының түзілу мүмкіндігін нұсқайды:
молекулярлық Н
2
+
ионына қарағанда Н
2
молекуласының байланыс ұзындығы аз, ал байланыс энергиясы үлкен. МО әдісі теріс зарядталған Н
2
-
ионының түзілу мүмкіндігін нұсқайды:
Н [1s 1 ] + Н - [1s 2 ] → Н 2 - [ (σ1s) 2 (σ ּ 1s) 1 ]
Байланысының реті
 тең. Оның байланыс энергиясы мен ұзындығы Н
2
+
ионының байланыс энергиясына және ұзындығына жақын болуы керек. Н
2
+
және Н
2
-
иондарында жұптаспаған электрондар бар және олар
парамагнитті.
тең. Оның байланыс энергиясы мен ұзындығы Н
2
+
ионының байланыс энергиясына және ұзындығына жақын болуы керек. Н
2
+
және Н
2
-
иондарында жұптаспаған электрондар бар және олар
парамагнитті.
Оттек молекуласының МО электрондармен толуын қарастырайық:
2О [K2s 2 2p 4 ] →
→ О 2 [ KK (σ2s) 2 (σ ּ 2s) 2 (π2p y ) 2 (π2p z ) 2 (σ2p х ) 2 (π ּ 2p y ) 1 (π ּ 2p z ) 1 ]
Қопсытушы π ּ 2p y және π ּ 2p z -орбитальдарында спиндері бірдей екі жұптаспаған электрон болады. Байланыс реті екіге тең. Сондықтан оттек парамагнитті. Оттектің парамагниттік қасиетін алдын ала болжамдау МО теориясында маңызды жетістік болып табылады.
МО әдісі әмбебаптау және көптеген қосылыстардағы байланыстардың пайда болуы мен сипатын түсіндіре алады. Бірақ та бұл әдіс молекуладағы жекеленген атомдардың және молекула бөліктерінің сипаттамасын ашпайды. ВБ әдісі көрнекілеу және химиялық байланыстар мен көптеген қосылыстардың қасиеттерін түсіндіреді. Сондықтан ВБ және МО әдістері бірін бірі толықтырады.
Иондық байланыс
1916 жылы В. Коссель енгізген иондық байланыс жайлы түсінік бойынша элементтердің реакцияласу қабілеттілігі, олардың атомдарының асыл газдардың электрондық конфигурациясын алуға ұмтылуына әкеледі. Мұндай конфигурацияның түзілуі электрондардың бір атомдардан басқа атомдарға толық ауысу салдарынан болады. Мұндайда түзілген әртүрлі таңбамен зарядталған иондар электростатикалық тартылу күштерімен ұсталады.
Иондардың электростатикалық тартылу күштері арқылы жүзеге асатын химиялық байланыс иондық байланыс деп аталады.
Na 0 - e → Na +
Cl 0 + e → Cl -
Na + + Cl - → NaCl
Осындай жолмен түзілетін қосылыстарды иондық деп атайды. Иондық байланыс тек өзінің электртерістілігі бойынша едәуір өзгеше болатын атомдардың арасында ғана түзіледі. Бұл қосылыстардың балқу және қайнау температуралары жоғары, суда ерігенде немесе балқығанда күшті электролиттің қасиеттерін көрсетеді.
Металдық байланыс
Атомдардың электрондық қауыздарының құрылысы бойынша металдарға барлық s-элементтер (сутек және гелийден басқасы), барлық d- және ƒ-элементтер және бірқатар р-элементтер (алюминий, қалайы және т. б. ) жатады. Қатты немесе сұйық күйдегі металдар жылу және электр өткізгіш, иілгіш және соғылғыш, балқу және қайнау температуралары жоғары болады. . Металдардың бұл қасиеттерін олардағы ерекше химиялық байланыстың болуымен түсіндіруге болады және ол байланысты металдық байланыс деп атайды. Оның түзілуіне, өзінің ядросымен едәуір әлсіз байланысқан, валенттік электрондар қатысады. Металдағы атомнан электрондар тұрақты түрде бөлінеді де металдың күллі массасы бойынша қозғалады. Электрондарын берген металл атомдары оң зарядталған иондарға түрленеді, ал олар өз кезегінде тұрақты қозғалыстағы электрондарды өзіне тартуға ұмтылады.
Мұнымен қатар, бір мезетте басқа металл атомы өзінің электрондарын береді, яғни металдың ішінде “электрондық газ” (бос электрондар) тұрақты айналып жүреді, олар металдың барлық атомдарын өзара берік байланыстырады да металл торының беріктігін қамтамасыз етеді.
Электростатикалық тартылу нәтижесінде металл иондары мен жалпыланған электрондар арасында түзілетін химиялық байланысты металдық байланыс деп атайды.
Металдық байланыстың энергиясы коваленттік байланыс энергиясының мәнінен 3-4 есе кіші.
Сутектік байланыс
Сутектік байланыс табиғатта кең таралған және оның көптеген химиялық және биологиялық процестер үшін маңызы зор. Сутектік байланысты тек молекуласындағы сутек атомы күшті электртерістілікті атомдармен (F, О, Cl, N, S, және т. б. ) байланысқан зат қана түзе алады.
Сутектік байланыс тек молекулааралық қана (әртүрлі молекулалар арасында) болмай, ол бір молекуланың ішінде де (бір молекула ішіндегі әртүрлі топтар арасында) бола алады. Сутек атомы - ішкі электрондық қауызы жоқ және өте кіші өлшемде болғандықтан, көрші теріс полюстенген атомның электрондық қауызы ішіне еніп кетуге қабілетті. Мысалы, құмырсқа қышқылындағы Н-О байланысты түзуші электрондар, электртерістілеу оттек атомына ығысқан. Сутек атомының ядросында (протонда) электрондық бұлт мүлдем қалмайды, мұндайда осы сутек атомы ядросы мен теріс зарядталған қышқылдың көрші молекуласындағы оттек атомының арасында электростатикалық тартылу туындайды. Бұл сутектік байланыстың пайда болуына әкеледі. Бұл байланыстың түзілуіне сутек атомындағы “жартылай бос” 1s-орбиталімен және электртерістілікті атомның бөлінбеген электрон жұбы орбиталінің донорлы - акцепторлық әрекеттесуі белгілі бір дәрежеде үлес қосады. Сутектік байланыстың түзілуін көрнекілеп, оны үш нүкте арқылы белгілей отырып көрсетуге болады.
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz