SCS және сіңдіру әдістерімен дайындалған Co-Al катализаторларының құрылымы және метанның CO2-пен риформингіндегі катализдік тиімділігі


3. 2 Co-Al катализаторларындағы метанның синтез-газға көмірқышқылды конверсиялануы
Метанның көміртегі диоксидімен CH 4 + CO 2 → 2CO + 2H 2 катализдік риформингіленуі соңғы екі онжылдықта синтез газын өндірудің балама әдісі ретінде қызығушылық тудыруда. Бұл үрдіс H 2 / CO өнімдері қатынасының төмен және Фишер-Тропш синтезінің үрдістеріне қолайлы болуына байланысты өнеркәсіптік тұрғыдан да маңызды [ 158 ] . Көптеген зерттеушілер Fe, Co және Ni негізіндегі катализаторлардың бұл үрдіс үшін өте белсенді екенін хабарлайды. Дегенмен, көміртектің (кокс) түзілуінің салдарынан катализаторларды дезактивациялау - бұл үрдістің жүруінде туындайтын негізгі мәселелердің бірі болып табылады. Соңғы онжылдықта никельді катализаторлар кеңінен зерттелді [159-160 ], дегенмен Co және Со-құрамды катализаторларды зерттеу туралы мәліметтер әлі де болса жеткіліксіз екенін айта кеткен жөн [ 161 ] .
Осы бөлімде кобальт пен алюминий нитраттары және карбамидті қолдана отырып, дәстүрлі сіңдіру әдісімен және алдын ала 500°С температурада қыздыру арқылы ерітіндіде жану SCS әдістерімен синтезделген Co және Al сериясы негізіндегі дайындалған катализаторлар зерттелді [ 162 ] . SCS жану режимі кезінде шамамен жүруі мүмкін деп болжанған реакциялар 4-кестеде көрсетілген.
Кесте 4 - Co(NO 3 ) 2 + Al(NO 3 ) 3 + H 2 O + карбамид жүйесінің SCS бойынша жануы кезінде жүретін реакциялардың сериясы
ΔН о 278 = -3352 кДж / моль, экзотермиялық реакция.
Тотықсыздандырылған металдар ішінара тотығуы немесе басқа металдармен әрекеттесуі мүмкін
Бастапқы шихтаның құрамы, жану үрдісінің жүру шарттары және түзілген катализаторлардың соңғы құрамы 5-кестеде келтірілген. Дайындалған катализаторлардың құрамындағы металдар әр түрлі болғанымен, сапалық құрамы ұқсас болды, бірақ фазаларының қатынастарының әр түрлі болуымен ерекшеленді.
Фазалар арасындағы қатынастар әр фаза үшін рентген сәулелерінің дифракция шыңдарының салыстырмалы қарқындылығымен есептелініп, анықталынды, 11-сурет.
Ерітіндіде жану барысында температураны өлшеу барысында температуралық қисықтың бойында екінші шың пайда болды, 12-сурет.
Кесте 5 - Бастапқы шихтадағы тұздардың құрамы мен SCS әдісімен синтезделгеннен кейінгі катализаторлардың соңғы құрамы
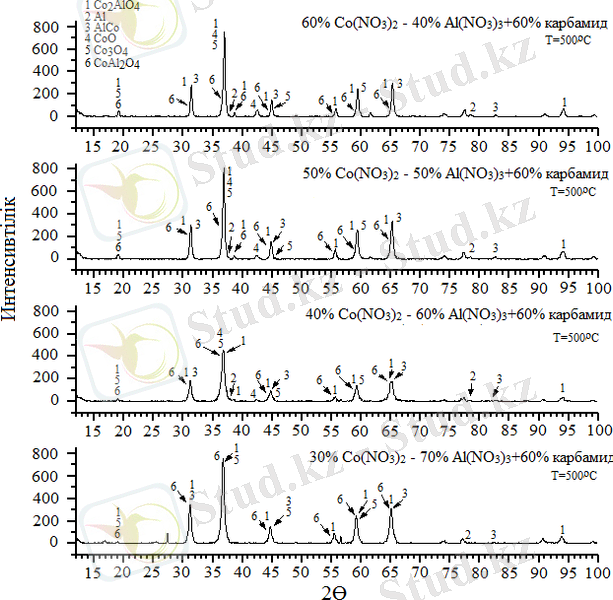
Сурет 11 - Бастапқы қоспаны алдын ала 500°C-та қыздырғандағы Co(NO 3 ) 2 - Al(NO 3 ) 3 /карбамид + H 2 O жүйесінің рентген спектрлері
Мұны көміртектің металл оксидтерімен реакцияға түсуімен түсіндіруге болады. Тек 2Al 2 O 3 + 3C → 4Al + 3СО 2 реакциясы ғана реакция өнімінде Al-дің болуын түсіндіре алады, себебі реакцияның жүруі кезінде пайда болатын сутегі синтезделу жағдайында түзілетін Al 2 O 3 -ті тотықсыздандыра алмайды.
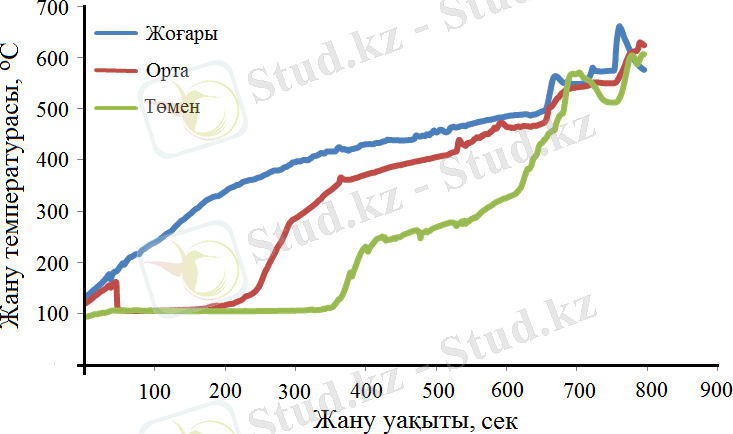
Сурет 12 - Бастапқы 30% Co(ΝΟ 3 ) 2 - 70% Al(NO 3 ) 3 /60% карбамид үлгісінің көлемді жану режимінің температуралы-уақытты профилі
Ерітіндідегі Al(NO 3 ) 3 концентрациясының жоғары болуы түзілген соңғы өнімнің құрамында Co 2 AlO 4 және CoAl 2 O 4 шпинельдерінің де концентрацияларының жоғары болуына әсер еткенін 13а және 13в - суреттерден көруге болады. Интерметаллдық қосылыстардың концентрациясы шпинельдерге қарағанда бірнеше есе төмен болатындығы және бастапқы қоспаның құрамындағы Al(NO 3 ) 3 жоғарылауымен шпинельдердің концентрациясының жоғарылауының жалпы заңдылығына іс жүзінде әсер етпейтінін 13в және 13г -суреттерден көруге болады. 13a және 13б суреттерде көрсетілгендей, шпинельдердің концентрациясы CoO-ға қарағанда едәуір жоғары және Co 3 O 4 концентрациясымен салыстырғанда мәндері шамалас екендігін байқауға болады.
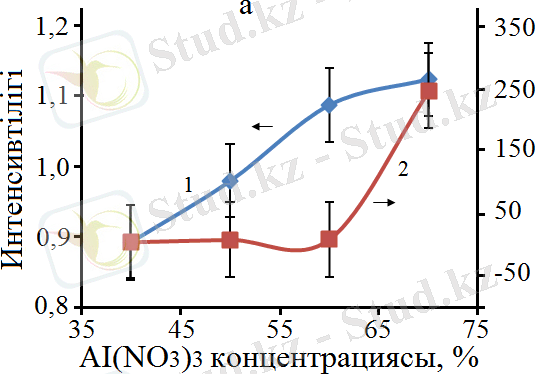
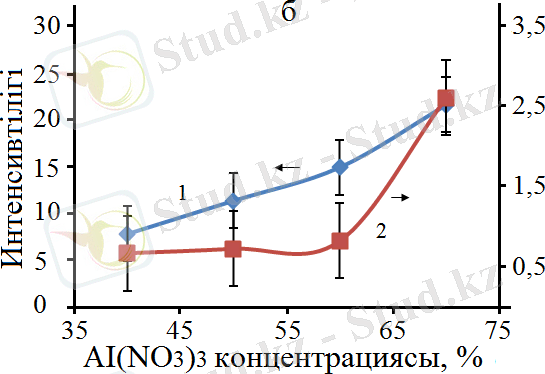
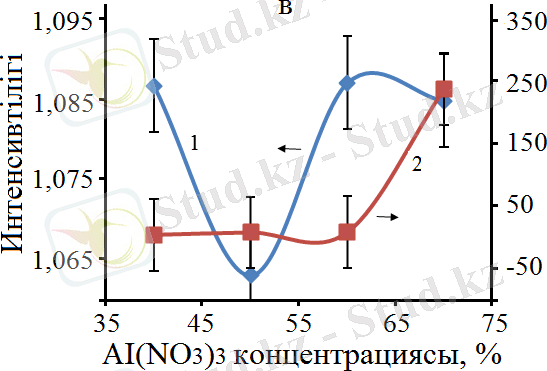
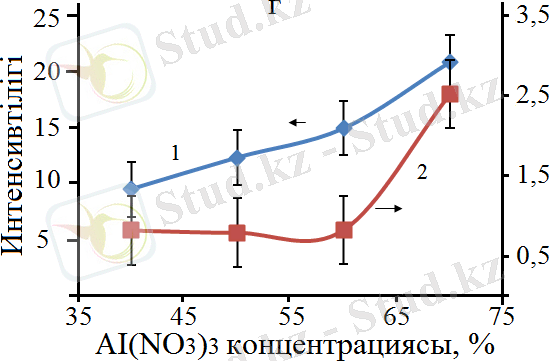
Белгіленулері: а: 1 - CoAl 2 O 4 /Co 3 O 4 , 2 - CoAl 2 O 4 /CoO; б: 1 - CoAl 2 O 4 /Al, 2 - CoAl 2 O 4 /AlCo; в: 1 - Co 2 AlO 4 /Co 3 O 4 , 2 - Co 2 AlO 4 /CoO; г: 1 - Co 2 AlO 4 /Al, 2 - Co 2 AlO 4 /AlCo.
Сурет 13 - Бастапқы қоспадағы Al(ΝΟ 3 ) 3 концентрациясына байланысты рентген шыңдарының интенсивтілігінің өзгеруі
Al(ΝΟ 3 ) 3 концентрациясы кристалдық тордың деформациясында маңызды рөл атқарады. Бастапқы ерітіндідегі Al(ΝΟ 3 ) 3 концентрациясы неғұрлым жоғары болса, соғұрлым Co 2+ (0, 72 Ǻ) иондары матрицадағы Al 3+ (0, 51 Ǻ) иондарын алмастыра алады, дегенмен, әдетте Co 2+ катиондары Al 2 O 3 матрицасындағы бос орындарға орналаса алады, бұл рентгенфазалық талдауларда байқалмайды. Мұны шпинель мен кобальт оксидтерінің кристалдық торларының көлемінің ұлғаюымен көруге болады. Интерметалдық қосылыстар мен алюминийде құрылымдық өзгерістер байқалмады, 14-сурет.
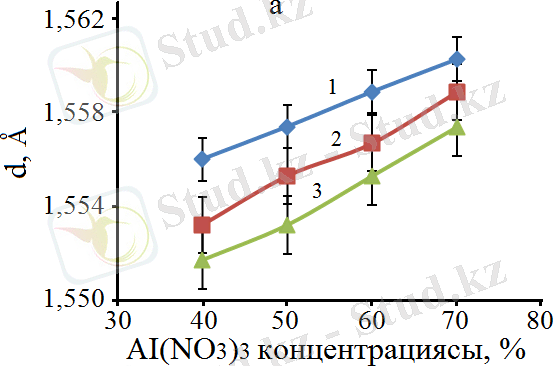
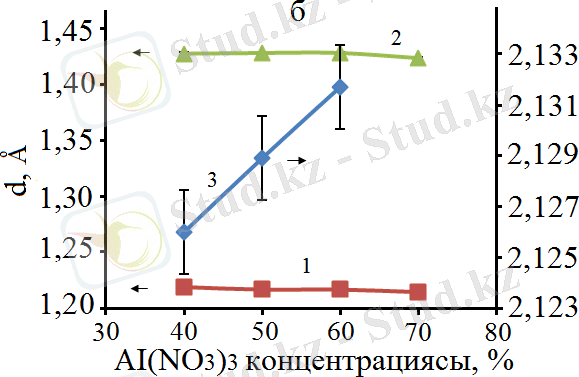
Белгіленулері: а: 1 - CoAl 2 O 4 (hkl = 511), 2 - Co 2 AlO 4 (hkl = 511), 3 - Co 3 O 4 (hkl = 511) ; б: 1 - Al (hkl = 311), 2 - AlCo (hkl = 200), 3 - CoO (hkl = 200) .
Сурет 14 - Бастапқы қоспадағы Αl(ΝΟ 3 ) 3 концентрациясының CoAl 2 O 4 , Co 2 AlO 4 , Co 3 O 4 , CoO, AlCo, Αl-дің кристалды торларының размеріне әсері
Дайындалған катализаторлардың кристаллиттерінің орташа мөлшері РФТ нәтижесінде алынған шыңдарының ені бойынша есептелінді. 15-суретте келтірілген нәтижелерден бөлшектердің орташа мөлшері Al(ΝΟ 3 ) 3 концентрациясының жоғарылауымен төмендейтінін көрсетеді.
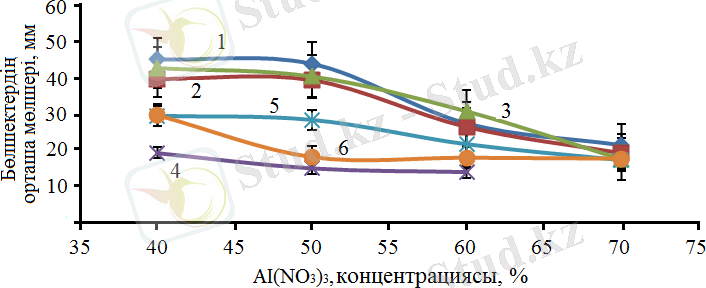
Белгіленулері: 1 - CO 2 O 4 (511), 2 - Co 2 AlO 4 (511), 3 - Co 3 O 4 (511), 4 - CoO (200), 5 - AlCo (200), 6 - Al (311) .
Сурет 15 - Кристаллиттердің мөлшерінің Al(NO 3 ) 3 концентрациясына тәуелділігі
Дайындалған барлық катализаторлардың беткі ауданы БЭТ әдісімен өлшенді. Катализаторлардың беттік аудандарының мәндері бір-біріне өте жақын 33, 1 - 33, 4 м 2 г -1 аралығында екені анықталды.
Синтезделген катализаторлардың беттік құрылымы мен морфологиясын зерттеу үшін сканерлі электронды микроскопия әдісі қолданылды.
Негізінен, бастапқы қоспада алдын-ала 500°C дейін қыздырылған пеште синтезделіп алынған құрамында 30% және 60% Co(ΝΟ 3 ) 2 бар катализаторлар зерттелді, 16 - 17 - суреттер . Наноөлшемді бөлшектер SCS әдісімен дайындалған катализаторларда анықталды. Сондай-ақ, катализатордың құрамын анықтау үшін EDS талдауы жүргізілді. Зерттеудің нәтижесінде келесі қосылыстардың бар екендігі анықталды: CO 2 O 4 , Co 2 AlO 4 (кубтық), Co x Al y (кубтық), Co 3 O 4 , Al и СоО (кубтық) .

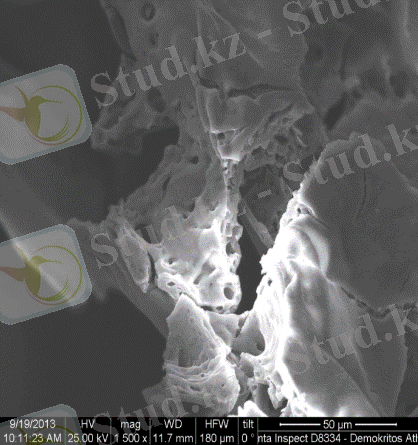
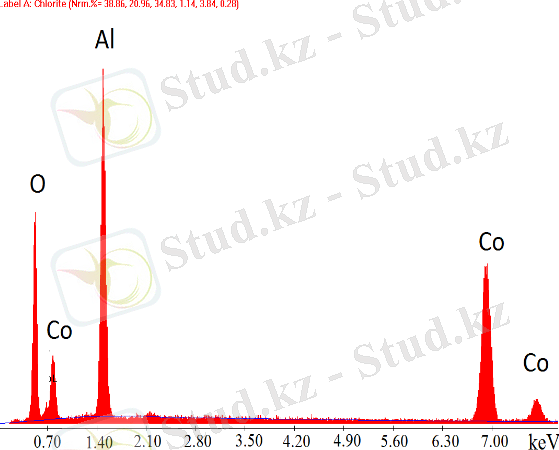
Сурет 16 - Шихтадағы бастапқы құрамы 30% Co - 70% Al болатын 500 о C-та дайындалған катализатордың суреттегі көрсетілген нүктедегі EDS және СЭМ суреттері

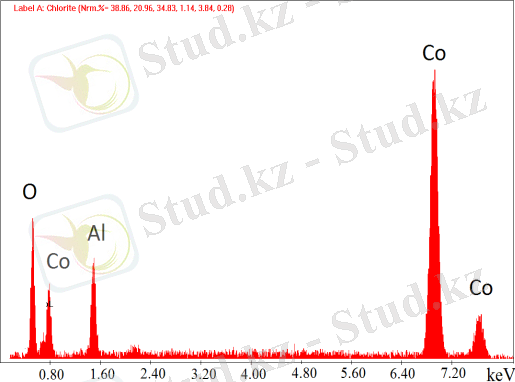
Рисунок 17 - Шихтадағы бастапқы құрамы 60% Co - 40% Al болатын 500 о C-та дайындалған катализатордың суреттегі көрсетілген нүктедегі EDS және СЭМ суреттері
Ерітіндіде жану әдісімен синтезделген катализаторлар, метанның көміртегі диоксидімен көмірқышқылды конверсиялану үрдісінде 750-ден 900°С аралығында сынақтан өткізілді. Зерттеу нәтижелерінің барысында алынған CH 4 және CO 2 конверсияларының мәндері, сондай-ақ реакция өнімдеріндегі H 2 /CO қатынасы үшін белсенділік көрсеткен катализаторлардан 60% Co - 40% Al және 30% Co - 70% Al алынған мәліметтер 18-суретте келтірілген.
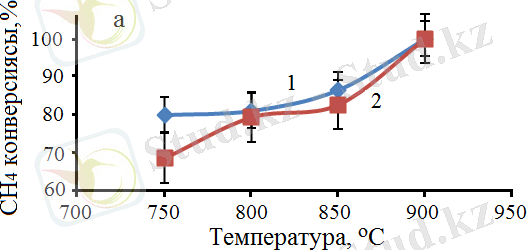
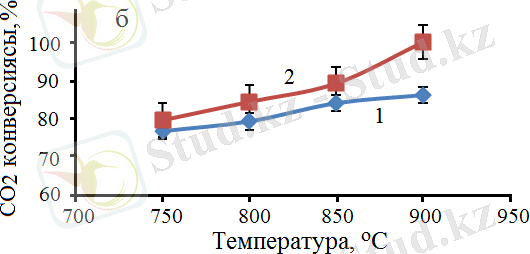
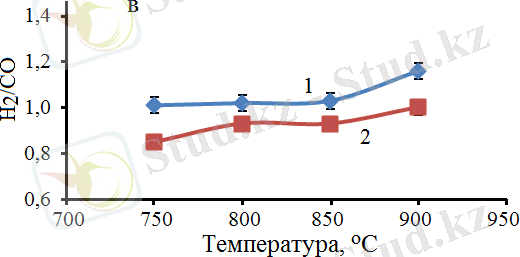
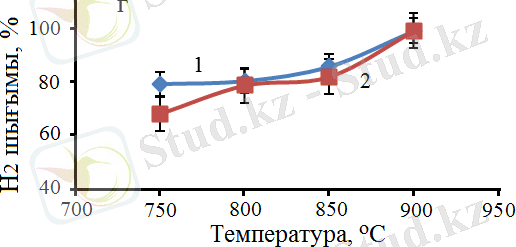
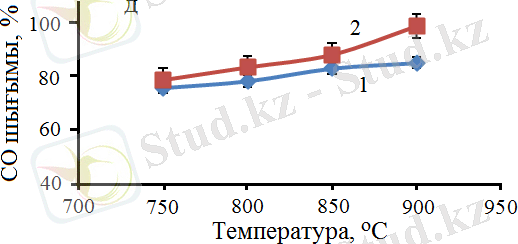
Белгіленулері: 1 - 60% Co - 40% Al/60% карбамид, 2 - 30% Co - 70% Al/60% карбамид, W = 860 сағ -1 .
Сурет 18 - SCS әдісімен дайындалған Со катализаторларының қатысында алынған CH 4 (а) мен CO 2 (б) конверсиясы, H 2 /CO қатынасы (в), Η 2 (г) және CО (д) шығымдарының реакцияның температурасына тәуелділігі
Алынған нәтижелердегі мәліметтер бойынша метанның 100% конверсиясы 900°C температурада 30% Co -70% Al катализаторында байқалатындығы анықталды. Сонымен қатар, бұл катализаторда СО 2 -нің де конверсиясы 100 %-ды көрсететіндігі анықталды. Реакцияның өнімдеріндегі H 2 /CO қатынасы екі катализатор үшін де 0, 8-1, 2 аралығын құрайды. Реакцияның температурасының жоғарылауы өнімдердегі H 2 /CO қатынасының жоғарылауына әкеледі. Әдетте, H 2 /CO қатынасы 1 : 1 болғанда, отын ретінде пайдалануға болатын диметил эфирін өндіру үшін өте маңызды болып табылады. CH 4 конверсиясы 60% Co - 40% Al катализаторының қатысуымен 900°C кезінде 100% құрады, ал CO 2 конверсиясы тек 86, 2% - ға жетті. Реакцияның өнімдері болып табылатын H 2 және CO шығымдары сәйкесінше 99, 2% және 85, 4% құрады, 18-сурет . Метанның көмірқышқылды конверсиясы үрдісінде сынақтан өткізілген 30% Co - 70% Al катализаторында бастапқы газдардың CH 4 және CO 2 максималды 100% конверсиясына қол жеткізуге болатындығы анықталды. Ал, 900°C температурада түзілген өнімдердің шығымдарының мәндері 99, 2% H 2 және 99, 1% CO болатындығы анықталды, 18-сурет.
Метанның көмірқышқылды конверсиясы үрдісінде көлемдік жылдамдықтың әсері CO 2 конверсиясына қарағанда CH 4 конверсиясы үшін маңызды, 19 а - сурет . Бұл реакцияда метан сутегі алудың негізгі көзі болғандықтан, алынатын өнімдегі H 2 /CО қатынасы көлемдік жылдамдықтың жоғарылауымен төмендейді, 19 б - сурет . Бұл құбылысты CH 4 молекулаларының мөлшері (3, 99 Å) CO 2 (2, 3 Å) молекулаларының мөлшерімен салыстырғанда шамамен екі есе көп болатындығымен түсіндіруге болады. Сондықтан CH 4 молекулаларының адсорбциялануы мен десорбциялануының жүруі көлемдік жылдамдықты жоғарылатқан сайын реакцияның жүру жағдайында CO 2 молекулаларына қарағанда анағұрлым шектеулі екендігімен түсіндіріледі.
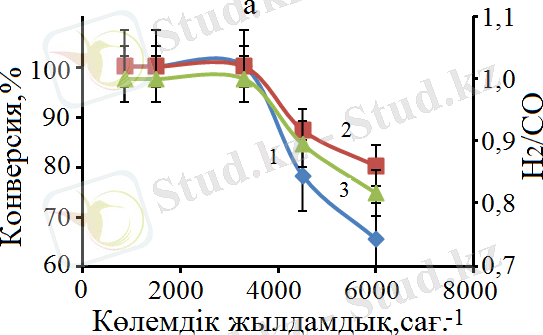
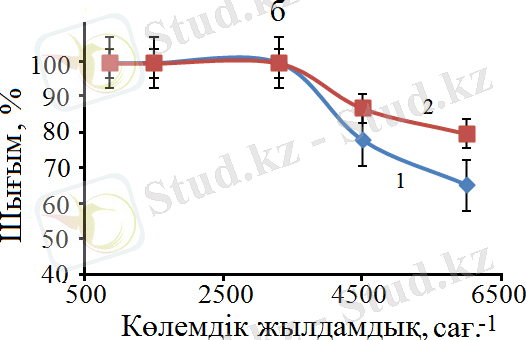
Белгіленулері: а: 1 - СН 4 конверсиясы, 2 - СО 2 конверсиясы, 3 - Н 2 /СО қатынасы; б: 1 - Н 2 шығымы, 2 - СО шығымы.
Сурет 19 - Көлемдік жылдамдықтың СН 4 , СО 2 конверсиясына, Н 2 /СО қатынасына (а) және реакцияның өнімдерінің Н 2 және СО (б) шығымына әсері, Т=900°С
Тәжірибені жүргізу барысында жоғары катализдік белсенділік көрсеткен (19-суретте) катализатордың (бастапқы құрамы 30% Co - 70% Al) тұрақтылығы W = 3300 сағ -1 кезінде катализатордың тұрақтылығы зерттелді, 20-сурет. Аталған катализатор 7 сағат аралығында жоғары катализдік белсенділікке ие: CH 4 конверсиясы 90%, ал CO 2 конверсиясы 94%, 20а-сурет , H 2 шығымы 89% және CО шығымы 93%, 20б-сурет және H 2 /CO қатынасы 1 болғанын айтуға болады, 20а-сурет .

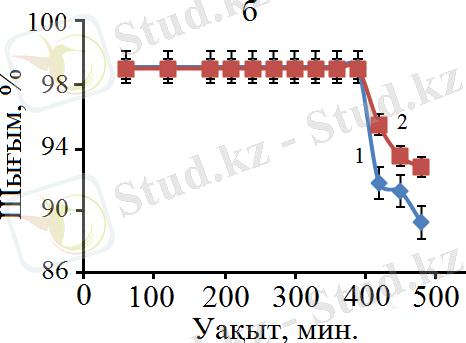
Белгіленулері: а: 1 - СН 4 конверсиясы, 2 - СО 2 конверсиясы, 3 - Н 2 /СО қатынасы; б: 1 - Н 2 шығымы, 2 - СО шығымы; W = 3300 сағ -1 .
Сурет 20 - CH 4 , CO 2 конверсиясының, Η 2 /CO қатынасы мен өнімнің шығымының тәжірибенің жүру ұзақтығына тәуелділігі
Метанның көмірқышқылды конверсиялануында 850 және 900°C температурада ерітіндіде жану және ылғал сыйымдылығы бойынша сіңдіру әдістерімен дайындалған 30% Co - 70% Al катализаторларының белсенділігі зерттелді. Осы катализаторларда 3300 сағ -1 көлемдік жылдамдығында алынған өнімдерінің H 2 және CO шығымының нәтижелері 21-суретте көрсетілген.
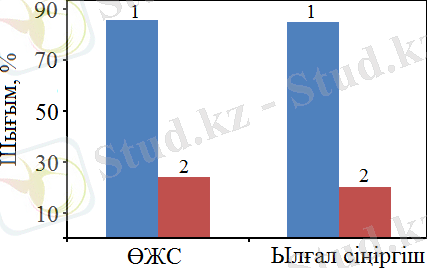
Белгіленулері: 1 - H 2 шығым, 2 - CO шығым, W = 3300 сағ -1 .
Сурет 21 - Катализаторларды дайындау әдістерінің (900 o C, 30% Cο - 70% Al/60% карбамид катализаторларында) өнімдердің H 2 және CO шығымына әсері
Ылғал сыйымдылығы бойынша сіңдіру және SCS әдісімен дайындалған 30% Cο - 70% Al/60% карбамид катализаторларындағы метанның көмірқышқылды конверсиясы үрдісінен алынған мәліметтерді салыстыру барысында алынған көрсеткіштерінің мәндерінде аз ғана айырмашылық байқалатындығы және SCS әдісінің шамалы артықшылығы бар екендігі анықталды. Түзілген H 2 өнімдерінің шығымдары 85% (ылғалдылық бойынша сіңдіру әдісімен дайындалған катализаторларда) бен 87 % (SCS) аралығында болатындығы ал, СО шығымы 20%-дан (ылғалдылық бойынша сіңдіру әдісі) 24%-ға дейін (SCS) болатындығы анықталды. Бастапқы реакциялық қоспаға су буының әсерін анықтау үшін 2500 сағ -1 көлемдік жылдамдықта SCS әдісімен дайындалған жоғарыда көрсетілген катализатор зерттеліп, CH 4 конверсиясы есептелді. Үрдістің жүруі барысында өнімдердің шығымы мен селективтілігіне су буының әсері 22а және 22б -суреттерінде көрсетілген.
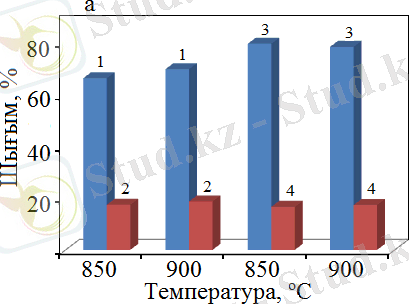
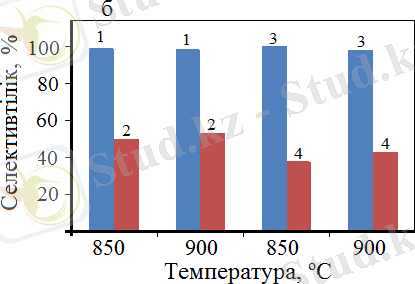
Белгіленулері: су буының қатысынсыз алынған 1 - H 2 , 2 - CO шығымдары; су буының қатысында алынған 3- H 2 , 4 - CO селективтіліктері.
Сурет 22 - Реакциялық қоспаға су буы қосылған кезде өнімдердің шығымы (а) мен селективтілігінің (б) температураға тәуелділігі
МКК үрдісін су буының қатысында жүргізу барысында температураны өзгерте отырып, 900°C-та негізгі өнімдер болып табылатын Н 2 және СО-ның шығымының да, селективтілігінің де ең жоғары мәндеріне қол жеткізуге мүмкіндік беретіні анықталды. Су буларының болуы өнімнің шығымына айтарлықтай әсер етеді, ал селективтілікке аз мөлшерде әсер етеді. Сондай-ақ, сіңдіру әдісімен дайындалған катализаторларда су буы ешқандай әсер етпейтіні көрсетілген. ӨЖС және сіңдіру әдісімен дайындалған катализаторларды 2500 сағ -1 көлемдік жылдамдықта зерттеп, алынған өнімдердің нәтижелерін салыстыру барысында ӨЖС әдісімен дайындалған катализаторлардың сіңдіру әдісіне қарағанда шамамен 7-9% - ға жоғары мәнге ие болатындығы анықталды.
CoAl 2 O 4 шпинелі негізгі катализдік компонент болғандықтан, CH 4 конверсиясы осы шпинельдің кристалды торының параметрлеріне байланысты болады. Метан реакцияның механизміне сәйкес үзілуі керек С-Н байланысының ұзындығы 1, 54 Å құрайды. Шпинельде кристалдық тордың мөлшері 1, 559-дан 1, 561 Å-ге дейін. Кристалдық тор параметрлерінің өзгеруі кобальт оксидінің кристалдық торындағы Al мөлшерінің артуына байланысты. Бұл параметрлер байланыс параметріне өте жақын, сондықтан катализаторлар 60% Co - 40% Al және 30% Co - 70% Al жоғары белсенділікті көрсетеді.
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz