Биологиялық макромолекулалардың құрылысы мен қызметі: ақуыздар, нуклеин қышқылдары, липидтер және көмірсулар



СӨЖ
Тақырыбы: Биологиялық макромолекула құрылысы және қызметі. (нәруыз, нүклейн қышқылы, липид, майлар)
Орындаған: Қалыбек А. Т. 114-топ
Факультет: Жалпы медицина
Тексерген: Алтаева Н. З
Нұр-Сұлтан, 2019 ж.
Жоспары:
- Кіріспе.
- Негізгі бөлім:
- Нуклеин қышқылдары
- Нәруыз
- Липид
- Көмірсу
- Қорытынды.
- Пайдаланылған әдебиеттер
Кіріспе
Жасушаның химиялық құрамы - жасушаның құрамына кіретін барлық заттардың жиынтығы. Жасушаның құрамында химиялық элементтердің периодтық жүйесінің 86 элементі бар, оларың ішінде 25 элемент ағзаның өмірінің тіршілік әрекеті үшін керекті болса, 16-18 элемент зәру қажет.
Жасушаның құрамында 80-нен астам химиялық элементтер кездеседі. Олар жасушадағы зат алмасу процестеріне қатысады. Əрбір жасушаның құрамы органикалық заттар жəне бейорганикалық
заттар қосылыстардан тұрады. Органикалық заттар: нəруыздар (10-20%), майлар(1-5%), көмірсулар(0, 2-2%) жəне нуклеин қышқылдары(1-2%) жатады. Бейорганикалық заттар :су(70-80 %) мен минералды тұздар (1-1, 5 %) Ағзалық қосылыстар жасуша құрамының 20-30% үлесіне тең.
Нəруыздар - көміртегі, сутегі, оттегі, азот, күкірт жəне т. б. элементтерден тұратын күрделі ағзалық заттар. Нəруыздар 45°С - 80°С ұйиды. Олардың құрамы 20 амин қышқылынан тұрады.
Майлар - үш элементтен құралған, олар: көміртегі, сутегі, оттегі. Майлар судан жеңіл, суда ерімейді. Май глецерин мен май қышқылынан тұрады.
Көмірсулар - майларға ұқсас, көміртегі, сутегі, оттегіден тұрады. Көмірсу деп аталу себебі, сутегі мен оттегінің арақатынасы сумен бірдей. Демек, сутегі атомы оттегі атомынан 2 есе көп деген сөз. Көмірсуларға əртүрлі суда тез еритін тəтті (кристалды) қанттар жатады. Бұлардың ішінде көбірек таралғандары - глюкоза (жүзім қанты) мен гликоген (жануар крахмалы) . Гликоген бауыр мен бұлшықеттер жасушаларында кездеседі.
Жасушаның бейорганикалық заттары - су мен минералды тұздар. Жасуша цитоплазмасында су мөлшері аздау болады. Сондықтан цитоплазма - қоймалжың, жартылай созылмалы сұйықтық. Су жасушаға еріткіш ретінде өте қажет. Себебі жасушадағы түрлі химиялық реакциялар тек еріген заттардың арасында жүреді. Қорек заттары жасушаға тек сұйық (еріген) күйінде қабылданады. Жасушаның 80%-ы су. Ондағы қажетсіз өнімдер мен зиянды заттар су арқылы сыртқа шығарылады.
2. 1 Нуклеин қышқылдары (лат. nucleus - ядро) - құрамында фосфоры бар биополемерлер. Табиғатта өте көп тараған. Молекулалары нуклеотидтерден тұрады, бір нуклеоидтік 5'-фосфор арасындағы эфирлік байланысы мен келесі нуклеотидтің углевод қалдығының 3'-гидроксилі арасы эфир байланысымен нуклеин қышқылдары углеводты-фосфатты қаққасын калайды. Нуклеин қышқылдары жоғарғы полимерлі тізбектері ондаған немесе жүздеген нуклеотидтің қалдықтарынан тұрады. Олардың м. с. 105-1010. Нуклеин қышқылдары құрамына кіретін мономерлерінің (дезокси- немесе рибонуклеотидтер) түріне қарай ДНҚ жәңе РНҚ деп бөлінеді.
Нуклеин қышқылдары тірі жасуша ядросының маңызды құрам бөлігі. Нуклеин қышқылдары (НҚ) рибонуклеин қышқылы (РНҚ) және дезоксирибонуклеин қышқылы (ДНҚ) болып екі үлкен түрге бөлінеді. Тірі организмнің құрамына нуклеин қышқылдарының екі түрі де кіреді. Нуклеин қышқылдары жоғары молекулалы гетерополимерлі қосылыстар.
Нуклеин қышқылдарының құрамы мен құрылысы
Нуклеин қышқылдарының толық емес гидролизі нәтижесінде нуклеотидтер түзіледі (25-сызбанұсқа) . Олар нуклеин қышқылдары полимер тізбегінде қайталанып отыратын күрделі құрылым буындары (монометрлері) . Ал нуклеотидтерді одан әрі гидролиздесе, ортофосфор қышқылын және пентоза мен азотты негізге айырылатын нуклеозидтерді түзеді.
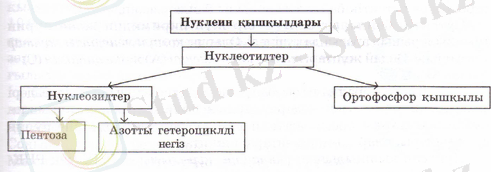
Яғни, нуклеин қышқылдарының құрамына азотты негіздер (пиримидинді, пуринді), фосфор қышқылы және моносахаридтер (рибоза мен дезоксирибоза) кіреді. Нуклеин қышқылдары құрамындағы моносахаридтердің қалдығына байланысты рибонуклеин қышқылы және дезоксирибонуклеин қышқылы болып екіге бөлінеді. ДНҚ молекулалық массалары бірнеше мыңнан ондаған миллионға жетеді.
ДНҚ мен РНҚ құрамының айырмашылығы - нуклеин қышқылын толық гидролиздеу арқылы анықталды. Оларды гидролиздегенде, әр түрлі заттардың қоспасы түзіледі (36 кесте) .
Нуклеин қышқылдары құрамында көмірсудың гидроксил тобы мен фосфор қышқылының арасында күрделі эфирлік байланыс түзіледі, ал азотты негіз көмірсудың жанынан жалғасады. Полинуклеотидтің құрылысын сызбанұсқамен былай өрнектеуге болады:
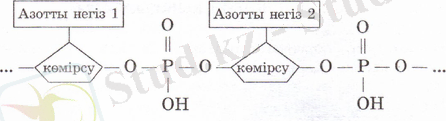
ақуыздар сияқты нуклеин қышқылдары әр түрлі болады. Олардың организмдегі функциясы да әр алуан. Нуклеин қышқылдарының да ақуыздар сияқты әр түрлі құрылымдары болады.
Нуклеин қышқылының бірінші құрылымында мононуклеотидтер белгілі тәртіппен орналасады.
Нуклеин қышқылының екінші құрылымы макромолекулалардың кеңістікте қос шиыршық болып орналасуын көрсетеді. Бұл кезде молекулалар арасында және молекула ішінде сутектік байланыс арқылы әрекеттесу болады.
НҚ-ның макромолекуласы екі полинуклеотидті тізбектен құралады. Олар кеңістікте қос оралма түзеді (54-сурет) . Оралманы фосфор қышқылының полиэфирі түзеді, пиримидин және пурин туындыларының жазық молекуласы оралманың ішінде болады.
Нуклеин қышқылының макромолекуласындағы бірінің ішінде бірі жатқан ширатылған екі оралмада, пиримидин және пурин қалдықтары өзара сутектік байланыс арқылы байланыскан.
Сутектік байланыс белгілі бір жұп пиримидин және пурин туындыларының арасында түзіледі. Оларды комплементарлы жұптар деп атайды. Ондай жұптар: тимин (Т) - аденин (А) және цитозин (С) - гуанин (G) .
ДНҚ-ның қос оралмалы сызбанұсқасында таспамен көрсетілгендері фосфор қышқылымен көмірсулардың полиэфирінің макромолекуласы. Бұларды қосып жатқан түзулер пиримидин және пурин туындылары, олар комплементарлы жұптар.
Нуклеин қышқылының үшіншілік щрылымы - ДНҚ мен РНҚ-ның кеңістікте шумақталып орналасуы.

Нуклеин қышқылдарының маңызы
Нуклеин қышқылдары биологиялық тұрғыдан маңызды рөл атқарады. Олар тірі организмдердегі генетикалық ақпаратты сақтайтын және тасымалдайтын жасушаның (жасушаның) маңызды кұрам бөліктері болып табылады. Нуклеин қышқылдары ақуыз биосинтезіне қатысады және тірі организмдерде тұқым қуалаушылықты сақтап, оның бір ұрпақтан екінші ұрпаққа берілуін қамтамасыз етеді. ДНҚ жасуша ядросының хромосомасында (99%), рибосомаларда және хлоропластарда, ал РНҚ ядрошықтарда, рибосомаларда, митохондрияда, пластидтер мен дитоплазмада кездеседі.
Олар жасушаның қай бөлігінде шоғырланса, соған байланысты қызмет атқарады. Жоғарыда айтылғандай, ДНҚ организмдегі тұқым қуалаушылық ақпаратты сақтайтын гендердің құрылыс материалы болып табылады. Ал РНҚ үш түрлі болғандықтан: рибосомдық (р-РНҚ) ; тасымалдаушы (т-РНҚ) және ақпараттық (а-РНҚ) әр түрлі қызметтер атқарады. ДНҚ мен РНҚ қызметтері 1940 жылдардан бастап анықталып, түрлі биологиялық тәжірибелер арқылы дәлелденген. Осы зерттеулер нәтижесінде молекулалық генетика ғылымы жедел дами бастады.
Соңғы жылдары ғалымдар жоғары организмдердің гендерін бактериялар мен ашытқы саңырауқұлақтарының организміне енгізуді іске асырды. Соңынан оларды ақуыз синтездеуге пайдаланды. Мысалы, инсулин генін осылайша "жұмыс істеткізді". Адам инсулині ең алғаш рет Е. соlі деген бактерияның көмегімен 1982 жылы алынды.
Осылайша бір типтегі организмнен алынған генді басқа типтегі организмге енгізуді гендік инженерия деп атайды. Жоғарыда айтылған ипсулин, өсу гормоны - соматотропин, сондай-ақ гемофилия ауруына қолданылатын VIII фактор - гендік инженерияның өнімдері. Қазіргі кезде гендік инженерияның көмегімен түрлі жұқпалы ауруларға қарсы вакциналар өндіріле бастады.
2. 2 Ақуыз - молекулалары өте күрделі болатын аминқышқылдарынан құралған органикалық зат; тірі организмдерге тән азотты күрделі органикалық қосылыс. Аминқышқылдары қалдықтарынан құралған жоғары молекуларлық органикалық түзілістер. Ақуыз организмдер тіршілігінде олардың құрылысы дамуы мен зат алмасуына қатысуы арқылы әртүрлі және өте маңызды қызмет атқарады. Ақуызды зат - құрамында міндетті түрде азоты бар күрделі органикалық қосылыс.
Құрылымы
Ақуыз жасуша құрамына кіретін тірі құрылымдар - ядро, митохондрия, рибосома, цитоплазма негіздерін құрайды. Сондықтан ол организмде үлкен орын алады. Мысалы, адам мен жануарлар денесінің құрғақ заттарында 45%, жасыл өсімдіктерде 9 - 16%, дақыл тұқымында 10 - 20%, бұршақ тұқымдастар дәнінде 24 - 35%, бактерия жасушаларында 50 - 93% ақуыздық заттар бар. Ақуыз барлық организмге ортақ зат болғанымен, әртүрлі организм ақуыздарының құрылымы түрліше болады. Сондай-ақ, организм түрлерінің бір-біріне ұқсамауы, олардың эволюция жолымен үздіксіз өзгеріп дамуы да ақуыз қасиеттерінің үнемі өзгеріп отыруына байланысты.
Организмнің күнделікті тіршілігі оның жасушаларында жүріп жататын көптеген биохимиялық реакцияларға негізделген. Осы реакциялар нәтижесінде өсімдіктерде, бір жағынан, тіршілікке қажетті химиялық қосылыстар - ақуыздар, нуклеин қышқылдары, көмірсулар, майлар, витаминдер синтезделетін болса, екінші жағынан, онда ферменттер арқылы күрделі заттар ыдырап, өсімдіктің қоректенуіне, тозған жасушаларын жаңартуына, организмге қуат беруге жұмсалады. Бұл құбылыстарды метаболизм [[] ] деп атайды. Осы реакциялардың бәрінде де ақуыз катализаторлық қызмет атқарады. Қан құрамындағы ерекше ақуыз - гемоглобин бүкіл денеге оттек таратады. Жасушалардағы тотығу ферменттері - цитохромдар тыныс алу процесін реттеп отырады. Сондай-ақ организм тіршілігіне аса қажетті заттар гормондар да ақуыздан құралған. Ерімтал ақуыздар - гидрофильді коллоидтар - суды бойына көп тартады. Олардың ерітінділері желім сияқты: осмостық қысымы төмен, қозғалу қабілеті нашар, өсімдік пен жануарлар мембранасынан өте алмайды. Ақуыздардың тағы бір қасиеті - олар амфотерлі электролиттер. Молекулаларында бос карбоксил және амин топтары болатындықтан, олар оң немесе теріс электр зарядты болады. Химиялық табиғаты жағынан ақуыз биополимерлер тобына жатады.
Ақуыздың құрамында жиырма түрлі аминқышқылдар болады. Әртүрлі ақуыздардың аминқышқылы құрамы жағынан да, олардың тізбектегі орналасу тәртібі жағынан да бір-бірінен айырмашылығы зор. Табиғатта ақуыз түрлерінің көп болуы да осыған байланысты. Мысалы, үш аминқышқылының қосылуынан алты түрлі, төрт қышқылдан жиырма төрт түрлі ақуыз изомерлері пайда болады. Ақуыз молекуласы амин қышқылдарының өзара моншақтай тізіле байланысқан полипептидтік тізбегінен құралады. Ақуыз молекуласының сыртқы пішіні екі түрлі болады.
- Шар тәрізді домалақ - глобулярлы ақуыздар. Бұларға альбуминдер, глобулиндер, гемоглобин, пепсин және өсімдік жасушасының ақуыздары жатады.
- Фибриллярлық (талшық тәріздес) ақуыздар. Бұларға бұлшық ет ақуызы - миозин, актин, сіңір ақуызы - коллаген және малдың жүні мен піллә жібегі ақуыздары жатады.
Ақуыз молекуласының өзіне тән ерекшеліктері мен құрылымдылық дәрежелері көптеген сутектік байланыстар, электрстатикалық қуаттар, күкірттен құралатын дисульфидтік байланыстар, т. б. жағдайлар арқылы қамтамасыз етіледі. Ақуыз ерітіндісін қыздырса немесе оған күшті қышқылмен әсер етсе, ол өзінің табиғи қасиеттерін (ферменттік, гормондық) жояды, кейде ұйып та қалады. Мұндай құбылысты денатурация деп атайды. Ақуыз - адам тағамы мен жануарлар қорегінің, сондай-ақ тері, жүн, жібек сияқты табиғи талшық заттардың негізгі құраушысы болғандықтан, 20 ғасырдың екінші жартысынан бастап оны қолдан өндірудің (микробиологиялық синтез) маңызы артып отыр.
Ақуыздың түзілуі - бұл өте күрделі жасушадағы ұсақ бөлшектер-рибосомаларда жүретін процесс. Қашан, қанша және қандай ақуыз түзілуі керектігі жайлы мәлімет жасуша ядросындағы ДНҚ, РНҚ арқылы жеткізіледі.
Ақыздардың қасиеттерін олардың құрамы мен құрылымы анықтайды. Ақуыз молекуласындағы а-аминқышқылдары қалдықтарының саны әртүрлі болады, кейде бірнеше мыңға дейін жетеді. Әр ақуызда а-аминқышқылдары тек осы ақуызға ғана тән ретімен орналасады. Олардың молекулалық массалары бірнеше мыңнан миллионға дейін жетеді. Мысалы, жұмыртқа ақуызының молекулалық массасы 36000, бұлшық ет ақуызының молекулалық массасы - 15, адам гемоглобині 67000, ал көптеген ақуыздардікі > 3 шамасында. Олар, негізінен, көміртек (50-55%), оттек (20-24%), азот (15-19%), сутектен (6-7%) тұрады. Кейбір ақуыздардың құрамына бұлардан басқа күкірт, фосфор, темір кіреді. Ақуыздар гидролизденгенде а-аминқышқылдарының қоспасы түзіледі. Әрбір организмнің өзіне тән ақуыздары бар. Барлық ақуыздар 20-дан астам әртүрлі а-аминқышқылынан құралады. А-аминқышқылдарының жалпы формуласы:
R-CHNH 2 -COOH
Ақуыз түзілетін a-аминқышқылдарының радикалды құрамында ашық тізбек те, тұйық тізбекті әртүрлі сақиналар мен функционалдық топтар да кездеседі.
Полипептид тізбегінің құрылысы
Ақуыздардың құрылысы өте күрделі. Ақуыз молекуласы құрылымын: бірінші реттік, екінші реттік, үшінші реттік және төртінші реттік деп бөліп қарастырады.
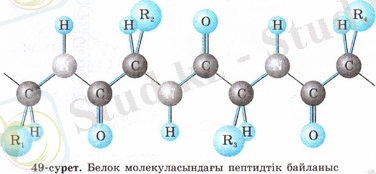
Полипептидтік тізбектегі аминқышқылдары қалдықтарының қатаң тәртіппен бірінен кейін бірінің орналасуын бірініші реттік құрылым анықтайды. Ақуызды құрайтын жүздеген, мыңдаған, миллиондаған а-аминқышқылдарының қалдықтары өзара пептидтік байланыс (- CO - NH -) арқылы жалғасады (49-сурет) .
Полипептид тізбегіндегі аминқышқылының бір қалдығының басқасымен ауысуы немесе оның орнының алмасуы осы ақуыздың қызметін бұзады. Мысалы, адам гемоглобиніндегі 564 аминқышқылдары қалдықтарынан құралған полипептид тізбегіндегі бір қышқылдың қалдығы екіншісіне ауысса, адам ауыр сырқатқа ұшырайды.
Аминқышқылдары қалдықтарының инсулиннің кейбір бөлігінде орналасуын мынадай тізбек түрінде көрсетуге болады: глицин-изолейцин-валин-глутамин, т. с. с. 50-суретте 2-полипептидтік тізбектен тұратын инсулиннің бірінші реттік құрылымы келтірілген.
Табиғатта ақуыздардың кейбіреуі тек созылыңқы полипептидтік тізбекте болады. Мысалы, табиғи жібек талшығы - фибрионның құрылымы осындай.
Ақуыздардың көбінің кеңістікте спираль тәрізді оратылуы екінші реттік құрылым деп аталады. Бұл құрылым, негізінен, спираль оралымдарында орналасқан - CO . . . HN- арасындағы сутектік байланыстар арқылы іске асады. Шиыршықтың бір орамында 3 және 5 аминқышқылдарының қалдықтары болады. Оралымдардың арақашықтықтары 0, 54 нм шамасында.
Ақуыздық оралма тектес молекуласы биологиялық процестердің әсерінен, молекула арасындағы сутектік байланыс, -S-S- дисульфид көпіршесі, күрделі эфирлік көпірше және бүйір тізбектегі анион мен катиондар арасындағы иондық байланыстар арқылы өзара байланысады да, өте күрделі үшінші реттік құрылым түзіледі. Бұл кезде оралма құндақталып, шумаққа айналады (52-сурет) . Үшінші реттік құрылым ақуыздың өзіне тән қасиеттері мен белсенділігіне жауап береді.
Ақуыз молекуласы тек қана бір полипептидік тізбектен тұрса, оның құрылымдары бірінші, екінші және үшінші реттік болады. Ал ақуыз молекуласы екі және одан да көп полипепидік тізбектен құралса, онда төртінші реттік құрылым түзіледі. Төртінші реттік құрылым - кейбір ақуыздарда бірнеше полипептидтік тізбектердің бір-бірімен күрделі кешенді комплекстерге бірігуі. Мысалы, гемоглобин құрамына 141 аминқышқылының қалдығы кіретін төрт полипетидтік тізбектен және құрамында темір атомы бар ақуызды емес бөлшек гемнен комплекс түзеді. Гемоглобин тек осы құрылымда ғана оттекті тасымалдай алады.
Нәруыздардың күрделілігіне қарай 4 реттік құрылымы болады: бірінші реттік, екінші реттік, үшінші реттік және төртінші реттік құрылымдар.
Нәруыздың бірінші реттік құрылымы
Полипептидтік тізбектегі әртүрлі аминқышқылдар қалдықтарының бір-бірімен кезектесіп пептидтік байланысу ретін нәруыздың бірінші реттік құрылымы деп атайды. Көптеген полипептидтер тізбегі 300-ден 500-ге дейін аминқышқылы қалдығынан тұрады. Алғаш рет 1954 жылы Ф. Сенджеру нәруыз инсулин гормонының аминқышқылы қалдығының реттілігін анықтады. Инсулин гормоны 51 аминқышқылынан тұратыны белгілі болды.
Нәруыздың екінші реттік құрылымы
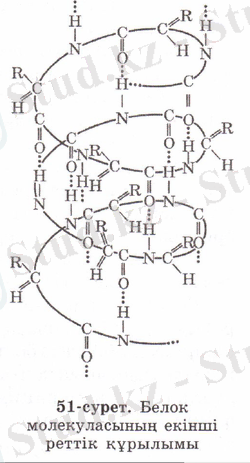
Нобель сыйлығының лауреаты, атақты ғалым Лайнус Полинг нәруыздың екінші реттік құрылымын ашқан. Полипептидті тізбектің кеңістіктегі оралма тәрізді болып келген пішінін нәруыздың екінші реттік құрылымы деп атайды. Бұған нәруыздың және тырнақтың нәруызы кератин жатады. Нәруыздың екінші реттік құрылымы мутектік байланыстар арқылы орындалады. Бір орамдығы NH-топтары мен көршілес орамдығы CO-топтары арасындығы түзілетін сутектік байланыс арқылы оралым ұсталынып тұрады. Сутектік байланыстар коваленттік байланыстардан анағұрлым әлсіз. Бірақ бірнеше рет қайталанғанда, олар берік байланысады. Көптеген сутектік байланыстар арқылы «тігілген» полипептидті оралым берік құрылым болып келеді. Нәруызда оралмалы бөліктерінің бар болуы, оған жылжымалылық, мықтылық, серпімділік қасиет береді.
Нәруызда цилиндр тәрізді оралым бөліктерінен басқа аминқышқылы пролиннен түзілетін, тізе тәрізді бүгілетін бөліктері де бар.
Нәруыздың үшінші реттік құрылымы
Үшінші реттік құрылымның түзілуіне дисульфидті байланыстар үлкен үлес қосады. Олар полипептидті тізбектің әртүрлі бөліктерін байланыстырып, өзіне тән ілмектер құрайлы. Бұл кезде құрамында S атомы бар аминқышқылы - цистеиннің радикалдарының арасында байланыс түзіледі. Бұл әлсіз байланыс, бірақ молекулалардың тағы да бүктеліп шумақталуының нәтижесінде беріктігі арта түседі. Мұны нәруыз молекуласының үшінші реттік құрылымы дейді.
Нәруыздың төртінші реттік құрылымы
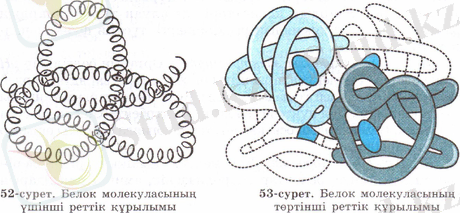
Кейбір нәруыздардың ерекше құрылымы болады. Олар бір-бірімен байланысқан бірнеше пептидтерден құралады. Құрылысы жағынан жақын бірнеше нәруыздың үшінші реттік құрылымының шумақ түзіп орналасуын нәруыз молекуласының төртінші реттік құрылымы дейді. Төртінші реттік құрылым- бірнеше нәруыз молекулаларының қосындысы, мысалы, гемоглобин нәруызы төрт шумақтан тұрады. Олар иондық, сутектік байланыстарме, байланысады. Осы төотінші реттік құрылыммен жаңа қасиет нәруыз қызметінің реттелуі пайда болады. Төртінші реттік құрылыммен реттелу процестерінің құпиясын ашқан - француз ғалымы, Нобель сыйлағының лауреаты- Жак Моно (1961 ж) . Төртінші реттік құрылымда субстратқа ұқсамайтын заттар - реттегіштер болады.
Ақуыздардың жіктелуі
Ақуыздардың мынадай белгілеріне қарап жіктейді:
- күрделілік дәрежесіне (қарапайым және күрделі), қарапайым протеиндер тек қана аминқышқылдары қалдықтарынан тұрады, күрделі протеидтер құрамына ақуызды заттардан басқа қосылыстардың қалдықтары кіреді;
- молекула пішініне (шар тәрізді және жіп тәрізді) ;
- кейбір еріткіштерде еру қабілетіне қарай (суда еритіндер, әлсіз түз ерітінділерінде еритіндер - альбуминдер, спиртте еритіндер - проламиндер, сұйытылған қышқыл және сілті ерітінділерінде еритіндер глутелиндер) ;
- атқаратын қызметтеріне қарай (мысалы, корға жиналатын ақуыздар, тірек қызметін атқаратын ақуыздар) .
Ақуыздың қызметі
Нәруыз жасуша тіршілігіне аса маңызды қызметтер атқарады.
Өршіткі қызметін атқаратын нәруыздар
Өршіткі қызметін атқаратын нәруыздар организмдегі химиялық реакцияларды жүзеге асырады. Ферменттің катализдік белсенділігі өте жоғары болады. Олар реакцияның жүруін ондаған, жүздеген мың есе тездетеді. Мысалы, қарын сөлінен бөлінетін пепсин ферменті нәруыздарды протеидтерге дейін гидролиздейді.
Тасымалдау
Нәруыздардың келесі маңызды қызметі - тасымалдау . Нәруыздардың бұл тобы әртүрлі маңызды заттарды жасуша ішінде және бүкіл организм бойынша бір жерден екінші жерге тасымалдау қызметін жүзеге асырады. Мысалы, қан нәруызы гемоглобин оттекті қосып алып, оны дененің бүкіл ұлпалары мен мүшелеріне таратады. Ал Альбумин жасушаның энергетикалық шикізаты- май қышқылын тасымалдайды.
Қозғалыс қызметін атқаратын нәруыздар
Бұлшықеттің маңызды нәруыздары - актин және миозин. Нәруыздардың бұл тобы жасуша мен организмдегі түрлі қозғалыс процестерін жүзеге асырады. Мысалы, хромосоманың, талшықтардың қозғалуы.
Нәруыздардың жабынды тіректік және құрылыстық қызметі
Бұл топқа көптеген нәруыздар жатады. Мысалға, тасбақа сауыты, құс тұмсығы, тырнақ, шаш, тері, ішек пен қантамырларлың қабырғасы осы нәруыздардан құралған. Құрылымдық нәруыздар - микрофибрилдер де осы топқа жатады.
Қорғаныштық қызмет атқаратын нәруыздар
Қорғаныштық қызмет атқаратын нәруыздарға, мысалы, денеге түскен бөгде заттарды зарарсыздандыратын антиденелер- Иммуноглобулиндер жатады. Фибриноген нәруызы қан ұюына қатысады. Бұл жарақаттанғанда қан кетуден сақтайды.
Қабылдағыш қызмет атқаратын нәруыздар
Қабылдағыш қызмет атқаратын нәруыздар әртүрлі сигналдарды қабылдап, оларды өңдеуде үлкен рөл атқарады. Мысалы, родопсин нәруызы жарық сигналдарын қабылдап алып таратады. Тілде болатын әртүрлі қабылдағыштар заттардың дәмін анықтайды.
Коректік заттармен қамтамасыз ететін нәруыздар
Организмді коректік заттармен қамтамасыз ететін нәруыздар , мысалы, сүт нәруызы - казеин жасушада аминқышқылына дейін ыдырайды. 1г нәруыз толық ыдырағанда 17, 6 кДЖ энергия бөлінеді.
2. 3 Липидтер - (гр. λίπος , lípos - май) - барлық тірі жасушалардың құрамына кіретін және тіршілік процестерінде маңызды рөл атқаратын май тәрізді заттар. Липидтер - табиғи заттар тобы. Олар іс жүзінде суда ерімейді, бірақ полярсыз еріткіштерде (хлороформ, эфир, этанол) ериді. Липид гректің lipos - май деген сөзінен шыққан. Липидтер молекуласында полярсыз (көмірсутекті) және полярлы (-СООН, -ОН, -NH2) аймақтар болады. Липидтер химиялық құрамы мен құрылымы жөнінде үш топқа бөлінеді: қарапайым липидтер, күрделі липидтер, стероидтар.
Қарапайым липидтерге май қышқылдары мен спирттердің күрделі эфирлері жатады. Бұл топты триацилглицеролдар мен балауыздар құрайды. Триацилглицерол - бұл үш атомды спирт глицерол мен май қышқылының үш молекуласынан құралған күрделі эфир.
Күрделі липидтерге фосфолипидтер жатады. Фосфолипид биологиялық мембрананың негізгі құрамдас бөлігі болып саналады. Барлық жасуша мембранасы құрамына фосфодиацилглицерин кіреді. Ол күрделі эфир, молекуласы глицерин қалдығынан, май қышқылының екі қалдығынан, фосфор қышқылының қалдығынан және азотты негіздерден тұрады.
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz