Этил спиртін өндіру цехының технологиялық жобасы


Этил спиртін өндіру цехын жобалау
тақырыбы
ДИПЛОМДЫҚ ЖҰМЫС
мамандығы: 0816000 «Химиялық технология және өндіріс»
Ақтау қаласы, 2023 жыл
МАЗМҰНЫ
І КІРІСПЕ
Қазіргі уақытта этил спирті өндіріс көлемі бойынша органикалық синтез өнімдері арасында алғашқы орындардың бірін алады. Ол еріткіш ретінде және әртүрлі синтездер үшін бастапқы қосылыс ретінде кеңінен қолданылады. Сондай-ақ, азық-түлік, медициналық және парфюмерия өнеркәсібінде, сондай-ақ ацетальдегид, хлороформ, сірке қышқылы, диэтил эфирін, синтетикалық каучукты, жасанды жібекті, түтінсіз оқ-дәріні және т. б., алу кезінде еріткіш, антифриз, жанғыш сұйық зымыран қозғалтқыштарының құрамдас бөлігі және негізгі органикалық синтездің жартылай өнімі ретінде кеңінен қолданылады. Соңғы уақытта мал шаруашылығы үшін жемшөп ашытқысын өндіруде микробиологиялық өнеркәсіпте этанолды тұтыну күрт өсті.
Әлемдік спирт өндірісі жылына шамамен 4 млн. тоннаны құрайды. Осыған байланысты этил спиртін өндіру ірі тонналы спирт санатына жатады, оны өндіру тәсілін таңдау кезінде ескеру қажет. Соңғысы экологиялық талаптарға сай және экономикалық тұрғыдан негізделген болуы керек. Этилен СН 2 =СН 2 , пропилен СН 2 =СН=СН 2 , бутилен СН 3 -СН 2 -СН=СН 2 , бутадиен (дивинил) СН 2 =СН-СН-СН 2 өте реактивті қосылыстар бола отырып, органикалық синтез саласында маңызды рөл атқарады. Олефиндер кіретін көптеген реакциялардың ішінде полимерлеу процестері (полиэтилен, полипропилен, полиизобутилен және т. б. ), гидраттау (спирттер), хлорлау (дихлорэтан, аллил хлориді және т. б. ), тотығу (этилен оксиді), оксосинтез және басқа да реакциялар тәжірибелік маңызды болып табылады. Олефинді көмірсутектерді гидраттау процестері кең таралған. Осындай әдіспен этил, изопропил және басқа спирттер алынады.
Қазіргі уақытта этил спирті өндіріс көлемі бойынша органикалық синтез өнімдері арасында алғашқы орындардың бірін алады. Ол еріткіш ретінде және әртүрлі синтездер үшін бастапқы қосылыс ретінде кеңінен қолданылады. Азық-түлік, медициналық және парфюмерия өнеркәсібінде, сондай-ақ еріткіш, антифриз, жанғыш сұйық зымыран қозғалтқыштарының құрамдас бөлігі және ацетальдегид, хлороформ, сірке қышқылы, диэтил эфирі, синтетикалық каучук, жасанды жібек, түтінсіз оқ-дәрі және т. б. алу кезінде негізгі органикалық синтездің жартылай өнімі ретінде кеңінен қолданылады
Этанол С 2 Н 5 ОН 78, 39 ⁰С температурада қайнайтын өзіне тән иісі мен күйдіргіш дәмі бар түссіз жеңіл қозғалатын сұйықтық болып табылады. Этил спирті судан жеңіл.
Барлық оттегі бар қосылыстар сияқты, этил спиртінің химиялық қасиеттері, ең алдымен, функционалды топтармен және белгілі бір дәрежеде радикалдың құрылымымен анықталады. Этанол - әдеттегі бір атомды алифатты спирт. Металдармен этилаттар түзеді, мысалы, С 2 Н 5 ОNa; бейорганикалық және органикалық қышқылдармен, галогенангидридтермен-күрделі эфирлер.
Этил спиртін келесі әдістердің бірімен алуға болады: азық-түлік шикізатын (астық, картоп және т. б. ) ашыту, сондай - ақ қант өндірісінің қалдықтары-меласса; өсімдік материалдарының гидролизі, сульфит сілтісін өңдеу, этиленді гидратациялау. Этил спиртін этиленді гидратациялау және ауылшаруашылық шикізаты мен оны қайта өңдеу өнімдерін ашыту арқылы алу өте маңызды.
Әрине, екі заттың ерітіндісінің қайнау температурасы-су (760 мм. сн. б. кезінде=100 °C) және этанол (760 мм. cн. б. кезінде tкип=78, 3 °C) жеке заттардың қайнау температурасы арасында болуы тиіс.
Қаныққан сулы-спиртті бу температурасының немесе осы екілік қоспаның қайнау (булану) температурасының Y буындағы спирт шоғырлануға тәуелділігі 1-кестеде келтірілген.
Бұл кестеде 96, 4 % шоғырлануы бар А нүктесі бар, температура 100 % этанолдың қайнау температурасынан да төмен екенін айта кету керек.
Реактор этиленді гидратациялауға арналған; құрылымдық жағынан, бұл қуыс тік аппаратты білдіреді. Реактор ішкі диаметрі 1260 мм цилиндрлік соғылған корпустан және оған дәнекерленген екі сфералық түбінен тұрады. Аппараттың жалпы биіктігі 10600 мм. Корпус, түбі және люктері болаттан жасалған. Аппараттағы температура 310 °С дейін, қысым 80 кгс/см 2 дейін рұқсат етіледі. Реактор жылу оқшауланған.
Фосфор қышқылының катализаторы реакторға салынады, ол қышқыл коррозиялық орта жасайды. Коррозиядан қорғау үшін құрылғы оның ішкі бетін толығымен жабатын мыс парақтармен қапталған. Мыс қаптаманы реактордың ішкі қабырғаларына дәнекерлеу арқылы сақиналы белдіктермен іліп қояды. Белдіктер арасындағы кеңістік мұқият саңылаусыздандырылған. Мыс қаптаманы пайдаланылған катализаторды түсіру кезінде тайып кетпейтіндей есеппен бекітеді. Жұмыс ортасының әсерінен қаптама сынғыш болады және оның бұл күйдегі саңылаусыздығы оңай бұзылуы мүмкін. Сондықтан катализатордың әр жүрісінен кейін қаптама мұқият тексеріліп, жарықтар болған кезде ақаулы жерлер ауыстырылады.
Реакторда екі люк бар (жоғарғы жағы катализаторды жүктеуге және бастапқы бу-газ қоспасының кіруіне, ал төменгі жағы катализаторды түсіруге және өнімнің шығуына арналған), термобуға арналған үш штуцер (жалғастық) және сақтандырғыш клапан арқылы апаттық қысымды түсіру үшін жоғарғы бөлігіндегі штуцер (жалғастық) .
Катализаторды жүктеу келесі тәртіппен жүзеге асырылады. Реактордың төменгі люгіне бейтараптандыру үштігін орнатады, сонымен қатар, төменгі люк пен үштіктің ернемегі арасында саңылаулары бар мыс парағының конусын жоғарғы жағымен орнатады. Конустағы саңылаулардың саны олардың жиынтық ауданы реактордың шығуындағы құбырдың қимасынан аз болатындай етіп жасалады. Жоғарғы люк арқылы конустың жоғарғы жағына 0, 4 м 3 Рашиг сақиналары, 0, 5-1 м 3 қышқыл сіңірілмеген тасымалдаушы және 9-10 м 3 катализатор салынады. Катализатор тиеу орнына 1 м 3 катализатор сиятын бункерлерде жеткізіледі. Бункер катализатор бөлімінен гидратация бөліміне жүк тиегіштермен жеткізіледі. Әрі қарай, арбадағы бункер монтаждық саңылауға жылжытылады, ол жерден жоғарғы қабатқа пневможүк көтергішпен көтеріледі. Катализаторды төменгі люк арқылы, өз бетімен бункерге түсіреді.
Реакторды пайдалану кезінде оның құрылымдық ерекшеліктерін ескеру қажет. Мысалы, қаптаманың ісінуіне жол бермеу үшін қысымды күрт төмендетуге болмайды. Будың конденсациясын және реактор қабырғаларының коррозиясын болдырмау үшін айналым, газ және бу арасындағы берілген қатынасты сақтау қажет.
Ректификациялық (тазарту) баған су-спирт конденсатын ректификациялауға (тазартуға) арналған. Бұл 50 торлы табақшасы бар цилиндрлік аппарат. Бағанада аппаратты ішкі қарауға және табақшаларды тазалауға арналған 4 люк бар. Әдетте толық бөліктің табақтары ластанады; оларды мезгіл-мезгіл тазартады. Табақ - өлшемі 150х4 мм параллель кертіктері бар металл дискті білдіреді. Табақтың төккіш стақандары жоқ; ол қаңқаның арқалықтарына қарнақ пен бұрандамалармен бекітілген жеке парақтардан тұрады. Табақтар екі көрші табақшаның кертіктері бір-біріне перпендикуляр болатындай етіп орнатылады. Қуат табағы - бұл будың өтуіне арналған үлкен тесіктері бар және сұйықтықты төгуге арналған кішкене тесіктері бар диск; тесіктер бүкіл табаққа біркелкі орналастырылған. Қуат табақшалары шикізатты қабылдау кезінде және флегманы қабылдау кезінде орнатылады. Баған қазандықтан бу шығаруға, буды дефлегматорға шығаруға, флегма мен қуат қабылдауға, текше өнімін шығаруға, текшедегі деңгей реттегішін қосуға арналған штуцермен, қысым мен температура импульстарын таңдауға арналған дөңесшемен жабдықталған.
Этанол синтезінің технологиялық сұлбалары бу, процестің бір сатылы, спирттің жоғары шығымдылығымен ерекшеленеді. Ең жетілдірілген схемаларда синтездеуге арналған су буы этанолды бөліп алғаннан кейін суды қайта өңдеу және су конденсатын қолдану арқылы алынады.
Жаңа және кері этилен компрессорларда 1, 2-ден 8 МПа-ға дейін сығылады, су буымен араластырылады, 4 жылу алмастырғышта реактордан шығатын қоспаның жылумен қыздырылады және 3 құбырлы пеште 275 °С-қа дейін қыздырылады, содан кейін 5 реактор - гидрататорға беріледі. Реакторға кірер алдында катализаторды қуаттандыру үшін фосфор қышқылы ағынға енгізіледі, бұл оның қызмет ету мерзімін ұзартады.
Реактор - бұл биіктігі және диаметрі 1, 5 м қуыс баған, ол керемет ығысу режимінде жұмыс істейді. Фосфор қышқылынан коррозияның әсерін болдырмау үшін ол қызыл мыс парақтарымен қапталған.
Реакциялық газдарда натрий гидроксидімен бейтараптандырылатын шығарылған фосфор қышқылының буы болады, ал түзілген тұздар 6 тұз бөлгіште шығарылады. Фосфор қышқылының шығарылуы 1 м З катализатордан 0, 4-0, 5 т/сағ құрайды.
Бөлінетін реакциялық газдардың жылуы кіретін қоспаны қыздыру үшін 4 жылу алмастырғышта қалпына келтіріледі. 7 тоңазытқышта реакция өнімдерінің конденсациясы жүреді, ал 8 сепараторда сұйық және газ ағындары бөлінеді. Су аз ұшпа компонент ретінде көп мөлшерде жиналады. Сондықтан спиртті қосымша бөлу үшін оны 9 абсорберде сумен жуу жүргізіледі. Құрамында 90-92 % этилен бар реакцияланбаған газ 2 компрессормен қайта өңделеді, ал жүйеде қоспалардың жиналуын болдырмас үшін оның бір бөлігі тасталады. Үрлеу енгізілген этиленнің шамамен 20 % -ын құрайды және этиленді бөлу үшін газ бөлу қондырғысына жіберіледі.
8 сепаратордан кейін су конденсаты және 9 абсорберден алынған сұйықтық дроссельденеді (қысымды босатады), нәтижесінде 10 төмен қысымды сепараторда бөлінетін және отын желісіне жіберілетін ерітілген газдар шығады.
10 сепаратордан алынған сұйық фаза құрамында диэтилді эфир, ацетальдегид және этиленнің төмен молекулалы полимерлерінің қоспалары бар этанолдың 15 % сулы ерітіндісі болып табылады. Бұл ерітінді 11 және 12 ректификациялық (тазарту) бағандарда тазартылады. Біріншісінде ең ұшпа диэтил эфирі мен ацетальдегид, ал екіншісінде - құрамында 95 % этанол мен 5 % су бар азеотропты қоспа түріндегі этил спирті шығарылады. Бағанды жылыту өткір бумен жүзеге асырылады. 12 бағананың текшесінде су қалады, оны 13 ион алмасу қондырғысында тұздан тазартады және технологиялық су бойынша тұйық цикл ұйымдастыра отырып, гидратацияға қайтарады. Бұл таза су шығынын едәуір азайтуға, ағынды суларға ағызуды болдырмауға және этанол шығынын азайтуға мүмкіндік береді.
Экономика. Өндіріс процесін жүзеге асыру үшін жұмыс күшін өндіріс құралдарымен біріктіру қажет. Өндіріс құралдары - бұл экономикалық мазмұндағы екі түрлі бөліктің жиынтығы: еңбек заттары және еңбек құралдары.
Химия өнеркәсібіндегі еңбек заттары - бұл материалдар мен жартылай өнімдер, электр энергиясы, жанармай, пластикалық массалардан немесе резеңке массадан бөлшектерді дайындау үшін қажетті қалыптар және пресс құралы, реактивтер, зертханалық ыдыстар және т. б.
Еңбек құралдары - бұл машиналар, аппараттар, құбырлар және масса өткізгіштер, желдеткіш құрылғылар, көлік құралдары мен құрылғылар, сондай - ақ пресс - қалыптар және ұзақ пайдаланылатын өзге де құралдар (бір жылдан астам) .
Этанол өндірісінде атмосфераны ластайтын зиянды заттар шығарылады. Диэтилсульфат, этилсульфат, диэтил эфирі, фосфор эфирлері және басқа ұшпа заттар сияқты.
Сондықтан қалдық газдарды тазарту қажет. Ауа бассейнін зиянды заттармен ластану түріндегі теріс антропогендік әсерден қорғау үшін келесі шаралар қолданылады: технологиялық процестерді экологияландыру; газ шығарындыларын зиянды қоспалардан тазарту; атмосферадағы газ шығарындыларының таралуы; санитарлық-қорғау аймақтарын, сәулет-жоспарлау шешімдерін және т. б. орнату.
Этил спирті азық-түлік, химия өнеркәсібінде, парфюмерия мен медицинада қолданылады, сондықтан алынған спирттің біздің еліміздің МЕМСТ-қа сәйкестігін бақылау қажет. Қазір көптеген елдерде халықтың алкогольді тұтынуы өте қиын жағдай. Біздің азық-түлік өнеркәсібімізге спирттің сапасын, жерасты өндірісін және спирттік ішімдіктерді заңсыз сатуды бақылау қажет. Осылайша, өлім-жітімді азайтуға болады және алкогольді ішу қауіпсіз болады.
2 НЕГІЗГІ БӨЛІМ
2. 1 Этанолдың физикалық және химиялық қасиеттері

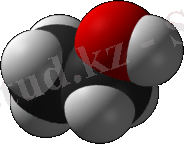
Сурет 1. Этанолдың құрылымы
Кесте 1
Этанолдың қасиеттерінің сипатталуы
Кесте 2
Әр түрлі температурадағы этанолдың тығыздығы
Кесте 3
20 °C кезінде этанолдың сулы ерітінділерінің тығыздығы
Кесте 4
20 °C кезінде этанолдың сулы ерітінділерінің сыну көрсеткіші
Кесте 5
Этанолдың беттік керілуі
Кесте 6
Атмосферадан төмен қысым кезінде этанолдың қайнау температурасы
95, 57 % этанол + 4, 43 % су қоспасы азеотропты болып табылады, яғни айырып шығару кезінде бөлінбейді.
Этил спирті мен су қоспасының қату температурасының қоспадағы спирт концентрациясына тәуелділігі келесі кестеде келтірілген [2] .
Кесте 7
Этил спирті мен су қоспасының қату температурасының қоспадағы спирт концентрациясына тәуелділігі
мас. %
г/см³
айн. %
°C
Этил спирті сумен, спиртпен, диэтилді эфирмен, глицеринмен, хлороформмен, ацетальдегидпен, бензинмен және т. б., барлық қатынаста араласады. Ауамен 3-20 % (айн. ) концентрация шегінде жарылыс қаупі бар қоспалар түзеді. Азеотропты қоспаларды түзеді: сумен құрамында 95, 6 % спирт бар және 78, 1 °C қайнаған азеотропты қоспаны береді (мұндай ректификат түрінде этанол әдетте техникада қолданылады) ; бензолмен (32, 4 %; 68, 24 °C) ; гексанмен (21 %; 58, 7 °C) ; этилацетатпен (30, 8 %; 71, 8 °C) .
Этил спирті бозғылт көк жалынмен жанады. Судағы будың ерігіштік коэффициенті 1412 (40 °C кезінде) ; адам қанында 1370-1580 (37 °C Cкезінде) . МЕМСТ 8314-57 сәйкес ағаштан (гидролизбен) алынған спирттегі қоспалардың құрамы күрт шектелген. МЕМСТ 9674-61 синтетикалық этил спиртіне.
Тұтану температурасы 13 °C, өздігінен тұтану температурасы 404 °C, жарылу шегі: температуралық шегі 11 41С, концентрация шегі 3, 6 19 % (айн. ) . Атмосфералық ауадағы ШРК 5 мг/м 3 ; Жұмыс аймағының ауасындағы ШРК 1000 мг/м 3 .
Ағзаға әсер етудің жалпы сипаты: алдымен қозуды, содан кейін орталық жүйке жүйесінің сал ауруын тудыратын есірткі. Жеті сағаттық жұмыс күні ішінде өндірістік үй-жайларда (ішке қабылдаусыз) этил спиртінің буымен қатты улану іс жүзінде мүмкін емес [3] .
Химиялық қасиеттері. Барлық оттегі бар қосылыстар сияқты, этил спиртінің химиялық қасиеттері, ең алдымен, функционалды топтармен және белгілі бір дәрежеде радикалдың құрылымымен анықталады.
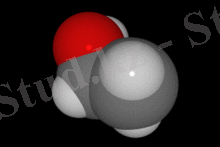
Сурет 2. Этанол молекуласының үш өлшемді бейнесі
Этилаттар (немесе жалпы жағдайда - алкоголь) және сутегі түзе отырып, сілтілік металдармен әрекеттеседі.
2C 2 H 5 OH + 2К = 2С 2 Н 5 ОК + Н 2 .
Күрделі эфир түзе отырып, карбон қышқылдарымен әрекеттеседі:
RCOOH + HOCH 2 CH 3 → RCOOCH 2 CH 3 + H 2 O
Диэтилді эфир түзе отырып, күкірт қышқылының қатысуымен (120 °C кезінде) дегидратация реакциясына түседі:
2CH 3 CH 2 OH → CH 3 CH 2 OCH 2 CH 3 + H 2 O
Ауада және оттегіде жылу бөле отырып жанады:
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz