Химиялық реакция жылдамдығының температураға әсері: активтену энергиясы мен активтену энтропиясын анықтау әдістері


ЖОСПАР:
- Кіріспе
- Негізгі бөлім
- Активтену энергиясы және активтену энтропиясы
- Химиялық реакцияның жылдамдығына температураның әсері
- Пайланылған әдебиеттер
ТАҚЫРЫБЫ: Химиялық реакцияның жылдамдығына температураның әсері. Активтену энергиясы анықталатын әдістері.
Химиялық реакциялардың жүру заңдылықтарын зерттеу химияның негiзгi мәселесi. Бiр заттар басқа бiр заттарға айналу кезiнде оларды құрайтын атомдардың электрондық орбитальдары қайтадан топтасқандықтан екi байланыстар үзiлiп жаға байланыстар түзiлiп отырады.
Раекцияның жүру механизмiн, жылдамдығын және сол жылдамдықта әрекеттесетiн заттардың концентрацияларының, температураның, қысымның, катализатордың әсерлерiн зерттейтiн химияның бөлiмiн химиялық кинетика дейдi.
Әр түрлi реакциялар әр түрлi жылдамдықпен жүредi. Кейбiр реакциялар өте жай жүредi, ал басқа бiреулерi өте тез қопарылыс бере жүредi. Бiр реакцияның өзi жағдайларға байланысты әр түрлi жылдамдықпен жүредi. Сөйтiп, химиялық реакцияның жылдамдығын кесiмдi уақыт iшiнде реакцияласушы заттардың концентрациясының өзгеруiмен өлшейдi.
Активтену энергиясы және активтену энтропиясы
Химиялық реакциялардың жүруіне және жылдамдығын арттыруға активтену энергиясы мен активтену энтропиясының маңызы зор.
 Активтену энергиясы әрекеттесетін молекулаларды актив күйге келтіру үшін жұмсалады. Активтену энергиясы әрекеттесетін молекулалардағы атомдардың арасындағы ескі байланыстардың үзілуі үшін, реакцияның нәтижесінде алынған заттар атомдарының арасында жаңа байланыстар түзілу үшін қажет.
Активтену энергиясы әрекеттесетін молекулаларды актив күйге келтіру үшін жұмсалады. Активтену энергиясы әрекеттесетін молекулалардағы атомдардың арасындағы ескі байланыстардың үзілуі үшін, реакцияның нәтижесінде алынған заттар атомдарының арасында жаңа байланыстар түзілу үшін қажет.
Аралық қосылыс теориясы бойынша әрекеттесетін заттардың молекулалары активтену энергиясын сіңіріп алып аралық қосылыс немесе активтелген комплекс түзеді. Активтелген комплексте ескі байланыстар әлсіреген жаңа байланыстар түзіле бастаған күйде балады. Бұл күйде активтелген комплекс өте аз уақыт болады да, сіңірген энергиясының біразын бөліп шығарып жаңа заттарға айналады. Мысал ретінде сутегі мен иодтан иодсутек молекуласының түзілу схемесын келтіруге болады:
Н І Н - - І Н - І
+ → ¦ →
Н І Н - І Н - І
Бастапқы заттар Активтелген комплекс Түзілген заттар
Бұл реакцияда әрекеттесетін сутегі және иод молекулалары активтену энергиясын сіңіріп алып, түрақсыз активтелген комплекске айналады. Мұндағы ескі байланыстардың әлсірегені, жаңа байланыстардың түзіле бастағаны пунктирлі сызықтармен көрсетілген.
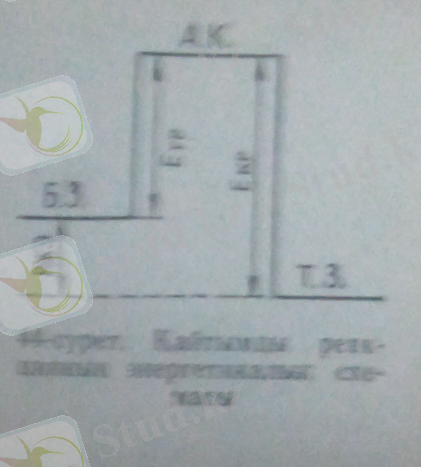
Активтелген комплекс (АК) тура реакция жүргенде де, кері реакция жүргенде түзіледі(44 - сурет) . Энергия жағынан бастапқы заттармен(Б, З) салыстарғанда активтелген комплекстің (АК) энергиясы тура реакцияны активтеуге кеткен энергияға (Е тр) артық болады, түзілген заттармен (ТЗ) салыстырғанда кері реакцияны активтеуге жұмсалған энергияға (Екр) артық болады. Тура реакция мен кері реакцияны активтеуге кеткен энергиялардың айырмасы осы реакцияның жылу эффектісіне (РЖЭ) тең болады.
Активтену энтропиясы әрекеттесетін молекулалардың бір - бірімен соқтығысар кезінде қолайлы бағытталуларының сандық мөлшерін көрсетеді. Жүйедегі әрекеттесетін заттар молекулаларының өзара қолайлы бағытталулары неғұрлым көп болса, активтендіру энтропиясының сандық мәні де соғұрлым жоғары болады, яғни реакция жылдам жүреді. Активтендіру энтропиясы ΔS акт. жүйедегі қолайлы бағытталулар санын жалпы бағытталулар санына бөлгенге тең:
Химиялық реакцияның жылдамдығына температураның әсері
Температураның жоғарлауына байланысты химиялық реакцияның жылдамдығы өте көп артады. Реакция жылдамдығына температураның әсерiн жуық мөлшерiн Я. Вант-Гофф ережесi анықтайды:
Температураны 10º -қа өсiргенде реакция жылдамдығы 2-4 есе артады .
Бұл заңның математикалық өрнегi:
Мұндағы 𝜗 1 және 𝜗 2 сәйкес t 1 және t 2 температураларындағы реакция жылдамдықтары, 𝛾 - температуралық коэффициент. Температуралық коэффициент тәжірибе жүзінде анықталады және оның мәні 2, 3, 4 болуы мүмкін.
Мысалы, реакцияның температуралық коэффициентi 2-ге тең болып температураны 100º арттырғанда реакция жылдамдығы 1024 есе артады.
Температураның жоғарлауына байланысты реакция жылдамдығының артуын әрекеттесетін заттар молекулаларының жиі соқтығусыларынан болады деп жорамалдауға болар еді. Бірақ есептеулер температураны 100º арттырғанда молекулалар арасындағы соқтығысу 1, 07 есе ғана артатынын, ал реакция жылдамдығы 1000 есеге жуық артатыны көрсетеді. Температураны арттырудың нәтижесінде әрекеттесетін молекулалардың соқтығысуының жиілеуі реакция жылдамдығын арттыруға аздап әсер етеді, бірақ шешуші фактор бола алмайды.
Температураның жоғарлауына байланыста реакция жылдамдығының артуына активтену энергиясы үлкен әсер етеді.
Химиялық реакциялардың жылдамдығына температураның әсерін швед ғалымы С. Аррениустың теңдеуі толығырақ және дәлдірек түсіндіреді.
Мұндағы Е а - активтену энергиясы, ΔS а - активтену энтропиясы, К - жылдамдық константасы немесе әрекеттесуші заттар концентрациялары 1 тең болғандағы реакция жылдамдығы; Z - жалпы саны, R - универсал газ тұрақтысы, Т - абсолютті температура, е - натурал логарифмнің негізі.
Бұл теңдеу жылдамдық константасының мәніне (реакция жылдамдығына) бөлшектердің соқтығусыларының жалпы саны, әсіресе, активтену энергиясы, активтену энтропиясы әсер ететінін көрсетеді. Мұнда температура дәреже көрсеткішінің құрамына кіретіндіктен температураның өзгеруі реакция жылдамдығына күшті әсер етеді.
Түрліше реакциялардың әр түрлі жылдамдықпен жүруі олардың табиғатына байланысты. Реакцияға қатысатын заттардың табиғаты олардың активтену энергиясы (Е а ) мен активтену энтропиясына (ΔS а ) байланысты болады.
Реакцияға қатысатын заттардың қолайлы бағытталуы неғұрлым көп болса, олардың активтену энтропиясыда (ΔSа) көп болады, соған сәйкес реакция жылдамдығыда артады.
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz