Этанол-су бинарлы қоспасын ректификациялау: тарелкалы колоннаның есептеу және жобалануы


Жоспар
Кіріспе . . . 3
1. Процесс сипаттамасы . . . 4
2. Бастапқы қоспа және алынған өнімнің сипаттамасы . . . 6
3. Аппараттың конструктивті материалын таңдау . . . 8
4. Негізгі аппаратты есептеу . . . 9
5. Қосымша аппаратты есептеу . . . 22
6. Негізгі және қосалқы аппараттарды таңдау . . . 26
Қорытынды . . . 29
Пайдаланылған әдебиеттер
Кіріспе
Өнеркәсіптің химиялық, мұнай‑химиялық, фармацевтикалық, тағам және басқа да салаларында екі немесе одан да көп сұйық қоспаларын жеке құрамдарға бөлу қажеттігі жиі туындайды. Ерекше мысалға мұнай өнімдерінің әртүрлі ұшпалық қасиеттері бар жеке фракцияларға бөлінуі жатады.
Бөліну процесі мынаған негізделген: қоспалар құрайтын барлық сұйықтарда әртүрлі ұшпалық қасиет болады, басқаша айтқанда - бірдей қысымда әртүрлі қайнау температурасы болады. Сұйықтардың осындай қасиетінің салдары болып сұйық қоспа үстіндегі бу компоненттері мөлшерінің әртүрлі болуы табылады. Қоспа үстіндегі бу - көбірек ұшқыш компоненттердің жалпыланған булары. Егер осындай булар қоспасын сұйық фазадан бөліп алса және толық конденсацияласа, онда алынған конденсаттың құрамы будың құрамындай болады. Демек, алынған жаңа сұйық қоспа бастапқыға қарағанда жоғары дәрежеде байытылған өте ұшқыш компонент болады.
Мұндай бөлу үшін ректификациялық колонна деп аталатын аппараттарда iске асатын ректификацияпроцесі кең қолданылады.
Ректификация - бу қоспасы мен сұйық қоспасының әрекеттесуі нәтижесінде біртекті сұйық қоспаларының құрайтын заттарға немесе құрайтын заттар топтарына бөлінуі.
Бұл курстық жобада этанол - су бинарлы қосылысты ректификация процесі арқылы бөлу қарастырылады. Сонымен қатар үздіксіз әрекетті ректификациялық колонна есептеліп, жобаланады.
Курстық жұмыстың мақсаты - этил спиртін этанол-су қоспасынан бөліп алу, ректификациялық қондырғының оптималды режимін таңдау, материалдық ағынды есептеу болып табылады.
- ПРОЦЕСС СИПАТТАМАСЫ
Ректификация процесі - қайнау температурамен ажыратылатын, яғни еритін компоненттегі сұйық қоспалардың бөлінуімен сипатталатын диффузиялық процесс болып табылады. Ректификация сұйықтардың біртіндеп булануы мен булардың конденсациялануының көп сатылы процесі түрінде болады. Аталған процесті бірнеше рет қатарынан сұйық және бу фазасының контактіленуі арқылы жүзеге асырылады. Егер бастапқы қоспа қайнау температуралары әр түрлі екі компоненттерден құралатын болса, онда төмен температурада қайнайтын компонент буға айналады, ал жоғары температурада қайнайтын компонент сұйық күйінде қалады. Пайда болған бу конденсацияланады. Алынған сұйықтық дистиллят деп аталады. Буланбай қалған сұйықтық қалдық деп аталады. Айдау нәтижесінде төмен температурада қайнайтын компонент дистиллятқа, ал жоғары температурада қайнайтын компонент қалдыққа өтеді. Бұл процесті жай айдау деп атайды. Жай айдауда қоспаны компоненттерге толық бөліп, таза күйінде алу мүмкін емес.
Алғашқыда қарастырылған сұйық пен бу фазалары тепе - теңдік күйінде болмайды, бірақ та фазалар өзара бүкіл процесс бойымен жүргенде осы күйге келуге тырысады. Сонымен қатар әрбір фазада температура мен қысым бірте - бірте бірқалыпты күйге келіп отырады да, олардың арасында компоненттері де өз ретімен орын ауыстырып қалыпқа келеді. Осы бу мен сұйық фазасының контактісі, яғни тепе - теңдік күйге келген жүйесі - идеалды немесе теориялық, ал бұл контактты жүзеге асыратын қондырғы - теоретикалық тәрелке деп аталады.
Сондай-ақ бұл процесс - көп жағдайда абсорбция процесінде де қолданылатын контактілі элементтері (насадка, тәрелке) бар коллонналы аппараттарда жүзеге асырылады. Абсорбция процесімен ұқсастық белгілері бар болғанмен ректификация өзіндік жақтарымен (коллонаның үстіңгі және астыңғы бөлігінде сұйық пен бу фазасындағы әртүрлі жүктіліктің арақатынастарымен, биіктігі бойынша анықталу коэффициентінің түрленуімен сонымен бірге масса және жылу процестерінің жүруімен ) ерекшеленеді.
Біртекті сұйық қоспаларды компоненттерге толық бөлу ректификация процесімен атқарылады.
Ректификация процесін қарапайым көп сатылы қондырғыда өткізуге болады: I-сатыда бастапқы қоспа буланады; II-сатыға I-сатыда қалған сұйық беріліп буланады; III-сатыға II-сатыда қалған сұйық беріледі және т. с. с.
Сұйық қоспаларын ықшамды ректификациялық колонналарда толық ажырату экономикалық тиімді.
Ректификация процесі мерзімді және үздіксіз әрекетті қондырғыларда әр түрлі қысымда (атмосфералық, вакуумда және атмосфералық қысымнан жоғары) өткізіледі.
Жоғары температурада қайнайтын қоспаларды вакуумда, ал қалыпты температурада газ күйінде болатын қоспаларды жоғары қысымда ажыратады.
Ректификация процесінің 2 түрі бар: экстрактивті ректификация және азеотропты ректификация.
Қайнау температуралары бір-біріне жақын компоненттерден құралған қоспаларды бөлу - экстрактивті ректификация деп аталады. Ал, бөлінетін азеотропты қоспаға үшінші компонентті қосу арқылы бөлу - азеотропты ректификация деп аталады.
Ректификациялық қондырғыларда негізінен 3 түрлі аппараттар қолданылады: табақшалы, насадкалы және қабықшалы.
Табақшалы-үлкен өнімділікті және бу мен сұйық көлемдерін үлкен аралықта өзгертетін қондырғылар.
Насадкалы-аппараттағы қысымдар айырмасы аз болғанда және үлкен мөлшерде сұйықтың ұсталып қалуы қажет болғанда қолданылады.
Қабықшалы-ысытқанда термиялық беріктігі аз қоспаларды вакуумда ректификациялау үшін қолданылады.
2. Бастапқы қоспа мен алынған өнім сипаттамасы
Этил спирті (этанол) - өзіне тән иісі бар түссіз сұйықтық. Қайнау температурасы - 78, 3°С. Сумен барлық мөлшерде араласады. Егер спирттің құрамында 4-4, 5% су болса, оны ректификат, ал сусыз спиртті абсолютті спирт деп атайды. Сусыз спиртті су тартқыш заттар (СаО, СuSO 4 ) қосып қайнатып алады. Соның бірі - глюкозадан (жүзім қанты) ашытқы қатысында мына жалпы реакция бойынша алады:
С 6 Н 12 О 6 → 2С 2 Н 5 ОН + 2СО 2
Мұндай жолмен алынған спирт таза болады, тамақ өнеркәсібінде және медицинада пайдаланылады. Целлюлозаны гидролиздеп алынған спиртті гидролиз спирті деп атайды:
(С 6 Н 10 О 5 ) n + nH 2 O → nC 2 H 5 OH
Бұл әдіс өте тиімді, себебі тамақ өнімдері, картоп, бидай пайдаланбайды. Бірақ гидролиз спиртінде басқа қосымша өнімдер болады, соның бірі - этанол. Сондықтан мұндай спирт көбіне техникада қолданылады, тамақ өнімдері үшін пайдалануға болмайды. Синтездік жолмен этил спиртін этиленді гидратациялап алады. Этанол дәрі-дәрмек жасауда, зарарсыздандырғыш зат ретінде медицинада пайдаланылады. Этил спирті химия өнеркәсібінде сірке қышқылын, бояу, синтездік каучук, диэтил эфирін және т. б. заттар алуда қолданылады. Ең арзан еріткіштердің бірі. Этанол адам организміне есірткілік әсер етеді. Спирт миға әсер етіп, жүйке клеткаларын уландырады. Осыдан адамның ақыл-ойы, сөйлеу, ойлау қабілеттері, қимыл үйлесімділігі бұзылады.
Су - түссіз, иіссіз, дәмсіз сұйықтық. Массалық құрамы: Н -11, 19%, О - 88, 81%. Молекулалық массасы 18, 0153. Су планетамыздағы ең көп тараған заттардың бірі. Су - біршама инертті биологиялық еріткіш сұйықтық, онда көптеген органикалық және бейорганикалық заттар ериді, бірақ олардың ерігіштіктері әр түрлі.
Су табиғатта ең көп таралған зат: ол жер шарының ¾ бөлігін алады. Бу түріндегі су атмосферада көп. Таза су - түссіз және иіссіз сұйықтық. Судың қайнау температурасы 100 0 С, ал қату температурасы 0 0 С. +4 0 С кезіндегі судың тығыздығы 1г/мл, бұл оның ең жоғарғы мәні. Мұз судан жеңіл. Су - тұрақты зат. Оның сутекке және оттекке ыдырауы 1000 0 С-тан жоғары температурада жүреді. Су химиялық белсенді қосылысқа жатады. Судың тазалығының өлшемі оның қасиеттерінің тұрақтылығы мен электрөткізгіштігі болып саналады. Тек 35-40 рет вакуумда қайталап, айдағаннан кейін ғана судың қасиеттері өзгермейді. Су өте көп қолданылады. Сусыз тіршілік жоқ. Суды сутек алуда шикізат ретінде пайдаланады, органикалық синтезге қатысады, қатты отынды газдандыру үшін қолданылады. Су негізгі химиялық өнеркәсіптің (азот және күкірт қышқылдарының өндірісі және т. б. ) басты салаларында қолданылады.
- . Аппараттың конструктивті материалын таңдау
Химиялық технологияда машиналарды дайындауда қара металл және қорытпалары (болат, шойын) негізгі конструктивті материал ретінде қолданылады.
Этанол және су коррозиялық активті заттар болып саналмайды. Олардың колоннадағы жұмыс температурасы 100°С-тан аспайды, сондықтан аппараттың негізгі детальдарының конструктивті материалы ретінде болатты таңдаймыз, Ст 3 ГОСТ 380-94. Бұл 10-нан 200°С-қа дейін температурада агрессивті емес ортада жұмыс істейтін химиялық аппараттың жабдықтарын дайындау үшін қолданылады.
4. Негізгі аппаратты есептеу
Этанол-су бинарлы қоспасын бөлуге арналған ректификациялық колоннаны есептеу.
- Бастапқы қоспа үшін өнімділігі F = 6 кг/с.
- Жеңіл қайнайтын компоненттің құрамы ( % есебімен ) бастапқы қоспада xf= 34%; дистиллятта xp= 93%; кубтық қалдықта xw= 3, 2% .
- Суытатын судың бастапқы температурасы tб= 240С.
- Бастапқы қоспа қайнау температурасына дейін қаныққан су буымен р = 0, 25 МПа қыздырылады.
- Дефлегматордың су кеңістігіндегі қысым 0, 1 МПа.
- Ректификациялық колоннаның типі - тарелкалы деп таңдалды.
Материалдық баланс
Колоннаның өнімділігін дистиллят Р және кубтық қалдық W бойынша материалдық баланс теңдеуінен табамыз:
F = x p + x w (4. 1)
мұндағы: F - бастапқы қоспа өнімділігі, кг/с; x p - дистиллятта жеңіл қайнайтын компоненттің құрамы, кмоль/кмоль; x w - кубтық қалдықта жеңіл қайнайтын компоненттің құрамы, кмоль/кмоль.
6 = Р + W
6 ∙ 0, 34 = Р ∙ 0, 93 + W ∙ 0, 032
Осыдан табамыз:
W =
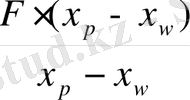 , (4. 2)
, (4. 2)
мұндағы: F - бастапқы қоспа өнімділігі, кг/с; x p - дистиллятта жеңіл қайнайтын компоненттің құрамы, кмоль/кмоль; x w - кубтық қалдықта жеңіл қайнайтын компоненттің құрамы, кмоль/кмоль; р - қысым, МПа
W =
= 3, 94 кг/с.
Р = F - W (4. 3)
мұндағы: Р - дистиллят, кмоль/кмоль; W - кубтық қалдық, кмоль/кмоль; F - бастапқы қоспа өнімділігі, кг/с.
Р = 6 - 3, 94 = 2, 06 кг/с.
Келесі есептеулерді жүргізу үшін бастапқы қоспа, дистиллят пен кубтық қалдық концентрациясын мольдік үлеспен анықтау керек:
X
F
=
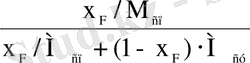 , (4. 4)
, (4. 4)
мұндағы: X F - бастапқы қоспада жеңіл қайнайтын компоненттің құрамы, кмоль/кмоль; М сп және М су - этил спирті және судың молекулалық массасы, кг/кмоль.
X
F
=
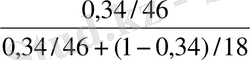 = 0, 168;
= 0, 168;
мұндағы: 46, 18 - этил спирті мен судың молекулалық массасы, кг/кмоль.
x
p
=
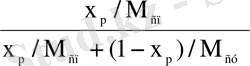 ,
,
мұндағы: x p - дистиллятта жеңіл қайнайтын компоненттің құрамы, кмоль/кмоль; М сп және М су - этил спирті және судың молекулалық массасы, кг/кмоль
x
p
=
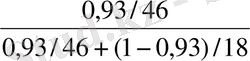 = 0, 83.
= 0, 83.
x
w
=
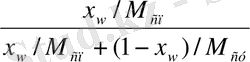 , (4. 5)
, (4. 5)
мұндағы: x w - кубтық қалдықта жеңіл қайнайтын компоненттің құрамы, кмоль/кмоль; М сп және М су - этил спирті және судың молекулалық массасы, кг/кмоль.
x
w
=
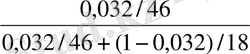 = 0, 013.
= 0, 013.
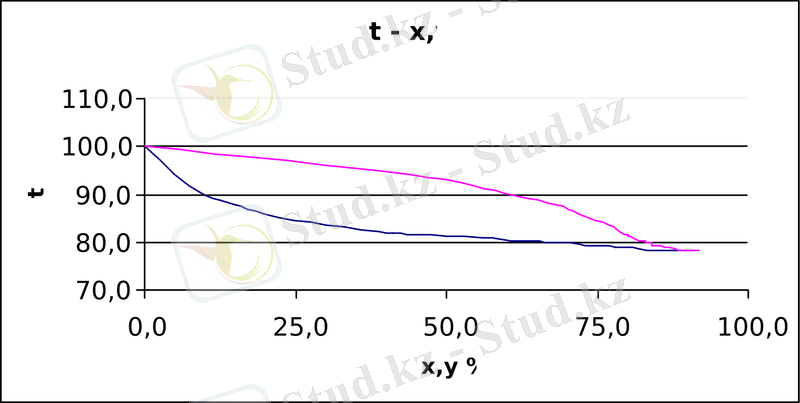
Анықтамадан алынған мәліметтер бойынша 0, 1 МПа сұйық пен будың тепе - теңдіктегі қайнау температуралары мен құрамы арқылы бинарлы қоспаның қайнау температурасының қисығы және х - у координатасында тепе - теңдік қисығын саламыз.
Диаграммадан (1) А нүктесін x w = у w = 0, 013 және С нүктесін x p = у p = 0, 83 координаталарымен салады, ал тепе - теңдік қисығында абцисса x F = 0, 168 В′ салады. С нүктесінен В′ нүктесі арқылы диаграмма ординатасына дейін сызықты жүргізеді. Ордината осінде қима шығады, ол өзара В max = 0, 435.
Яғни,
В max = x р / (R min + 1) (4. 6)
мұндағы: x p - дистиллятта жеңіл қайнайтын компоненттің құрамы, кмоль/кмоль.
R
min
=
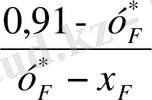 ; (4. 7)
; (4. 7)
мұндағы: R min - флегманың минималды саны; у ٭ F - тепе - теңдік күйде болатын будағы компоненттің концентрациясы; х F - бастапқы қоспада жеңіл қайнайтын компоненттің құрамы, кмоль/кмоль.
R
min
=
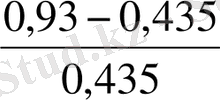 = 0, 91.
= 0, 91.
R = R min ∙β (4. 8)
мұндағы: R min - флегманың минималды саны; R - жұмысшы флегма саны; β - флегманың шығыс коэффициенті.
Флегманың минималды санын R min келесідей формула арқылы анықтаймыз:
R
min
=
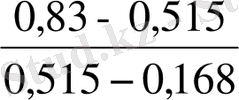 = 0, 91
= 0, 91
мұндағы у ٭ F = 0, 515 тең болады.
Флегманың шығыс коэффициенті β = 1, 7 деп қабылдаймыз.
Жұмысшы флегма саны
R = 1, 7 ∙ 0, 91 = 1, 547
Жылулық баланс
Жылулық балансты есептеу үшін бастапқы қоспаның кубтық қалдықпен дистилляттың қайнау температурасын анықтаймыз.
Қайнау температурасын анықтау үшін абцисса осінде кубтық қалдықтың x w = 0, 013, бастапқы қоспаның x F = 0, 168 және дистилляттың х р = 0, 83 құрамын енгіземіз. Алынған нүктелерден тігінен сызықты жүргіземіз. Қайнау температуралары қиылысу нүктелеріне сәйкес келеді. Бұл жағдайда кубтық қалдық үшін қайнау температурасы t w = 99 0 C, бастапқы қоспа үшін t F = 87 0 C, дистиллят үшін t p = 78 0 C.
Бастапқы қоспа, дистиллят және кубтық қалдықтың жылу сыйымдылықтары (этил спирті және су қоспасын беретін) келесідей формула бойынша анықталады:
С р = 3226, 3 ∙ х р + 4190 ∙ х w ; (4. 9)
мұндағы: С р - дистилляттың жылу сыйымдылығы, Дж / (кг∙ К) ; 3226, 3 - 78 0 С - ғы этил спиртінің жылу сыйымдылығы, Дж/(кг∙ К) ; x p - дистиллятта жеңіл қайнайтын компоненттің құрамы, кмоль/кмоль; x w - кубтық қалдықта жеңіл қайнайтын компоненттің құрамы, кмоль/кмоль.
С р = 3226, 3 ∙ 0, 93 + 4190 ∙ 0, 07 = 3293, 76 Дж/ (кг ∙ К ) .
С w = 3394 ∙ х w + 4190 ∙ х р (4. 10)
мұндағы: С w - кубтық қалдықтың жылу сыйымдылығы, Дж / (кг∙ К) ; 3394 - 87 0 С - ғы этил спиртінің жылу сыйымдылығы, Дж / (кг∙ К) ; x w - кубтық қалдықта жеңіл қайнайтын компоненттің құрамы, кмоль/кмоль; x p - дистиллятта жеңіл қайнайтын компоненттің құрамы, кмоль/кмоль; 4190 - судың тұрақты жылу сыйымдылығы, Дж / (кг∙ К) .
С F = 3394 ∙ 0, 032 + 4190 ∙ 0, 968 = 4164, 53 Дж/ (кг∙К) .
С F = 3477, 7 ∙ х р + 4190 ∙ х F ; (4. 11)
мұндағы: С F - бастапқы қоспаның жылу сыйымдылығы, Дж / (кг∙ К) ; 3477, 7 - 99 0 С - ғы этил спиртінің жылу сыйымдылығы, Дж / (кг∙ К) ; х F - бастапқы қоспада жеңіл қайнайтын компоненттің құрамы, кмоль/кмоль; x p - дистиллятта жеңіл қайнайтын компоненттің құрамы, кмоль/кмоль; 4190 - судың тұрақты жылу сыйымдылығы, Дж / (кг∙ К) .
С F = 3477, 7 ∙ 0, 34 + 4190 ∙ 0, 65 = 3947, 82 Дж/ (кг ∙ К) .
t = 78 0 C болғандағы флегма буының қалыптасу жылуын анықталады:
r ф = 845 ∙ 0, 93 + 2307 (1- 0, 93) = 947, 34 кДЖ/кг = 947, 34∙ 10 3 Дж/кг;
мұндағы: r = 845 кДЖ/кг - этил спиртінің t = 78 0 C болғандағы будың меншікті жылуы; r = 2307 кДЖ/кг - су буының меншікті жылуы.
Колоннадан шығатын бу энтальпиясы келесі формуламен анықталады:
І бу =r ф + с р ∙ 78;
мұндағы: r ф - t = 78 0 C-ғы флегма буының қалыптасу жылуы, Дж/(кг∙К) ; с р - дистилляттың жылу сыйымдылығы, Дж / (кг∙ К)
І бу = 947, 34 ∙ 10 3 + 3293, 76 ∙ 78 = 1204253, 28 Дж/кг
Кубтағы шығысы бойынша жылуды 3 % тең деп қабылданды.
Жылулық жоғалтуларды ескере отырып, колоннаның кубтық бөлігінде жылу шығысын келесі формула бойынша анықталады:
Q = 3, 94 ∙ ( 4164, 53 ∙ 99- 3947, 82 ∙ 87) + 2, 06 ∙ 1, 547 ∙ 947, 34 ∙ 10 3 +
+ 2, 06 (1204253, 28 - 3947, 82 ∙ 87) + 0, 03; (4. 12)
мұндағы: Q - жылу шығысы, Вт; Q = 5063418, 4 Вт.
Колонна түбіндегі ысытатын будың шығысы :
G
r п
=
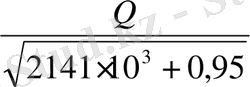 ; (4. 13)
; (4. 13)
мұндағы: Q - жылу шығысы, Вт; G г. п - бу шығысы; кг/с.
G
г. п
=
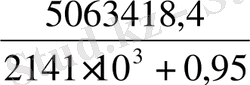 = 2, 36 кг/с ;
= 2, 36 кг/с ;
Тоңазытқыштарда су температурасының 20 0 С көтерілуін қабылдай отырып, дефлегматордағы су шығысын анықтаймыз:
G′ = р ∙ (1 +
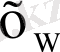 ) ∙ r
ф
/ (4190 ∙ 20) (4. 14)
) ∙ r
ф
/ (4190 ∙ 20) (4. 14)
мұндағы: G′ - дефлегматордағы су шығысы, кг/с; р - дистиллят, кмоль/кмоль; x w - кубтық қалдықта жеңіл қайнайтын компоненттің құрамы, r ф - t = 78 0 C-ғы флегма буының қалыптасу жылуы, Дж / (кг∙К) ; кмоль/кмоль; 4190 - судың тұрақты жылу сыйымдылығы, Дж / (кг∙ К) .
G′ = 2, 06∙ (1 + 1, 547 ) ∙ 947, 34∙ 10 3 / (4190 ∙ 20 ) = 59, 3 кг/с;
Дистиллят тоңазытқышында:
G′′ = р ∙ с р (78 - 30) / (4190 ∙ 20) ; (4. 15)
мұндағы: G′′ - дистилляттағы тоңазытқыштың су шығысы, кг/с; р - дистиллят құрамы, кмоль/кмоль; с р - дистиллятта қайнайтын компонент құрамы, кмоль/кмоль; 4190 - судың тұрақты жылу сыйымдылығы, Дж / (кг∙ К) .
G′′ = 3, 94 ∙ 3293, 76 (78 - 30) / (4190 ∙ 20) = 7, 4 кг/с;
Кубтық қалдықтың тоңазытқышында :
G′′′ = р ∙ с w ( 99 - 30) / (4190 ∙ 20) (4. 16)
мұндағы: G′′′ - кубтық қалдықтың тоңазытқыштағы су шығысы, кг/с; р - дистиллят құрамы, кмоль/кмоль; с w - кубтық қалдықта жеңіл қайнайтын компоненттің құрамы, кмоль/кмоль; 4190 - судың тұрақты жылу сыйымдылығы, Дж / (кг∙ К) .
G′′′ = 3, 94 ∙ 4164, 53 (99 - 30) / (4190 ∙ 20) = 13, 5 кг/с;
Судың жалпы шығыны мынаған тең болады:
G су = G′ + G′′ + G′′′ (4. 17)
мұндағы: G су - судың жалпы шығыны, кг/с; G′ - дефлегматордағы бу шығысы, кг/с; G′′ - дистилляттағы тоңазытқыштың су шығысы, кг/с; G′′′ - кубтық қалдықтың тоңазытқыштағы су шығысы, кг/с;
G су = 59, 3 + 7, 4 + 13, 5 = 80, 2 кг/с.
Технологиялық есептеу
Колонна арқылы өтетін бу мен сұйықтың көлемін анықтау.
Ең алдымен бу мен сұйықтың мольдік массаларын, колоннадағы сұйық пен будың орташа мольдік және массалық концентрацияларын анықтаймыз.
Колоннаның жоғарғы бөлігіндегі сұйықтың орташа мольдік құрамы:
х ж. орт. м = ( х р + х F ) / 2; (4. 18)
мұндағы: x p - дистиллятта жеңіл қайнайтын компоненттің құрамы, кмоль/кмоль; х F - бастапқы қоспада жеңіл қайнайтын компоненттің құрамы, кмоль/кмоль.
х ж. орт. м = (0, 83 + 0, 168) /2 = 0, 499.
Колоннаның төменгі бөлігінде:
х төм. орт. м = ( х F + x w ) / 2; (4. 19 )
мұндағы: х F - бастапқы қоспаның құрамы, кмоль/кмоль; x w - кубтық қалдықтың құрамы, кмоль/кмоль.
х төм. орт. м = ( 0, 168 + 0, 013) /2 = 0, 09.
Колоннаның жоғарғы бөлігіндегі сұйықтың орташа массалық құрамы:
 ж. орт. су
= ( х
р
+ х
F
) / 2; (4. 20)
ж. орт. су
= ( х
р
+ х
F
) / 2; (4. 20)
мұндағы: х F - бастапқы қоспада жеңіл қайнайтын компоненттің құрамы, кмоль/кмоль; x p - дистиллятта жеңіл қайнайтын компоненттің құрамы, кмоль/кмоль.
 ж. орт. су
= (0, 93 + 0, 34) /2 = 0, 635.
ж. орт. су
= (0, 93 + 0, 34) /2 = 0, 635.
Колоннаның төменгі бөлігінде:
 төм. орт. су
= ( х
F
+ x
w
) / 2; (4. 21)
төм. орт. су
= ( х
F
+ x
w
) / 2; (4. 21)
мұндағы: x w - кубтық қалдықта жеңіл қайнайтын компоненттің құрамы, кмоль/кмоль; х F - бастапқы қоспада жеңіл қайнайтын компоненттің құрамы, кмоль/кмоль.
 төм. орт. су
= ( 0, 34 + 0, 032) /2 = 0, 186.
төм. орт. су
= ( 0, 34 + 0, 032) /2 = 0, 186.
Колоннаның жоғарғы бөлігіндегі сұйықтың орташа мольдік массасы:
М су = М сп ∙ х ж. орт. м + М су ∙ 0, 377 (4. 22)
мұндағы: х ж. орт. м - сұйықтың орташа мольдік құрамы; М сп және М су - этил спирті және судың молекулалық масасы, кг / кмоль.
М ж = 46 ∙ 0, 499 + 18 ∙ 0, 501 = 32 кг/кмоль;
Колоннаның төменгі бөлігінде:
М т = М сп ∙ 0, 09 + М су ∙ 0, 91; (4. 23)
мұндағы: М сп - этил спирті молекулалық масасы, кг / кмоль; М су - судың молекулалық масасы, кг / кмоль.
М т = 46 ∙ 0, 09 + 18 ∙ 0, 91 = 20, 52 кг/кмоль
Дистилляттың мольдік массасы:
М р = М сп ∙ х р + М су (1 - х р ) ; (4. 24)
мұндағы: М сп және М су - этил спирті және судың молекулалық масасы, кг/кмоль; x p - дистиллят құрамы, кмоль/кмоль.
М р = 46 ∙ 0, 83 + 18 ∙ (1 - 0, 83) = 41, 24 кг/кмоль
Бастапқы қоспаның мольдік массасы:
М F = М сп ∙ х F + М су ( 1- х F ) ; (4. 25)
мұндағы: х F - бастапқы қоспа құрамы, кмоль/кмоль; М сп және М су - этил спирті және судың молекулалық масасы, кг/кмоль.
М F =46 ∙ 0, 168 + 18 ∙ (1 - 0, 168) = 22, 704 кг/кмоль.
Кубтық қалдықтың мольдік массасы:
M w = М сп ∙ х w + М су ( 1- х w ) ; (4. 26)
мұндағы: х w - кубтық қалдық құрамы, кмоль/кмоль; М сп және М су - этил спирті және судың молекулалық масасы, кг / кмоль.
M w =46 ∙ 0, 032 + 18 ∙ (1 - 0, 032) = 18, 9 кг/кмоль.
Колоннаның үстіңгі бөлігіндегі будың орташа мольдік құрамы:
у үст. бу. орт = (х р + 0, 553) / 2; (4. 27)
мұндағы: x p - дистиллят құрамы, кмоль/кмоль.
у үст. бу. орт = ( 0, 83 + 0, 553) /2 = 0, 69.
Колоннаның төменгі бөлігінде: .
у төм. бу = ( 0, 553 + х w ) / 2; (4. 28)
мұндағы: х w - кубтық қалдық құрамы, кмоль/кмоль
у төм. бу = ( 0, 553 + 0, 013) /2 = 0, 283.
Колоннаның үстіңгі бөлігіндегі будың орташа мольдік масасы:
М үст. = М сп ∙ у үст. бу + М су ( 1- у үст. бу ) ; (4. 29)
мұндағы: М сп және М су - этил спирті және судың молекулалық масасы, кг/кмоль; у үст. бу - колоннаның үстіңгі бөлігіндегі будың орташа мольдік құрамы.
М үст. =46 ∙ 0, 69 + 18 ( 1- 0, 69) = 37, 32.
Колоннаның төменгі бөлігінде:
М төм = М сп ∙ у төм. бу + М су ( 1- у төм. бу ) ; (4. 30)
мұндағы: М сп және М су - этил спирті және судың молекулалық масасы, кг/ кмоль; у төм. бу - колоннаның төмеңгі бөлігіштегі будың орташа мольдік құрамы.
М төм = 46 ∙ 0, 283 + 18 ( 1- 0, 283) = 25, 92.
Колоннаның үстіңгі бөлігіндегі сұйықтың орташа тығыздығы:
ρ
үст
= 733
 ж. орт. м
+ 968( 1 - х
ж. орт. м
) (4. 31)
ж. орт. м
+ 968( 1 - х
ж. орт. м
) (4. 31)
- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz