Термиялық фосфор қышқылы өндірісінің технологиясы және шығындарын есептеу


ЖОСПАР
Кіріспе
- Фосфор және термиялық фосфор қышқылы
- Термиялық фосфор қытқылын алу.
- Термиялық фосфор қышқылы шығындарын есептеу.
Қорытынды
Пайдаланған әдебиеттер
Кіріспе
Химия өнеркәсіп және оның өнімдері адам өмірінің күнделікті тіршілінде, халық шаруашылығының көитеген салаларында қолдапылуда. Табиға немесе өндеу арқылы алынған барлық бейорганикалық тұздар дүние жүзілік өндіріс бойынша жылына миллион немесе ондаған миллион тонна келемінде өндірілуде. Олар ауыл-шарушшлығанда минералды тыңайтқыштар есебінде көптеп қолданылады. Тьңайтқышгардың өсімдіктермен жақсы ciңipyi оның өнімділігін арттырып жер қыртысын жаксартады.
Kaзіpri уақытта минералды тыңайтқыштардың көптеген түрлері шығарылуда. Оларға жай суперфосфат, қос суперфосфат, аммоний фосфаты, күрделі тыңайтқыштар т. б. жатады. Бұл тыңайтқыштар фосфор және күкіртті т. б. қышқылдарды, тиімді әдістерді қолдану арқылы өнделуде. Өндеу процестерінің химиялық өзгеіpic, реакцияның жүруіне температура, қысым әрекеттесуші заттардың күйлері мен қоршаған ортаға экологиялық әсерін білу қажет және оларды "Бейорганикалық заттардың технологиясы" саласъшдағы ілім зерттейді.
Ұсынылып отырған оқулықта қазақ тілінде алғаш рет тыңайтқыштар технологиясы бойынша білім алған студенттердің, техника саласындағы инженер, аспиранттар талап - тілегіне сәйкес қарастырылып дайындалған.
Мұнда оқулықтың әp6ip тарауын қарапайым тілмен, жан-жақты баяндап,
минералды тыңайтқыштарға қажетті шикізат, оны дайындау, өндеу технологаясы, негізгі көpceткіштepi мен техиологиялық үлгісі көрсетілген. Минералды тыңайтқышты өндеуде қолданылатын негізгі жабдықтар, шикізат шығымы мен жылу баланстарың есептеулер, өндіріс қалдықтарын өндеу әдістері қамтылған. Оқулықты қазақша дайындау мақсаты қазақ, тілінде дәріс алатын студент жастарды " Бейорганикалық, заттардың, технолгиясы" пәнінің негіздері және технологиясымен таныстыра отырьп, алған білімдерін өндірісте, ғылыми зертгеу жұмыстарында қолдануға бағыттау және олардың ой-тұжырымдарын қалыптастыру.
Бұл оқу құралының орта және орта-арнаулы оқу оръшдарыньң қырмандарына да жәрдем көрсетері даусыз. Қолжазбаны мұқият оқып құнды ұсыныс, бағалы ескертпелер пiкip жазған техника ғылымының докторы, професссор Юнусов У. И. (Ғылыми-инженеритті институт), химия ғылымының докторы Утелбаев Б. У. (М. Әуезов атындағы Оңтүстік Қазакстан мемлекеттік университеті) жолдастарға зор ризашылығымызды білдіреміз.
- Фосфор және термиялық фосфор қышқылы
Фосфорды элекротермялык әдіспен алады, яғни табиғи фосфатты көміртегімен тотықсыздандырады. Бұл процесс жоғары температурада электр пештерінде өтедді Электрлі пештен бөлінген фосфор буын сұйылтканда сұйық фосфор тұзіледі, оны қоршақан орта температурасына дейін суытқанда қатты өнім алынады.
Сұйық фосфорды және оның буын тотықтыру (жандыру) жолымен фосфор пентатотығын алады, оны гидратацияға түсіргенде фосфор қышқылы түзіледі Бұл әдіспен алынған қышқыл термиялық фосфор қышқылы (ТФҚ) деп аталады.
Үнемді, сондай-ақ кең тараған фосфор қышқылының өндipici фосфатты күкірт қышқылымен экстракицялау. Бұл жағдайда енімді экстракциялық фосфор қышқылы деп атайды.
Фосфатты элсктротермиялық өндеудің артықшылығы барлық фосфаттардан, соның ішінде төмен сапалы фосфатты қолдануда жоғары дәрежелі таза шоғырлы фосфор қышқылын алуға болады. Қышқыл ендеуге жоғары сапалы емес шоғырлы және қоспалармен қатты ластанған фосфориттер қолданылады.
Реактивтер сияқты жемдік және техникалық фосфаттар таза болу керек, сонымен, одан ТФҚ алады, бірақ ол ЭФҚ қарағанда қьмбат. Фосфорқұрамдас тыңайтқыш алуда басты белігіне арзан ЭФҚ қолданады.
ГОСТ 10678-76 сәйкес ТФҚ екі маркасы шығарады - А (тамақ өндірісінде) жәнс Б (техникалық) . Б маркасында 73% кем емес НРО (52, 9% Р Э О 5 ) болады. 1 және 3 сортты техниқалық қышқыл құрамындағы қоспалар (% көп емес) : хлоридтер 0, 01 және 0, 02, сульфаттар 0, 015 және 0, 02; нитраттар 0, 0005 және 0, 001, темір 0, 001 және 0, 015; ауыр металдар (Рв) 0, 002 және 0, 005, мышьяк 0, 006 және 0, 008. Тамаққа қажетті қышқылдар: мышъяк 0, 0003 қорғасын 0, 0005, NO 3 - 0, 0003.
2. Термиялық фосфор қытқылын алу.
Термиялық фосфор қышқылын элементті фосфорды тотықтыру (жандыру) (Р 4 +5О 3 =Р 4 О 10 ) және түзілген пентотық фосфорды гидратациялау арқылы алады. P 2 O 5 -i гидратациялау 6ipiнен соң бipi өтетін мета-, пиро- және ортофосфор қышқылы алынғанша
жүргізіледі:
700°С-та n Р 4 О 10 +2nH 2 O=HPO 3 ) n
450°С-та 4(HPO 3 ) n +2nH 2 O=2nH 4 P 2 O 7
250°С-та 2пН 4 Р 2 О 7 +2пН 2 О=4 n Н 3 РО 4
Гидратацияиың жалпы теңдеуі:
Р 4 О 10 +6Н 2 О-4Н 3 РО 4
Бөлінетін жылу мөлшері 1 кг фосфорды жандырғанда 23614 кДж) гидратацияда - 3035 кДж (немссе 1 кг Н 3 РО 4 - ке 1017 кДж) құрайды. H 3 PO 4 -тi сумен қышқыл өніміне дейін еріткенде қосымша жылу бөлінеді. Техникалық термиялық қышқыл құрамында 73% кем емсс Н 3 РО 4 болады.
Термиялық фосфор қышқылын eкi әдіспен - 6ip сатылы және eкi сатылы әдіспен алуға болады. Бірінші әдісте пештен шьққан фосфоркұрамдас газды жағып, одан соң пайда болған P 2 O 5 -тi гидратацияға түсіреді. Бұл әдістің қарапайымдылығына қарамай, біздің елде қодданылмайды, себебі пеш газындағы фосфор буының шоғырының аз болуынан өте алып, үлкен көлемді қондырғылар қолданылады, ал газ құрамындағы қоспалар (шаң) алынған фосфор қышқылын ластайды. Бұл әдістің кемшілігі фосфор пешінің синхронды жұмыс істеуін кажет етеді.
ТМД зауытгарында термиялық фосфор қышқылын eкi сатылы әдіспен алады, яғни фосфор пешінің газынан фосфорды конденсациялайды, сонаи соң оны қьшқылға өндейді. Бұл жағдайда таза қышқыл алынады, фосфорды конденсациялап алудан қалған газды пайдалануға мүмкіндік туады, фосфорды тотыктырғанда және Р, О 5 гидратаииясьгнда бөлінген үлкен мөлшерлі жылуды әзірше қайта өңдемейді. Жылуды алу әдісінше байланысты өндipicтi екіге беледі циркуляциялық (суытылған сумен жылуды алу) және буландырғаш (буланатын сумен жылуды алу) . Циркуляциялық жүйесі кең тарады: электрлі сүзгі немесе скрубберлі, циркуляциялық 6іp мұнаралы жүйе және циркуляциялық екі. мұнаралы жүйелср. Соңғысы өте кең тараған. Буландырғыш жүйелер болашағы бар жүйелерге жатады. Циркуляцйялықтан айнрмашылығы олар насосты-мұздатқыш қондырғысын қажет етпсйді], сәйкесінше аз энергиялық шығын жұмсалады. Бipaқ олардың кемшілігі - шығатын газдың үлкен көлемде болуы, яғни ол газдар гидратация мұнарасында судың булануынан түзіледі және сондыктан қышқылды ұстауға үлкен көлемді элсктрлі сүзгі қажет.
3. Термиялық фосфор қышқылы шығындарын есептеу.
Фосфор қышқылын термиялық әдіспен өндіріп аду үшін қолданылатын негізгі өнім- элементті фосфор. Оны электрлі пеште кеміртегімен кремнезем қатысуымен фосфаттардан алады.
Ca 3 (PO 4 ) 2 +5C+2SiO 2 P 2 +5CO+Ca 3 Si 2 O 7 - 1460 кДж/моль Алынған фосфор-фосфор ангидридіне дейін тотығады, сонында сумен гидратгайды. Нәтижеде ортофосфорлы қ ышқыл пайда болады:
2Р 2 +5О 2 2Р 2 О 5 Р 3 О 5 +3Н 3 О 2Н 3 РО 4
Фосфорды электрлі-термия әдісімен ұшыру және оны ары карай өндеу Н 3 РО 4 алудың екі тәсілін анықтады: 6ip сатылы (қазігі уақытта қолданылмайды) және eкi сатылы.
Екі сатылы тәсіде элекгрлі пештен бөлінетін газ түріндегі өнімдер фосфорды конденсациялау үшін салқындатылады. Конденсацияға түскен фосфорды жандыру арқылы және фосфор қышқылында гидратациялау арқылы қышқылға өндейді.
Осы тәсілмен өте таза қышқыл алады. Сонымен қатар керек кезде өнім ретінде тағы сары фосфорды алуға және көмipтeri тотығын қайта өддеуге болады.
ГОСТ 10678-83 бойынша термиялық фосфор қышқылы (техникалық I және II сорттар) кұрамында 75% Н 3 РО 4 аз емес және өте аз мөлшерде қоспалар (хлоркдтердің, ауыр металдардың, фторлардың және т. б. ) болуы керек.
-суретте сұйық фосфордан Н 3 РО 4 өндіріп алудың үлгісі көрсетілген. Сұйық фосфорды жағу мұнарасында жағады. Айналмалы фосфор қышқылының газдарды салқындатудың әсерінен мұнарадан шығудағы температурасы 145-160°С. Сонымен пеште бөлінген фосфор ангидридінің 6ipaз бөлігі гидратация мұнарасынан берілетін қышқылмен сіңірледі. Жағу мғнарасынан өнімді қышқыл бөлінеді. Қалған газ массасы жағу мұнарасынан гидратация мұнарасына келіп түседі, онда фосфор ангидридінің қалған бөлігі ұсталады да Н 3 РО 4 пешке берілу гидратация мұнарасы кайтарымды сұйытылған фосфор қышқылымен шайылады. Әсерлеспеген газдар гидратация мұнарасынан 5О-6О°С температурасынмен электрлі сүзгіш фильтрге келіп түседі. Онда газды тазалап атмосфераға жібереді
Ауа шығыны Vауа (м 3 ) және G (кг), А кг фосфорды жағу үшін
керекті мөлшерін төмендегі теңдеумен есептейді:
А · 5 ·22, 4а·100х А · 5 · 22, 4ах
Vауа = = 4, 301· 10² А ах (1)
4·31· 100 · 21 4 ·31· 21
А•5•22, 4а• 1, 29х
G=Vауа • 1, 29 = = 5, 55 • 10 Аах (2)
4 • 31 • 21
Мұндағы: 31 - фосфордьң атомдық, массасы;
а - техникалық сары (сұйық) фосфор құрамындағы элементті фосфор мөлшері,
21 - ауадағы оттeгi мөлшері, % (көл. ) ;
2 - стехиометриялық. мөлшерге қатысты ауаның шығын шамасы; әр уақытта 1, 9-2, 1;
1, 29 - ауа тығыздығы, кг/ м 3
Пайда бoлған қышқыл мөлшері
A • 98
Gk = = 3, 16 • 10- 2 . А • а
100 • 31
G k 100 Аа • 98 Аа
b % Н 3 РО 4 шоғырымен G¹ k = = = 3, 16
b b•31 b
с % Р 2 О 5 шоғырымеи
G k 71• 100 Aa • 71 Аа
G ¹¹ = = = 2, 29
С•98 С•31 С
Егерде жағу мұнарасында q { кг, гидратация мұнарасында q 2 кг, ал электрлі сүзгіште g 3 кг 100%-тік Н 3 РО 4 пайда болса, онда
g 1 = 0, 01·m 1 G k ; g 2 =0, 01·m 2 G k ; g 3 -0, 01·m 3 G k ; мұндағы: m 1 , m 2 , m 3 - жағу, гидратациялау және электрлі сүзгіш мұнараларындағы фосфор ангидридінің ұсталу дережесі, %.
Пайда болатын фосфор ангидрид! мелшерш V a (M 3 ) жэне G a төмсндегі теңдеумен табады;

Бұл жерде Р 2 О 5 Р 4 О-ға өтyi ескеріледі, сондықтан 22, 4м 3 кмолъ көлемі ассоциацияланған Р О 0 молекуласына берілген G, кг су мөлшерін аныктайтын тендеудер:
Қышқылды түзеуге арналғаны (фосфор ангидридінің гидратациялануына)
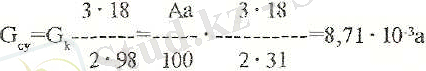
- в % Н 3 РО 4 шоғырына дейін моногидрат фосфор қышқылын сұйылту үшін қажетті мөлшері:

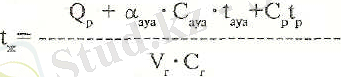 Фосфордың жану температурасын темендеп теңдеу аркылы табуга болады:
Фосфордың жану температурасын темендеп теңдеу аркылы табуга болады:
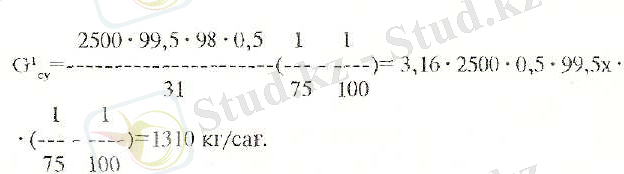
Фосфор ангидридін гидратациялау үшіа және Н 3 РО 4 сүйылту үшін жалпы су шығыны:
1083+1310-2393 = 2400 кг/сағ.
Есепбі:
1000 кг жағылатын фосфорға есептегендегі өндірілген Н 3 РО 4 материалдық балансын тап, темендегі берілгендерге сүйене отырып:
- жануға келіп түсетін фосфор құрамындағы қоспаО, 5%;
- фосфор ангидридін сіңіру дәрежелері жағу мұнарасында 50%; гидратация мұнарасында 44, 5% және электр сүзгіште 5, 5% оның жалпы мөлшерінен;
- пайда болу Н 3 РО 4 шоғыры жағу . мұнарасында 75%, гидратация мүнарасында 65% және электр сүзгіште 75% Н, РО 4 шығарылатын өнімді фосфор қышқылы құрамы 75% Н 3 РО, ;
- 1000 кг фосфорды жағуға шығьшдалатын ауа практикалық. берігені бойынша 10370, 8 кг (8055 м 3 қ. ж. бойынша) келіп түсетін ауа ылғалдылығын ескермейді;
- газдардың ылғалдылығы: жағу мұнарасынан шығатын 0, 18; салқындату мұнарасынан 0, 116 және электр сүзгіштің шығысында 0, 1 кг/кг;
ШЕШУІ:
Kipic: Жағу мұнарасына келіп түсетін фосфор мелшері 1000 кг. Жағу мұнарасына берілетін ауа мөлшері - 10370, 8 кг; сонын ішінде; оттегі 2416, 5 және азот 7954, 3 кг.
Фосфор қышқылын сұйылту және пайда болу үшін, сонымен бөлінетін газбен 6ipre кететін су мөлшерін, бөлінетін газ және пайда болған қышқыл мөлшерлерін анықтағанда табады.
Шьгғыс:
Пайда болатын Н 3 Ю 4 мөлшері, кг:
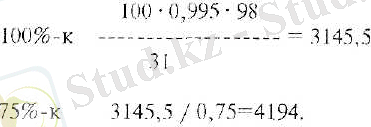
Сонымен техлологиялық процестің әр сатысында пайда болған Н РО кг:
Жағу мұнарасында 50%. Жалпы қышқыл мөлшерінен 3145, 5-0, 5 - 1572, 75 кг (100% Н 3 РО) 1562, 75 0, 75 = 2097 (75% Н 3 РО 4 )
электр сүзгіште 5, 5% жалпы мөлшерден: 3145, 5-0, 055 -173 кг немесе
3145, 5 - 1572, 75 . . . 1399, 7 = 173 (100% Н РО 4 ) .
173 / 0, 75 = 230, 6 (75% Н 3 РО 4 )
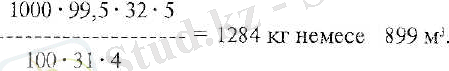 Технологиялық процестің жүйесінен және белек сатыларынан бөлінетін газ мөлшерін табамыз. т фосфорды жаққанда шығьшдалағын қышқыл:
Технологиялық процестің жүйесінен және белек сатыларынан бөлінетін газ мөлшерін табамыз. т фосфорды жаққанда шығьшдалағын қышқыл:
Сонымеи, келіп түсксн 10370, 8 кг ауадан жағу және гидратация мұнараларынан және электр сүзгішітен кeтетiнi:
10370, 8 - 1. 284 - 9086, 8 кг
Оның құрамында (2. 25-мысал), кг:
N 2 7954, 3
О 2416, 5- 1284 - 1132, 5
Онымен 6ipre су булары кетеді, олардың ылғалдықтарымен келісіліп әртүрлі температураларда:
Жану мұнарасының шығысында 9086, 8 • 0, 18 = 1635, 6
Гидратация мұнарасының шығысында 9086, 8 0, 116 = 1054
Электр сүзгіштің шығысында 9086, 8 0, 11 = 1000
Су буын есептегендегі бөлінетін газдың жалпы мөлшері
9086, 8 + 1000 = 10086, 8 кг
қойылатын ағын құрамындағы су мөлшері Н 3 РО 4 -те:
4149-3145, 5 кг - алыггатыи 75%-К лоне 100%-к кышкьгл мөлшері;
866, 5 кг- моногидрат құрамындағы су мөлшері
Бөлінетін газда 1000.
Сонымен, жүйеге енгізуге керекті су мелшері:

1-суреттс термиялық, фосфор қышқылын циркуляциялық 6ip мұнаралы жүйеде алу үлгісі берілген. Сұйық фосфор булы инжектор форсунка 1 кемегімен шашыратылады және ауа ағынында мұнарада 2 жанады, ішкі қабырғасымен қышқыл ағьн, жинағышта 4 жиналады. Мұнара конус тәріздес болып келеді бұл қабырғамен жұка түрде қышқылдың ағуына жағдай жасайды, Бұл ыстық фосфор жалынынан қабырғаны қорғайды. Фосфордың термиялық жану температурасы 3500°С көтеріледі.
Бірақ фосфорды жағу ауаның екі есе шығынында жүргізіледі, сондықтан температуралар да 2100-1800°С-қа дейін төмендейді. Газды одан әpi суыту қышқылдан суды буландыру нәтижесінде жүргіз. Ауаның артық шығыны гидратацияға фосфорлы және фосфорлы қышқылға айналатын төмен фосфор тотығы түзілмеу үшін беріледі.
Р 2 О 5 гидратациясы кезіндегі газдың жоғары температурасының (800-1000°С) әcepiнeн, алдымен бу тектес метафосфор қышқылы түзіледі, оны онан әpi суыту және гидратация нәтижесінде ортофосфор қышқылы түзіледі. Қышқылды шашыратуға мүмкіндік беретін ұлу 3, мұнараның ішкі бетіне орналасқан. Болат мұнара полиизобутиленмен диабаза плиткасымен және графиттелген блокпен қапталған. Жанатын фосфордьң 1 т-сағ өнімділі бойынша есептегенде мұнараның орташа диаметрі 3 м , биіктігі 13 м.
Жииағыштан 4 насоспен 5 жылуалмастырғышка 6 суытуға қышқылды береді. Сонан соң жинағышқа 7 жинайды. Оньң бip болігі қоймаға, калғаны мұнараға cіңipy үшін қайтарылады. Мұнарадан газдар 16О°С дейін суытылып шығарылады: Н 3 РО 4 тұмаңынан тазалау үшін желдеткішпен 9 электрлі сүзгі 8 арқылы сорылады және атмосфераға шығарылып тасталады. Электрлі сүзгідегі қышқылды жинағыш 10 аркылы коймаға береді. Сұйық фосфорды коймадан артпалы насоспен қыздырылған фосфор құбырымен дозаторға айдалады, одан жандыру мұнарасының 2 форсункасында 1 насоспен берілетін сумен сығылады, фосфордың шашыратылуы бумен 70-80°С дейін қыздырылған (косымша бipіншi ауа) сығылған ауамен іске асырылады (3 сурет) . Қосымша ауа жану мұнарасынаұлу 3 аркылы сорылады. Фосфорды тотықтыруда бөлінген жылу қайтарымды сумен сіңіріледі. Қайтарымды суды мұнараның қақпағының - градирнінен келіп түскен және артпалы насос кемегімен 4 циркуляцияланған, яғни ол жинағыш 5 арқылы және жылу алмастырғыштан 6, 46-50°С-қа дейін қыздырылған су мұнараның жоғарғы жағынан қабырғамен және қабатпен ағады.
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz