Pb2+, Hg+, Hg2+, Cd2+ иондарының ағаш сорбенттердегі сорбциясы


Тақырыбы: Қатты металдардың (Pb 2+ , Hg + , Hg 2+ , Cd 2+ ) ағаш сорбенттеріндегі сорбциясы
ДИПЛОМДЫҚ ЖҰМЫС
«Фармацевтикалық өндіріс технологиясы»
МАЗМҰНЫ
Кіріспе
Тарау 1 Әдебиеттік шолу
- Фармацевтика өндірісінің ағын суларының сипаттамасы (зерттеу объектілері)
- Ағын суларын органикалық қоспалардан тазарту әдістері. Адсорбциялық тазарту.
- Адсорбцияның физика - химиялық негіздері.
- Көміртек сорбенттерінің сипаттамасы.
Тарау 2 Тәжірибелік бөлім
КІРІСПЕ
Химиялық ластану-жақсы таралған, тұрақты және таралу аумағы кен. Ол органикалық(фенолдар, нафтенді қышқылдар, пестицидтер және т. б), бейорганикалық(тұздар, қышқылдар, сілтілер), улы (күшән, сынап қосылыстары, қорғасын, кадмий және т. б) және усыз.
Бактериялы ластану суда патогенді бактериялар, вирустар (700-ге жуық), қарапайым саңырақұлақтардың пайда болуымен байқалады.
Механикалық ластану суда әртүрлі механикалық қоспалардың (құм, шлам, балшық және т. б) түсүімен сипатталады. Механикалық қоспалар судың органолептикалық көрсеткішін айтарлықтай төмендетуі мүмкін.
Тарау 1 Әдебиеттік шолу
1. 1 Фармацевтикалық өндірістегі ағынды сулардың сипаттамасы( зерттелетін объект)
Судағы фенол: қалай түседі?
Бұрынғы кезенде барлық химиялық өндірістер технологиясы қоршаған ортаға әсерін елемей өндірілген. Расымен, целлюлоза технологиясы және мұнай өндірісі қоршаған ортаға айтарлықтай әсері болмаған кезде өндіріле бастады. Сол себепті бұл маселеге ешкім аса мән берген жоқ. Ақырындап химиялық өндіріс ауқымы кеңейе бастады, сонымен қатар қалдық көлемі де артты. Тазалау технологиясы жасалып, қолданысқа ене бастады және қолданылған шаралар нәтижесінде ластану нәтижесі төмендеді. Бірақ химиялық өндірістің өркендеуімен қатар, ластану көлемі де өсу де. Табиғи жағдайда ерімейтін және зарарсызданбайтын жаңа химиялық қосылыстар пайда болды. Ал олардың тірі организмге әсері ауқымды болуы мүмкін.
Химиялық өндіріс салаларында пайда болған, ластанған заттардың жалпы саны ауқымды. Әуе бассейніндегі маңызды ластанандырғыш болып көміртек тотығы, күкіртті газ, азот тотығы, шаң, қара күйе, канцерогенді заттар, фтор, металл аэрозольдары болып табылады. сулы бассейннің ластаушысы- әртүрлі тұздар, сілтілер мен қышқылдар, кадмий, сынап, күшән, мұнай және оның қайта өңделген өнімдері, цианидтер мен фенолдар.
Фенолдар өнеркәсіп ағындарымен бірге су бетіне түсетін анағұрлым кең таралған ластағыштардың бірі болып табылады. Фенол суларының су қоймасы мен ағын суына тасталуы олардың жалпы санитарлық жағдайын кенеттен нашарлатады, тірі ағзаларға тек өзінің уыттылығын ғана тигізіп қоймай, сол сияқты биогендік элементтер мен еріткіш газдардың (сутегі, көмірқышқыл газы) режимдерінің біршама өзгерісіне әсерін тигізеді. Су қоймаларының фенолдардан өзіндік тазартылу процесі біршама ақырын өтеді және оның іздері өзен ағынымен үлкен арақашықтыққа апаруы мүмкін, осыған байланысты фенолқұрамды ағынның тасталуынан бұрын қажетті тазартылуға ұшыратылады. Фенол қосылыстары дегеніміз - молекула ядро құрамында бір немесе одан да көп гидроксил топтары бар ароматты (бензолды) қосылыс. Фенол қосылыстарының қарапайым өкілі - фенол:
Фенол
Құрамындағы ОН - тобының санына байланысты біратомды фенолдар (мысалдар, жоғарыда келтірілген фенолдар мен крезолдар) және көпатомды фенолдар деп ажыратылады. Екіатомды фенолдар (диоксибензол) үш қосылыс түрінде кездеседі: пиракатехин, резорцин, гидрохинон
Келтірілген мысалдардан көріп отырғанымыздай, фенолдарға құрылыстық изомерлену тән (гидрокси топтардың орналасу изомерленуі) .
Танымал фенол қосылыстарының саны көп. Қазіргі таңда олардың бірнеше мыңнан астам түрі бар және жыл санап олардың саны артуда. Фенол қосылыстары екі топқа бөлінеді:
- ұшқыш фенолдар (фенол, крезол, ксиленол, гваякол, тимол) ;
- ұшқыш емесе фенолдар (резорцин, пирокатехин, гидрохинон, пирогаллол және басқа да көпатомды фенолы) .
Ұшқыш фенолдар анағұрлым улы және өткір иіске ие болады.
Әдетте фенолдар қалыпты жағдайда сулы ағзаларда метаболизм процесінде, биохимиялық ыдырауда және су қалыңдығында және су түбіндегі шөгінділерінде өтетін органикалық заттардың транформациясында түзіледі. Тірі өсімдік ұлпаларының фенол қосылыстарын патогенді саңырауқұлақтардың өсуін ингибирлейтін немесе вирустардың көбею жылдамдығын азайтатын потенциалды уытты заттар ретінде қарастыруға болады.
Фенолдар әлсіз қышқылдар (рКа фенол үшін 9, 98) болып табылады. Тотығу реакцияларндағы фенолдардың жоғары реакциялық қабілеттілігі фенол қосылыстарын майларды автототықтыру процестерінде ингибитор ретінде қолдану кезінде техникалық қолдануға ие болады және табиғи фенол қосылыстарының биосинтезінде үлкен мәнге ие. Бөліну және идентификациясы бойынша фенолдардың анағұрлым маңызды қасиеттері металдармен тұз түзуінде. Кішігірім шектеулерге орай, барлық фенол қосылыстары қатты, ал түсі ашық - сарыдан қызылға, қоңыр немесе қызыл күрең түске дейін өзгереді. Фенолдар су бетіне өнеркәсіп ағындарынан, соның ішінде мұнай өңдейтін, тақта тас өндіретін, орман - химиялық, коксохимиялық, аналин бояу өнеркәсібінен кеп түсетін, нәтижесінде гидролиз өнеркәсібімен (тағам емес целлюлозды - қағаз өсімдік шикізаты және аздап тоқыма мата шикізаты) бірге неғұрлым көп таралған ластаушылар.
Өнеркәсіп орындарының ағын суларындағы фенол құрамы түрлі үйлесімде 5-10 г/л болуы мүмкін, осы жағдайда фенолдардың ішетін су мен балық шаруашылығы су қоймаларындағы шекті концентрация құрамы 1 мкг/л құрайды. Фенолдардың коксохимия зауытының ағындарындағы концентрациясы үлкен 20 г/л дейін, ал заманауи коксохимия зауыттары тәулігіне су қоймасына 4-10 т фенолмен ластайды. Фенол бойынша қалыпты аясының жоғарылауы су қоймаларының ластануынан байқалады. Фенолмен ластанған табиғи сулардағы құрамы бір литрде ондықтан жүз микрограмға дейін жетуі мүмкін. Су қоймасының суы бояға ие, карбол тәрізді спецификалық иісті, флуоресценцияланатын жұқа қабықшамен қапталған, ол су қоймасындағы биологиялық процестердің қалыпты өтуіне кедергі келтіреді. Фенол 75 мг/л концентрацияда су қоймасындағы биологиялық тазарту процесін тежейді, 0, 01-0, 1 мг/л концентрацияда балық етінде жағымсыз дәм пайда болады; жағымсыз дәм мен судың иісі тек концентрациясы 0, 11 мг/л фенолын қосқанда ғана жоғалады. Су бетінде фенолдар еріген күйдегі фенолят, фенолят - ион және бос фенол түрінде кездеседі.
Судағы фенолдар күрделі гумус тәрізді және басқа да тұрақты қосылыстар түзетін конденсациялану және полимерлену реакцияларына түсуі мүмкін. Табиғи су қоймасы жағдайында фенолдардың асорбциялық процесі су түбіндегі шөгінділермен және қоспалармен азын - аулақ рөлге ие болады.
Фенол суларының су қоймасы мен ағын суына тасталуы олардың жалпы санитарлық жағдайын кенеттен нашарлатады, тірі ағзаларға тек өзінің уыттылығын ғана тигізіп қоймай, сол сияқты биогендік элементтер мен еріткіш газдардың (сутегі, көмірқышқыл газы) режимдерінің біршама өзгерісіне әсерін тигізеді. Нәтижесінде құрамында фенолы бар суды хлорлағанда хлорфенол тұрақты қосылыстары түзіледі. Олардың кішігірім іздері (0, 1 мкг/дм3) суға сипаттамалық дәм мен иіс береді. Уыттылық пен органолептикалық қатынаста фенолдар бірдей емес. Ұшқыш фенолдар анағұрлым уытты және хлорлау кезінде қарқынды иіске ие болады. Неғұрлым өткір иістілері қарапайым фенол мен крезол.
Фенолмен фенол қосылыстары түрлі өндіріс салаларында кеңінен қолданылады. Егер өнеркәсіпте таза фенол қосылыстарын көп мөлшерде және арнайы тағайындалған болса, онда ГОСТке сәйкес аллергия, демікпе, экземнің пайда болуына әкеп соғады. Ауру белгілері бірден пайда болмай, бір апта немесе бір айдан кейін таза қосылыстармен бейімсізденген жағдайда байланысқаннан пайда болады. Фенолдардың атмосфералық ауада болуы, мамандардың зерттеуі бойынша, қан айналым ауруларына да шалдықтырады.
Өте уытты қосылыстар нитрофенолды қосылыстар - нитроцен (таскөмірлі фенолдар өнімі), динитрофенолдар және т. б. Бұл қосылыстар инсектицид, фунгицид және гербицид ретінде пайдаланылады. Ұлпалардағы тотығу процесіне әсер ете отырып, олар тотығу форсоризация диссоциациясына ұшырайды, бұл өз кезегінде, жасушалық тотығу процесін жоғарылатады, оттегідегі жасуша қажеттілігін ұлғайтады және жылу өнімділігі мен жылу реттеуді бұзады.
ПДК су қоймаларында фенол үшін 0, 001 мг/л концентрация бекітілген. Каспий теңізіндегі суы аз аумақтарындағы фенол құрамы - фенолмен өте ластанған су қоймасында мөлшері 8 мкг/л жетті. Солтүстік Каспий суындағы фенолдардың орташа құрамы 6 мкг/л, ал бұл аумақ үшін орташа мән 3 мкг/л құрайды.
Мамандардың айтуы бойынша, соңғы уақытта солтүстік Каспий суындағы фенолдың орташа концентрациясы 6 ПДК (0. 006 мг/л) ұлғайды. 1995 жылдан бастап 2000 жылға дейінгі периодта фенол құрамының орташа мәні 3. 0 мкг/л ден 9. 0 мкг/л дейін өзгерді. Максималды 30. 0 мкг/л концентрация Орал және Орал жыртылған жері сағасындағы теңіздік бөлігінде белгіленді. 2001 жылдық ақпанында Амурдың фенол органикалық қосылыстарымен қатты ластануынан Еврей автономиялық облысында ішкі сауда және Жапонияға экспортталған тынық мұхиттық миног деликатес балығын қысқы аулауға алғаш рет тыйым салынды. Мұз астынан арнайы балық аулағыш арқылы балықтарды аулаған кезде оларда өткір дәріханалық иістің байқалуынан тыйым салынған болатын. Миног осы уақыт ішінде Тынық мұхиттан орталық Амурге дейін уылдырық шашып үлгерген. Дәрігерлер фенол қосылыстары адам ағзасынан шығарылмайтындықтан, оны тағамға пайдалануға мүлдем тыйым салынған.
Фенолдар химиялық тұрақсыз және сулы ортада белсенді ыдырайды. Судың фенолдардан өздігінен тазартылу процесі микроағзаларда пайда болатын ферменттердің әсерінен биохимиялық тотығу жолымен жүзеге асады.
Қарапайым фенолдар бастапқы негізде биохимиялық тотығуға ұшырайды. 1 мг/л концентрациясынан жоғары болатын фенолдың бұзылуы жылдам өтеді, үш тәуліктегі фенолдың шығыны 50-75% құрайды, бір литрдегі бірнеше ондық микрограм сәйкес келгенде бұл процес баяулайды, ал шығын бұл уақытта 10-15%. Бәрінен жылдам бұзылатыны фенолдар, одан баяуы крезол, ал одан да баяу өтетіні ксиленолдар. Көпатомды фенолдар негізінен химиялық тотығу жолымен бұзылады.
Мұнай ластануының болуы фенолдардың ыдырауын баяулатады, яғни, мұнай көмірсутектерінің биодеградациясы ластануды ұлғайта отырып жеке фенолдарды түзеді. Су бетіндегі фенолардың концентрациясы маусымдық өзгертілуге әкеп соғады. Жазғы маусымда фенолдардың құрамы төмендейді (температура ұлғайған сайын ыдырау жылдамдығы да ұлғаяды) . Су қоймаларының фенолдардан өздігінен тазартылуы біршама аз жүреді және оның іздері өзен ағынымен ұзақ қашықтыққа өтіп кетуі мүмкін, осыған байланысты лақтырмас бұрын фенолқұрамды ағынды жеткілікті тазартуға ұшыратады. Ағын сулардағы фенол қосылыстарынан жою үшін пероксидаз бен талькты қолдану арқылы Клибанов әдісін модификациялау арқылы жойылады. Перокисдаза фенол қосылыстарын суда ерімейтін полифенолға дейін деградациялайды. Бұл әдісті модификациялағанда, реакциялық қоспаға талькты қосқанда, талькте реакцияның ерімейтін өнімдері абсорбцияланады және ерітіндіден тұнбаға түсуі өтеді. Осы әдіске орай ерітіндіден фенолды толық жоюға мүмкіндік туады және реакция өнімдерінің жойылуы жүреді. Алғашқыда фенол қосылыстарын жою үшін поливинилпироллидин қолданылды. Біршама арзан болғандықтан келесіде тальк пайдаланылды.
Коксохимия зауыттарында фенол құрамды ағын сулар химиялық заттарды аулауға шығындалған шихта ылғалы мен бу конденсатынан түзіледі. Шихта құрамындағы ылғал және пирогенетикалық ылғал кокстеу процесінде түзіліп, кокс газымен бірге камерадан шығады. Газды салқындатқан кезде су буы мен фенол конденсацияланады. Коксохимия зауыттарындағы фенол суының шамамен үштен екісі кокс пешінің камерасына шихтамен берілоген ылғал есебінен түзіледі. Бұл судың мөлшерін азайту үшін көмірді кептіреді. Шихта ылғалдылығын 6 пайызға төмендеткен кезде, Ресейдегі фенол суларын жылына 4 млн. шаршы метрге дейін азайтуға мүмкіндік береді.
Қазіргі уақытта әлем бойынша планетаның су ресурсын ластайтын дәрі - дәрмектер мен оның өнімдерінің метаболизмі санының өсуін белгілейді. Негізінен, дәрі - дәрмектер өзенге түсіп және кейін тұрмыстық канализация мен жануарлар асырайтын ферма арқылы ішетін суға кеп түседі. Фармацевтика зауыттарының ағын суларында біраз мөлшерде активті құрамалар кездеседі.
Егер дәрі өндірісінде уытты қосылыстар қолданылса, ағындар жергілікті тазарту құрылымымен өңдеуге ұшыратады. Ағындарды жергілікті тазарту арқылы қоршаған ортаға тек биологиялық ыдырайтын заттар ғана кеп түсетініне кепілдік береді. Мексикада жаңа фармацевтикалық фабрика салуға шешім қабылдауда осыған ұқсас мәселемен Roche AG компаниясы да соқтығысты. Осы өндірістік аумақтарда ісікті емдеу үшін жоғары эффективті препараттың екі типі өндіріледі. Талдау көрсеткендей, бұл өндірістің ағын сулары қоршаған ортаға критикалық әсер ететін екі түрлі препараттан тұруы мүмкін, сондықтан, зауыттың жалпы канализациясына түспес бұрын жергілікті тазарту құралдарынан өтуі керек. Тазарту құралдарының өнімділігі тәулігіне 10 м 3 құрайды. Бір уақытта ағын суларда жоғарыда келтірілген препараттың тек біреуі ғана қатысады. Roche AG компаниясы EnviroChemie GmbH лабораториялық жағдайда ағындардан микофенолат мофетилді жою әдісі арқылы бірнеге әдістерін ойлап табуды ұсынды және алынған нәтижелерге негіздей отырып, толық масштабты тазартуды жобалау мен құруды алға қояды. Әдісті өңдеудің басты міндеті жоғары емесе эксплуатациялық шығында және құрал бағасы аз болатын жағдайда ағын сулардан дәрілік препараттарды жоюға мүмкіндік туғызу. Капецитабинмен (capecitabine) тәжірибені Германияда Дуйсбург қаласынының IUTA (Institute of Energy and Environmental Technology e. V. ) институтында өткізілді. Мүмкіндікті анықтауда ағын суларды өңдеу үшін активтелген көмірді қолдану Швейцарияда Roche Basel зерттеу орталығында өткізіледі. Зерттеушілер лабораториялық жағдайда ағын сулардан белсенді құрамаларды жоюдың үш әдісін зерттеді. Ағын құрамындағы фармацевтикалық препараттардың ыдырауының эффективтілігі жағынан және экономикалық көзқарас бойынша әрбір тазарту әдісі бағаланды. Ультракүлгін сәулелендірумен тотықтыру мен сутек пероксидімен (H 2 O 2 ) немесе актвителген көмірмен адсорбиялау әдістеріне қарағанда анағұрлым эффективті әдіс ретінде озонмен тотықтыру танылған. Сол сияқты берілген зауыттың басқа да аумақтарында қолданылатын қышқыл, негіздермен немесе натрий гипохлоридімен өңдеу мүмкіндіктері де қарастырылды, бірақ бұл реагенттер бірнеше себептерге байланысты қолданылмайды. Лабораториялық зерттеу нәтижелері көрсеткендей, микофенолат мофетил икапецитабенді жою үшін үш әдістің кез келген біреуі қолданылуы мүмкін, бірақ нақты жағдайда тазартуды оптималды жолмен жүргізуге мүмкіндік беретін патенттелген Envochem ® технология бойынша озондау әдісімен өтеді.
Капецитабинді озонмен тотықтыру зерттеу нәтижелері 1 суретте көрсетілген. Тәжірибе үшін концентрациясы 200 мг/л болатын сынамалар таңдалды. Тотығу процесі 20 минут аралығында өтеді және 18, 33 г озонды қолданады. Бүл мәліметтер негізінде өнеркәіптік қондырғыда озонды максималды қолдану 917 г (38 г/сағ) аспайды.
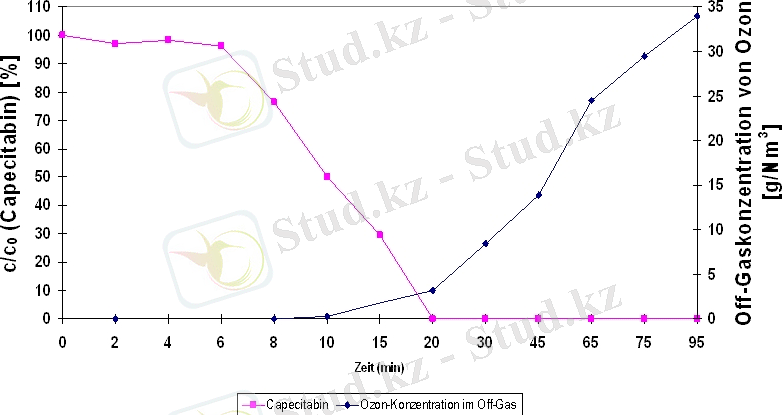
Сур. 1 Капецитабиннің озонмен тотығу зерттеуінің нәтижелері
Микофенолат мофетилдің ыдырау процесі мен өнімдерінің гидролизін зерттеу үшін концентрациясы 25 мг/л болатын сынамалар таңдалды. Бірінші сатыда гидролиз өнімдері зерттелді. Бір тәулік өткен кезде дк ағын суда әрекет ететін құраманың шамамен 80% бар екені анықталды (сур 2) . Тотықтырғыш ретінде озонды қолданғанда барлық микофенолат мофетил толығымен бірнеше минуттың ішінде ыдырап кетеді. Пайдаланатын озонның есептеу саны тәулігіне шамамен 460 г құрайды. Осылайша, екі белсенді құраманы тотықтыру үшін озондағы қажеттілікті салыстыра отырып, мофетилді тотықтыру үшін озонды қолдану көлемі тазартатын құрал өлшемі тағайындалады.
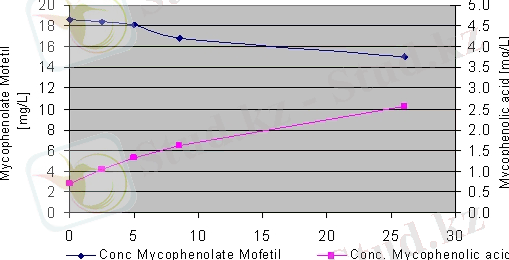
Сур 2. 30 сағат шамасындағы гидролиз нәтижесі
Лабораториялық зерттеу нәтижелеріне негізделе отырып, EnviroChemie GmbH компаниясы Мексикадағы Roche фармацевтикалық зауытының ағын суларының жеке параметрлеріне жауап беретін тазарту құралдарын жобалауды бастады. Жұмыстың нәтижесі бойынша жиырма тонна контейнері бар ағын суларды тазалайтын қондырғы құрыла бастады. Тазартқыш құралдар тәулігіне 24 сағ бойына жұмыс істейді, бұл ағын суларды үздіксіз өңдеуге мүмкіндік береді. Дәрі өндірісінде түзілетін ағын сулар көлемі 15 м 3 болатын жинағыш қорға кеп түседі және кейін ағын суды тазартқыш Envochem ® қондырғысына түседі. Тазартылуға берілетін ағын көлемі жиілікті түрлендіргіші және индуктивті типті шығын өлшемді насоспен реттеліп отырады . Жинағыз қордағы сұйықтық деңгейіне байланысты су шығыны 0, 4 м 3 /сағ - тан 0, 8 м 3 /сағ дейін тербеледі. Өлшенген заттар икемделген фильтрде ұсталып қалады.
1. 2 Ағын суарды органикалық қоспалардан тазарту әдістері. Адсорбциялық тазарту.
Өндірістік ағындарды суда еріген органикалық заттардан толық тазарту мәселесі, соның ішінде фенолдар, анағұрлым маңызды және біруақытта шетелдік өңдеулер болып табылуы мүмкін, берілген мәселені шешімсіз деп айтуға болмайды. Себептері бірнеше болуы мүмкін. Біріншіден, химиялық қиын шешілетін жүйелердің алуан түрлілігі. Осыған қарамастан отандық санның көп болуы мен құрамв және түзілу жағдайына қарамастан әрбір жағдай үшін жекелей зерттеуді қажет етеді, ал бұл әрдайым мүмкін бола бермейді. Екіншіден, суды толық тазарту үшін, ереже бойынша, ерекше жағдайларды талап ететін тәжірибеде қиын орындалатын технологияларды қамтамаыз ете алмайды. Үшіншіден, терең тазартудың көптеген эффективті әдістері үлкен қаржылық және ресурстық шығындарға әкеп соғады, дефицит реагенттерді келесі регенерациямен, утилизациялаумен немесе қалдықтарды көмумен жүзеге асады; және бұл кейбір өнеркәсіптерге орындауға қиындық келтіреді. Сондықтан, өнеркәсіптік ағын суларды тазартудың жаңа эффективті әдістерін табу өзекті мәселе болып қала береді. Көптеген фундаменттік зерттеулерде берілген мәселе бойынша су мен негізгі қоспа фенолдан тұратын моделді жүйелер қарастырылады. Бұл кезде ілескен заттарға жеткілікті мән берілмейді. Суды тазартудың әдістері түрлі қоспа кластарына жекелей қарастырылады: минералды заттар, органикалық өнімдер, еріген газдар және коллоидтық ерітінділер.
Судағы мұнай өнімдерінің концентрациясын ПДК деңгейіне дейін төмендету үшін терең тазарту әдісі қолданылады, ереже бойынша, тазартудың қорытынды сатысында жүзеге асырылады.
Күкірттің жеткілікті жоғары концентрациясында мұнайды өңдеуде ағын құрамы түзіледі, мг/л: мұнай өнімдері - 3000; ұшқыш фенолдар - 5000; БПКтолық - 75000; ХПК - 85000; сульфидтер - 26000; жалпы күкірт -35000; жалпы сілтілік 1 құрайды, рН көрсеткіші 14 тең.
Судағы еріген мұнай өнімдерінің концентрациясы ластау молекуласының химиялық құрамы мен құрылысымен анықталады. Төменде суда анағұрлым көп таралған мұнай өнімдерінің ерігіштік мәндері келтірілген (кесте 1) .
Кесте 1 Суда анағұрлым көп таралған мұнай өнімдерінің ерігіштігі
Келтірілрген талдауға сүйенсек, фенолдың суда жақсы ерігіштігі ерекше қауіпті. Оның басқа да цикллды және ароматты қосылыстары мен спирттері де қауіпті. Судағы фенолдарды қауіпсіздендіру әдісін таңдауда, ең бірінші, ондағы ластың химиялық және топтық құрамын анықтау керек. Кейін талап негізінде, су қалпы мен оның көлеміне неғұрлым эффективті және арзан тазарту әдісі таңдалады. Терең тазартуды шартты түрде екі топқа бөлуге болады: регенеративті и деструктивті.
Ағын суларды еріген фенолдан зиянсыздандырудың деструктивті әдісіне термототықтыру, тотықтырғыш әдістер, сол сияқты электрохимиялық тотықтыру және гидролиз жатады. Деструктивті әдістер ағын сулардан қоспаларды алуда мүмкін болмаған жағдайда немесе экономикалық мақсатта қолданалылады, осы жағдайда, өндіріске фенолды қайтадан қайтармайтын ЭЛОУ-АВТ-4 қондырғысында ағын суларда фенол қоспаларының аз болуы кпезінде жасалады. Ағын суларды зиянсыздандыру үшін дестррутивті әдісті таңдау бастапқы негізде ағын судың шығымы, фенолдың құрамы мен мөлшері тазартылған судың сапасына және оны қайта пайдалануға мүмкіндік туғызуын есепке алады.
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz