Кристалдану энергиясының термодинамикалық негіздері және жылулық әсерлері


МАЗМҰНЫ
- КІРІСПЕ3
- НЕГІЗГІ БӨЛІМ
Кристалдану энергиясы . . . 4
- ҚОРЫТЫНДЫ. . …. . . 8
ҚОЛДАНЫЛҒАН ӘДЕБИЕТТЕР ТІЗІМІ. . . . . 9
КІРІСПЕ
Кристалдану - кристалдардың булардан, ерітінділерден, балқымалардан, қатты күйдегі (аморфты және басқа кристалдық күйдегі) заттардан, электролиз процесі кезінде электролиттерден (электрлік крис-талдану), сондай-ақ химиялық реакциядан пайда болуы. Кристалдану үшін алғашқы (аналық) ортаның термодинамикалық тепе-теңдігі бұзылуы, яғни ерітіндінің немесе будың аса құрғауы, балқыманың асқын суынуы және т. б. жағдайлар орындалуы тиіс. Кристалдануға қажетті аса құрғау немесе аса суыну температураның, концентрацияның, қысымның, фазааралық электр потенциалының тепе-теңдік мәндерінен ауытқуымен сипатталады.
Кристалдану - заттың аса суыған (құрғаған) аналық ортасынан еркін энергиясы төмен кристалдық күйге фазалық ауысуы. Бұл ауысу кезінде артық жылу кристалданудың жасырын жылуы түрінде бөлінеді. Осы жылудың бір бөлігі механикалық жұмысқа айналып, өсетін кристалл үстіне қойылған жүкті көтеріп, ондаған кгс/см 2 қысымға шыдауы мүмкін. Жасырын жылудың бөлінуі балқыманы қыздырып, аса суынуды азайтады да, кристалдануды баяулатады. Нәтижесінде заттың қалыптасуы аяқталады немесе температурасы, қысымы және концентрациясы тепе-теңдік күйге көшеді. Аса суытылған орта кристалданбай, ұзақ уақыт орнықсыз күйде болуы мүмкін. Нашар суытылған булардан, ерітінділерден және балқымалардан пішіні көп жақты кристалдар алынады.
Кристалдану сызаттары (Трещина кристаллизационная) - жік аумағында қыздыру, суыту жылдамдығының өзара алшақты болуынан жікте кристаллиттер аралығында сызаттану, тұтастығының бұзылуы орын алады.
Кристалдану энергиясы
Химиялық таза заттың күйі Т температурамен, p қысыммен және V көлеммен анықталады. Егер осы параметрлердің біреуі өзгерсе зат жаңа күйге өтеді. Егер күйге өту кезінде зат бірінші күйден екінші күйге өткенде үш нұсқаудың біреуі басқаларының шекті және шексіз өзгеруіне шыдамдылық көрсетенде, онда заттың екі күйі де әр түрлі фазаға жатады. Осы аморфтық және сұйық күйлерін негізге ала отырып, бір фазалыққа жатқызуға болады.
Осы үш өлшемнің Т, p, V ішінде екуі ғана тәуелсіз болып келеді. Математикалық тәуелділігі
(1. 1)
Т, p, V өлшемдерін байланыстыратын және үшіншісін екеуінің көмегімен анықтауға болатынын күйдің теңдеуін айтамыз. Күй теңдкуінің нақты математикалық формасы барлық фазаларының айналуына мүмкіндік береді. Тәжрибенің шарттарының анықталуы Т, p, V арасында осы өлшемдерді өлшеу негізінде әр затқа графикалық тәуелділік салуға тәжрибе мүмкіндік береді. Фазалық диаграмма деп осы өлшемдердің арасында тәуелділік орнататын бейнесі мен үлгісін айтамыз.
Заттың энергиясын Т, p, V өлшемдерінің күйін анықтайтын ішкі энергия ретінде санауға болады.
(1. 2)
Мұндағы формуланың мағынасын энергияның өзі емес, ал оның бір күйден екінші күйге өтуі болып табылады. Есептелген 1 г затқа немесе осы өлшемнің шекті немесе шексіз аз болу болмау тәуелділігімен анықталады.
(1. 2) теңдеудің дифференциалды түрі
(1. 3)
немесе
.
Осылайша, Т, p, V өзгеруі ішкі энергияның өзгеруіне сәйкес үш топқа бөлуге болады:
-дың аз өлшемінде бұл қосындылар тәуелсіз және өзгеретін температура, қысым және көлемінің энергиясы болып табылады. Барлық қосынды бірдей энергетикалық бірліктерде анықталуы тиіс.
Пропорционалдық коеффициенті
, (1. 4)
Яғни жылу сыйымдылығы жылыту немесе салқындату кезінде 1г заттың 1°С-қа жұмсалған колорияның санының нөлге жуықтауы. Өлшенетін тұрақты көлем және тұрақты қысымның жылу сыйымдылықтарын және көрсетеді.
Егер зат тұрақты қысым кезінде жаңа күйге өтетін болса, онда теңдеу мынадай түрге келеді:
(1. 5)
Мұнда
Заттың тұрақты көлем кезінде жаңа күйге өткенде мынадай түрге ие болады:
(1. 6)
Практикада кристаллдық заттардың жылу сыйымдылығы тұрақты атмосфералық қысым кезінде -дің аз мәнінде және . Бұл жағдайда мынаны алуға болады:
Жылу сыйымдылықтың температураға тәуелділігінің жалпы заңы (Льюис пен Гибсон бойынша) 1-суретте корсетілген. Х осі бойынша , мұнда және - берілген затты сипаттайтын тұрақтылар. Көптеген заттар үшін =1, өлшемін температураның сипаттамасын айтады.
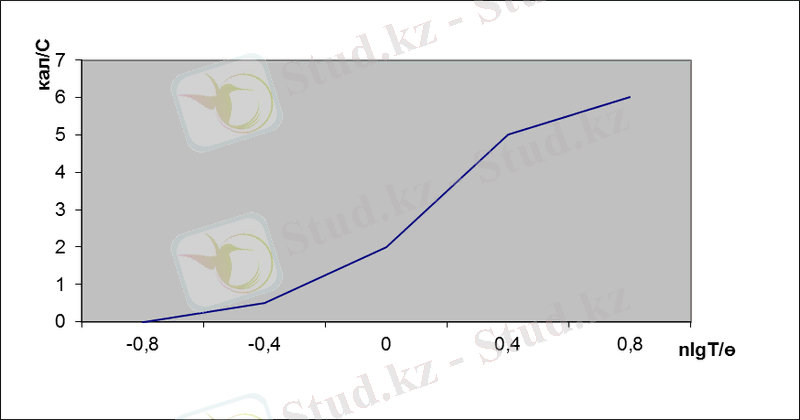
1-сурет. Жылу сыйымдылықтың температураға тәуелдіктің жалпы заңы.
Егер зат бір фазадан екінші фазаға өтетін болса, онда заттың ішкі энергиясы мен жылдам өзгереді, осыған сәйкес жаңа фаза үшін (1. 3) теңдеу мына түрге ие болады:
$dU = c`dT + h`dp + l`dV. $ (1. 7)
Кристалдану кезіндегі жылу сыйымдылық әрқашан бөлінген жылумен сипатталады. Кристалдану кезінде әрқашан энергия; температура бөлінеді де, тұрақты болуы мүмкін.
1г заттың кристалдану энергиясы деп кристалданудың жылу эффектісін айтамыз. Балқу кезінде энергия жойылады. Бірнеше заттар үшін кристалданудың жылу эффектісінің мәндерін келтірейік (1-кесте) . С. Кромптон таза металлдар үшін кристалданудың жылу эффектісінің атомдық салмағын абсолютті балқу температурасына бөлгенде жуықтап 2, 2-ге тең болады:
1-кесте. Бірнеше 1г зат үшін қалыпты қысым кезіндегі кристалдану энергиясы.
П. И. Вальден химиялық байланыс үшін балқудан кейін сұйықтың малекулалық массасымен М аналогиялық тәуелділігін берді:
К. С. Кирхгоф кристалданудың жылу эффектісінің температураға нақты тәуелділігін келесі түрде орнатты. Кристалдануға дейін зат салқындатылған сұйық түрінде Т температураға ие болса, ал кристалданудан кейін - температураға ие болады. Кристалдану процесін екі түрде алуға болады: біріншіден сұйықтың кристалдануын Т температурада іске асыру, ары қарай кристалдық затты температураға дейін жеткізеді.
Заттың кристалдану энергиясының маңызды сипаттамасы ретінде жұмысты алуға болады, яғни заттың өзгеру нәтижесінде алуға болады. Заттың өзгеруі кез келген өзгеріске ұшырасын, ары қарай ішкі энергиясы , жылу эффектісі Q және А жұмысы өзгереді. Бұл өзгерістер заттың жаңа күйге, жаңа фазаға өтуі мүмкін. Энергияның сақталу заңына сәйкес U ішкі энергия Q жылу эффектісі мен A жұмыстың алгебралық қосындысына тең болуы тиіс:
(1. 8)
... жалғасыТермодинамиканың екінші заңына сәйкес
- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz