Spark кешені арқылы әртүрлі еттердің каталаза белсенділігін анықтау және өнім сапасын бағалау


Қарағанды қаласы Химия-биология бағытындағы
Назарбаев Зияткерлік мектебі
Секция: Химия
Ғылыми жоба
Тақырыбы: Spark кешені арқылы әр түрлі еттердегі ферменттердің белсенділігі арқылы олардың сапасын анықтау
Орындаған: 10C сынып оқушысы Акишев Арслан & 10D сынып оқушысы Зарубай Алихан
Жетекшісі: Химия пәнінің мұғалімі Казбекова М. Т.
Қарағанды 2014
Мазмұны
Кіріспе . . ……… . . . ……… . . . 3
I. Теориялық бөлім. … . . . 3
1. 1 Каталаза . . . … . . . …. 3
1. 2 Сутегінің асқын отығы. 51. 3 Липидтердің асқын отығы . . . 6
II. Тәжірибелік бөлім …. . . . . … . . . 12
Өнім сапасын анықтау . . . … . . . ……… . . . 12
Тәжірибелік бөлімі . . . . … . . . 16
Фотоесеп . . . 22
Қорытынды . . . 15
Әдебиет тізімі . . . 16
КІРІСПЕ
Жұмыстың жалпы сипаттамасы
Мәселенің өзектілігі: бүгінгі таңда біз өнімнің сапасыз жеткізілу мәселесімен таныспыз. Еттерді сатып алған кезде оның нақты сақталу мерзімін білмейміз және әр түрлі сақтау мерзімімен сатылады. Ет өнімдерін қоймаларда сақталу нормаларын сәйкес емес. Сонымен, сақтау кезіндегі Еттің сақталу мерзімін қалай анықтауға болады?
Жұмыстың мақсаты: еттердегі каталазаның бөліну деңгейін талдап және берілген өнімнің нақты сақталу мерзімінің уақытын білу.
Жұмыстың мәселелері:
- Ұзақ мерзімді сақтау кезіндегі еттер өнімінің сапасын анықтау.
- Уақыт бойынша ет өнімдерінің сақтау мерзімін анықтау.
- Spark кешеніарқылы каталаза бөлінуімен сутек асқын отығының еттерге әсер етуі кезіндегі ет өнімдерінің сапасын анықтау.
- Spark кешеніарқылы нәтижелерін талдау және еттердегі каталазаның бөлінуі жөніндегі есеп кестесін құрастыру.
- Зерттеу бойынша қорытынды.
I. ТЕОРИЯЛЫҚ БӨЛІМ
1. Каталаза
КАТАЛАЗА -метаболизмнің ең жоғары жылдамдығы бар кең таралған антиоксидантты фермент. Ол тірі тіндерде болады және сутегі асқын тотығын су мен молекулалық оттегіге дейін ыдыратуға қатысатын негізгі клиникалық фермент болып табылады. Құрылымы мен реттілігіне сәйкес каталазаларды үш классқа бөлуге болады, атап айтқанда монофункционалды каталаза немесе Типтік каталаза, каталаза-пероксидаза және псевдокаталаза немесе Mn-каталаза. Заттарының ыдырауы Н2О2 көмегімен тотығуы кесте бойынша:
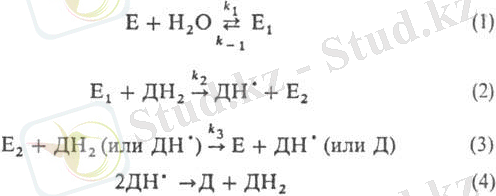
E, E1 и E2- каталазаның бастапқысы және оның тотыққан түрлері; ДН2, ДН• и Д- бастапқысы, жартылай тотыққан және тотыққан субстраттар; k-реакция жылдамдығының константасы.
1 Реакция кері жүрмейді (k1/k_1 > 108) . Ең ақырын кезең - 3 реакция. Каталаза H2O2ге жоғары белсенді және субстраттқада (жоғары өзіндікті көрсететіндер Каталаза белгілі)
Каталаза барлық ферменттердің ішіндегі ең жоғары ферментативті реакция жылдамдығына ие; бір каталаза молекуласы миллиондаған сутегі асқын тотығы молекулаларын секундына су мен оттегіге айналдыра алады. Каталаза-әрқайсысының ұзындығы 500-ден астам аминқышқылдарының қалдықтары бар 4 полипептидтік тізбектің тетрамері. Оның құрамында ферменттің сутегі асқын тотығымен әрекеттесуін қамтамасыз ететін 4 гемма (порфирин+темір) бар. Жануар каталазасы үшін оңтайлы рН мәні шамамен 7 және өте кең максимумға ие (реакция жылдамдығы 6. 8 - 7. 5 РН мәндері арасында айтарлықтай өзгермейді) . Жануарларда каталазаның ең жоғары деңгейі бауырда, бүйректе және эритроциттерде кездеседі, онда ол сутегі асқын тотығының ыдырау реакциясының көп бөлігін катализдейді деп есептеледі.
Каталазадағы сутегі асқын тотығы белсенді орталыққа жеткенде, ол asn148 (148 позициядағы аспарагин) және His75 аминқышқылдарымен әрекеттеспейді, бұл оттегі атомдары арасында Протонның (сутегі ионының) тасымалдануын тудырады. Бос оттегі атомы жаңадан пайда болған су молекуласын босату арқылы үйлестіріледі және Fe(IV) =O. Fe(IV) = O екінші сутегі асқын тотығы молекуласымен әрекеттесіп, Fe (III) -E түзіп, су мен оттегі түзеді.
Каталаза жануарлар жасушаларында кең тараған(жасуша жағдайында және цитоплазмада болады) ; олар фотосинтезде, пероксидтердің мен витаминдердің ауысуында қатысады. Каталаза Белсенділігі және изоферменттік құрамы қатты күйзеліс жағдайда, ағзаға вирустық ауру жұққанда өзгереді.
Каталаза әр түрлі мақсаттарда қолданады(мысалы H2O2 микросанын анықтау үшін, аминдерді, қаршаған ортаның ластануын), сонымен қатар имуннферменттік талдауда. Белсенділік жөніндегі мәліметтер еттерді селкциялау кезінде оқылады.
Каталаза Каталаза сонымен қатар формальдегид, құмырсқа қышқылы, фенолдар, ацетальдегид және спирттерді қоса алғанда, әртүрлі метаболиттер мен токсиндердің сутегі асқын тотығуын катализдей алады. Бұл келесі реакцияға сәйкес жүреді:
H2O2 + H2R → 2H2O + R
Бұл реакцияның нақты механизмі белгісіз.
Пероксидтелген каталаза аралық өнімдерінің үш өлшемді ақуыз құрылымдары ақуыз деректер банкінде бар. Бірақ фермент субстраттардың бірге тотығу реакцияларында ерекшелігін көрсете алады. Биологиялық жүйеде жүріп жатқан процесстеріндегі функционалды рөлін көрсету үшін ғана емес, сонымен қатар ферменттердің әсер ету механизімін түсіндіреді. Жануарлардың арнайы органдарында ферменттердің әсер ету мүмкіндігін келтіру.
I) қосылыстың түзілуі
Сутегі асқын тотығы молекуласы каталазаның гем тобымен байланысқан кезде темір атомы тыныштық күйінен (Fe(III) ) аралық күйге (Fe(IV) ) тотығады, сонымен бірге сутегі асқын тотығы молекуласын су молекуласына (H2O) дейін төмендетеді. Бұл реакция құрамында жоғары реактивті оксоферрил орталығы (Fe(IV) =O) және порфирин негізіндегі радикал (π-катиондық радикал) бар I қосылыс деп аталатын аралық өнімнің пайда болуына әкеледі.
II) қосылыстың пайда болуы және тыныштық күйін қалпына келтіру
Екінші кезеңде сутегі асқын тотығының басқа молекуласы порфирин негізіндегі радикалға электронды тасымалдау және оксоферрил орталығын тыныштық күйіне келтіру арқылы i қосылысымен байланысады (Fe(III) ) . Бұл реакция басқа су молекуласын және молекулалық оттегін (O2) түзеді, осылайша ферменттің тыныштық күйін қалпына келтіреді.
Бірге тотығу реакциясын орындау үшін фермент(каталаза) және бірнеше субстраттар қажет, сөйтіп жүйені құрастыратын. Сонымен қатар, субстраттардың бірі ферментті тотығы жағдайына ауыстырады (Е1 и Е2) . Бірақ реакция кезінде, кезекті тотығуда анықталатын, субстраттардың бір біріне әсер етуі байқалады. Жүйенің жұмыс істеу нәтижесінде, бір субстраттың басқа субстратқа әсер етуі, тотығудың жылдамдығын он есе және жүз есе арттырады.
1. 2 Сутек асқын тотығы
Түссіз сұйытқы, қысымы 1, 4649 г/см³ ( о С) . Қысым температурасы -0, 46, т. -қайнау - 80, 2 °С. Азот қышқылына ұқсайды. Сумен, этил спиртымен, диэтил эфирымен араласады.
Жоғары концентратты препарат органикалық заттарды жандырады. МnО2 байланыс жанумен коршалады. Денеге тиген кезде, Н2O2 күйдіріп қышыманы болдырады, сол кезде дене ағарады. Зақымдалған жерді сумен жуған кезде олардың бәрі жойылады.
Сақтау кезінде сутек сумен оттекке ыдырайды. Тұрақтылығы қосылғанда көбейеді. Таза препарат (Н2O2 99, 2% барлығымен) жылына 30°С кезінде Н2O2 0, 5-1% жоғалтады. Сутектің ыдырауы сілтіліктік қосындыларды, ауыр металдар тұздарын, органикалық заттарды тездетеді.
Н2O2 ертінділері шыны ыдыста сақталған кезде шыныда сілтілерді алады, сондықтан сутекті сақтау үшін іші парафинмен жабылған ыдысты қолдану қажет. Н2O2 өз өзі ыдырау кезінде қатты жауып керек емес( бірақ препартты шаң түсуден қорғау қажет) . Н2O2 қатты ертінділері(10% жоғары) бар ыдыстарға резиналық тығындарды пайдалануға болмайды.
Н2O2 Сатылатын, ыдырауды белсендету үшін қосылатын(тұрақтандырғыштардың) көптеген санын ұстайды. Бұны Н2O2 таза заттарды алу үшін қолданған кезде есте сақтау қажет.
1. 3 Липидтердің пероксидтік тотығуы
ЛПТ механизімі
Липидтердің пероксидтік тотығуы (ЛПТ ) липидтердің тотығу деградациясы, бос радикалдардың әрекет етуінде негізделеді.
Осы процесстің өнімдерінде малондиальдегид және гидроксиноненал-4. Биологиялық тотығу реакциялары бос радикалдардың, бөлшектердің пайда болуымен сопровождается. Осы радикалдардың химиялық белсенділігін арттырады. Мысалы, олар мембраналардың байытылмаған майлы қышқылдармен реакциясына қатысып, құрылымын бұзады. Антиоксиданттар босрадикалды тотығуды болдырмайды.
1. 4 Антиоксиданттық қорғаныс
Антиоксиданттық қорғаныс бұл оттектің белсенді түрлерінен ағзаның ішкі қорғанысы.
Бұл қалай болады?
Жасушамен алынатын Оттектің 95-98% тотықтыра фосфорилдеу процесін өткен кезде, митохондрий күшімен, суға айналады. Қалған 2-5% ферменттік реакция кезінде оттектің белсенді түріне (ОБТ) айналады.
Сол қалған 2-5% «қарақшылардын» ағза арнайы антиоксиданттық ферменттермен(супероксиддисмутаза, каталаза және ) және мыс пен темір иондарын байланыстыратын арнайы белоктармен (қан альбуминдер, трансферрин, ферритин, лактоферрин) қорғалады. Ақырғылар оксиданттық процестердін өршіткілері болып табылады.
Ағзаның антиоксиданттық қорғанысы:
Антиоксиданттар, бос радикалдардың электрондарын байланыстыра, бейтараптандыратын биологиялық белсенді заттар. Антиоксиданттар ағзада жай жолмен пайда болған бос радикалдардың санын бақылауға алады. Антиоксиданттар ағзадағы органикалық заттардың босрадикалды тотығуы процестеріне бөгет жасайды.
Бос радикалдар бір бос жұптас емес электроны бар атом немесе атом тобы. Қалыпты химиялық қосылыста барлық электрондар(кері зарядталған частица) заряды атом ядросының протондардың оң зарядтарымен теңеседі. Егер электрон жұпсыз болса, оған молекула немесе атом оңай қосылады. Сөйтіп, ағзаға зиян келтіретін химиялық реакция пайда болады.
Бос радикалдар ағзада аздаған мөлшерде болады, оларды сау ағза бақылайды. Қалыпта иммундық жүйесінің бос радикалдары вирустармен бактерийларды жояды, басқа бос радикалдар гармондардың өндірілуімен ферменттік процесстердің белсенділігінде, энергияның өңдеуінде және басқа да маңызды процесстерде қатысады.
Бос радикалдардың көпшілігі олардың санын көбейтеді, бұл ағзаның жұмысы қиындатып оған зардабын тигізеді. Бос радикалдардың көптігінен генетикалық кодтын ауысуы мүмкін және ақуыздардың құрылымы бұзылады. Иммун жүйесімен келген аққуыздар бөтен деп танылып, оларды жоюға тырысады. Ақуыздардың өзгерген сандарының өсуі, жағдайға байланысты әр түрлі аурулардың себебі болуы мүмкін, мысалы жүрек, ісік аурулары.
Бос радикалдар жасуша мембраналарын бұза алады; ісік процесстеріне, ағзаның тез қартаюына келтіреді. Сонымен қатар ағзаның кальцийді қабылдау мүмкіндігі мен деңгейі азайаып әр түрлі ауруларға әкеп соғады. Оттектің бос радикалдары, сутек оттығы, липидтер пероксиды және басқа белсенді тотықтырғыштар ағзаның терісінде бірнеше субстраттардың биологиялық тотығу реакциясы кезінде қалыптасады.
Оттек, өмірді қамтамасыз етуде - маңызды болып есептеледі: онсыз өмір сүре алмаймыз, бірақ оның артықтығы да зиянды! Бақытымызға орай, ағза онымен, яғни оттектен пайда болған «бос радикалдар» деп аталатын зиянды өнімдермен күресетін әдіс тапты. Бұл бізге жоғары дәрежеде оттектің тотығу қасиеттерін қолдануға мүмкіндік береді, сонымен қатар тірі жүруге (жанбауға) . Антиоксиданттардың аса тотығуынан ағзаны қорғайды.
Осы заттардың ағзада болмағанынан бірнеше секунд ішінде біз қайтыс болушы едік. Біз асты қортқан кезде, энергияны алу үшін, қорғау рөлін, тотығу процесстерін шектейтін антиоксиданттар атқарады.
Антиоксиданттар эндогенді(қалыпта ағзамен өнделетін) және сырттан алынатын ас қорыту заттар, кейбір ферменттер және бізді зиянды өнімдерден қорғайтын басқа биологиялық белсенді заттар. Сізге әсер ететін бос радикалдардың саны не ғұрлым көп болғаны және жалғасуы мен әсер етуінің белсенділігі жоғары болғаны, антиоксиданттардың шығуымен биологиялық бнлсенді заттардың аспен бірге ағзаға түсуі жоғары болу қажет.
Бос радикалдар көзі: жағынды газдар, түтіндеу, соның ішінде темекі түтіні, гербицидтер, пестицидтер және басқа қауіпті химиялық қосындылар, ионды сәулелі оттар, ультрадыбыс, күнде ұзақ қыздырылуы, озонмен, оттекпен немесе басқа да тотықтырғыштармен улану, көңіл күй стресі, физикалық жүктеу соның ішінде жаттығулар, спорт, аэробика, консеванттер мен майлылығы көп тағамдар, аурулардың түрлері: ісік процесстері, артеросклероз және де басқалар.
Биологиялық антиоксидантардың ағзадағы болуы ағзаның қартаюымен, витаминдердің жетіспеушілігімен (мысалы А, Е, С, Р гиповитаминоздарында, улану кезінде) микроэлементтердің әсіресе мырыш пен селеннің жетіспеушілігі кезінде азайады. Адам ағзасындағы кейбір антиоксиданттардың(глутатион, метионин, фосфолипидтер, ) синтездеуіне қарамастан, антиоксиданттық жүйенің басты компаненті болып аспен келетін антиоксиданттық әсердегі нутрицевтиктер саналады.
Антиоксиданттар болып саналатын:
Ферменттер: ағзада синтезделетін супероксиддисмутаза, метионин - редуктаза, каталаза және глутатионпероксидаза;
Кейбір витаминдер мен микроэлементтер: А, С, Е витаминдері, бета-каротин, ликопин, мырыш және селен;
Мелатонин гармоны, таурин аминоқышқылы;
Шөптер - қара жидек, гинко билоба, жүзім, көк шай;
Өсімдіктен алынған биологиялық белсенді компоненттер: теополифенол(көк шай жапырақтарынан) және пентафиллум, ресвератрол (жүзім шырыны), биофлаваноиды және какратиноиды.
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz