Ас тұзы мен теңіз тұзының химиялық құрамының салыстырмалы талдауы


ҚАЗАҚСТАН РЕСПУБЛИКАСЫНЫҢ ҒЫЛЫМ ЖӘНЕ
БІЛІМ МИНИСТРЛІГІ
СЕМЕЙ қаласының ШӘКӘРІМ атындағы МЕМЛЕКЕТТІК УНИВЕРСИТЕТІ
Инженерлік-технологиялық факультет
«Химия және химиялық технологиялар» кафедрасы
Ас тұзы мен теңіз тұзының құрамын салыстырмалы анализдеу тақырыбында
«Табиғи объектілер анализі» пәні бойынша
КУРСТЫҚ ЖҰМЫС
Орындаған:
тобының студенті
Сәлімхан Ернұр
(қолы) (студенттің аты, жөні)
Жетекші
(жетекшінің Т. А. Ж. )
(бағасы) (қолы) (күні)
Семей
2024
Мазмұны
Кіріспе
Натрий хлориді (NaCl) - суда жақсы еритін тұз, ас тұзы деген атаумен белгілі. Тұз - минералды зат болып табылады. Ол өсімдіктердің, жануарлардың және адамның тіршілігі үшін өте маңызды, себебі ол ағзаларда маңызды физиологиялық үрдістерді қамтамасыз етеді: олар қанда тұз қызыл қан жасушаларының тіршілік етуіне қажетті жағдай жасайды, бұлшықеттерде қозғыштық қабілетін қамтамасыз етеді, одан бөлек асқазанда тұз ас қорыту мен тағамды сіңіруге мүмкіндік беретін тұз қышқылын түзеді.
Қазіргі уақытта тұзсыз ешкім дерлік өмір сүре алмайды. Натрий хлориді тұрмыста ас тұзы деген атаумен белгілі, ол оның негізгі құрамдас бөлігі болып табылады. Бұл зат теңіз суында айтарлықтай көп мөлшерде кездеседі, теңіздің тұзды жерін қалыптастырады.
Тұздың өмір үшін қажеттілігі бұрынғы заманнан белгілі болған.
Ас тұзын өндіру ол біздің дәуірімізге дейінгі 3-4 мың жыл бұрын басталғаны туралы деректерді байқауға болады [1] .
Бұрынғы кездері тұз өте қымбат тауар болған. Ломоносов ғалым өз еңбектерінде төрт кішкентай тұз кесегі үшін құл сатып алуға болатынын жазған.
Сол уақыттары тұзды үстелге қымбат тұз салғыштарда қойған, оны сақтап, үнемдеген және мақтан еткен: үстел үстінде тұздың болуы дәулет пен амандықтың белгісі саналған.
Курстық жұмыстың мақсаты:
Осыған байланысты келесі міндеттер қойылды:
1. Ас тұзы мен теңіз тұзынның тарихын, түрлерін, құрамын зерттеу.
2. Зерттеу әдістемесін, реактивтері және материалдарын дайындау.
3. Ас тұзы мен теңіз тұзының құрамын салыстырмалы анализдеуді жүргізу.
1 Теориялық бөлім
1. 1 Тұздың тарихы
Тұздың тіршілік үшін қажеттілігі ежелгі заманнан белгілі болды. Ас тұзын өндіру біздің дәуірімізге дейін 3-4 мың жыл жүргізілгені туралы дәлелдер бар. Апат жағдайларына арнайы тұз жиналып, ақшаның орнына төленді. «Жалақы» мағынасын білдіретін латын тіліндегі "salarium" және ағылшын тіліндегі "salary" сөздері "тұздан" шыққан. Тұздың салдарынан әйгілі "тұз көтерілістері" сияқты халық толқулары мен әскери қақтығыстар, тас тұзы кен орындары мен тұзды су қоймалары үшін соғыстар болды.

Сурет 1. Ең алғашқы тұздың алынуы
Тұз бір кездері қымбат тауар болған. Ломоносов сол кезде төрт кішкене тұзға құл сатып алуға болатынын жазды. Тұз үстелге қымбат тұз шайғыштарда ұсынылды, ол сақталды, үнемделді, онымен мақтанды: үстелде тұздың болуы байлық пен жақсылықтың белгісі болды.
Ресейде тұз жасау туралы алғашқы ескерту 12 ғасырға жатады. Бірақ ол кезде тұз саудасы еркін сауда болды. Ол аң жүні, тері, балауыз және балмен қатар сатылды. Сонымен қатар, тұзды көп мөлшерде шетелге шығаруға рұқсат етілмеді. Ал Михаил Федорович патша тұсында шетелдіктерге тұз сату өлім жазасымен жазаланды. Тұзды алу әрқашан қиын болды. Тас тұзының ең ірі кен орындары Оралда, Донбасс аймағында және Каспий маңы ойпатында болды[2] .
1. 2 Тұздың түрлері және олардың алыну технологиясы
Тұзды алу технологиялары. Кейбір өсімдіктердің жағымды тұзды дәмі бар екені бұрыннан анықталған. Мұндай өсімдіктерді ежелгі адамдар кептіріп, кейін отқа жағып жіберген. Алынған күл тағамға дәмдеуіш ретінде пайдаланылды. Кейінірек адамдар отта жанып жатқан ағаш кесектеріне теңіз немесе көлдің тұзды суын сеуіп, қалған күлді тамаққа пайдалануды үйренді.
Біздің дәуірімізге дейінгі екі мың жыл бұрын қытайлықтар ас тұзын теңіз суын буландыру арқылы алуды үйренді. Теңіз суынан тұзды буландыру арқылы алу әдісі басқа елдерде де дербес ойлап табылған. Бастапқыда ол климаты құрғақ және ыстық елдерде - Үндістан, Греция, Римде пайда болды. Кейін тұзды осы әдіспен Франция, Испания және Қырымда өндіре бастады.

Сурет 2. Тұздың әр түрлері
Еліміздің солтүстігінде теңіз суы үлкен ыдыстарда буландырылған (қайнатылған), ал энергия көзі ретінде ағаш пайдаланылды. Дегенмен, солтүстік облыстарда, атап айтқанда, Ақ теңіз жағалауында теңіз суынан тұз алу әдісі айтарлықтай жетілдірілді. Поморлар теңіз суы қатқан кезде мұздың тұзсызданатынын, ал қалған қатпаған судың әлдеқайда тұзды болатынын бұрыннан байқаған. Мұзды еріту арқылы теңіз суынан тұщы су алуға болады, ал тұзды ерітіндіден ас тұзы аз энергия шығынымен қайнатып алынды [2] .
Теңіз суының ащы дәмі бар және ас тұзының сулы ерітіндісіне ұқсамайды. Бұл теңіз суында натрий хлоридінен басқа да тұздардың бар екенін білдіреді. Теңіз суындағы тұздардың орташа мөлшері (%) келесідей: NaCl - 77, 8, MgCl2 - 10, 9, MgSO4 - 4, 7, KC1, K2SO4 - 2, 5, CaCO3, Ca(HCO3) 2 - 0, 3, басқа тұздар - 0, 2. Теңіз суының ащы дәмін дәл осы магний тұздары тудырады.
Теңіз суы 20-35°С температурада буланған кезде ең алдымен аз еритін тұздар - кальций, магний карбонаттары және кальций сульфаты бөлінеді. Содан кейін көбірек еритін тұздар - натрий және магний сульфаттары, натрий, калий, магний хлоридтері және олардан кейін калий және магний сульфаттары шөгеді. Тұздардың кристалдану реті және алынған шөгінділердің құрамы температураға, булану жылдамдығына және басқа жағдайларға байланысты біршама өзгеруі мүмкін. Ылғалды ауадағы ас тұзы дымқыл болады[3] .

Сурет 3. Тұздың алынуы
Таза натрий хлориді-гигроскопиялық емес зат, яғни ол ылғалды тартпайды. Магний мен кальций хлоридтері гигроскопиялық болып келеді. Олардың қоспалары әрдайым дерлік ас тұзында болады және олардың арқасында ылғал сіңеді. Бүгінгі таңда тұзды алудың әртүрлі технологиялары бар.
Бүгінгі таңда тұздың көптеген түрлері бар. Олардың арасында классикалық және экзотикалық түрлері бар деуге болады. Біріншісі біздің рационымызға әлдеқашан енген. Олар ұзақ уақыт бойы және бүгінгі күнге дейін тамақ дайындауда және әртүрлі дәрілік және косметикалық өнімдерді жасауда қолданылады:
⎯ Ас тұзы-көп қоспасыз қарапайым тұз.
⎯ Йодталған тұз-йодпен жасанды түрде байытылған натрий хлоры, ол адамдар йод тапшылығынан зардап шегетін аймақтарда өте танымал.
⎯ Фторланған тұз-фтормен байытылған, тіске пайдалы.
⎯ Диеталық тұз құрамында натрийдің аздығымен ерекшеленеді, бұл оның дәмін сәл өзгеше етеді.
⎯ Теңіз тұзы-теңіз суынан алынатын тұз, әдетте табиғи түрде (күн сәулесінің әсерінен судың булануы) немесе буландыру арқылы.
Ас тұзы келесі түрлерге бөлінеді:
- алыну әдісі бойынша - буландырылған тұз, тас тұзы, тұндырылған және таза тұндырылан тұз;
- сапасы бойынша сұрыптар - экстра, жоғары, бірінші және екінші;
- түрі бойынша - қоспасы бар және қоспасыз тұз;
- ірілігі бойынша - буландырылған және 0, 1, 2 және 3 типті ұнтақталған.
- Тас тұзы жылу және сумен өңделмей, шахталық және карьерлік әдістермен алынады. Осы ұзақ уақыт бойы барланған тас тұз кен орындарының бірі Орынбор облысындағы Илецк қаласына жақын жерде орналасқан. Бұл кен орнының тұзды күмбезінің ұзындығы 2 км, ені 1 км, тереңдігі 1 км. Пермь облысында ең бай сильвинит кен орны пайдаланылады. Бұл NaCl және KCl-ден тұратын тұзды тау жынысы. Оны тыңайтқышқа өңдегенде KC1 алынады, ал NaCl қалдық болып табылады.
Қарапайым сумен жуу арқылы (KCl NaCl-ге қарағанда жақсы ериді) 98% техникалық тұз алынады[4] .
- Буландырылған тұз табиғи жер асты тұз ерітінділерінен буландыру арқылы алынады. Біздің елімізде татар ханы Бату мен оның ұрпақтарының билігінен бастап, климаты құрғақ және ыстық Төменгі Еділ бойындағы көлдерден тұз алынды.
- Тұндырылған тұз теңіз немесе тұзды көл суын арнайы бассейндерде булану арқылы түзіледі. Оның құрамындағы натрий хлориді басқа түрлерге қарағанда аз (94-98%) . Сонымен қатар, тұндырылған тұзда басқа да көптеген иондар бар, соның арқасында дәмі әртүрлі болуы мүмкін.
- Таза тұндырылған тұз тұзды көлдердің түбінен алынады - табиғи жолмен тұнып қалады. Біздің еліміздегі мұндай тұздың ең ірі кен орындары Элтон және Басқұншақ көлдері болып табылады.
Элтон көлінің зерттеу оның төменгі қабаты саз қабатымен бөлінген екі күшті тас тұзы қабаттарынан тұратынын көрсетті. Төменгі қабаттың қалыңдығы орта есеппен 14, 4 м, ал жоғарғы қабат 18, 25 м. Бұл қабат 150 км2-ден асады . Элтон көлінде ас тұзының мол қоры бар, алайда бұл тұзға қазіргі уақытта Төменгі Еділ бойындағы негізгі шикізат базасы болып табылатын Басқұншақ көлі одан да бай.
1. 3 Ас тұзы мен теңіз тұзының құрамы
Табиғи теңіз тұзының құрамында 97% NaCl (натрий хлориді) және 3% дейін басқа минералдар бар: магний тұздары, кальций тұздары, калий тұздары, марганец тұздары, фосфор тұздары, йод тұздары және т. б. Барлығы 80 химиялық элементтен тұратын 100-ден астам минералдардан тұрады - себебі осының барлығы теңіз суында бар. Бұл тұзды тіршіліктің басынан - теңіз өсімдіктері, жануарлар мен адамдар пайдаланған.
ГОСТ-қа сәйкес, натрий хлоридінен басқа, дәмдеуіштерде аз мөлшерде калий, магний және темір болуы мүмкін. Рұқсат етілген нормалар кестеде көрсетілген:
Кесте 1.
Ас тұзының құрамы
Сондай-ақ ас тұзының сапасының маңызды көрсеткіштері - қосындылардың саны мен мөлшері - сұрыпқа байланысты анықталады. Экстра құрамында шамамен 99, 7% натрий хлориді бар, мұнда бөлшектердің кем дегенде 75% -ы 0, 8 мм-ге дейін, 25% - 1, 2 мм-ге дейін.
Асханалық тас тұзы (тазартылған тұз - экстра) 99. 70% NaCl-нен (натрий хлоридінен) тұрады, өйткені тазарту нәтижесінде барлық микроэлементтер жойылады. Бұл процесс химиялық заттар мен жоғары температураны қолдану арқылы жүреді. Тұз үлкен жасанды пештерде 650 градустан жоғары температурада кептіріледі. Осы процестерден кейін ас тұзы өзінің кристалдық құрылымын өзгертеді, бұл оның адам ағзасында сіңу жағдайларының өзгеруіне әкеледі. Адам ағзасында мұндай тұздың дұрыс сіңірілмеуі денсаулықтың елеулі теңгерімсіздігін тудыруы мүмкін [5] .
Ашық мұхит суында абсолютті концентрацияға қарамастан, негізгі ион концентрациялары арасындағы сандық қатынастар әрқашан бірдей. Тұз құрамының тұрақтылығы, 1884 жылы теңіз суының осы қасиетін дәлелдеген ағылшын химигінің атымен, Дитмар заңы деп аталды. Тұз құрамының тұрақтылығы ірі өзендердің сағалық аймақтарында, сондай-ақ мұхитпен су алмасуы әлсіз болғандықтан айтарлықтай тұзсыздандырылған континентальды теңіздерде (Азов, Қара және Балтық сияқты) сақталмайды. Теңіз тұзының минералды құрамы оны алу технологиясына айтарлықтай байланысты. Сондықтан әдебиетте әдетте мұхит суының бастапқы минералды құрамы қалыпты тұздылықпен беріледі.
Тұздылығы 35 ‰ болғанда мұхит суындағы теңіз тұзының иондық құрамы:
Кесте 2.
Теңіз тұзының құрамы
1. 4 Ас тұзы мен теңіз тұзының химиялық қасиеттері
Егер ас тұзының кристалы суға түссе, ол тез ериді. Na+ және Cl- иондары бір-бірінен оңай бөлінеді. Бұған олардың бетінде оң және теріс зарядтар алып жүретін су молекулалары көмектеседі, олар дипольдер деп аталады.
Бұл процесс электролиз деп аталады: 2 NaCl+ 2H2O= Cl2+ H2+ 2NaOH. Сондықтан ас тұзының ерітіндісі электр тогының өткізгіші, яғни электролиз болып табылады.
Тұздардың химиялық қасиеттері олардың құрамына кіретін катиондар мен аниондардың қасиеттерімен анықталады.
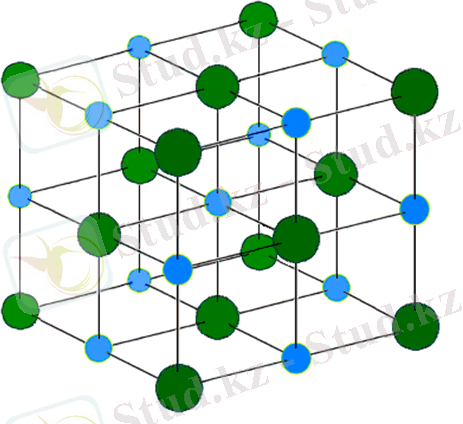
Сурет 4. NaCl криссталдық құрылымының сызбасы
1. Су ерітіндісінде натрий хлориді иондарға диссоциацияланады:NaCl↔︎Na+ + Cl-.
2. Натрий хлориді қышқылдармен және басқа тұздармен алмасу реакцияларына түсуге қабілетті: NaCl + H2SO4 (conc) = NaHSO4 + HCl↑ (pH = 7) (қышқылдармен) ; NaCl + AgNO2 = NaNO2 + AgCl↓ (басқа тұздар) ; NaCl + AgNO3 = NaNO3 + AgCl↓ (басқа тұздар) .
3. Тотығу-тотықсыздану реакцияларында натрий хлориді әлсіз тотықсыздандырғыштың қасиеттерін көрсетеді: 2NaCl + 4H2SO4 (conc) + PbO2 = Cl2↑ + Pb(HSO4) 2 + 2NaHSO4 + 2H2O; 2NaCl + 2H2SO4 (conc) + MnO2 = Cl2↑ + MnSO4 + Na2SO4 + 2H2O.
4. Аммиак пен көмірқышқыл газынан тұратын газдар қоспасын натрий хлоридінің қаныққан ерітіндісі арқылы өткізгенде, натрий гидрокарбонатын алуға болады (тұнбаға түседі) : NaCl + H2O + CO2 + NH3 = NaHCO3↓ + NH4Cl.
5. Балқыма және натрий хлориді ерітіндісі электролизге ұшырайды: 2NaCl + 2H2O = H2↑ + Cl2↑ + 2NaOH; 2NaCl = 2Na + Cl2↑
1. 5 Ас тұзы мен теңіз тұзының қолданылуы
Ас тұзы - химия өнеркәсібінің ең маңызды шикізаты. Одан сода, хлор, тұз қышқылы, натрий гидроксиді, металдық натрий алынады. Топырақтың қасиеттерін зерттеген кезде ғалымдар топырақ натрий хлоридімен қаныққандықтан судың өтуіне жол бермейтінін анықтады. Бұл жаңалық суару каналдары мен су қоймаларын салуда пайдаланылды. Егер су қоймасының түбі NaCl сіңдірілген топырақ қабатымен жабылған болса, онда судың ағуы болмайды. Ол үшін әрине техникалық тұз қолданылады[6] .
Құрылысшылар жер қыста тоңып, қатты тасқа айналмас үшін натрий хлоридін пайдаланады. Ол үшін топырақтың алынуы жоспарланған жерлеріне күзде NaCl қалың себіледі. Бұл жағдайда қатты аяз кезінде жердің бұл жерлері жұмсақ күйінде қалады. Химиктер ұсақ ұнтақталған мұзды ас тұзымен араластыру арқылы тиімді салқындату қоспасын жасауға болатынын жақсы біледі.
Мысалы, 100 г мұзға 30 г NaCl құрамының қоспасы - 20°C температураға дейін салқындайды. Бұл сулы тұз ерітіндісінің нөлден төмен температурада қататындығына байланысты. Демек, температурасы шамамен 0°C болатын мұз қоршаған ортадан жылуды алып, осындай ерітіндіде ериді. Мұз бен ас тұзы қоспасының бұл қасиетін үй шаруасындағы әйелдер де қолдана алады.
Натрий хлориді тағам дайындаудағы ең маңызды дәмдеуіш болып табылады. Ерекше дәмі бар дәмдеуіш, онсыз тағам адамға татымсыз және дәмсіз болып көрінеді. Барлығы адам физиологиясына байланысты. Бірақ адамдар тұзды көбінесе ағзаға қажет мөлшерден көп тұтынады. Тұз дәмдеуіш рөлінен басқа, бұл салада тағы бір маңызды қызмет атқара алады. Кейбір антисептикалық қасиеттеріне байланысты ол консервант ретінде белсенді қолданылады. 10-15% тұз шіріткіш бактериялардың көбеюіне жол бермейді.
Медицинада натрий хлоридінің сулы ерітіндісі (0, 9% немесе 1 литр суға 9 грамм тұз) улы заттарды ағзадан шығару құралы ретінде, дегидратация жағдайында дене жүйелерінің күйін түзету үшін, басқа дәрілік заттардың еріткіші ретінде, іріңді жараларды емдеу үшін (жергілікті) қолданылады. Офтальмологияда жергілікті құрал ретінде натрий хлоридінің ерітіндісі ісінуді басатын әсерге ие.
Ветеринарияда бұл препарат асқазан сөлінің хлорсутек қышқылын түзудің негізгі көзі болып табылады. Ішке қабылдағанда асқазан-ішек жолдарынан жақсы сіңеді, ал ішке енгізгенде тіндер мен мүшелерге таңдамалы түрде әсер ете отырып, қан айналымы жүйесі арқылы таралады. Мұнда медицинадағы сияқты изотоникалық, гипертониялық және гипотоникалық ерітінділер қолданылады. Олардың әрқайсысы белгілі бір мақсаттарға арналған.
Әдіс йодид иондарын сілтілі ортада калий перманганатымен йод иондарына дейін тотықтыруға, қышқыл ортада калий перманганатының артық мөлшерін қымыздық қышқылымен кетіруге, йод иондарын калий йодидімен йодқа дейін тотықсыздандыруға және крахмалдың қатысуымен бөлінген йодты натрий тиосульфатымен титрлеуге негізделген [7] .
2 Эксперименттік бөлім
2. 1 Зерттеу анализ әдістемесі
Зерттеу мақсаты: теңіз тұзының құрамын ас тұзының құрамымен салыстырмалы анализдеу.
Зерттеу міндеттері
- Теңіз және ас тұздарының құрамындағы йодтың массалық үлесін анықтау
- Йод құрамының тұз түріне байланысты айырмашылықтарын бағалау
- Теңіз тұзы мен ас тұзының құрамының ерекшеліктерін аналитикалық әдістер арқылы зерттеу.
Зерттеу әдістемесі
1. Үлгілер дайындау
Зерттеу үшін екі түрлі тұз үлгілері алынды:


Бұл тұздардың құрамындағы йодты анықтау үшін, олардың бірдей мөлшері дәл таразыда өлшеніп, эксперименттер үшін дайындалды.


2. Йодтың массалық үлесін анықтау әдісі
Бұл әдіс калий йодидімен өңделген тұздағы йодтың массалық үлесін анықтауға негізделген.
Әдіс келесі кезеңдерден тұрады:
- Йодид-иондарының тотығуы: Калий перманганаты сілтілі ортада йодид-иондарын йодат-иондарына дейін тотықтырады
- Артық калий перманганатын жою: Қышқыл ортада артық калий перманганаты қымыздық қышқылымен бейтараптандырылады
- Йодтың бөлінуі: Йодат-иондары калий йодидімен қалпына келтіріліп, бос йод бөлінеді
- Титрлеу: Бөлінген йод натрий тиосульфаты ерітіндісімен титрленеді. Бұл үдерісте индикатор ретінде крахмал қолданылады.
2. 2 Зерттеу обьектісі, реактивтері және материалдары
1-кесте. Әдісті орындау үшін қажетті өлшеу құралдары мен қосалқы құрылғылар
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz