Органикалық химия: дәрілік заттардың өндірісі мен синтезі (бром мен йод, алифаттық галоген туындылары, хлороформ және йодоформ, спирттер мен эфирлер, альдегидтер, карбон қышқылдары және уреидтер)


Қазақстан Республикасы Білім және ғылым министрлігі
Е. А. Бөкетов атындағы Қарағанды мемлекеттік университеті
Химия факультеті
Органикалық химия және полимерлер кафедрасы
«Органикалық химия»
1. 8 Әдебиеттер тізімі
Негізгі әдебиет:
1. О. Дайсон, П. Мей. Химия синтетических лекарственных средств. М. : Мир, 1964 - 234 с.
2. Л. Н. Яхонтов, Р. Г. Глушков. Синтетические лекарственные средства. - М. : Медицина, 1983 - 345 с.
3. Л. Д. Проценко, З. П. Булкина. Химия и фармакология синтетических противоопухолевых препаратов. Справочник. - Киев. : Наукова Думка, 1985 - 258 с.
4. М. В. Рубцов, А. Г. Байчиков. Синтетические лекарственные средства. - М. : Мир, 1971 - 267 с.
5. В. В. Племенков. Введению в химию природных соединений. - Казань, 2001 - 376 с.
6. Б. В. Пассет. Основные процессы химического синтеза биологически активных веществ. М. : ГЭОТАР - МЕД, 2002 - 376 с.
7. Р. С. Вартанян. Синтез основных лекарственных средств. М. : МИА, 2004 - 845 с.
8. А. Т. Солдатенков, Н. М. Клядина, И. В. Шендрик. Основы органической химии лекарственных веществ. М. : Химия. 2001 - 192 с.
Қосымша әдебиет:
1. Дж. Марч. Органическая химия. М. : Мир, 1987 (4 т)
2. Г. Беккер. Введение в электронную теорию органических реакций. М. : Мир, 1977
3. А. Е. Агрономов. Избранные главы органической химии. М. : Химия, 1990
4. П. Сайкс. Механизмы реакций в органической химии. М. : Химия, 2006
5. Ли М. Л. Инновационный практикум по органической химии. Электронный учебник. КарГУ, 2003 г.
6. Кенжетаева С. О., Бұркеев М. Ж. Органикалық қосылыстардың теориялық негіздері, Қарағанды, ҚарМУ баспасы, 2007; электрондық оқулық W085 03. 03. 2008 ж.
АНОРГАНИКАЛЫҚ ДӘРІЛІК ЗАТТАР
Көптеген анорганикалық заттар ертеден медицинада қолданылған Олардың негізгі бөлімі тұздарға жатады. Анорганикалық дәрілік заттардың қатарына периодтық жүйедегі барлық топтар элементтері кіреді.
БРОМ ЖӘНЕ ЙОД ДӘРІЛІК ПРЕПАРАТТАРЫН АЛУ
Бром және йод препараттарын алу мәселесі біздің елімізде тек Кеңес өкіметі жылдарында шешілген. 1924-1925 жж. О. Ю. Магидсонның жетекшілігімен бурғылау сулардан йодтың өнеркәсіптік алыну әдісі өңделген. Иод бурғылау суларында төмен концентрацияларда болады (20-40 мг/л) . Бірақ бұл сулардың қорлары үлкен және олар йодты алудың экономикалық тиімді әдісі болып табылады. Йод бұрғылау суларында йод-анионы түрінде болады, сондықтан иодид-анионын I - молекулалық йодқа ауыстыру үшін бурғылау суларын күкірт қышқылымен және натрий нитритімен өңдейді:
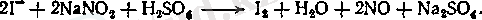
Бөлінген йодты активтендірілген көмірмен адсорбциялайды. Адсорбцияланған йоды бар көмірді бөліп алады және десорбция сатысына қайта жібереді. Десорбцияны немесе 10-15% күйдіргіш натрий ерітіндісімен немесе сульфитпен жүргізеді:
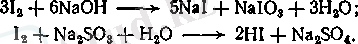
Йодтың көмірдегі концентрациясы 40% дейін жетеді, сол себептен йод тұздарының концентрациясы десорбциядан кейін алынған ерітіндіде бұрғылау суларындағыдан және 4% жетеді. Йодидтің тазартылған ерітінділерін калий хлоратымен немесе натрий нитритімен қышқылдық ортада тотықтырады:
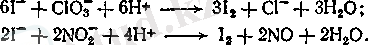
Тотығуды 40-50 °С бірнеше сағат шамасында өткізеді. Бөлінген бос йод түбіне түседі. Оны сүзеді, сумен жуады және 5-7 кг түрінде плиткаларға престейді. Йодтың жақсы сапасын онда минералды қоспалардың және механикалық кірлердің, мысалы, графиттің болмауы бойынша бағалайды. Соңғыны ұнтақталған йодты тиосульфатта еріту әдісімен анықтайды.
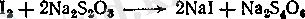
Мөлдір ерітіндінің пайда болуы ерімейтін қоспалардың жоқ екенін көрсетеді. Қазіргі кезде республикамыз йодтың қажеттілігін толығынан өтейді.
Медициналық практикада йодтың 10% және 5% спирттік ерітінділері қолданылады. Йодтың спирттегі 10% ерітіндісін йодты 96% спиртте еріту арқылы, ал 5% спирттегі ерітіндісін- сұйтылған спиртте 2% калий йодидін қосу арқылы дайындайды.
Бромды да бұрғылау суларынан алуға болады жоғарыда сипатталған әдіс бойынша. Сонымен қатар оны теңіз қолтықтарының рапаларынан алуға болады. Теңіз суларында бром көбіне магнийлық тұздар түрінде болады. Тотықтырғыш ретінде бромды бөліп алуда хлорды қолданады:

Молекулалық бром алу үшін оның су буымен айдалу қабілетін қолданады. Бром алу үшін қажет шикізатқа сонымен бірге құрамында осы элемент бар әртүрлі минералдар (карналлит, сильвинит) жатады.
Бром - көптеген дәрілік заттардың синтезінде қолданылатын маңызды шикізат.
Бромидтер және йодидтер (натрийдің және калийдің) медициналық практикада кеңінен қолданылады және фармакопеялық препараттар ретінде шығарылады.
Өнеркәсіпте бромидтерді және йодидтерді әдетте темірдің галоидтық туындылары арқылы алады. Бромидтерді алуда темір жоңқаларын әуелі еритін темір бромидіне айналдырады:

соңынан бромдылау-бромды теміргео:
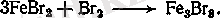
Осы алынған ерітіндіні буландырады және оған натрий карбонатының ерітіндісін қосады:
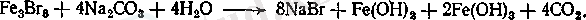
Темір гидрооксидтерінің қоспасын сүзеді. Фильтраттан буландырудан кейін натрий бромиді кристалданады. Натрий иодидін осындай тәсілмен алады:
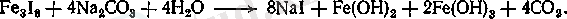
Калийлық тұздарын алу үшін натрий карбонатының орнына калий карбонатын алады.
АЛИФАТТЫҚ ҚАТАР КӨМІРСУТЕКТЕРІНІҢ ГАЛОГЕНТУЫНДЫЛАРЫ
Алифаттық қосылыс молекуласына галоген атомын енгізу бұл қосылыстың биологиялық белсенділігін арттырады және онда есіртетін әсердің пайда болуына әкеледі. Егер метанға СН 4 есіртетін әсер тән болмаса, оның туындысы- хлорлы метил СН 3 С1 адам организміне әлсіз есіртетін әсер тигізеді. Хлорлы метиленде СН 2 С1 2 бұл әсер анық көрсетілетіні сонша, тіпті оны нарозға қажет құрал ретінде ұсынған, әсіресе хлороформның қолданылуы құстыратын жағдайларда. Хлороформ СНСl 3 қазіргі кезде хирургиялық операцияларда наркоз үшін қолданылады. Төртхлорлы көміртек CCl 4 олардан да күшті есіртетін әрекетке ие, бірақ оның улы болуынан оны медициналық мақсаттарда қолданбайды.
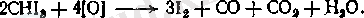
Хлороформ жергілікті жансыздандыратын және жеңіл қоздыратын құрал ретінде сыртқы қолдануға мазьдердің құрамында және химия фармацетикалық өндірісінде еріткіш ретінде қолданылады. Ингаляциялық наркоз үшін хлороформға хирургиялық операцияларда препараттың тазалығы жағынан ерекше талаптар қойылады. Ол жарықта дымқылмен әсер еткенде хлороформ өте күшті улы зат - фосгенді бөліп, баяу ыдырайды:

Сондықтан тиянақты тазартудан кейін наркоздық хлороформды 1% спирт қосып, тұрақтыландырады. Спирттің қатысында фосген зиянсыз қосылыс -көмір қышқылының диэтил эфиріне ауысады:
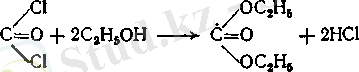
Өнеркәсіпте хлороформды спирттен немесе ацетоннан олардың кальций гипохлоритімен немесе хлорлы әкпен әрекеттесуі арқылы алады. Процесс бумен қыздыруға және сумен суытуға арналған көйлекшесі бар жәнеараластырғыш пен кері салқындатқышы бар болат аппаратында өткізіледі. Реакторға кальций гипохлоритінің 10% ерітіндісін және этил спиртін енгізеді. Реакция басталу үшін қоспаны 45 °С дейін қыздырады. Әрі қарай қайнағанша қыздыру жүретін экзотермиялық реакцияның жылу эффектісі есебінен жүреді. Реакциялық массаны жайлап қайнатуды көйлекшеге алма кезек ауыстырып бу және салқын су жіберу арқылы іске асырылады. Хлороформның түзілуі үш саты арқылы жүреді. Бірінші сатыда спирт ацетальдегидке дейін тотығады:
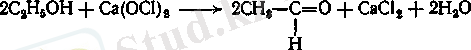
Түзілген ацетальдегид трихлорацетальдегидке (хлораля) дейін хлорланады:
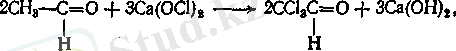
ал хлораль хлороформға және құмырсқа қышқылының кальцийлық тұзына дейін (кальций формиаты) айналады.

Реакцияны келесі реакциялардың қосындысымен бейнелеуге болады:
С 4 Н 6 ОН + 4Са(ОС1) 2СНС1 3 + СаС1 2 + 2Са(ОН) 2 +
Са(НСОО) 2 + Н 2 О
Атап кететін жағдай, хлороформды өндіру барысында жабдықтардың герметизациясы тек қана қауіпсіз жұмыс жағдайларын туғызуға ғана емес, сонымен қатар ауаның қоспасы бу тәріздес хлороформды тотықтырып, оның сапасын төмендетін болғандықтан қажет.
Таза хлороформ түссіз мөлдір сұйықтық болып табылады, арнайы иісі мен өткір дәмі бар. Хлороформның тығыздығы 1, 486 г/см 3 , қайнау температурасы 61, 2 °С, балқу температурасы -63, 5 °С. Хлороформ суда нашар ериді, бірақ спиртпен, эфирмен, бензинмен барлық қатынаста жақсы араласады. Хлороформды спирттен ғана емес, ацетоннан да алады:
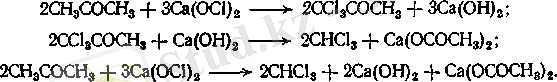
Кальций гипохлоритінің орнына хлорлы әкті CaClOCl қолдануға болады. .
Спирт және ацетон хлороформды электролиттік әдіспен де алуға шикізат болып табылады. Мұнда электролизге спирт немесе ацетонның калий немесе натрий хлоридінің қоспасын да ұшыратады. Процестің схемасы келесідей көрсетіледі:
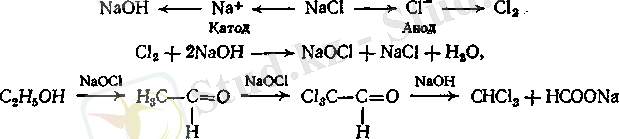
Йодоформды алу әдістері хлороформ алатын әдістерге ұқсас. Бастапқы зат ретінде тағы этил спирті немесе ацетон қолданылады. Тотықтырғыш ретінде калий немесе натрий гипойодитін (KOI, NaOI) қолданады. Бұл тұздар сақтау кезінде тұрақсыз болғандықтан, оларды өндіру барысында йодқа сілтімен әрекет етіп алады:
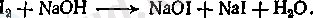
Әрі қарай процес хлороформ алу процесіне ұқсас жүреді.
Хлороформға қарағанда йодоформ қатты кристалдық зат сары түсті, арнайы жағымсыз иіске ие. Балқу температурасы таза йодоформдікі 119°С. 120ºС жоғары қыздырғанда йодоформ ыдырайды. Йодоформ тығыздығы 4, 008 г/см 3 тең. Йодоформ суда ерімейді және этанолда, эфирде және ацетонда жақсы ериді. Мемлекеттік фармакопея препараттағы таза йодоформның құрамын 99% кем болмауын талап етеді. Йодоформның үлкен кемшілігіне оның жағымсыз және қудалайтын иісі жатады. Оны сезіну шектеуі 0, 6 мг/л. Осы кемшілікті жою үшін йодоформға басқа иісі жақсы қосылыстарды (мысалы, ментолды) қосу немесе йодоформды байланыстыру дұрыс нәтижелерге әкелмеді.
СПИРТТЕР ЖӘНЕ ЖАЙ ЭФИРЛЕР
Көмірсутек молекуласына гидроксил тобын енгізу заттың есіртетін қасиетін арттырады. Бірақ молекулада гидроксил тобының саны көбейсе бұл әсер төмендейді. Мысалы, этил спиртінің есіртетін әсері этиленгликольмен салыстырғанда жоғары, ал глицерин мен маннитта мұндай әсер мүлдем жоқ. Манниттің изомері - сорбит қанттың алмастырғышы ретінде қолданылады диабет ауруымен ауратын адамдарға, себебі тәтті болып тадылады. Қалыпты біріншілік спирттердің физиологиялық әсері және улылығы көміртек қанқасының ұзындығы 6-8 атомға дейін артады, соңынан төмендейді. Метил спиртінің ерекше улылығын одан ағзада улы формальдегид және құмырсқа қышқылы түзілетіндігімен түсіндіруге болады. Метил спиртіжүйке және қан тамырларына әсер ететін улы зат, кумулятивті қасиетке ие. Мемлекеттік фармакопея осы топқа жататын келесі препараттардың сипаттайды: спирт этилді, хлорбутанолгидрат, глицерин.
Медициналық практикада этил спирті сыртқы компрестер мен сүртінуге қажет антисептикалық және қоздырушы құрал ретінде қолданылады. ческое Этил спирті жақсы дезинфекциялайтын қасиетке ие және хирургиялық инструменттерді және қолды дезинфекциялауға қолданылады. Спиртті әртүрліше сұйытып, настойка, экстракт және басқа да дәрілік үлгілерді дайындауға қолданылады. Фармацевтикалық практикада спирттің концентрациясын көлемдік пайыз (градус) арқылы өлшейді. Мемлекеттік фармакопея этил спиртінің келесідей препараттарын: сусыз (яғни абсолютті) және шараптық этил спирті 95°, 90°, 70° және 40° деп сипаттайды.
Глицерин мазьдердің негізі және кейбір дәрілік заттардың еріткіші ретінде қолданылады.
Жай эфирлер ингаляциялық наркоз үшін қолданылады. Анестетиктер ретінде олар алифаттық қатардың галогентуындыларына көп ұқсас келеді. Этилді эфирді этил спиртінің күкірт қышқылымен әрекеттесуі арқылы алады. Реакция этилкүкірт қышқылы түзілетін саты арқылы жүреді:
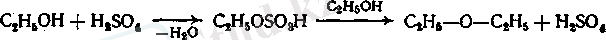
Медициналық эфирді дайындау үшін спирт-ректификат 96° және контактты әдіспен алынған күкірт қышқылы (ең тазалауы) қолданылады. Процесс қорғасынмен жабылған болат аппаратында температуре 130-140 °С жүреді; сонда тұзілген эфир мен су айдалады және енгізілген этил спиртінің бөлшектері. Спирттің реакторға берілуісу, спирт және эфир қоспаларының айдалуы сияқты үздіксіз жүреді.
Эфир өндірісі тұтанғыш және жарылғыш келеді. Эфирдің және спирттің булары жарылғыш қоспалар түзеді. Эфирдің жарылғыш концентрацияларының шектеулері ауамен қосқанда 1, 85-40% (көлем бойынша) құрады. Цехтарда от шығатын жағдай болмау керек және элктрқондырғылары жарылмайтын жерледе болу керек. Инструменттер қоладан немесе мысталған болу керек. Аяқ-киім темір шегелерсіз және тағасыз болу керек. Ауаның дымқылдығыбөлмелерде 70% төмен болма керек. .
АЛЬДЕГИДТЕР, АЛЬДЕГИД ҚЫШҚЫЛДАРЫ ЖӘНЕ ОЛАРДЫҢ ТУЫНДЫЛАРЫ
Альдегидтерде спирттерге тән есіртетін қасиет сақталады. Алкил радикалдарының ұзартылуы улылықтың және физиологиялық әсердің артуына әкеледі. Есіртетін қасиеттер альдегид молекуласына галогенді енгізгенде немесе қанықпаған қосылыстарға көшкенде күрт артады. Альдегид молекуласына карбоксил тобын енгізу оның улылығын күрт төмендетеді. Салыстырмалы төмен улылық гидратты форма түзуге бейім альдегидтерде байқалады. Мысал ретінде хлоральгидратты көрсетуге болады:
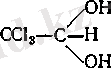
Ол хлоральдың гидраттық формасы болып табылады:
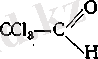
Бқл кластың жеке өкілдері ішінен медициналық практикада қолданылып жүрген және Мемлекеттік фармакопеяға енгізілген формальдегид, уротропин және хлоралгидрат.
Формальдегид СН 2 О 40% сулы ерітінді түрінде өндіріледі. Улылығы жоғары болғандықтан - ол формальдегидтің ақуыздарды байланыстыру қабілетіне ие - ол тек сыртқы дезинфекциялайтын зат ретінде қолданылады. Формальдегид ерітіндісі тканьдерді қатыратын болғандықтан, оны анатомиялық және биологиялық препараттарды консервациялау үшін қолданады. Формальдегидті метил спиртінің катализдік тотығуы арқылы алады:
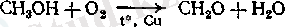
Гексаметилентетрамин (уротропин) формальдегидтің аммиакпен әрекеттесу өнімі. Уротропин альдегидке жатпайды, бірақ күшті қышқылдық ортада қыздырғанда формальдегид түзіп ыдырайды:
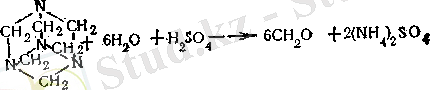
1860 ж. А. М. Бутлеров алған, бірақ медициналық практикада оны тек 35-40 жылдан кейін қолдана бастады. Оны формальдегидтен және аммиактан сұйықфазалық және газофазалық әдістермен алады. Сұйықфазалық әдісте 40% формальдегид ерітіндісіне 25% аммиак ерітіндісінің сәл артық мөлшерін қосады және реакциялық массаны 40-50 °С температурасында араластырады:

Қоспаны активтендірілген көмірмен тазартады, соңынан сүзеді. Фильтратты вакуумда кристалданғанға дейін буландырады. Салқындатқанда уротропин кристаллдары түзіледі, оларды сүзеді, жуады және 30-35 °С температураларында кептіреді. Қосымша тазарту мақсатымен спирттен қайта кристаллдандырады. Газофазалық әдісте газ тәріздес формальдегид, аммиак және азот қоспаларын ыстық реактор арқылы өткізеді. Түзілген су бу түрінде реактордан азотпен бірге кетіп отырады, ал уротропин реактордың түбінде жиналады:
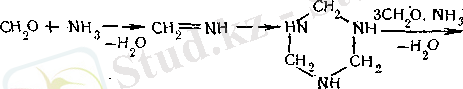

Газофазалық әдіспен алынған гексаметилентетрамин жоғары сапамен алынады. Сонымен қатар бұл әдісте энергия және сулы ерітінділердің булануына жұмалатын уақыт әлдеқайда азырақ жұмсалады.
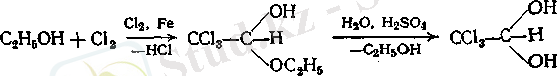
Хлоралгидрат тыныштандыратын және ұйықтататын құрал болып табылады. Үлкен дозаларда ол есірткі зат ретінде әсер етеді және психиатриялық практикада қолданылады. Препараттың қолданылуы дәрігердің бақылауымен жүреді. Хлоралгидратты этил спиртінен алады:
Химиялық сипаттары бойынша осы қосылыстар тобына L-аскорбин қышқылын да жатқызуға болады (витамин С), ол γ-лактон 2, 3-дегидро-L-гулон қышқылының (γ-лактон L-трео-2, 3, 4, 5, 6-пентаоксигексен-2-овой кислоты) .
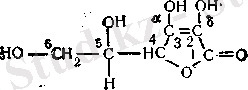
Аскорбин қышқылының молекуласында γ-лактонды сақина бар және γ-лактонның екі қосарланған қос байланыстармен тобы:
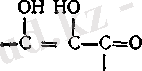
Мұндай жүйелердің маңызды қасиеттеріне олардың қайтымды тотығу-тотықсыздану реакцияларына бейімділігі:
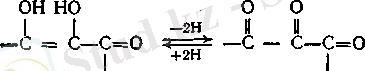
Адамның С витаминіне физиологиялық қажеттілігі күніне 70-100 мг болып табылады. Ауыр қара жұмыстарда және еметін баллары бар аналарға бұл норма күніне 200 мг дейін артады . L-Аскорбин қышқылы жаңа көкөністерде және жемістерде бар.
L-Аскорбин қышқылын концентраттар түрінде"итмұрын жемістерінен, болгар бұрышынан, жасыл грек жаңғағынан алады. Бірақ синтетикалық алыну дістері тиімділеу болады. Синтетикалық аскорбин қышқылын алуда бірінші аралық өнім алтыатмды спирт D-сорбит, оны D-глюкозаның скелетті никель катализаторының үстінде тотықсыздандыру арқылы алады. Тотықсыздануды мыс-хром және темір-кобальт катализаторларының қатысында жүргізеді. Перспективті тотықсыздану әдісіне Д-глюкозаның электролиттік тотықсыздануы жатады.
Аскорбин қышқылы қатты кристалдық зат ақ түсті балқу температурасы 192°С (ыдырайдым) . Ол суда жне метанолда жақсы ериді, баяу - этил спиртінде, нашар - амиловспиртінде, эфирде, бензинде, бензолда және басқа полюссіз еріткіштерде ерімейді. Құрғақ және таза кристалды аскорбин қышқылы ауаның оттегісіне қатысты тұрақты. Сулы ерітінділерде ауаның қатысында, әсіресе сілтілік және қышқылдық орталарда ол тез тотығады.
Таза L-аскорбин қышқылынан басқа, оның тұздары ( натрий, кальций, темір аскорбинаттары) және эфирлері (пальмитаты) медициналық практикада және тағам өнімдерін витаминдерге толтыру үшін қолданылады.
КАРБОН ҚЫШҚЫЛДАРЫ ЖӘНЕ ОЛАРДЫҢ ТУЫНДЫЛАРЫ
Зат молекуласының құрамына карбоксил тобын енгізу оның және улылығын төмендетеді. Органикалық қышқылдардың өзін дәрілік заттар ретінде олардың төмен биологиялық белсенділігінен шектеулі. Майлы карбон қышқылдардың туындылары табиғатта кең таралған және тағамдық заттардыңвых кислот широко расп, әсіресе майлардың құрамында кқп кездеседі. Көміртек тізбегі тармақталған қышқылдардың физиологиялық белсенділігі қалыпты құрылымдағы қышқылдардың белсенділігінен жоғары болады. Карбон қышқылдары фармацевтикалық анализде кең қолданыс тапқан. Медициналық практикада органикалық қышқылдардың кейбір тұздары қолданылады ( калий ацетаты, кальций және темір лактаттары, натрий және мыс цитраттары, кальций глюконаты), олардың эфирлері және амидтері.
Қаныұпаған карбон қышқылдарының биологиялық белсенділігі, барлық қанықпаған қосылыстардікіндей, әлдеқайда жоғары болып келеді. Қанықпаған жоғарғы карбон қышқлдары ішінде үш қышқыл (линоль, линолен және арахидон) ағзада синтезделмейді, бірақ ағзаның дөрыс өмір сүруіне қажетті болады. Бөл қышқылдар алмастырылмайтын майлы қышқылдар болып табылады және оларды кейде F тобының витаминдеріне жатқызады, ол дөрыс емес. Бөл қышқылдар құрамында 18 немесе 20 көміртек атомдары бар және оқшауланған екіден төртке дейін цис-конфигурациялы қанықпаған байланыстар болады:
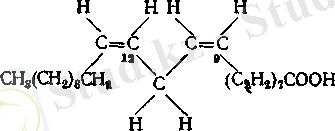
Линоль қышқылы (C 18 ) -9, 12-ди-цис-октадекадиен қышқылы.
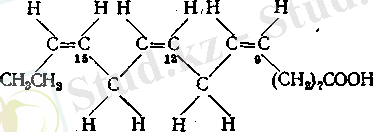
Линолен қышқылы (C 18 ) -9, 12, 15-три-цис-октадекатриен қышқылы.
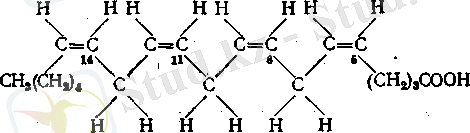
Арахидон қышқылы (C 20 ) -5, 8, 11, 14-тетра-цис-эйкозатетраен қышқылы.
Алмастырылмайтын майлы қышқылдар жануарлар ағзасында қаныққан майлы қышқылдардың тотығуына қатысады, сонсымен майлардың сіңірілуіне және майлардың алмасуына қатысады. Арахидон қышқылының биологиялық белсенділігі линоль және линолен қышқылдарынан 10 есе жоғары.
Линоль және линолен қышқылдары өсімдік майларының құрамында триглицеридтер түрінде, ал кейбір жануарлар тағамдарының құрамында фосфолипидтер түрінде кездеседі. Арахидон қышқылы тек жануарлар майларында кездеседі. Дұрыс тағам құрамында 0, 1% арахидон қышқылы және 1% линоль және линолен қышқылдары болу қажет.
Көмір қышқылына екі амид - толық емес (карбамин қышқылы) және толық (карбамид) сәйкес келеді;
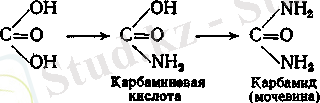
Карбамин қышқылының эфирлерін уретандар деп атайды. Көптеген уретандар ұйықтататын әсерге ие. Мочевина туындылары ішінде медицина үшін оның ацилді туындылары маңызды. Мочевинаның ацилді туындыларын алғаш рет Н. Н. Зинин алған жіне оларды уреидтер деп атайды. Уреидтер ашық тізбекті (ациклді) және тұйық тізбекті (циклді) :
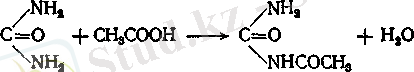
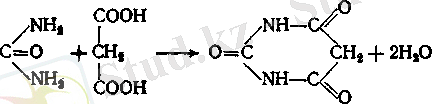
Ашық уреидтер тобына жататын дәрілік заттарға бромизовалды (бромурал) және карбромалды (адалин) жатқызуға болады.
Карбромал адам ағзасына тыныштандыратын және ұйықтататын әсер көрсетеді.
Бромизовал (бромурал), карбромал сияқты, адам ағзасына тыныштандыратын және ұйықтататын әсер көрсетеді.
Техникалық бромизовалды изопропил спиртінен қайта кристалдандырып тазартады. Таза бромизовал - ақ кристалды ұнтақ, ащы дәмді, әлсіз иісті, балқу температурасы 145- 150°С. Ол суда нашар ериді (1:450), бірақ спиртте және эфирде ериді.
Бромурал өндірісінде маңызды мәселе бромның утилизациясы, ол дефицитті шикізат болып табылады. Құрамында бромидтері бар маточный ерітінділерді күкірт қышқылымен өңдейді, ал бөлінген бромсутекті хлормен бромға дейін тотықтырады. Алынған техникалық бромды айдау арқылы тазартады және қайтадан өндірісте пайдаланады.
Медицинаға аса маңызды циклді уреид болып барбитур қышқылы табылады, оның туындылары ұйықтататын препараттар тобын құрайды. Барбитур қышқылы дәрілік қасиеттерге ие емес. Оның қышқылдық қасиеттері оның енодық формасының болуымен түсіндіріледі:
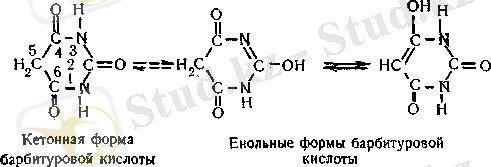
Синтездеу мақсатымен малон қышқылын емес, малон эфирінің туындыларын қолданады, себебі малон қышқылы термиялық тұрақсыз және қыздырғанда жеңіл декарбоксилденеді. Малон эфиріне орынбасушыларды енгізу металдық натриймен және сәйкес бромды алкилмен әсер ету арқылы іске асады:
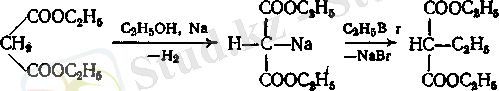
Немесе мырышпен және йодты алкилмен әсер ету арқылы:
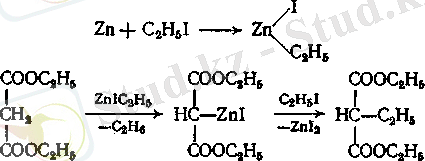 жоғарыда
жоғарыда
Метилен тобының екінші сутегі атомын алкилді орынбасушыға алмастыру үшін процесті қайталайды.
Барбитур қышқылының туындыларын синтездеудің басқа да жолдарын қолданады, кейбіреулерін төменде наұтылы мысалдарда қарастырамыз.
Бұл қатардың препараттары ішінде ең кеңінен таралғаны барбитал (5, 5-диэтилбарбитур қышқылы) . Барбитал (веронал) ең бірінші ұйықтататын құралдардың бірі Ол алғаш рет 1881 ж. сипатталған және медициналық практикада 1905 жылдан бастап қолданылады. Бұл препаратты жоғарыда сипатталған әдіс бойынша алады. Диэтилмалон қышқылының диэтил эфирінің мочевинамен конденсациясын натрий алкоголятының қатысында жүргізеді. Нәтижесінде барбиталдың натрийлық тұзы - мединал алынады:
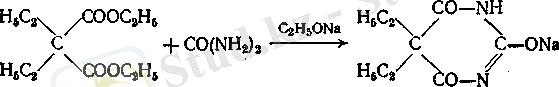
Мединал ерітіндісін таза тұз қышқылымен тотықтырғанда тұнбаға барбитал түседі:
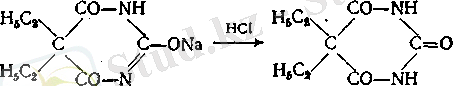
Тұнбаны сүзіп алады және дистилденген судан активтендірілген көмірмен өңдеп, қайта кристалдандырады.
АЛИФАТТЫҚ АМИНДЕР, АМИН ҚЫШҚЫЛДАРЫ ЖӘНЕ ОЛАРДЫҢ ТУЫНДЫЛАРЫ
Алифаттық аминдердің ішінде медициналық практикаға мағызы жоғары болып бис (β-хлорэтил) амин туындылары табылады, себебі олар қауіпті ісіктерге қарсы құралдар ретінде қолданылады. Қауіпті ісіктер - іскен жасушалардың тез көбейіп, жанындағы органдарға қысып әсер етіп, ағзаның жалпы жұмысын бұзатын аурулар.
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz