Күкірт қышқылы өндірісінің технологиясы, шикізаттары және материалдық баланстары


Кіріспе
Химиялық өндіріс күрделі химиялық технологиялық жүйе болып табылады, оның күрделігі көптеген байланыстар саны, элементтер мен жүйелер, сонымен қатар шешілетін мәселелердің әртүрлігіне негізделген. Химиялық өндірістің негізгі мақсаты берілген қасиеті бар химиялық өнімді шикізаттың және қаражаттың аз мөлшерінде алу болып табылады. Химиялық технологиялық жүйенің анализі мен оптимизациялау мүмкіндігі үшін, біріншіден элементтер арасындағы байланыс пен олардың бір-біріне әсерін көрсететін процесс моделін жасау керек. Мұндай модельдің негізгі жүйедегі массалардың балансы болып табылады.
Материалдық балансты есептеу инженер химик-технологтардың проектілі жұмысындағы негізгі сатысы. Материалды баланстар негізінде бірқатар маңызды техникалы-экономикалық көрсеткіштер мен негізгі аппараттардың сипаттамалары анықталады. Материалды баланс мәліметтері бойынша анықтайды: берілген өндіріс үшін шикізат пен керекті материалдар шығымы; жылулық баланс пен оған сәйкес энергия шығымы мен аппаратураның жылуалмасуын; өндірістің экономикалық балансы, өнімнің өзқұңдылығы мен оған сәйкес өндірістің өнімділігі. Материалды баланс өндірісті дамыту дәрежесін (шикізатты қолданудың комплекстілігін, қалдық номенклатурасы мен көлемін), сонымен қатар шығым себептерін анализдеуге мүмкіндік береді. Балансты есептегенде ереже бойынша 5 % аспайтын, механикалық шығымды негізге алады. Бұл шығымдар технологияның дамыуның арта қалуымен немесе аппаратураның істен шығуымен ғана емес, сонымен қатар жалпы өндірістің мәдениетімен анықталады [1] .
КҮКІРТ ҚЫШҚЫЛЫНЫҢ ТЕХНОЛОГИЯСЫ.
Химиялық өндіріспен өндірілетін, химиялық минералдар арасында күкірт қышқылы өнідіріс көлемі мен тұтыну көлемі бойынша бірінші орында. Бұл оның басқа қышқылдарға қарағанда арзандығымен және қасиетімен түсіндіріледі. Күкірт қышқылы түтінденбейді, концентрленген түрде қара металлдарды бұзбайды, сонымен қатар күшті қышқылдардың бірі болып табылады, температураның кең диапазонында (40-тан…-20-дан 260-336, 5 ºС) сұйық күйде болады.
Күкірт қышқылының қолданылу аясы өте кең. Оның маңызды бөлігі химиялық өндірістің салаларында жартылай өнім ретінде, біріншіден минералды тыңайтқыштар (30 дан 60%) алуға, сонымен қатар тұздар, қышқылдар, жарылғыш заттар алуда қолданылады. Күкірт қышқылы бояғыш заттар (2 ден 16%), химиялық талшықтар (5 тен 15%) өндірісінде, металлургияда (2 ден 3%), тоқыма және тамақ өнеркәсібінде қолданылады.
Сонау XIII ғасырда күкірт қышқылын аз мөлшерде темір купоросының FeSO 4 термиялық ыдырауы нәтижесінде алатын, сондықтан қазір де күкірт қышқылының кейбір түрлерін купоросты май деп атайды, дегенмен қазіргі уақытта күкірт қышқылы купоростан өңдірілмейді. Сурет 1 күкірт қышқылының қолданылу аясы көрсетілген.
Сурет 1. КҮКРТ ҚЫШҚЫЛЫНЫҢ ҚОЛДАНЫЛУ АЯСЫ.
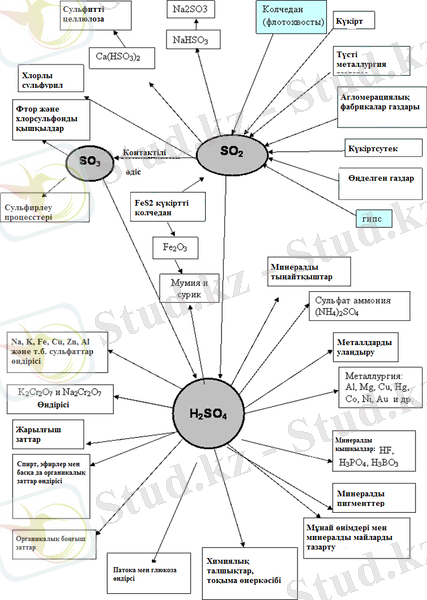
Күкірт қышқылы жекелей химиялық қосылыс H2SO4 ретінде, сонымен қатар сумен қосылыс түзіп те өмір сүре алады
H 2 SO4*2H 2 O, H 2 SO4*H 2 O, H 2 SO4 *4H 2 O және күкірт үш оксидімен H 2 SO4 *SO3, H 2 SO4*2SO3.
Техникада күкірт қышқылын сусыз H 2 SO4 және сулы ерітінділерін (іс жүзінде H 2 O мен H 2 SO4 және H 2 SO4*nH 2 O қосылыстар қоспасы), сусыз H 2 SO4 күкірттің үш оксиді - олеум атайды.
Сусыз күкірт қышқылы - ауыр, майлы, сумен және күкірттің үш оксидімен кез-келген қатынаста араласатын сұйықтық. Күкірт қышқылының тығыздық, кристаллизация, қайнау температуралары сияқты физикалық қасиеттері оның құрамына байланысты.
Сусыз 100% күкірт қышқылы салыстырмалы түрде жоғары кристалдану температурасына ие 10, 7ºC. Тасымалдау мен сақтау кезінде тауарлы өнімнің қатып қалу мүмкіндігін төмендету үшін техникалық күкірт қышқылының концентрациясын кристаллдану температурасы төмен болатындай таңдайды. Өндірісте тауарлы күкірт қышқылының үш түрін шығарады (мұнаралы, кантактілі күкірт қышқылы және олеум) .
Күкірт қышқылының қайнау температурасының атмосфералық қысым кезіндегі құрамына тәуелділігі сурет 2 көрсетілген. Фазалық тепе-теңдіктің бұл диаграмманың төмеңгі қисығы сұйық фаза құармына, жоғарғысы - қайнап жатқан сұйықтықпен тепе-теңдікте болатын булы фазасына сәйкес келеді. Диаграммадан күкірт қышқылы мен су максималды қайнау температурасы (336, 5˚С) бар, 98, 3% H2SO4 пен 1, 7% H2O тұратын азеотропты қоспа түзетіні байқалады. Сұйық және бу фазасында тепе-теңдікте болатын қышқылдың азеотропты концентрациясы үшін құрамдары бірдей; қышқылдың сұйытылған ерітінділерінде бу фазасында су буы артық болады, олеумның бу фазасында SO3 тепе-теңдік концентрациясы артық болады.
Сурет 2. Күкірт қышқылының атмосфералық қысымдағы қайн. температурасы.
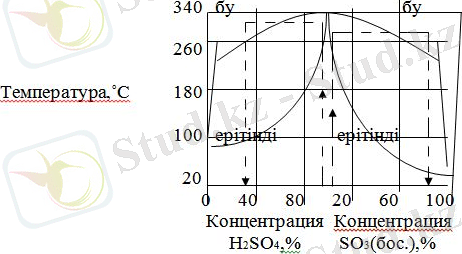
Күкірт қышқылының қарастырылған қасиеттері процесстің технологиялық режимін таңдауда, сонымен қатар жекелей аппараттарды проектілеуде ескеру қажет. Мысалға, цехты ашық жерде орналастырғанда, жоғары кристализация температурасына ие күкірт қышқылының циркуляцияланатын трубоөткізгіштердің жылуизоляциясын қарастыру керек. Сұйық пен будың фазалық тепе-теңдік диаграммасын ескеру нәтижесінде, мысалға күкіртті қышқылдың тұманның түзүлуі сияқты қосымша құбылыстарды болжауға және абсорбцияның жоғары дәрежесін қамтамасыз ететін, күкірттің үш оксидінің абсорбция сатысын жүргізудің тиімді жағдайларын таңдауға мүмкіндік береді[2] .
КҮКІРТ ҚЫШҚЫЛЫ ШИКІЗАТЫ МЕН АЛУ ӘДІСТЕРІ.
Күкірт қышқылының негізгі реагенттері ретінде, күкіртті немесе күкірттің диоксидін алуға болатын, күкірт немесе күкірт құрамды қосылыстар қолданылады.
Шикізаттың негізгі көзі күкірт және темір (күкіртті) колчеданы болып табылады. Күкірт қышқылының жартысына жуығы күкірттен алынса, үш бөлігі - колчеданнан алынады. Шикізаттың баланстағы маңызды орынды құрамында күкірт диоксиді болатын, түсті металлургиядан шығатын қалдық газдар алады.
Сол уақытта қалдық газдар - арзан шикізат, колчеданның да бағасы төмен, ал ең қымбат шикізат күкірт болып табылады. Яғни, күкірт қышқылын күкірттег өңдеу экономикалық тұрғыдан, колчедан мен қалдық газдардан өңдіруден анағұрлым арзан болу үшін, арнайы өңдеу сызбасын жасау қажеттілігі туындап отыр. Кесте 1 күкірт қышқылын әртүрлі шикізат түрлерінен өңдірудің негізгі техникалық-экономикалық көрсеткіштері 1 кестеде келтірілген.
Кесте 1. Күкіртті колчедан негізіндегі күкірт қышқылын өндірудің негізгі техникалық-экономикалық көрсеткіштері, %
Күкірт қышқылын алу бірнеше сатыдан тұрады. Бірінші сатысында күкірт құрамды шикізатты күкірт диоксидіне дейін күйдіреді (бұл саты шикізат ретінде қалдық газдарды қолданғанда, қолданылмайды, себебі бұл жағдайда сульфидтерді күйдіру басқа технологиялық процесстердің бөлігі болып табылады) . Келесі сатыда - күкірт (IV) оксидін күкірт (VI) оксидіна айналдыру. Бұл тотықтыру процессі аса жоғары активация энергиясымен сипатталады, оны төмеңдету үшін катализаторды қолданады. SO2 -ні SO3 - ке тотықтыру процессінің жүзеге асуына тәуелді күкірт қышқылын алудың екі түрі ажыратылады.
Күкірт қышқылын алудың контактілі әдісінде SO2 - ні SO3 -ке дейін тотықтыру қатты катализаторларда жүргізіледі.
Күкірттің үш оксидін күкірт қышқылына айналдыру соңғы сатысында - күкірттің үш оксидін абсорбциясында жүзеге асады, оны келесі теңдеумен сипаттауға болады:
SO3 + H 2 O🡪 H 2 SO4
Процессті нитрозды әдіс бойынша өткізгенде оттектің тасымалдаушысы ретінде азот оксидтерін қолданады.
Күкірт диоксидінің тотығуы сұйық фазада өтіп, нәтижесінде соңғы өнім күкірт қышқылы болады:
SO2 + N 2 O3 + H 2 O 🡪 H 2 SO4 + 2NO
Қазіргі уақытта өндірісте күкірт қышқылын өндірудің контактілі әдісі қолданылады, себебі бұл әдіс жоғары интенсивті аппараттарды қолдануға мүмкіндік береді [3] .
КҮКІРТ ҚЫШҚЫЛЫН ӨҢДІРУДІҢ КОНТАКТІЛІ ӘДІСІ.
Күкірт қышқылын екі түрлі шикізат түрінен алу процесстерін қарастырайық: күкіртті (темір) колчеданы мен күкірт.
H 2 SO 4 колчеданнан алу.
Процесстің бірінші сатысы құрамында күкірт диоксиді бар, шикізатты күйдіргіш газға дейін тотықтыру болып табылады. Шикізат түріне байланысты күйдірудің экзотермиялық химиялық реакциялары жүзеге асады:
4FeS 2 +11O 2 = 2Fe 2 O 3 + 8SO 2 (I)
S + O 2 → SO 2 (II)
(І) реакцияның өту барысында реакцияның газ тәрізді SO 2 басқа, газ фазасында шаң ретінде кездесетін Fe 2 O 3 қатты өнімі де түзіледі. Колчедан күйдіру процессінде газ фазасына өтетін, мышьяк пен фтор қосылыстарынан, әртүрлі қоспалардан тұрады. Бұл қосылыстардың күкірттің диоксидін контактілі тотықтыру кезінде болуы катализатордың улануына әкелуі мүмкін. Сондықтан реакциялық газды колчеданның күйдіру сатысынан кейін алдын-ала контактілі әдіске дайындайтын, яғни каталитикалық удан және су буын бөліп, сонымен қатар қосымша өнімдерді (Se мен Te) алуға жіберіледі.
Егер күйдіргіш газды күкіртті жағумен алса, онда қоспалардан тазарту қажеттілігі туындамайды. Дайындау сатысында газды кептіріп, жылуды утилизациялайды.
Үшінші саты күкірт диоксидінің контактілі тотығуының қайтымды экзотермиялық химиялық реакциясы өтеді:
SO 2 + 1/2O 2 ↔︎ SO 3 (III)
Процесстің соңғы сатысы - концентрленген күкірт қышқылының күкірттің үшоксидінің немесе олеумның абсорбциясы болып табылады.
Күкірт қышқылын өндірудегі маңызды міндеттің бірі SO 2 -нің SO 3 -ке айналу дәрежесін жоғарылату. Помимо увеличения производительности по серной кислоте выполнение этой задачи позволяет решить и экологические проблемы - снизить выбросы в окружающую среду вредного компонента SO 2 .
SO 2 айналу дәрежесін әртүрлі жолдармен жоғарлатуға болады. Олардың ішіндегі ең көп таралғаны екі реттік кантактілеу мен екі реттік абсорбция болып табылады.
H 2 SO 4 күкірттен алу.
Күкірт қышқылын күкірттен алудың технологиялық процессі колчеданнан алу процессінен бірқатар ерекшеліктері бар:
- пештік газды алуға арналған пештердің ерекше конструкциялары;
- пештік газдағы күкірт (IV) оксидінің жоғары мөлшері.
- пештік газды алдын-ала тазартудың қажет еместігі.
Күкірт қышқылын күкірттен екі реттік контактілеу мен екі реттік абсорбция әдістерімен өндіру (сур. 3) бірнеше сатыдан тұрады:
1. Ауаны шаңнан тазартқан соң, кептіргіш қоймаға жібереді, ол жерде ол көлем бойынша ылғалдылығы 0, 01% болатындай 93-98%-ті күкірт қышқылымен кептіріледі; алдын-ала контакт түйіндерінің жылуалмасқыштарының бірінде қыздырылған ауаны күкіртті пешке жібереді.
2. Күкірттің жануы қатты күйдегі күкірттің сұйық күйге, одан кейін ұшып кететін, гомогенді экзотермиялық реакция болып табылады:
S қ → S с → S бу
Осылайша, жану процессі газ фазасында алдын-ала кептірілген ауа ағынында жүреді және келесі теңдеумен сипатталады:
S + О 2 → SO 2 + 297, 028 кДж;
Контактілі тотығу 420-550˚C температурада ванадий катализаторы қатысында өтеді.
Сур. 3 Күкірт қышқылын күкірттен екі реттік контактілеу мен екі реттік абсорбция әдістерімен өндіру сызбасы
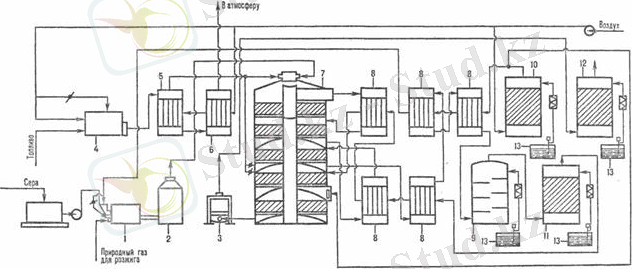
1-күкіртті пеш; 2-котел-утилизатор; 3 - экономайзер; 4-қосқыш топка; 5, 6-қосқыш топканың жылуалмастырғыштары; 7-контактілі аппарат; 8-жылуалмастырғыштар; 9-олеумді абсорбер; 10-кептіргіш башня; 11 және 12- бірінші және екінші моногидратты абсорберлер; 13-қышқыл жинағыштар[4] .
КҮЙДІРГІШ ГАЗДЫ КҮКІРТТЕН АЛУ.
Күкіртті жаққанда қайтымсыз экзотермиялық реакция өте көп мөлшерде жылу боліне жүреді: немесе масса бірлігінде есептегенде ∆H = -362, 4 кДж/моль, немесе масса бірлігіне есептегенде 362, 4/32 = 11, 325 кДж/т = 11325 кДж/кгS.
Күйдіруге әкетілетін, балқытылған сұйық күкірт 444, 6˚C температурада буланады (қайнайды) ; ұшу жылуы 288 кДж/кг құрайды. Келтірілген мәліметтерден көрініп тұрғандай, күкірттің жану реакциясының жылуы негізгі шикізатты буландыруға жетеді, сондықтан күкірт пен оттектің әрекеттесуі газ фазасында (гомогенді реакция) жүреді.
Өндірістегі күкіртті жағу келесідей жүргізіледі. Күкіртті алдын-ала балқытады (бұл үшін күкірттің негізгі жануының жылуын утилизациялағанда алынатын су буын қолдануға болады) . Күкірттің балқу температурасы салыстырмалы түрде төмен болғандықтан, тұндыру мен фильтрация арқылы күкірттен, сұйық күйге өтпеген механикалық қоспалардан айыруға болады, және тазалығы жеткілікті дәрежедегі негізгі шикізатты алуға мүмкіндік туады. Балқытылған күкіртті жағу үшін екі түрлі пештер қолданылады - форсункалы және циклонды. Осында жылдам булануы және аппараттың барлык бөлігінде қажетті байланысты орнату ушін сұйық күкірттің таралуын қамтамасыз ету керек.
Күйдіргіш газдағы күкірт диоксидінің концентрациясы жандыруға берілетін күкірт пен ауаның қатынасына тәуелді. Егер ауаны стехиометриялық мөлшерде алса, яғни күкірттің әр моліне 1 моль ауа алынса, онда күкірттің толық жануында концентрация оттектің ауадағы көлемдің үлесіне Cso 2 max =21% тең болады. Дегенмен ауаны артық мөлшерде алады, себебі кері жағдайда пеште тым жоғары температура болады.
Күкірттің адиабатикалық жануы кезінде стехиометриялық құрамды реакциялық қоспа үшін күйдіру температурасы ~ 1500ºC. Тәжірибелік жағдайларда пештегі температураны жоғарылату мүмкіндігі жоқ, себебі 1300ºC жоғарыласа пеш пен газ шығатын жердің футеровкасы бұзыла бастайды. Күкіртті жаққанда құрамында 13 - 14 % SО 2 бар күйдіргіш газ алады.
КҮЙДІРГІШ ГАЗДЫ КОЛЧЕДАННАН АЛУ.
Колчеданның жануының суммалық реакциясын (І) реакциясы түрінде келтіруге болады, мұндағы ∆Н=-853, 8 кДж⁄моль FeS 2 , немесе 7117 кДж ⁄кг. Фактілі түрде ол бірнеше бірінен кейін параллельді сатылардан кейін өтеді. Басында баяу темір дисульфидінің термиялық ыдырауының эндотермиялық реакциясы өтсе, кейіннен күкірт буының жануы мен темір сульфидінің FeS тотығуының қатты экзотермиялық реакциялары басталады.
Ауаның оттекті бөлігі темірдің тотығуына кететіндіктен, сондықтан күйдіргіш газдағы күкірт диоксидінің максималды мүмкін болатын концентрациясы бұл жағдайда күкірттің жануына қарағанда төмен болады.
Күйдіруге қолданылатын колчедан алдын-ала флотация әдісімен байытылады. Пириттен басқа FeS 2 флотациялық колчеданның құрамында бірқатар қоспалар болады (жекелей алғанда мышьяк, селен, теллур, фтор қосылыстары), олар күйдіру барысында күйдіргіш газдың құрамына As 2 O 3 , SeO 2 , TeO 2 оксидтерінің және фторқұрамды газтәрізді қосылыстарға HF, SiF 4 өтеді. Бұл қосылыстардың болуы газды келесідей тазартудан өткізіді қамтамасыз етеді.
Күйдіргіш газдың құрамына күкірт үш оксидінің SO 3 аз мөлшері болады, себебі темір оксиді жоғары температураларда SO 2 -ның SO 3 -ке тотығуының катализаторы ретінде қызмет атқарады.
Колчеданды күйдіру - «газ-қатты» жүйесіндегі типті гетерогенді процесс, оны реакция зонасының фронтальді ауысу моделімен сипаттауға болады. Бұл модельге сәйкес процесс бірқатар диффузиялық сатылар мен химиялық реакцияның өзінен, сонымен қатар көпстадиялы реакциялардан тұрады. Процесстің жылдамдығын жоғарылату үшін, алдымен диффузиялық сатылардың қарсыласуын төмендетуге тырысады, яғни колчеданды диффузиялық аймақта күйдірмейді. Бұған қатты фазаны уату мен ағынның турбулизациясының интенсивтілігі арқылы жүзеге асыруға болады. Бұл мақсат үшін аса оңтайлы аппарат ретінде колчеданның жалған сұйытылған қабаты бар пештер қолданылады («қайнау қабаты» бар пеш ҚҚ) .
Процесстің температурасы реакцияның жоғары жылдамдығын қамтамасыз ете алатындай жоғары болуы керек. Төмен температураларда (500˚C төмен) темір дисульфиді ыдырауының термиялық ыдырауының эндотермиялық реакциясы жүзеге аса алмайды. Дегенмен күйдіруді өте жоғары температураларда өткізу бөлшектердің үлкеюіне әкелетін, жанатын материалдың бөлшектерінің пісуі сияқты қажет емес физикалық процесстердің болуын туғыза алады. Нәтижесінде қатты бөлшектердің толықтай айналуының уақытын үлкейтіп τп және пештің өнімділігін төмендете алады. Пісу температурасы колчеданның құрамына байланысты 800 бен 900˚C аралығында өзгеруі мүмкін. Процессті адиабатикалық режимде өткізу нәтижесінде жоғары температураларға дейін қыздыруға әкелуші еді. Сондықтан, күйдіру жылуының жартысы пештің ішінде бұрылады. Бұл әдісті ҚҚ бар пештерде жүргізген оңай, себебі қатты материладың жалған сұйытылған қабатында колчеданның суытатын элементтердің қабатына жылу беру коэффициенті аса жоғары [~ 1000 кДж/(м²•ч•К) ] және «қайнатын» қабат суытқыш змеевиктарды енгізу мүмкіндігі болады.
Колчеданды күйдіру үшін үздіксіз жұмыс істейтін пештердің бірнеше түрін қолданады, оларда қатты фазаның қозғалу сипаты сияқты сұрақтар әртүрлі жолдармен шешіледі. Ескі күкіртқышқылды құрылғыларда механикалық пештерді кездестіруге болады. Ұсатылған колчедан мұндай пештерде бірнеше подаларда орналасып, бір подтан екінші подқа ауысу арқылы жанады. Шаңтәрізді күйдіру пештерінде колчедан бөлшектері камераға түскенде жанады. Циклонды пештерде колчедан ыстық ауамен жоғары жылдамдықта тангенциалды бұрышпен құлайды; пеште колчедан ауамен айналып жанады: балқытылған огарок арнайы түтікшелерден ағып өтеді.
Қазіргі уақытта күкіртқышқылды өндірісте колчеданды күйдіру үшін қатты материалдың жалған сұйытылған қабаты бар қайнау қабатты пештер қолданылады. Жалған сұйытылған қабатта диффузиялық және жылуалмасушы процесстердің жоғары жылдамдығы қамтамасыз етіледі (оттектің колчеданның бетіне әкелуі, күкірт диоксидін газ ағынына жіберу, жылуды шикізат бетінен газ ағынына жібереді) . Массалардың артқа тартқыш әсері мен жылуалмасудың болмауы колчеданды күйдіруді осындай пештерде жоғары жылдамдықта өткізуге мүмкіндік береді. ҚҚ пештері колчеданды күйдіруге арналған басқа конструкцияларға қарағанда максималды интенсивтілікке ие. ҚҚ пештердің кемшіліктеріне күйдіргіш газдың жоғары шаңдылығын жатқызуға болады.
КҮЙДІРГІШ ГАЗДЫ КОНТАКТІЛІ ТОТЫҚТЫРУҒА ДАЙЫНДАУ.
Күйдіргіш газды контактілі тотықтыруға дайындау, контактілі тотықтыру басталатын температураға дейін қызуды, келесі сатыларды жүргізуді қиындататын қосымша қоспалардан тазартудан тұрады.
ҚҚ пештерінде колчеданды жағу арқылы алынған күйдіргіш газ құрамында көп мөлшерде огарок шаңы, мышьяк, селен мен фтор қосылыстары болады. Күйдіргіш газды тазарту пеш бөлімдерінде басталады, онда циклон мен құрғақ электрофильтрлерде огарок шаңын тұндырады. Құрғақ тазартудың осы аппаратарынан кейінгі газдағы шаңның құрамы 50 мг/м³ аспауы қажет. Кейін газды дымқыл тазалау сатысына (шаю бөліміне) жібереді, онда күйдіргіш газдан щаң қалдықтарын, каталитикалық уды (мышьяк пен фтор қосылыстары), сонымен қатар селен қосылыстарынан тазартады.
Құрғақ тазартудан кейін аз мөлшерде болсын газда шаңның болуы аппараттардың гидравликалық қарсыласуын жоғарылатып және катализатордың огарок шаңына абсорбцияланған Аs қосылыстарымен улануына әкелуі мүмкін. Катализатор улануы газ фазасында мышьяк оксидтері As 2 O 3 немесе фтор қосылыстары (HF мен SiF 4 ) қалған жағдайда орын алады. SeO 2 селен диоксиді контактілі тотықтыру катализаторы үшін улы емес, дегенмен жартылай өткізгіштер өндірісінде негізгі шикізат ретінде өте бағалы.
Күйдіргіш газды дымқыл тазарту оны күкірт қышқылымен шаюға негізделеді. Бұл жағдайда бірқатар физикалық процесстер орын алады: конденсация, абсорбция және т. б.
Газ және бу тәрізді күйде болатын, күйдіргіш газдың негізгі қоспалары (As 2 O 3 , SeO 2 мен т. б. ) күкірт қышқылымен жуғанда бөлініп шығады. Қоспалардың бір бөлігі күкірт қышқылында ериді, бірақ олардың көп бөлігі күкіртқышқылды тұман құрамына өтеді. Тұманның пайда болуы күйдіргіш газ құрамына SO2-ден басқа күкірттің үш оксидінен тұрады, газды суытқанда олар күкірт қышқылының буын түзе отырып әрекеттесетіндігімен түсіндіруге болады. Бірінші шайғыш башняда газ жылдам суытылады; бұл кезде күкірт қышқылының булары көлем бойынша тұман түрінде конденсирленеді - ұсақ салмақты газ тамшылары.
Күкірт қышқылы тұманының тамшыларының суммалық беттік қабаты аса жоғары, сондықтан оларда көп мөлшерде As 2 O 3 мен SeO 2 оксидтері мен жуғыш башнялар мен электрофильдерден газдардан бөлінетін қоспалар да ериді. Газдарды тұманнан тазарту контакт массасын улайтын қоспалардан ғана тазартумен шектелмейді, күкірт қышқылы тамшыларын да тазарту керек, себебі газдың аппаратура арқылы өтуінде коррозия жүреді. Газды нашар тазалағанда күкірт қышқылы тұманының көп мөлшері нагнетательдерден шығуы мүмкін, себебі газдың жоғары айналмалы жылдамдығы қышқылдың ұсақ тамшыларының бөлінуіне әкеледі. Аса жоғары бұзғыш әрекетті контак бөліміндегі тұмантәріздес күкірт қышқылы әкелуі мүмкін. Контакт аппаратының металл түтіктерінің күкірт қышқылымен әрекеттесуі нәтижесінде түзілетін, коррозия өнімдері аппаратураның қарсыласуын жоғарылатып, жылуберу коэффициентін төмендетеді және қатты қабаттардың контакт массасының бірінші беттерінде тұңуын жоғарылатады.
Дымқыл электрофильдерден тұманның шығу жағдайларын жақсарту үшін газдың температурасын төмендетеді және екінші башнядағы байытылатын қышқылдың концентрациясын төмендетеді, ал сосын бірінші электрофильден кейін, нәзік күкірт қышқылымен байытылатын ылғалдандырғыш башня арқылы газ жібереді. Сонда газдың салыстырмалы ылғалдылығы артады, бұл су буын тұман тамшыларының жұтылуына яғни, олардың өлшемдерінің өзгеруіне әкеледі.
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz