Ниобий және тантал: тарихы, физика-химиялық қасиеттері, қосылыстары мен минералдық қорлары


Жоспар:
1. Тарихи мағлұматтар
2. Физикалық және химиялық қасиеттері
Ниобий (Nb) және тантал (Ta)
XVII ғасырда Солтүстік Америкада қара түсті слюданың алтын сызықтары бар минералы ашылған. Оны Англияға жібереді, бұл минерал Британ музейінде 150 жыл жатты. 1801 жылы химик Хатчет осы минералды зерттеуге кірісіп, құрамынан темірді немесе қышқылды оксидтің қасиеті бар белгісіз затты тапты. Бұл жаңа элементті колумби, ал минералды колумбит (минералды тапқан жер - Колумбия - Америка) деп аталады.
1802 жылы швед зеттеушісі Экеберг кейбір скандинав және фин минералдарында тағы жаңа зат тапты, оны тантал деп атады. Бұл атау грек философиясындағы - Тантал белгісіне қойылған, себебі жаңа элемент қышқылдарға тұрақтылығын көрсетеді. Тантал қасиеттері колумбидің қасиеттеріне өте жақын болып шықты, сондықтан көп ғалымдар колумбий мен тантал бір элемент деп санап жүрді.
Хатчет пен Экеберг танталдың және колумбийдің қоспасын ашты, бірінші-сінде - колумбийдің, екіншісінде - танталдың мөлшері көбірек болды.
1884 жылы Розе бір минералда екі элементті - тантал мен колумбийді тапты, оны ниобий деп атады (Ниобея - Танталдың қызы) .
1865 жылы Мариньяк танталдың және ниобийдің қасиеттерін зерттегенде металдарды бір-бірінен фторидті әдіспен бөлді. Таза тантал бірінші рет тек қана 1903 жылы, ал таза ниобий - бүдан да кейінірек алынған.
Тантал мен ниобий ванадий сияқты периодтык, жүйенің бесінші тобына кіреді. Бірақ ниобий, әсіресе тантал ванадиймен салыстырғанда өте ауыр тотықсызданады. Сондықтан тәжірибеде бес валентті қосылыстармен жұмыс істеледі. Атомдарының электрондық құрылысы: ниобий - 2, 8, 18, 12, 1; тантал - 2, 8, 18, 32, 11, 2.
1 кесте. Элементтердің негізгі сипаттамалары:
Тантал мен ниобийдің химиялық қасиеттері өте ұқсас, олар табиғатта бірге кездеседі, сондықтан оларды бір-бірінен бөлу өте қиын.
Сыртқы түріне қарағанда ниобий және тантал металы платинаға ұқсас. Металдардың физика-механикалық қасиеттері өте жоғары, бірақ бұл қасиет-тер металдардың тазалығына байланысты.
Металдардың ең бағалы қасиеттері - қышқылдарға тұрақтылығы жоғары, олар концентрлі азот және патша қышқылдарында ерімейді. Тантал өте тұрақты. Бұл қасиеттер 2 кестеде ниобий мен танталдың әр түрлі қышқылдарда корроииясының мәліметтерінен көрініп тұр.
2 кесте. Ниобий мен танталдың қышқылдардағы коррозиясы
Концентірлі тұз
қышқылы
Концентірлі азот
қышқылы
Концентірлі
күкірт
қышқылы
үлгі
толық
ериді
Кестеден қыздырғанда күкірт қышқылы ниобийді толық, ал танталды аздап ерітетінін көруге болады. Екі металл азотжәне фосор қышқылдарының қоспаларында ериді, бөлек фтор қышқылы ниобийге жай әсер етеді, ал танталға әсер етпейді. Тапталдың қышқылдарға жоғары тұрақтылығы кон-центрлі азот-, бром-, тұз қышқылдарын, сүйытылған бромды буландырғанда, ыдыс жасағанда пайдаланылады. Сілті ерітінділерінің ниобийге аздап әсері бар, ал танталға әсері жоқ. Ниобий мен тантал балқыған сілтілермен әрекет-тесіп, тұздар ниобаттар және танталаттар түзеді. Кез келген тұздардың бал-қымалары меи органикалық қосылыстары ниобий мен танталға әсәр стпейді.
Ниобий мен танталдың басқа маңызды қасиеттері: газдарды - сутекті (1 сурет), оттекті (9 сурет), азотты және т. б. сіңіруі. Бұл екі металл гидридтер түзеді: NbН, Та 2 Н, ТаН. Ниобий мен тантал оттекті 0, 8%-ке дейін ерітеді:
Nb
º
200 400 600 800 1000 1200 140
Температура, 0 С
1 сурет - Тантал мен ниобийдегі сутек ерігіштігінің
температурадан тәуелділігі
Ниобий мен тантал көп металдармен құймалар береді, көбінесе олардың бағалы қасиеттері бар, сондықтан тәжіри беде маңызы зор.
2 суретте металдағы оттек мөлшерінен оның электр қарсылығының тәуелділігі көрсетілген.
80
60
40
20
0
17 0
+117
+
+
+
•
∙
º
600 0 800 0
•
∙
º
+
•
∙
º
•
∙
º
0, 5 11, 52 2, 5
2 сурет - Металдағы оттек мөлшерінен оның электр қарсылығының тәуелділігі
Оттекпен қосылыстары
Ниобий мен тантал қышқылды қасиеттері бар оксидтер түзеді. Бірақ табиғатта өздері қышқылдардың тұздары түрінде кездеседі, сондықтан ұзақ уақыт бойы оларды - “жер қышқылдары” немесе “ащы жерлер” деп атап жүрді.
Ниобий (V) мен танталдың (V) оксидтері Nb 2 О 5 және Tа 2 O 5 - ақ түсті, ұсақ кристалл ұнтақтар, суда ерімейді, баяу балқиды. Ұнтақ ниобий металы 400°С температурада оттекте жанып оксид түзеді:
4Nb +5O
2

 2НЬ
2
O
5
.
2НЬ
2
O
5
.
Nb 2 O 5 1150°С температуралы вакуумда диссоциацияланады:
Nb
2
O
5

 2NЬO
2
+½ O
2
2NЬO
2
+½ O
2
Тантал оксиді тантал металын қыздыру арқылы алынады (ниобийге ұқсас) .
Ниобий мен танталдың оксидтері суда ерімейді, бірақ ең соңғы жұмыстарда олардың суда аз болса да еритіндігі көрсетілген: Nb 2 O 5 -тің суда ерігіштігі - 1793 мг/мл, ал Та 2 O 5 - 162 мг/л (3 сурет) .
2200
2100 2000 1900 1800 1700 900 800 700 600 500 400 300 200 100
°
°
0 2 4 6 8 10
°
°
°
°
×
×
×
×
×
×
○
Қышқылдың концентрациясы, н
3 сурет - Ниобий мен тантал оксидтерінің қышқылдарда ерігіштігі:
1 - ниобий оксидінің тұз қышқылында;
2 - тантал оксидінің тұз қышқылында; 3
3 - ниобий оксидінін күкірт қышқылында;
4 - тантал оксидінің күкірт қышқылында Nb 2 O 5 сутекпен немесе көміртекпен 1200-1300°С температурада тотықсыздандырғанда ниобийдің томенгі оксидтері алынады: Nb 3 O 5 , Nb 2 O 3 , Nb 2 O, NbO 2 , NbO.
Ниобий (IV) оксиді NbO 2 немесе Nb 2 O 4 қара-көк түсті зат, ауада тұрақты, 850°С температурада қыздырғанда тотығып, ниобий оксиді Nb 2 O 5 түзіледі. Төменгі оксидтердің тәжірибелік маңызы жоқ. Танталдың төменгі оксидтері тұрақсыз, қыздырғанда оңай тотығады.
Ниобий мен танталдың оксидтері конңентрациясы әр түрлі тұз және күкірт қышқылдарында ериді. Ерігіштіктері оксидтердің күйдіру температурасына байланысты.
Мысалы, 400°С температурада тұз қышқылында күйдіргенде Nb 2 O 5 жақсы ериді, ал Та 2 O 5 - 800°С температурада күйдіргенде - жақсы ериді. Оксидтер тұз қышқылымен әрекеттескенде - хлороксидтер, формуласы МеОС 13 , ал күкірт қышқылында ион МеО 3+ түзеді:
Nb 2 O 5 + 6НС1 → 2NbОС1 3 + ЗН 2 O;
Nb 2 O 5 + ЗН 2 SO 4 → (NbО 3 ) 2 +(SO 4 ) 3 + ЗН 2 O.
Танталаттар мен ниобаттар
Ниобийдің (V) және танталдың (V) оксидтерін сілтілермен балқытқанда ниобий және тантал қышқылдарының тұздары түзіледі. Тұздар - ниобаттар және танталаттар деп аталады. Олар судың ерітіндісінде оңай гидролизденеді. Тұздардың ерітінділерін көп сұйытқанда немесе қышқыл-датқанда тұнбаға гидратты оксидтер түседі, оның құрамындағы су молекуласының мөлшері айнымалы. Тұнбалардың жалпы формуласы - Ме 2 O 5 nН 2 О (Ме - ниобий немесе тантал) .
3 кесте. Сілті металда ниобат пен метатангалаттардың ерігіштігі және ерігіштік көбейтіндісі (25°с), мг/л
Nb 2 O 5 сілті металдардың сульфаттарымен, натрий және калий хроматымен және бурамен әрекеттескенде метаниобаттар түзіледі. Натрий мегафосфатымен әрекеттескенде құрамы метан немесе ортаноибатқа сәйкес емес басқа қосылыс түзеді. Nb 2 O 5 -ты сілті және сілті жер металдарының хлоридтерімен балқытқанда, ол 1000-1200°С температурада мета-немесе ортониобаттар түзу арқылы балқымаға ауысады. Басқа металдардың (кальций, барий және калий) хлоридтерімен балқытқандағы өнімдер жайында қазір мәліметтер жоқ.
Ниобий тұздары, титан, темір және сирек жер элементтер тұздары бар ерітіндіден аммиакпен тұндырғанда, кептіріп қыздырғаннан кейін құрамы Ме(NbОз) n формуласына сәйкес тұнбалар түседі. Бұл зерттеулер термогравияметрлік әдіспен жасалған.
1100°С температурада сирек жер элементтердің оксидтерін Nb 2 O 5 -пен кварц тостағында қыздыру арқылы церийдің, празеодимнің және неодимнің ортониобаттары алынған. Бұл өнімдердің құрамы МеNbO 4 формуласына сәйкес. Рентгенографиялық зерттеулермен бұл тұздардың табиги ортонибат- тармен изоморфты екені анықталды. Е. И. Крылов иттрий, празеодим және неодимнің ортотанталаттарын синтездеген.
Құрамы күрделі Pb 7 Nb 12 O 37 ·23H 2 O, Pb 8 Ta 12 O 38 ·33H 2 O формуласына сәйкес ниобий және тантал қышқылдарының қорғасын тұздары алынған.
Nb 2 O 5 -SO 3 -H 2 O жүйесін зерттегенде анықталған ниобийдің басқа тұздары, яғни сульфаттары және оның қос сульфаттары жайында NH 4 NbO(SO 4 ) 2 , (NH 4 ) 6 Nb 2 O (SO 4 ) 7 және (NH 4 ) 3 Nb(SO 4 ) 4 жайында мәліметтер белгілі. Бұл тұздар оңай гидролизденеді және судың өте аз мөлшерінде балқымаларда ғана тұрақты. Осы автор мұндай тұздарды тантал үшін де алған.
Ниобаттарға сонымен қатар ниобий бронзалары (вольфрам бронзасы сияқты) деп аталатын қосылыстарды жатқызуға болады. Бронзаның бірнеше түрлерін Р. П. Озеров алған, олар түсі стронций мөлшерінен қарадан қаныққызылға дейін өзгеретін, құрамы әр түрлі стронций бронзалары - Sr 0, 585 NbO 3 тен Sr 0, 82 NbO 2, 96 . Е. И. Крsшов бойынша ниобий бронзаларын волфрам бронзалары сияқты nМеО·mNbO 2 ·рNb 2 O 5 жалпы формуламен өрнектеуге болады.
Вакуумда 500-900°С температурада термиялық диссоциациямен алынған өнімдерді де ниобий бронзаларына жатқызуға болады. Бұл өнімдердің құрамы жалпы формулаға МеNbO 3-x сәйкес және х=0, 04-тен 0, 1 -ге дейін өзгереді.
Сонымен қатар натрий ниобаты мен танталаттарының қатты ерітінділері алынған және қыздырғанда бұл жүйелердегі фазааралық ауысулар зерттелген. Бұл жұмыстар ниобат пен танталаттардың сегнетоэлектрлік қасиеттерін зерттеулермен байланысты. Мысалы, кадмий және стронций ниобаттарының, соның ішінде Sr 2 Ta 2 O 7 , Cd 2 Nb 2 O 7 сегнетоэлектрик екені белгілі. Бұл қосылыстардың және осыларға ұқсас қосылыстардың кристалдық құрылымдарын коп ғалымдар зерттеген, мысалы И. Г. Исмаилзаде кадмий пиротанталатының сегнетоэлектрлік қасиеттерінің жоктығын анықтаған.
Пероксидті қосылыстары
Сілтілі ниобаттар мен танталаттардың ерітінділеріне сутек пероксидін қосқанда түссіз немесе сары түсті пероксид қосылыстары - перниобат K 3 NbO 8 , Na 3 NbO 8 немесе пертапталат- K 3 TaO 8 , Na 3 TaO 8 түзіледі. Бос күйінде бұл қосылыстарды спирт қосып бөлуге болады. Осылардың ерітінділеріне күкірт қышқылына қосқанда бос надкышқылдар -надниобий HnbO 4 және надтантал HTaO 4 қышқылдары түзіледі:
NaNbO
3
+ 2Н
2
O
2
+ 2NаОН
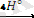
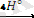 Na
3
NbO
8
+H
2
O;
Na
3
NbO
8
+H
2
O;
Na
3
NbO
8
+ 8Н
+
 → HNbO
4
+ 4H
2
O+3Na
+
→ HNbO
4
+ 4H
2
O+3Na
+
Надниобий қышқылының түзілу реакциясыи аналитикалық химияда ниобийді фотометрлік әдіспен аныктағанда пайдаланады.
Комплексті қосылыстары
Ниобий мен тантал әр түрлі комплексті қосылыстар түзедіді, әсіресе, органикалық қышқылдармен. Мысалы, рН 4 пен 6-ның арасында Nb (V) аммоний салицилатпен қара-қоңыр кристаллдық түнба түрінде түседі, рН мәнін жоғарылатқанда түсі қызғылт түске ауысады. Аммиакты ерітіндіде қызғылт сары-қызыл түсті комплексті қосылыс NbOSalSO 4 немесе дұрыстау [NbOSO 4 ] Sа1 түзіледі, (Sа1 - салицил қышқылының анионы) . Мұндай түсті комплекс тантал сульфосалицил қышқылымен де береді, бұл комплекс оксалат компілексінен тұрақтылау. Ниобийдің оксалатпен комплексінің дұрыс формуласы [NbO 2 C 2 O 4 ] - немесе [Nb(OH) 4С 2 O 4 ] - . А. Н. Невзоров ниобийдің оксалатпен комплексті қосылысын бос түрінде бөліп, оның формуласы К 3 [NbO(C 2 O 4 ) з] ·2Н 2 O, ал тұрақсыз константасының мәні 1, 8·10 -4 тең деп тапты. Танталдың оксалатпен комплексті қосылысының формуласы К 5 [Та(C 2 O 4 ) 5 ] .
Ниобий сонымен қатар кейбір сыртқы сферасына кіреді, мысалы фосфор молибден немесе силикомолибден қышқылдарға. Осы реакцияны пайдаланып кремнийді немесе фосфорды ниобийдің қатысында фотометрлік әдіспен анықтауға болады. Сонымен қатар осы реакцияны пайдаланып, ниобийді танталдың қатысында анықтауға болады, себебі тантал мұндай компілексті қосылыстарды түзбейді.
Тәжірибеде ниобийді анықтау үшін оның роданидті комплексті қосылыстарын (құрамы Н[NbО(CNS) 4 ] ) және ниобийдің әр түрлі комплексті қосылыстарын пайдаланады.
Галогендермен қосылыстары
Ниобий мен танталды хлормен қыздырғанда NbСІ 5 және ТаС1 5 түзіледі. NbС1 5 - сары түсті кристаллды зат, балқу температурасы 203, 4°С, қайнау температурасы - 247°С. ТаС1 5 - кристаллды зат, балқу температурасы 204-221°С, қайнау температурасы 236, 5°С. Таза ТаС1 5 - ақ түсті, ластанған ТаС1 5 - сары түсті.
Ниобийдің пентахлориді NbС1 5 СНС1 3 , СС1 4 көміртекте, хлорлы күкіртте, сонымен қатар спиртте, эфирде ериді, бірақ олардың қатысында ыдырап, оксид түзеді (гидролиз) .
Ниобийдің (V) және танталдың (V) галойд қосьшыстары сумен ыдырап, тұнбаға ниобий немесе тантал қышқылдар түрінде түседі.
Ниобий оксидінен Nb 2 O 5 ниобий пентахлоридін хлор қосып алғанда, біршама оксихлорид NbОСІз түзіледі. NbОСІз - түссіз кристалды зат, 322°С температурада айдалады. Жоғары температурада NbОСІз ажыратылып, Nb 2 O 5 және NbС1 5 түзіледі. Танталға сәйкес оксихлорид алынған жоқ. Ниобий оксигалогениді сумен ыдырап ниобий қышқылы түзіледі. Ниобий мен танталдың пентахлоридтері әр түрлі ком- плексті қосылыстар түзеді: МеNbCl, Ме(NbОС1 4 ) және Мe 2 (NbОС1 5 ) .
Пентахлоридтер сутекпен тотықсызданып NbС1 3 және ТаС1 3 түзіледі. Жоғары температурада ниобий металы иодпен әрекеттесіп ниобий иодидтерін түзеді, олардың құрамы - Nbl 5 , Nbl 4 , Nbl 3 , 2 . Оларды қыздырғанда иод бөлінеді, 600-630°С температурада ниобий иодиді айдалады, 700°С темпeратурада диспропорциялану реакциясы өтіп металл бөлінеді.
Ниобий мен иод ұнтақ түрінде қатынасы Nb:І=1, 5 болганда, вакуумда NbClз түзеді, бұл иодид 600°С температурада айдалады. Иодид суда немесе сілті ерітінділерінде гидролизденеді, осы жағдайда сутек бөлініп, ерітінді қаракөк немесе жасыл түске боялады, бұл түс үш валентті ниобийге тән.
300-400°С температурада алюминий немесе кремний иодидтері және ниобий мен танталдың хлоридтері арасындағы реакция арқылы ниобий мен танталдың иодидтерін алуға болады.
Тантал иодиді ТаІ 5 - қара, жалтыраған зат, 496°С температурада балқи-ды, 543°С температурада қайнайды, жоғары температурада ыдырап иод пен тантал металы бөлінеді. Иодид оңай гидролизденеді.
Ниобийдің томенгі иодидтері алынған: NbI 4 , NbI 3 , NbI 2 :
2Nb + 5І
2
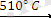
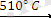 2NbI
5
;
2NbI
5
;
2NbI
5
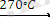
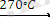 2NbI
4
+ І
2
;
2NbI
4
+ І
2
;
NbI
5
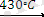
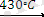 NbI
3
+ І
2
;
NbI
3
+ І
2
;
2NbI
3
+ Н
2
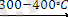
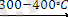 2NbI
2
+ 2НІ.
2NbI
2
+ 2НІ.
Ниобий мен танталдың фторидтері де белгілі NbҒ 5 , ТаҒ 5 , бұл түссіз кристалды заттар. Тәжірибеде маңызды әр түрлі фторид комплексті қосылыстар: К 2 [МеҒ 7 ], К[МеҒ 6 ] (Ме- ниобий немесе тантал), танталға белгілі комплекс К 3 [ТаҒ 8 ] . Ниобийдің қос оксифторидтері де белгілі. Комплексті фторидтердің ерігіштігі әр түрлі. Мысалы, ниобийдің қос оксифториді К 2 NbOF 5 суда жақсы ериді, ал танталдың қос фториді К 2 ТаҒ 5 қиын ериді. Осы қасиетті пайдаланып металдарды бір- бірінен бөлуге болады.
Көміртекпен қосылыстары
Ниобий мен тантал құрамы әр түрлі карбидтер түзеді: Nb 4 C, Nb 2 С, Та 2 С, NbС, ТаС. Олардың арасында ең маңыздысы монокарбидтер - NbС, ТаС. Бұл карбидтердің қаттылығы өте жоғары (NbС - микроқаттылығы 2055 кг/мм2, ТаС-1200-1547 кг/мм2), балқу температуралары да жоғары: NbС-3780°С, ТаС-3880°С. Тығыздықтары: NbС-7, 6г/см3, ТаС- 14, 85г/см 3 ) .
Монокарбидтер әр түрлі әдіспен алынады: балқытылған металды көмір-текпен тікелей әрекеттестіру немесе 1600-1700°С температурада оксидтерді көміртекпен тотықсыздандыру арқылы, т. б. Карбидтердің кристалдары 1100-1400°С температураға дейін ауада тұрақты, қышқылдарда қиын ериді. Ниобий монокарбидіне күкірт пен фтор қышқылдарының әсері бар. Монокарбидтер қатты болаттарды жасауда жоғары температуралық қондырғыларда пайдаланылады.
Азотпен, бормен, кремниймен қосылыстары
Ниобий мен танталдың нитридтері металдарды жоғары температурада азот пен аммиактың құйылысында қыздырғанда түзіледі. Температураға және қыздыру уақытына байланысты азоттың әр түрлі мөлшерінде нитрид-терді алуға болады. Нитридтерді сонымен қатар ниобий мен танталдың оксидтерін азот құйылысында коміртек қатысында қыздырып алуга болады. Ниобийге екі нитрид белгілі - Nb 2 N, NbN. Соңғысы әр түрлі қышқылдарға тұрақты, соның ішінде патша қышқылына да; қайнатқанда сілтілі ерітіндіде ыдырап аммиак бөлінеді. Ең маңыздысы 15, 6°К температурада жоғары өткіз-гіштік күйге айналуы. Қасиеттеріне байланысты NbN радиотехникада, элек-троникада, автоматикада пайдаланылады.
Тантал ниобий сияқты екі нитрид түзеді - Ta 2 N және ТaN.
Ниобий мен тантал бормен бірқатар қосылыстар түзеді, олардың арасында ең қызықтысы - NbB 2 және ТаВ 2 , балқу температурасы өте жоғары - 3050-3100°С, қышқылдарға тұрақты. Ауада қыздырғанда (500-600°С) оңай тотығады, қыздырғанда азот және фторид қышқылдардың қоспасында және концентрлі күкірт қышқылында калий сулфатын қосқанда оңай ыдырайды.
Ниобий кремниймен үш силицидтер түзеді - Nb 4 Si, Nb 5 Si 3 , NbSi 2 . Силицидтердің маңызды қасиеттері - жоғары қаттылығы және жоғары балқу температуралары: Nb 4 Si 2580°С температурада балқиды, Nb 5 Si 3 - 2400-2480°С, NbSi 2 - І950°С. Бірақ силицидтер оңай тотығады.
Тантал силицидтерінің құрамы және қасиеттері ниобийге ұқсас.
Электрохимиялық қасиеттері
Ниобий ванадийдің аналогі болса да, төменгі валенттілік күйі оған ерекше емес, ал тантал ерітіндіде тек қана бес валентті күйде болады. Тотығу-тотықсыздану жұптардың нормальды потенциалдары келесідей: Nb 2 O 5 /Nb 3+ =-0, 1В, Nb 3+ =-1, 1В, Та 2 O 5 /Та=-0, 81В.
Ниобийді төрт валентті күйге дейін электролизбен (сынап электродында) немесе мырыш амальгамасымен тотықсыздандырып алуға болады. Металдық ниобийді балқымсын электролиздеу арқылы алуға болады.
Ниобийдің полярографиялық бағыты бірнеше рет зерттелген, бірақ қазірге дейін тәжірибеде қолданбайды. Тұз қышқылды ерітінділерде бес валентті ниобий төрт валентті күйге дейін потенциалдың шамасы 0, 455 В болғанда тотықсызданады. Төртвалентті ниобий ақырын бес-және үшвалентті күйге дейін диспропорцияланады.
Бес валентті ниобий 70%-ті күкірт қышқылының фонында потенциалы-ның шамасы - 1, 05В болғанда тотықсызданьш жақсы көрінетіндей толқын-дар береді. Фон ретінде пирофосфорқышқылды пайдаланғанда ниобийді полярографиялық әдіспен титанның қатысында анықтауға болады.
Минералдары мен кендері
Табиғатта ниобий мен тантал негізінде ниобаттар мен танталаттар түрінде күрделі минераддардың құрамына кіреді. Металдардың қасиеті бірдей және атомдық пен иондық радиустары жақын болғандықтан, олар табиғатта бірдей кездеседі.
Ең белгілі және кең тараған минералдар: танталит пен колумбит - болса - тапталит , ниобий көп болса - калумбит депаталады. Қоспа түрінде минералда кездеседі Ті0 2 , WO 3 , ZnO 2 , SnO 2 т. б.
Танталит пен колумбит - ауыр, қараминералдар, сыртқы түріне қарағанда ильменитке және вольфрамитке ұқсас.
Танталиттің (колумбит) бай кен орны Австралияда, Бразилияда, АҚШ-та, Нигерияда кездеседі. Австралиядағы танталиттерде 50-70% Та 2 O 5 , колумбиттерде (АҚШ) - 10-40%Nb 2 O 5+ Ta 2 O 5 бар. Нигериядағы (Африка) колумбиттерде 45-55% Nb 2 O 5
Басқа минералдар - пирохлор NaCaNb 2 Ғ және микролит NaCaTa 2 O 6 Ғ. Олардың құрамында: 63% - 0% Nb 2 O 5 , 0- 77% Та 2 O 5 , 2-13, 5% ТіO 2 , 0-5% ТҺO 2 , 0-11, 4% UO 2 , 0-15, 5% UO 3 , 0-5, 7% ZrO 2 , иттрий тобының сирекжер элементтері 2- 13, 3%, церий тобының сирекжер элементтері 0-5, 1%, 0-4, 0% SnO 2 , 0-0, 3% WO 3 . Сонымен қатар минералдардың құрамына сілті және сілтіжер металдардың оксидтері кіреді.
Пирохлордың бір түрі копит деген минерал, оның құрамында церий тобының сирекжер элементтерінің мөлшері көбірек, химиялық құрамы, % келесідей:
Пирохлор цирканға және шеелитке ұқсас.
Ниобидің минералы - лопарит , оның құрамы, %:
Пирохлор , каппит және лопарит - комплексті шикізаттар, ниобиді және сирек жер элементтерді алу үшін қолданылады.
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz