Дисперстік жүйелер мен ерітінділер: классификациясы, еру механизмдері және физика-химиялық қасиеттері


ЕРІТІНДІЛЕР
Дисперстік жүйелер туралы жалпы түсінік
Бір немесе бірнеше заттардың ұсақ бөлшектерінің екінші бір заттың ұсақ бөлшектерінің арасында таралуын дисперстік жүйенің түзілуі дейді, ал соған сәйкес екі немесе одан да көп заттардан тұратын жүйені дисперстік жүйе дейді. Агрегаттық күйге дисперстік жүйенің күйіндей болатын затты дисперстік орта, ал сол ортада таралатйн затты (немесе заттарды) дисперстік фаза деп атайды.
Дисперстік фазалар мен дисперстік ортаның агрегаттық күйлеріне байланысты дйсперстік жүйенің 9 түрі болады. Бұл жүйелер-дисперстік ортаның агрегаттық күйіне сәйкес 3 түрлі агрегаттық күйде - газ, сұйық және қатты күйлерде болады. Мысалы, ауа, тұман, түтін - газ, эмульсиялар, қанттың судағы ерітіндісі сүйық, әр түрлі металдардың құймалары қатты дисперстік жүйенің мысалдары болады.
Дисперстік ортада таралған дисперстік фазалардың мөлшерлеріне байланысты дисперстік жүйелер үш топқа бөлінеді. Дисперстік ортада таралған бөлшектерінің радиустары 10 -5 -10 -7 м болатын дисперстік жүйелерді жүзгіндер, радиустары 10 -7 -10 -9 м-ға дейін болатындарын коллоидты ерітінділер, ал радиустары 10 -9 -10 -10 м болатындарын шын ерітінділер немесе ерітінділер деп атайды. Жүзгіндер мен коллоидты ерітінділер гетерогенді дисперстік жүйелерге жатады және тұрақсыз болады. Жүзгіндер суспензнялар және эмульсиялар болып бөлінеді. Қатты заттың бөлшектері сұйықта таралуынан суспензия түзіледі, мысалы оған лай суды келтіруге болады. Сұйық зат бөлшектерінің сұйықта таралуынан эмульсия түзіледі. Мысалы, сүтте сүйық май бөлшектері сұйықта таралған.
Коллоид ерітінділерінің мысалы ретінде жұмыртқа белогының ерітіндісін, желімді, желатина ерітіндісін келтіруге болады.
Ерітінділердің жалпы сипаттамасы
Ерітінділер деп екі немесе одан да көп компоненттерден тұратын біртекті (гомогенді) жүйені айтады. Ерітінділердің жай коспалардан айырмасы оны құрайтын бөлшектер ыдыстың көлемінде біркелкі таралады да қоспаларға тән тұнба түзбейді.
Ерітінділердің химиялық қосылыстардан айырмасы оның құ-рамы айнымалы болады да құрам тұрақтылық және еселік катынас заңдарына бағынбайды. Сонымен бірге еру процесі бір заттың бөлшектері екінші зат арасында механикалық таралуы емес, еріген зат пен еріткіш бөлшектерінің әрекеттесуінен түзілетін курделі процесс. Еріген зат бөлшектерінің еріткіш бөлшектерімен әрекеттесуі нәтиесінде түзілген заттарды сольваттар; ал судағы ерітінділерде түзілген заттарды гидраттар дейді. Осы процестер жүргенде химиялық реакциялар сияқты жылу шығарылады немесе сініріледі. Бұл сольваттар мен гидраттардың кейбіреуі тұракты болғандықтан ерітіндіні суалтып беліп алуға болады, ал басқалары тұрақсыз болғандыктан қыздырғанда ыдырап кетеді.
Сонымен ерітінді дегеніміз екі немесе одан да көп заттың тек механикалық қоспасы ғана емес және солардың әрекеттесуінен түзілген біртекті жүйе.
Д. И. Менделеев еру процесі мен ерітіндінің касиеттерін зерттей келіп, ерітінді өзінің құрамын температураның және концентрацияның әсерінен өзгертетін тұрақсыз химиялык қосылыс деген қо-рытындыға келді. Бұл теория ерітінділердің сольваттық теориясы деп аталды.
Еру процесін Аррениус, Вант-Гофф, Оствальд бір заттың екінші зат бөлшектерінің арасына механикалық түрде таралуы деп есептеді.
Кейінірек И. А. Каблуков пен В. А. Қистяновскийдін зерттеулері нәтижесінде еру физикалық және химиялык процестер - қатар жүретін физика-химиялык процесс екені дәлелденді. Ерітінділер қатты, сұйық және газ тәрізді болады. Ерітінді еріген з а т т а н және еріткіштен турады. Сұйықтықта көбірек мөлшерде еріген сұйықты е р і т к і ш деп атайды. Газ бен қатты зат суйыкта еріген болса, сұйықты еріткіш дейді, ал газ бен қатты затты еріген заттар дейді. Қатты затта еріген (мысалы мыс күміс құймасы) қатты заттың мөлшерінің көбірегін еріткіш дейді.
Әсіресе сұйық ерітінділердің табиғатта, техникада, тұрмыста маңызы зор. Өсімдіктер мен жануарлар организмінде өтетін процестер суйық ерітінділерде жүреді. Химия және металлургия т. б. өнеркәсіп орындарында негізгі өнімдер алу суйық ерітінділердің қатысуымен жүреді.
Заттардың ездігінен еру процесі
Ерітінді түзілу үшін әр түрлі заттар еріткіштерде еруі керек. Газдардың, сұйықтардың, қатты заттардың сұйық еріткіштерде еруі күрделі физика-химиялық процестер.
Біріншіден газдар, сұйықтар, қатты заттар (кристалдар) ерігенде олардың атомдарының (иондарының) арасындағы химиялық байланыстардың үзілу процесі жылу сіңіру арқылы жүреді, яғни жүйенің энтальпиясы артады. Екіншіден еріген заттың бөлшектері (молекулалар, иондар) еріткіштің молекулаларымен әрекеттесіп сольваттар немесе гидраттар түзу процесі жылу шығара жүреді, яғни жүйенін энтальпиясы азаяды. Үшіншіден түзілген сольваттардың немесе гидраттардык еріткіш молекулаларынын арасында біркелкі таралу процесі, яғни, диффузнясы жылу сіңіре журіп жүйенін энтальпиясын арттырады.
Сонымен зат еріген кезде бөлінетін немесе сінірілетін жылудың мөлшері химиялық байланыстардың үзілу энергиясының бөлшектердің гидраттану энергияларының және бөлшектердің диффузиялану энергиясының алгебралық қосындысына тең болады:
КА типтес екі бөлшектен тұратын кристалды қатты заттын еруі кезінде байқалатын жылу құбылыстарын былай түсіндіруге бо-лады:
Екі түрлі ионнан тұратын КА кристалды затын суда еріткенде су молекулаларының әсерінен иондардың арасындағы химиялық байланыстың
Атомдық немесе молекулалық кристалды заттарды да еріткенде бөлінетін немесе сінірілетін жылу осы заңдылыққа бағынады.
Сұйықтарды суда еріткенде сұйык молекулаларынын арасындағы әлсіз молекулалық байланысты үзуге энсргия аз жүмсалады да, бөлшектердің гидраттану кезінде бөлінетін энерпіяның ссебінен еру көбінесе жылу шығара жүреді.
Газдар еріген кезде жоғарыда көрсетілген процестср кезіндегі байқалатын жылулардан басқа жалпы еру жылуына газ көлемінін еріткіш су көлеміне дейін кішіреюі кезінде бөлінетін жылудың әсер ететінін еске алып еру жылуын былай жазады:
Газдар ерігенде молекулааралық байланысты үзуге жылу аз сіңірілетіндіктен еру процесі көбінесе жылу шығара жүреді.
Заттардың еріткіштерде еруі қанық ерітінді түзілгенше өздігінен жүретін процесс. Қез келген процесс өздігінен бос энергиясын немесе изобара-изотермалык потенциалын азайту бағытында жүретіні бұрын айтылды, ал изобара-изотермалық потенциалдың мәніне энтальпиялық және энтропиялық факторлар әсер етеді.
Теңдеу заттардың өздігінен еруіне энталышянын азаюы және энтропияның көбеюі көмектесетінін көрсетеді.
Жоғарыдағы айтылғандарға сәйкес кейбір кристалды қатты заттар ерігенде жылу бөлінуі, ал баска бір кристалды заттар ерігенде жылу сіңірілуі мүмкін, ал барлық кристалды заттар ерігенде жүйедегі тәртіпсіздік күшейіп, соған байланысты энтропиялары артады. Сондықтан еру кезінде энтролияныц артуы барлық катты заттардың еруіне көмектеседі. Жылу бөлу аркылы жүретін катты заттардың өздігінен еруіне энтальпияныц азаюы да және энтропияныц көбеюі де көмектеседі. Бұған мысал ретінде натрий гидроксидінің көп жылу шығарып еруін келтіруге болады. Қейбір қатты заттар ерігенде жылу сіңіріледі, ал энтальпиянын, көбеюі ол заттың ездігінеғг еруіне кедергі жасайды. Сондықтан мұндай қатты заттар энтропияның көбеюі нәтижесінде яғни, энтропиялық фактордың есебінен жүреді.
Энтропиялық факторды арттыру үшін көбінесе еру процесін жоғары температурада жүргізеді.
Бүған мысал ретінде жылу сіңіре еритін аммоний нитратының өздігінен еруін келтіруге болады.
Газдардың еруі энтальпиянын, да, энтропияның да азаюы арқылы жүреді. Энтропиянын. азаюы еруге кедергі жасайтындықтан, олардын, өздігінен еруі негізінен энтальпиялық фактордың есебінен жүреді. Теңдеуден температураны арттыру энтропиялық фактордың абсолюттік мәнін арттыратынын көрсетеді, ал ол энтальпиялық және эитропиялық факторлардың өзара теңестіріледі.
Тұрақти температура газда-дың ерігіштігі қысымның өсуіне тура пропорционал.
Сұйықтардың сұйықта ерігіштігі температураның жоғарылауына байланысты артады, ал қысымға байланысты болмайды. Қатты зат-тардың сүиыкта ерігіштігі температура өскен сайын артады, ал кысым онша әсер етпейді.
Ерітінділердің концентрациясын көрсету жолдары
Ерітінділердің маңызды сипаттамаларының біріне концентрация жатады. Концентрация - ерітіндінің немесе еріткіштің белгілі мөлшеріндегі еріген заттың мөлшері.
Ерітіндінің концентрациясын шамамен анықтау үшін коицент р а ц и я л ы қ және с ұ й ы т ы л ғ а н деген түсініктер колданылады.
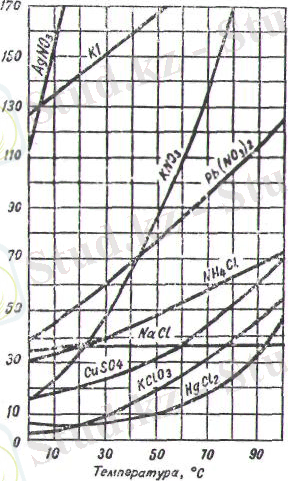
Кейбір тұздардьщ ерігіштігінің температураға байланыстылығы концентрацнялы ерітіндіде еріген заттың мөлшері көп болады, ал сұйытылған ерітіндіде еріген заттын. мөлшері аз болады.
Мысалы 100 г суда 50 г калий иодиды еріген болса бұл концентрациялы, ал 100 г суда 0, 5 г, калий иодиді еріген десе бұл сұйытылған ерітінді, себебі бірінші ерітіндіде еріген заттың мөлшері көп, екінші ерітіндіде аз.
Концентрациялы және сұйытылған деген ұғымдар еріген заттың дәл мөлшерін көрсете алмайды және бұл екі ерітіндінің арасында белгілі бір шек болмайды.
Ерітіндінін. массасы тұрақты болғанда оның концентрациясы үлеспен немесе процентпен көрсетіледі.
Массалық үлес - еріген зат массасы ерітінді массасының неше үлесі екенін көрсететін сан.
Массалық процент - ерітіндініқ 100 массалық бірлігінде еріген заттың неше массалық бірлігі бар екенін көрсететін сан.
Массалық процент, массалық үлестен 100 есе көп болады, яғни массалық үлестен массалык процентке көшу үшін массалық үлесті 100 көбейту керек.
Молярлык үлес ерітіндідегі барлық молекулалардын каншасы еріген заттың молекулаларыныц үлесіне тиетініи көрсететін сан. Еріген зат пен еріткіш молекулаларының үлестерінің косындысы 1, ал олардың молекулалық проценттеріиін қосындысы 100 тен. Жай заттардан тұратын ерітінділердін, (құймалардын, жер кыртысындағы элементтердің таралуын) концентрацияларын а т о м д ы қ ү л е с п е н немесе атомдық процентпен керсетеді.
Көлемі түрақты ерітінділердін. концентрациясын еріген заттардың молі, эквиваленті, массасының санымен көрсетеді.
Молярлық концентрация 1 л ерітіндіде еріген заттьщ моль санымен өлшенеді. Ерітіндінің 1 л еріген заттың моль санына байланысты ерітіндінің концентрациясын бір молярлы (1), екі моляр-лы (2), децимолярлы (0, 1), сантимолярлы (0, 01) т. б. деп атайды. Нормальдық концентрация 1 л ерітіндіде еріген заттын. эквивалент санымен өлшенеді. Нормальдық концентрацияда еріген заттың 1 л эквивалент санына байланысты бір нормальды (1), екі нормальды (2), децинормальды (0, 1) т. б. деп аталады.
Эквиваленттер заңына сәйкес нормальдық концентрациялары бірдей заттардың бірдей келемдері реакцияға қатысады.
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz