Газдардың тұтқырлығы мен диффузиясының кинетикалық теориялық негіздері


ГАЗДАРДЫН ТҰТҚЫРЛЫҒЫ (ІШКІ КЕДЕРГІ)
 Газдардың тұтқырлығы (мұны сұйықтар жайлы да айтуға болады) дегеніміз газдың түрліше қабаттарының қозғалыс жылдамдықтарының теңгерісу қасиеті болып табылады. Газдың түрліше жылдамдықтардағы іргелес қабаттарының жылдамдықтарының теңесуі газдың үлкенірек жылдамдықтағы қабатынан азырақ жылдамдықпен қозғалатын қабатына импульс тасымалдаудың, әсерінен болады.
Газдардың тұтқырлығы (мұны сұйықтар жайлы да айтуға болады) дегеніміз газдың түрліше қабаттарының қозғалыс жылдамдықтарының теңгерісу қасиеті болып табылады. Газдың түрліше жылдамдықтардағы іргелес қабаттарының жылдамдықтарының теңесуі газдың үлкенірек жылдамдықтағы қабатынан азырақ жылдамдықпен қозғалатын қабатына импульс тасымалдаудың, әсерінен болады.
Егер сыртқы күштер түрліше қабаттардың қоз-ғалыс жылдамдықтарының айырымының тұрақ-тылығын қамтамасыз ете алатын болса, онда қабаттан қабатқа импульс ағыны да тұрақты (ста-ционар) болады, әрі бұл ағын жылдамдықтың түсу бағытында бағытталады.
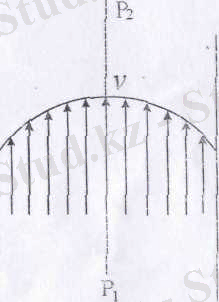
Газ түтіктің бойымен аққан кезде түрліше қабаттардың жылдамдықтары 7. 8-суретте көрсетілгендей болады, онда тілшіктер газдың қозғалыс жылдамдының векторлары болып табылады. Ең үлкен жылдамдық ортада, түтіктің өсіне тақау жерлерде болады да ал түтіктің қабырғасына жуықталған сайын жылдамдықтар азайып, ақыры, түтіктің қабырғасына тақау қабат тыныштықта болады.
Мұндай ағыс кезінде импульс жылдамдығы максимал болатын газдың орталық қабатынан баяуырақ қозғалатын қабаттарға қарай беріледі. Бұл процесс кезінде импульс өзгеретін болғандықтан, газдың бұл ағыны оған сыртқы күш әсер ететін секілді өтеді (ішкі үйкеліс күші) .
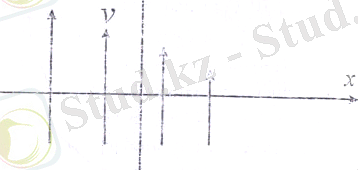 Импульс тасымалдауды да сандық жағынан жылу өткізгіштік кезіндегі энергияның тасымалдануы тәрізді қарастыруға болады. Газдың қозғалыс жылдамдығының өзгерісі бұл жағдайда газдың қозғалыс жылдамдығы бағытын перпендикуляр болатын Х өсінің бағытында өсетін болсын.
Импульс тасымалдауды да сандық жағынан жылу өткізгіштік кезіндегі энергияның тасымалдануы тәрізді қарастыруға болады. Газдың қозғалыс жылдамдығының өзгерісі бұл жағдайда газдың қозғалыс жылдамдығы бағытын перпендикуляр болатын Х өсінің бағытында өсетін болсын.
Х өсіне перпендикуляр бағытта қозғалыс жылдамдығы барлық нүктелерде бірдей болады. Бұл дегеніміз V жылдамдық тек Х кординаттың ған функциясы болып табылады деген сөз. Онда тәжірбие, көрсеткендей, 1с ішінде х өсіне перпендикуляр орналасқан 1 см 2 қима арқылы алынып өтілетін Z импульс
Z = n du
dx (7. 14)
теңдеуімен анықталады, мұндағы du/ dx - жылдамдықтың х өсі бойындағы градиенті, ол - жылдамдықтың осы өстің бойындағы өзгеріс жылдамдығын сипаттайды. Минус таңбасы импульстың жылдамдықтың төмендеу бағытында тасымалданатындығын көрсетеді.
n коэфиценті тұтқырлық немесе газдың ішкі кедергісі коэффиценті деп аталады, ол да, дифуиза коэффиценті және жылу өткізгіштік коэффиценті тәрізді газдың қасиеттеріне тәуелді болады. Теңдіктен анықталған n коэффиценті кейде динамикалық тұтқырлық коэффиценті деп аталады да, ал қатынасымен анықталатын коэффицентті кинематикалық тұтқырлық коэффиценті деп аталады, мұндағы р- газдың тығыздығы.
Тұтқырлық коэффиценті бірлік уақытта 1см қима арқылы жылдамдықтың бірлік градиенті кезінде тасымалданатын импульске тең болады. СИ дегі тұтқырлықтың өлшем бірлігі 1кг/м с= 1 G7f7c7
Газдардың тұтқырлық коэффицентін есептеу шығару. Егер газ қайсыбір р жылдамдықпен ағып жатса онда оның барлық молекулаларының олардың шылулық қозғалысы жылдамдығына үстеме осындай жылдамдығының болатындығы. Демек, әрбір молекуланың барлық молекулалар үшін бірдей бағытталған ту импульсы болады. Көбіне газдың ағым жылдамдығыоның молекулаларының жылулық қозғалысының орташа жылдамдығының көш кіші болады.
Газдың ағыс жылдамдығына параллель демек, импульстің тасымалдау бағытына перпендикуляр орналасқан S ауданшаны қарастырайық. Газдың ағым жылдамдығы Х өсі бағытында төмендейтін болсын, яғни ауданшаның оң жағында ағыс жылдамдығы оның сол
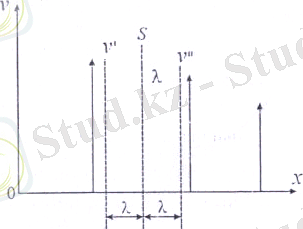 жағындағы қарағанда төменірек. Газдың екі қабаттарының арасындағы молекулалар алмасудың арқасында (мұндай алмасулар молекулалардың жылулық қозғалысының әсеріне болады) бұл айырмашылық төмендейді S ауданшаның оң жағындағы молекулаларсол жатқан келген жылдамдықтары жоғарырақ болатын демек, импульстері жоғарырақ молекулалармен алмасады. Осы молекулалардың осыған дейін S ауданшаның оң жағында болған кезінде, ағыстың үлкен жылдамдығы оң жақта болған барлық молекулаларға таралып осы қабаттың ағыс жылдамдығы, демек импулсіартады, ал S ауданшаның сол жағындағы газ қабатының импульсі төмендейді.
жағындағы қарағанда төменірек. Газдың екі қабаттарының арасындағы молекулалар алмасудың арқасында (мұндай алмасулар молекулалардың жылулық қозғалысының әсеріне болады) бұл айырмашылық төмендейді S ауданшаның оң жағындағы молекулаларсол жатқан келген жылдамдықтары жоғарырақ болатын демек, импульстері жоғарырақ молекулалармен алмасады. Осы молекулалардың осыған дейін S ауданшаның оң жағында болған кезінде, ағыстың үлкен жылдамдығы оң жақта болған барлық молекулаларға таралып осы қабаттың ағыс жылдамдығы, демек импулсіартады, ал S ауданшаның сол жағындағы газ қабатының импульсі төмендейді.
Басқаша айтқанда жылулық қозғалыстың арқасында пайда болатын молекулалар алмасу газдың түрліше қабаттарының ағыс ыжлдамдықтарының теңгерісуіне әкеп тірейді. Газ ағысындағы бір қабаттан екінші қабатқа Х өсінің бағытында импулс тасымалдау механизмі осындай болып табылады. S ауданшаның бірлік ауданы арқылы бірлік уақытта тасмалданатын импулс ағынының L шамасы S ауданшаны солдан оңға және оңнан солға кесіп өтетін молекулалардың алып өтетін L 1 және L 2 импулстерінің айырымымен анықталады. Молекулалардың солдан оңға қарай алып өтетін L 1 импульсі бір молекуланың импульсін бірлік уақытта бірлік ауданы кесіп өтетін молекулалар санына көбейткенде тең болады. Бұл молекулалар саны (1/6) болады (п-бірлік көлемдегі мелекулалар саны v - молекуласының жылулық қозғалысының орташа жылдамдығы) . Жеке молекуланың S ауданды кесіп өткен кезде алып өтетін импульсі оның ауданшаны кесіп өтердің алдындағы соқығысу кезіндегі импульсі яғни оның S ауданшаданорташа еркін өту жолына тең қашықтықтағы импульсі болып табылады. Егер газ ағыс жылдамдығы S ауданшаның сол жағынан қашықтыққа V болса, онда молекуланың газдың ағыс жылдамдығына байланысты импульсі болады. (m - молекуланың массасы) . Сонымен:
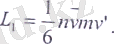
Дәл осы тәрізді S ауданшаның оңнан солға қарай кесіп өтетін молекулалар үшін.
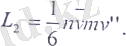
Мұндағы V- S ауданшаның оң жағынан L қашықтықтағы газдығ ағыс жылдамдығы. Бірлік аудан арқылы бірлік уақытта алынып өтілетін қорытқы L импульс
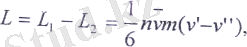
мұндағы V 1 - V 11 - газ ағымының бір-бірінен 22 қашықтықта орналасқан айырымы, яғни
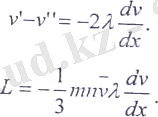
Осы өрнекті (7. 14) өрнектеп салыстырып, тұтқырлық коэффиценті үшін мынаған келеміз:
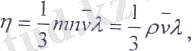
Мұндағы р - газдың тығыздығы.
Осы алған өрнектеп көріп отырғанымыздай, тұтқырлық коэффиценті қысымға тәуелсіз болады, тәжірбиеде осыны дәлелдейді.
Жылу өткізгіштік коэффиценті мен тұтқырлық коэффицентің арасында қарапайым байланыс бар:
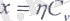
Мұндағы С- тұрақты көлем кезіндегі меншікті жылу сыйымдылық.
Жылу сыйымдылық коэффиценті тәрізді тұтқырлық коэффиценті де температураға заңы бойынша тәуелді болады, себебі оның құрамына да орташа жылдамдық v кіреді.
Газдардағы тасымалдау құбылыстары.
Диффузия. Газ молекулалары тәртіпсіз қозғалып тұратындықтан олар өнебойы араласып отырады, осыдан барып тиісіп тұрған әр текті екі газ бірінің ішіне бірі кіріп араласады-диффузияланады. Газдардағы ішкі үйкеліс және жылу өткізгіштік құбылыстарының механизмі де газ молекулаларының бір орыннан екінші орынға келіп тұруына байланысты. Молекулалардың қозғалысына байланысты болатын осы кұбылыстардың барлығы да көшу кұбылысы немесе тасымалдау құбылысы. деп аталады.
Газдардың кинетикалық теориясының дамуы кезінде бұл теорияға мына түрде карсы пікірлер болды: егер молекулалар козғалысының жылдамдығы, газдардың кинетнкалық теориясында айтылғандай, секундына бірнеше жүз метр шамасында болатын болса, молекулалар өте жылдам араласуы керек. Мысалы, егер бөлменің бір жерінде иісі шығатын заты бар ыдыстың аузын ашқанда, иіс бөлменің барлық жеріне бірден білінуі, керек еді, өйткені зат молекулаларының бөліменің ол шетінен бұл шетіне ұшып баруына секунттық үлестеріндей ғана уақыт кетеді. Ал анығында атмосфералық қысымда газдардың диффузиясы өте жай болады; мысалы, оның ішінде иіс өте жай тарайды. Бұлай деп ойлаудағы қателік - атмосфералық кысымда еркін жолдың ұзындығы аз болатындықтан, молекулалар басқа молекулалар мен үэдіксіз соқтығысып отыратындығын, сонымен катар олар бір орында «тыпырлап» тұрып қалатындығын еске алмауда болып отыр.
Жылдамдығының үлкендігіне қарамастан молекула өзінің бастапқы тұрған жерінен бір секундта өте аз жерге ғана жылжып бара алады; оның жүрген жолы өте күрделі және шатасқан сынақ сызық сияқты болады.
Ең алдымен диффузия құбылысын қарастырамыз. Бақылауларға карағанда диффузия кезінде бір кішкене, ДS ауданы арқылы өтетін (тасымалданатын) газдың ДМ массасы, осы ДS аудан неғұрлым үлкен болса, диффузияны бақылау уақыты Дt неғұрлым ұзақ болса және диффузияланатын газдың р парциялық тығыздығы ДS ауданға перпендикуляр бағыт бойынша неғұрлым тезірек өзгерсе, соғұрлым көп болады. ДS ауданға нормаль етіп, 0X өсін жүргізейік; қарастырылып отырған газдың бірінен-бірі Ах кашықтықта тұрған екі нүктедегі парциналық тығыздығының айырмасы Др болсын, сонда D/p D/x шама газдың р тығыздығының ОХ өсінің бағыты бойынша бір ұзындық бірлігіне келетін өзгерісін сипаттайды; бұл шама т ығыздық градиенгі деп аталады. Бұл айтылғандардан, АМ масса мөлшері Др D /х тығыздық градиентіне, ДS ауданның шамасына және Дt уақытқа пропорционал болып шығады:
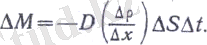
Газдың сортына және оның қандай жағдайда екендігіне байланысты болатын О шама диффузая коэффициенті деп аталады. Минус таңбасы массаның тығыздықтың кему жағына қарай тасымалданатындығын көрсетеді.
(1) формула диффузия кұбылысын макроскопиялық тұрғыдан сипаттайды.
Енді диффузия кұбылысың газдардың молекула-гинетикалық теориясы тұрғысыпан қарастырайық. Өз ара араласатын әр түрлі екі газ алайық та, қарастыруды жеңілдету үшін, олардың молекулалары, массалары және эффективті қималары біріне-бірі тең деп айтарлықтай, ұксас болсын делік.
Мұндай молекулалардың бірдей жағдайларда еркін жолының ұзындықтары да, жылдамдықтары да бірдей болады.
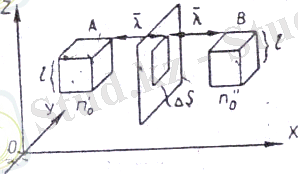 Бұл екі газдың біреуінің ДS аудан арқылы өтетін молекулаларының саның есеп-тейік, бұл ДS аудан бойын қуалай газдың тығыздығы өзгеретін
ОХ
өске перпендикуляр болсын. Ауданның он жағынан да, сол жағынан да, еркін жолдың орташа ұзындығының мәніне тең аралықтан А және В куб көлемдерді алайық. Сонда осы екі куптың қайсысынан болса да ұшып шыққан молекулалар басқа молекулаларға соқтығыспай ДС ауданға келіп жетеді деп айтуға болады.
Бұл екі газдың біреуінің ДS аудан арқылы өтетін молекулаларының саның есеп-тейік, бұл ДS аудан бойын қуалай газдың тығыздығы өзгеретін
ОХ
өске перпендикуляр болсын. Ауданның он жағынан да, сол жағынан да, еркін жолдың орташа ұзындығының мәніне тең аралықтан А және В куб көлемдерді алайық. Сонда осы екі куптың қайсысынан болса да ұшып шыққан молекулалар басқа молекулаларға соқтығыспай ДС ауданға келіп жетеді деп айтуға болады.
А мен В кубтердің бүйір жақтары DS ауданға параллел және шамасы жағынан оған тең болсын; кубтер қырының ұзындығын әріппен белгілейміз; сонда І = DS екендігі өзінен өзі түсінікті. Қарастырылып отырған газдың А кубтегі молекулаларының санын п А деп белгілейміз. Молекулалардың қозғалысы тегісімен тәртіпсіз болатындықтан, 46-парагорвта анықталғандайосы молекулалардың 1/3, үлесі ОХ өсінің бойымен қозғалады, ал бұлардың жартысы ОХ өсінің оң бағытына қарай екінші жартысы сол бағытына қарай бағытталады деп есептеуге болады.
Сонымен А кубтегі пА молекулаларың алтыдан бір бөлігі яғни 1/6 пА молекуласы DS ауданқа қарай ұшады. DS аудан кубтен 2 аралықта тұрғандықтан осы молекулалардың барлығы да DS ауданға соқтығыспай ұшып жетеді де, әрі қарай өтеді. Осы 1/6 пА молекулалардың DS ауданнан ұшып өтулеріне кететін уақыт А кубтен шыққан молекулалардың ең соңғылары DS ауданға алдыңғыларынан кешііп келген уақытындай уақытқа тең болады; бұдан дt = t мұндағы v - молекулалардың DnA саны мыналарға тең болады: v
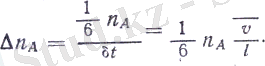
- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz