Көміртек, кремний, азот, фосфор, оттек, күкірт, хлор, йод және судың периодтық орны, таралуы, физикалық-химиялық қасиеттері, алынуы және қолданылуы


Көміртек, кремний, азот, фосфор, оттек, күкірт, хлор, йод, су
- Периодтық жүйедегі орны, атом құрылысы
- Табиғатта таралуы
- Физикалық қасиеттері
- Химиялық қасиеттері
- Алынуы
- Қолданылуы
Көміртек
- Көміртек II период, IV топтың негізгі топшасының элементі, реттік нөмірі 6. Оның ядросында 6 протон мен 6 нейтроны бар, электрондары да алтау. Олар екі қабатқа былай бөлініп орналасады: 1s22s22р2(көміртектің электрондық формуласы) . Көміртек химиялық элементтердің периодтық жүйесінің 6-элементі. Олар екі энергетикалық деңгейге бөлініп орналасқан: 2е, егер периодтағы көрші тұрған элементтерді салыстырсақ, олардың бәрінің бірінші деңгейлері бірдей, екі электроны бар (1s2), ал сыртқы деңгейлеріндегі электрон сандары ядро зарядының артуына байланысты әр түрлі.
- Көміртек бос күйінде алмаз, графит, карбин деп аталатын аллотропиялық күйлерінде кездеседі. Табиғи қосылыстары карбонаттар (СаСО3• MgCО3- доломит, СаСО3- мәрмәр, MgCО3- магнезит) . Байланысқан күйде көмірде, мұнайда, табиғи газдарда кездеседі. Бос күйінде көміртек улы емес, ал оның қосылыстары CO - иіс газы, ССl4- төрт хлорлы көміртек, CS3- күкіртті көміртек улы заттар.
- Алмазең катты зат, графитмай тәрізді жылтыр сұр түсті жұмсақ зат. Графит 2000°С-да, төменгі . Жаңадан алынған фуллерен деген түрі де бар, ол футбол добы сияқты құрылысты болады. Көміртектің бұл түр өзгерістеріне аморфты көміртекті қосуға болады. Оны ағаш көмірін, тас көмірді ауа қатысынсыз құрғақ айдау арқылы алады. Сонда алынған көмірде өз бетіне газдарды, сұйықтарды сіңіретін қасиет (адсорбция) пайда болады.
- Көміртек көптеген жай заттармен оңай әрекеттеседі.
1) Жану реакциясы
a) 2С + О 2 = 2СО
ә) С + О 2 = CO 2
Хлормен әрекеттескенде көміртек тек жарық сәулесінің әсерінен төрт хлорлы көміртек түзіледі:
С + 2Cl 2 = CCl 4 (бағалы еріткіш) өрт сөндіруде қолданылады.
Металдармен әрекеттесіл карбидтер түзеді:
2С + Са = СаС 2 (бұдан ацителин алынады)
Күкіртпен күкіртті көміртек түзеді:
С + 2S = CS 2 (еріткіш)
Сутекпен әрекеттескенде метан түзіледі:
С + 2Н 2 →СН 4 (отын - ол табиғи газдың негізгі құрам белігі)
- Көміртек ағашты ауасыз ыдырату арқылы, органикалық заттардың көмірленуі нәтижесінде түзіледі.
Кремний
- (Sіlіcіum), Sі - элементтердің периодтық жүйесінің ІV тобындағы элемент. Тұрақты 3 изотопы -28Sі, 29Sі және 30Sібар. Жер қыртысындағы мөлшері 29, 5%. Табиғатта оттектен кейінгі көп тараған элемент. Электрондық формуласы 1s22s22p63s23p2
- Кремний - оттектен кейінгі жер бетінде ең таралған элемент. Ол жер қыртысының 27, 6% -ын құрайды. Табиғи кремнийдің едәуір бөлігі құм немесе кварц түрінде кездесетін кремнезем деп аталатын кремний оксиді болып табылады. Өте таза кристаллкүйдегі кремний оксиді тау хрусталі деп аталатын минерал түрінде кездеседі
Кремнийдің түсі күңгірт-сұр, шайырдай жылтыр, салмағы 2, 32 г/м 3 , балқу t 1420С, қайнау t 2600С-қа жуық. Өнеркәсіпте Кремний кремнеземді қыздырып, кокспен тотықсыздандыру, ал таза кремний төрт хлорлы кремнийді мырыш буымен тотықсыздандыру арқылы алынады.
Қыздырғанда сутектен басқа кез келген бейметалмен қосыла алады. Төменгі температурада инертті. Таза кремний темір, мыс, алюминий, қорғасын қорытпаларында қолданылады. Ол мұндай қорытпалардың қышқылдарға төзімді, мықты, электрлік және магниттік қасиеттерін арттырады.
Кремний тау хрусталі немесе кварц (Si0 2 ) құрамында болады; ол (Si) қиын балқитын, металдық жылтыры бар, сұр түсті қатты зат. Оның каттылығы алмаздан төмендеу.
Аморфты кремний коңыр түсті ұнтақ, реакцияға түсуі оңай зат.
- Жай заттармен:
- Si + 02= Si02(кремний оксиді)
- Si + 2F2= SiF4(кремний фториді)
- Si + C = SiC (карборунд)
- Si + 2Mg = Mg2Si (магний силициді)
Күрделі заттармен: Сілтінің ерітіндісімен қыздырғанда әрекеттеседі. Si + 2NaOH + Н 2 0 = Na 2 Si0 3 + 2Н 2 ↑
- зертханадаSi02+ 2Mg = Si + 2MgO
өндірісте Si0 2 + 2C = Si + 2CO
Азот
- Азот( гр. ázōos- тіршіліксіз) - химиялық элемент- N - элементтердің периодты жүйесінің V тобындағы химиялық элемент, реттік нөмірі - 7, атом салмағы - 14. 0067. Табиғатта екі изотопы кездеседі:14N (99. 635%), 15N (0. 365%) . Электрондық формуласы 1s22s22p3
- Aзот табиғатта өте көп тараған элементтің бірі болып есептеледі. Жер бетіндегі оның негізгі түрлері - литосферадағы байланысқан және атмосферадағы молекулалық азот. Атмосферадағы бос азотты өсімдіктер өздігінен сіңіре алмайды. Органикалық заттар шірігенде ондағы азоттың біраз бөлігі аммиакқа айналады. Топырақтағы нитрлеуші бактериялардың көмегімен сол аммиак азот қышқылына дейін тотығады. Өз кезегінде топырақтағы карбонаттар СаС03 қышқылмен реакцияға түсіп, нитратқа айналады да өсімдікке сіңеді. Шіру процесі кезінде азоттың біраз бөлігі атмосфераға бос күйінде бөлініп отырады. Табиғи жағдайда топырақтағы байланысқан азоттың мөлшері кемімейді. Ауадағы бос азот та түрлі себептермен толықтырылып отырады. Мысалы, ағаш, шымтезек (торф), таскөмірді жаққанда, органикалық заттар шірігенде, атмосфераға азот бөлінеді
- Азот көлемі бойынша ауаның 78%-ын құрайды. Ол - түссіз, иіссіз, суда нашар еритін, ауадан сәл ғана жеңіл D (ауа) = 0, 97, D (H2) = 14 болатын, жануды қолдамайтын, тыныс алуға жарамсыз газ. Ауадағы 1 л азот газының массасы 1, 25 г. Азот -196°С-та сұйылады, -210°С-та қатады (қар тектес) .
- Aзотхимиялық реакцияларда әрі тотықтырғыш, әрі тотықсыздандырғыш. Азот оттегімен, фтормен әрекеттескенде тотықсыздандырғыш болса; фосформен, сутегімен, алюминиймен әрекеттескенде тотықтырғыш болады. Азот молекуласы өте берік болуына байланысты реакцияга түсу қабілеті төмен, химиялык енжар зат. Жоғары температура мен кысымда, өршіткі (катализатор) қатысында азот сутекпен тікелей әрекеттесіп, аммиак түзеді:
N2 + 3H2 = 2NH3
Бос күйдегі азот оттекпен электр ұшқыны кезінде әрекеттеседі. Табиғатта бұл реакция найзағай жарқылдағанда жүреді:
N2 + О2 = 2NO
Бөлме температурасында азот тотықтырғыш ретінде тек металл литиймен әрекеттеседі:
N2 + 6Li = 2Li3N
Қыздырғанда басқа металдармен де осылайша әрекеттеседі:
3Mg + N2 = Mg3N2
- Азот молекуласы - берік қосылыс. Ол тотықтырғыш ретінде ерекше жағдайда металлдармен, сутекпен әрекеттеседі. Табиғатта азот бос күйінде кездеседі, ол ауаның негізгі құрам бөлігі. Селигралардың құрамында болады. Азот адам және жануарлар, өсімдіктер организмінде маңызды тіршілік процестерін жүзеге асыратын нәруыздың құрамына кіреді
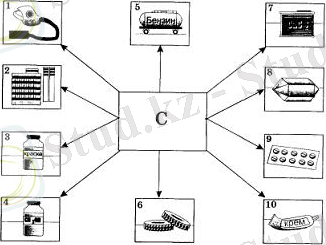
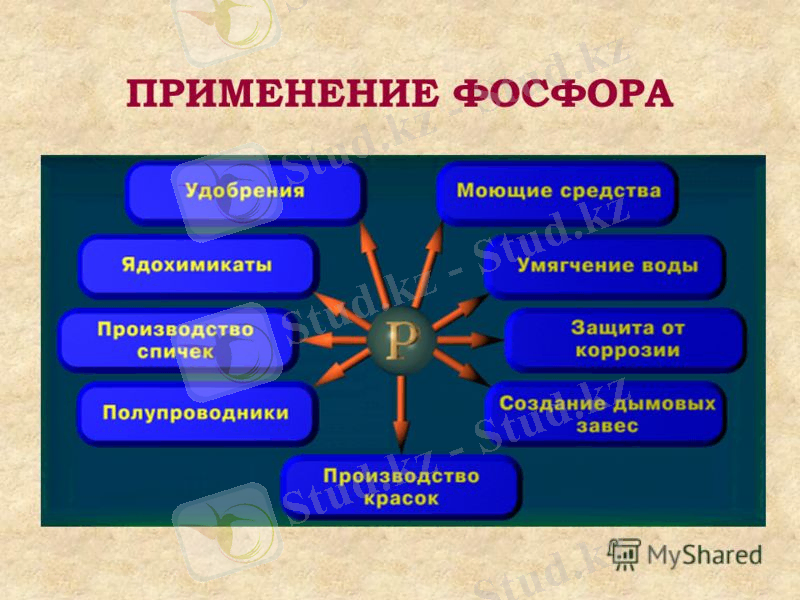
- Азот химиялық синтезде инертті атмосфера жасау үшін пайдаланылады. Тоңазытқышта, медицинада, аммиак алу үшін қолданылады. [4] Сұйық азот салқындаткыш жүйелер саласында кеңінен қолданылады. Азот, негізінен, аммиак алуға, одан әрі азот қышкылы және азот тыңайтқыштарын алу үшін қолданылады. Азотты салғырт (инертті) атмосфералық орта жасау үшін де пайдаланады (электр лампасын толтыруға, т. б. ) .
.

Фосфор
- Фосфор(лат. Phosphorus), P - элементтердің периодтық жүйесінің V тобындағы химиялық элемент, реттік нөмірі - 15, атомдық массасы 30, 97. Фосфордың соңғы энергетикалық қабатында бес электрон бар, оның үшеуі жұптаспаған. Фосфор атомындағы электрондардың орналасуы:
Электрондық формуласы:
1s 2 2s 2 2р 6 3s 2 3f
Фосфор косылыстарында -3, +3, +5 тотығу дәрежесін көрсетеді. Фосфордың ұшқыш сутекті қосылысы фосфин РН3мен аммиак NH3 молекулалары формасы жағынан ұқсас болғанмен, фосфин молекуласы берік емес, улы, тұрақсыз газ, тез тотығып кетеді.
- Табиғатта фосфор тау жыныстары мен минералдарда қосылыс түрінде кездеседі. Мысалы, фосфорит және апатитте кальций фосфаты Са3(РO4) 2түрінде болады. Қазақстанда Жамбыл облысындағы Қаратау маңында фосфорит кенінің мол коры бар екені 1935 жылдан белгілі. Қазір Қаратау бассейні негізінде "Жаңатас байыту комбинаты" жүмыс істейді. Ақтөбе облысында фосфорит кен орнын (Шилісай, т. б. ) игеру жоспарланып отыр. Осы кен орындары негізінде фосфорды өңдейтін зауыттар Таразда, Шымкентте және Ақтөбеде бар. Азот тәрізді фосфор да өсімдік пен жануар нәруызының негізгі құрам бөлігі. Фосфор өсімдіктердің дәнінде, жануарлардың сүтінде, қанда, ми мен жүйке ұлпаларында кездеседі. Мысалы, ересек адамдардың сүйегінде 600 г, ет ұлпасында 56 г, жүйке жүйесінде 5 г-ға дейін фосфор болады.
- Фосфор элементі жай зат ретінде бірнеше аллотропиялық түрөзгерісін түзеді. Оның маңыздылары - ақ және қызыл фосфор. Ақ фосфор улы жөне тез тұтанатын болғандықтан аса ұқыптылықты қажет етеді. Оның буымен демалуға болмайды. Ақ фосфорды шыны ыдыста, су астында, сыртынан құм салынған металл банкаға орналастырып сақтайды. Ақ фосфор ауасыз кеңістікте қыздырғанда қызыл фосфорға, ал жоғары қысымда қара фосфорға айналады. Қара фосфор аз кездеседі (20-сурет) . 6-кестеде ақ жөне қызыл фосфордың қасиеттері салыстырмалы түрде берілген.
- 2Р + ЗСl2= 2РСl3галогендермен галогенидтер береді
2Р + 3S = P 2 S 3 күкіртпен сульфид түзеді
ЗСа + 2Р = Са 3 Р 2 металмен фосфид түзеді
Фосфор өзінің аталуына сәйкес (грекшеден аударғанда “жарық шығарғыш” деген мағынаны білдіреді) ауада оттекпен жарық шығара отырып, қарқынды әрекеттеседі. Осы тәжірибені жасап көрейік. Әуелі шыны қалпақшының тығыны зат жағатын темір қасықшаны өткізеді. Себебі фосфор жанғанда, ақ түтін будақтап, оның оксиді түзіледі. Ол ауада шашылмас үшін қасыққа салынған фосфорды спирт шамы жалынында қыздырып, жана бастағанда шыны қалпақшаға кіргізіп тығындайды. Сонда түзілген фосфор (V) оксиді бірте-бірте төмен қонып, суда ериді. Енді реакция теңдеуін жазайық:
- Бос күйіндегі фосфорды алу үшін табиғи фосфатты электр пеште кремний (IV) оксиді мен көмірді косып қыздырады. Бөлінген фосфордың буын су астында ақ фосфор Р түрінде бөліп алады. Реакция теңдеуі:
Са 3 (РО 4 ) 2 + 3SiО 2 + 5С = 3CaSiО 3 + 5CО↑ + 2Р
Оттек
- Элементтердің периодтық жүйесінің VІ тобындағы хим. элемент, ат. н. 8, ат. м. 15, 9994. Қалыпты жағдайда О. түссіз, иіссіз, дәмсіз газ. Үш изотопы (16О, 17О, 18О) бар. Электрондық формуласы: 1s22s22p4. Өнеркәсіпте оттекті көп мөлшерде сұйық ауаны айдау арқылы алады. Ол үшін ауаны алдымен шаң- тозаңнан, ылғалдан және көмірқышқыл газынан тазартады. Одан соң ауаны қатты қысып суытады. -200°С-та ауаның құрамындағы оттек пен азот сұйық күйге ауысады да көкшіл сұйықтыққа айналады. Енді оттекті азоттан бөліп алу үшін аздап қыздырады.
- Оттегі - жер қыртысында ең көп таралған элемент, оның үлесі ( қосылыстардың түрлі тұратын, негізінен силикаттар ) қатты жер қыртысының массасының шамамен 47 % құрайды . 85, 82 % ( салмағы бойынша ) - Теңіз және тұщы су оттегі үлкен мөлшерін қамтиды. Оның құрамы қосылыстардың қыртысының 1500-ден астам оттегі құрамында
- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz