Атмосферадағы оттегінің эволюциясы мен фотосинтез процесі


Қазақстан Республикасы Білім жене Ғылым министрлігі Шәкәрім атындағы Семей мемлекеттік университеті
СӨЖ
Тақырыбы : Атмосферадағы оттегі эволюциясы және фотосинтез
Тексерген: Татенов А. Б
Орындаған: Мухамедиева Г. С
Топ: БЛ - 209
Семей - 2015 жыл
Оттегі (латынша Oxygenium), O - элементтердің периодты жүйесінің VI-тобындағы химиялық элемент. Реттік нөмірі 8, атом массасы 15, 999. Оттегі -химияның ең маңызды элементі және Жер бетіндегі көптеген тірі ағзалардың тыныс алуын қамтамасыз етеді. Оттегісіз біз бірнеше минут қана өмір сүре аламыз. Жасушалар мен талшықтар өмір тіршілігіне қажетті өздеріндегі энергияны босата отырып, органикалық заттарды тотықтыру үшін оттегіні пайдаланады. Оттегінің физиологиялық әсері өте көп қырлы, алайда, оның емдік әсерінде маңызды рөлді ағза талшықтардағы оттегі жетіспеушілігін орнына қайта келтіру қабілеті атқарады.
Адам ағзасының барлық мүшелері мен талшықтары қалыпты жұмыс істеуі үшін біздің айналамыздағы ауаның құрамында кем дегенде 21% таза оттегі болуы керек. Үлкен қала - бұл өте жылдам өмір ырғағы (біз күн сайын энергия жоғалтамыз), газдалған ауа (созылмалы гипоксия) ! Ірі мегаполис тұрғындарының оттегіне мұқтаждықтары орасан зор. Экологиялық ахуалдың жалпы деңгейде нашарлауы ірі қалаларда ауадағы таза оттегі мөлшері кейде 10-12%-дан артпауына алып келді. Осының салдарынан гипоксия (оттегі жетіспеушілігі) туындайды.
Оттегінің алынуы
Оттегін өнеркәсіпте ауаны қысып сұйылтады да, азот пен оттегінің қайнау температураларының айырмашылығына қарай буландырып бөліп алады. Осылайша алынған оттегі көгілдір түсті баллондарда сақталады, себебі сұйық оттегі ашық-көгілдір түсті болады. Ал зертханалық алу әдістері кейбір оттегіге бай күрделі қосылыстарды айыруға негізделген .
- Тұрмыста жиі қолданылатын «марганцовканы» айыру. Ол үшін құрғақ сынауыққа аздаған түйірлерін салып, оның аузын газ шығатын түтігі бар тығынмен жауып қыздырамыз. Сонда мына реакция жүреді:

Шоқтанған шырпыны түтіктің аузына апарсақ, ол лап етіп жанады, себебі оттегі жануды қолдайтынын сендер бұрыннан білесіңдер.
- Калий хлоратын айыру. Бұл реакцияның жүруін тездету үшін марганец (IV) диоксидін (өршіткі) қосамыз, сонда оттегі көп мөлшерде бөліне бастайды:
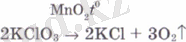
Өршіткі - реакцияның жылдамдығын өзгертетін, бірақ өзі жұмсалмайтын зат (МnO 2 - өршіткі (катализатор) .
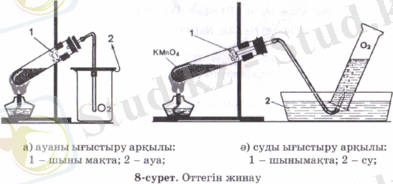
Бөлінген оттегін екі әдіспен жинауға болады.
- Ауадан сөл ауыр болғандықтан (Мr(O2) =32, Мr(ауа) =29) ауаны ығыстыру арқылы (8, а-сурет) .
- Суда нашар еритіндігінен суды ығыстыру арқылы жинау.
Оттегін сынап (II) оксидін (HgO) айырып ағылшын ғалымы Д. Пристли алған (1774) .
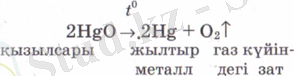
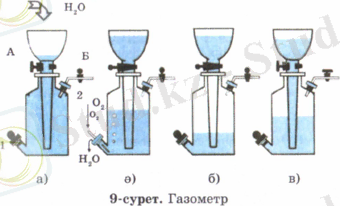
Газдарды зертханада жинайтын құрал газометр деп аталады. Ол қалың қабырғалы шыныдан жасалған екі бөлімнен тұратын ыдыс, оның сол жағында табанына жақын жерде (1) және оң жақ иығында (2) тығындалатын екі тесігі бар. Ал үстіңгі бөлігі (тубус) ұзын түтікті құйғы сияқты болып жасалған, ол астыңғы бөлігіне кигізілген. Оған газ жинау үшін тубустың шүмегін (А) ашып сумен толтырамыз. Одан кейін тубустың шүмегін жауып, астыңғы тығынға кигізілген шүмекті ашамыз да, осы жерден оттегін жібереміз, ол суды ығыстырып шығарады. Газды жинап болғаннан кейін астыңғы шүмекті жабамыз. Тәжірибеге оттегі керек болғанда тубустың шүмегін ашамыз, одан аққан су оттегін ығыстырады, ол жоғары оң жақ, иықтағы шүмектен (Б) шығады, оны бір ыдысқа жинап алу керек (9-сурет) .
Оттегінің қасиеттері Физикалық қасиеттеріОттегі (O 2 ) түссіз, суда аз еритін (20°С-та судың 100 көлемінде 3, 1 көлем O 2 ериді) газ күйіндегі зат. Қалыпты жағдайда (0°С, 1 атм=101, 3 кПа) 1 л оттегінің салмағы 1, 43 г, ал 1 л ауа - 1, 29 г болады.
Химиялық қасиеттеріОттегі қыздырған кезде көптеген заттармен әрекеттеседі, бұл үдеріс жану деп аталады, ол жылу мен жарықты бөле жүреді.
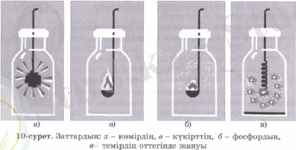


Бейметалдармен әрекеттесуін көру үшін оттегі толтырылған сынауыққа көмірдің түйірін салсақ, ол жарқырап жана бастайды (10-сурет) :
С + O 2 = СO 2
Түзілген көмір қышқыл газын әк суына жіберсек оның лайланатыны сендерге белгілі. Бұдан басқа күкірт, фосфор, т. б. бейметалдар да оттегінде жанады (11-сурет) :
S + O 2 = SO 2
4Р + 5O 2 = 2Р 2 O 5
Кейбір металдар да оттегінде жанып оксидтер түзеді. Мысалы, оттегімен толтырылған сынауыққа магний ұнтақтарын сепсек, оның жарқырап жанғанын көруге болады.
2Mg + O 2 = 2МgО
Болат сымның ұшына кішкентай көмір түйірін шаншып алып, оны тұтатып оттегімен толтырылған ыдысқа салсақ жанған көмірден бөлінген жылудың әсерінен темір жана бастайды (12-сурет) .
ЗFе + 2O 2 = Fе 3 O 4 (FеO•Fе 2 O 3 )
Элементтер оттегімен әрекеттесіп оксидтер түзеді, бұл тотығу үдерісі.
Оксидтер дегеніміз молекула құрамы екі элементтен тұрып, оның бірі оттек болатын күрделі заттар.
Оксидтерді атағанда элемент таңбасынан кейін жақшаның ішіне валенттілігі көрсетіледі де оксиді деген сөз қосылады. Мысалы, SO 2 - күкірт (IV) оксиді, SО 3 күкірт (VI) оксиді. Халықаралық номенклатура (атау әдісі) бойынша оксидтердің құрамындағы элемент атомдарының сандары грек сандарымен көрсетіліп аталады: CO - кеміртек монооксиді, СО 2 - көміртек диоксиді, МnO 2 - марганец диоксиді, Мn 2 O 7 - димарганец гептаоксиді.
Күрделі заттармен әрекеттесуіКейбір күрделі заттар да оттегінде жанып оксидтер береді, мысалы, тамақ пісіргенде ас үйдегі газ пешінде қолданылатын пропанның (С 3 Н 8 ) жануы:
С 3 Н 8 + 5O 2 = ЗСO 2 + 4Н 2 O
Автогендік әдіспен металдарды кесу мен жалғауда мына реакция жүреді:
2С 2 Н 2 + 5O 2 = 4СO 2 + 2Н 2 O
Металлургия өндірісінде өртеу пештерінде күрделі заттардың тотығу реакциялары жүреді:
2ZnS+3O 2 = 2ZnO + 2SO 2
Cu 2 S + 2O 2 = 2CuO + SO 2
Сонымен, оттегі жай және күрделі заттармен әрекеттескенде жану реакциялары жүріп, нәтижесінде әр түрлі оксидтер түзіледі.
Оттегінің табиғаттағы айналымы және қолданылуыТабиғатта оттегі негізінен фотосинтез нәтижесінде түзіледі, ол жапырақтарда және теңіз балдырларында жүретін үдеріс.
6СO 2 + 6Н 2 O → С 6 Н 12 O 6 + 6O 2 ↑
Осы оттегімен адамдар мен жануарлар тыныс алады, одан басқа жер қыртысындағы минералдар түзіледі. Табиғатта оттегінің қатысуымен тоттану, шіру, aшy сияқты бүліну үдерістері де жүріп жатады. Оттегінін, атмосферадағы қоры 1, 5•10
15
т, оның 1•10
10
тоннасы жану үшін жұмсалады. Тыныс алу жеке ағзаның өмірі үшін, ал шіру - эволюция (даму) үшін маңызды үдерістер.
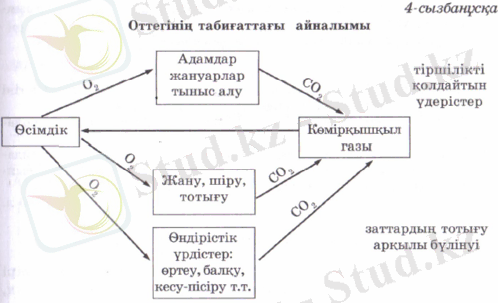
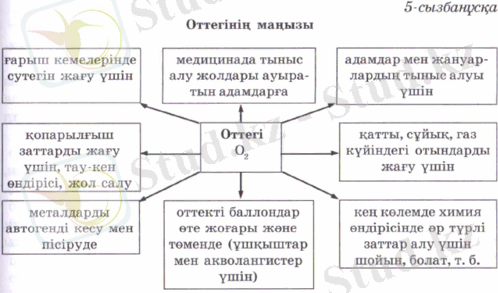
Оттегінің қолданылуы оның қасиеттеріне негізделген, ол мына 4, 5-сызбанұсқаларда көрсетілген.
Оттегі табиғатта екі түрлі жай зат күйінде кездеседі, оның бірі O 2 , екіншісі O 3 , ол озон деп аталады. Енді озонмен жете таныссақ, озон найзағай ойнағанда ауада пайда болады. Сонда электр заря- дының әсерінен мына реакция жүреді:
3O 2 → 2O 3
Бір элементтің бірнеше жай зат күйінде болу құбылысы аллотропия деп аталады.
Озонның формуласы О 3 , салыстырмалы молекулалық массасы 48, оттегінен 1, 5 есе ауыр (48 : 32 = 1, 5), суда аз еритін, -112°С-да қайнайтын, -193°С-да балқитын газ күйінде қою-көк түсті, ал қатты күйінде көктен қара-күлгін түске дейін боялады.
Озонның химиялық қасиеттеріОзон оттегіне қарағанда химиялық белсенді зат. Ол тіпті алтын, күміс, платина сияқты асыл металдарды да тотықтыра алады (7-кесте) .
6Ag + O 3 = 3Ag 2 O
Нөсер жаңбырдан кейін орманға барсақ, онда ауа тазарып дем алу жеңілдейді, себебі ауада пайда болған озон айырылып, ауаны тазартады. Озонның атмосферадағы мөлшері өте аз - 0, 004%.
О 3 → O 2 + "О"
Озоннан молекулалық және атом күйіндегі оттек бөлінеді, соңғысы күштірек тотықтырғыш, ауадағы бактерияларды жояды. Озон осы қасиетіне қарай ауыз суды, құдыктарды, өндірістік сарқын суларды тазарту үшін (залалсыздандыру) және ағартқыш зат ретінде қолданылады. Атмосфераның жоғары қабатында, жерден 25 км биіктікте (стратосферада) күн сәулесінің әсерінен жерді қорғап тұратын өте жұқа озон қабаты әр түрлі кері әсерлердің салдарынан «тесіліп», сол жерлерден күннің ультракүлгін сәулелері жер бетіне жетіп, ондағы әр түрлі табиғи апаттарға әкеліп соғады. Олар: жер бетінің температурасының біртіндеп артуы, мәңгілік мұздақтар мен мұхиттардағы мұзтауларының еруі, терінің қауіпті ісігі көбейеді. Озонды зертханада озонатор деп аталатын құралда алуға болады.
Фотосинтез процесі
Фотосинтезді зерттеу барысындағы ең басты мәселелердің бірі - осы процестің өсімдіктердің жасыл жапырақтарында жүзеге асуы құбылысын ашу. Бұл сұраққа нақты жауап берген неміс ғалымы Т. В. Энгельман болды. Ол фотосинтез процесінің хлоропластарда жүретінін дәлелдеу үшін жасушаның әр түрлі бөліктерін кішкене сәуле шоқтарымен жарықтандыруға болатын микроскоп құрастырды. Жасушаның жеке бөліктерін жарықтандыра отырып, оның қай бөлігінің фотосинтезге кабілетті екенін зерттеді. Сөйтіп, ол жасушаның қай бөлігі фотосинтез процесі үшін жарық қабылдағышы бола алатынын дәлелдеді. Фотосинтездік белсенділікке талдау жасау үшін ол тек анаэробты жағдайды ғана талдап алды. Ол үшін қозғала алатын және оттектің концентрациясы жоғары болатын аймақ бағытына қарай жылжитын бактерияларды қолданды. Сонда Т. В. Энгельман бактериялардың жасушаның жарық түскен хлоропластарына жылжитынын басқа жарық түскен органоидтеріне жылжымайтынын байқаған. Бұдан Энгельман: «Хлоропластар жасушалары оттек орталығы болып табылады және фотосинтез процесі нәтижесінде оттек бөлінеді» деген тұжырым жасаған. Сонымен фотосинтез процесі кезіндегі жарықтың сіңірілуі мен оттектің бөлінуі тек хлоропластарда жүретіні анықталды.
Фотосинтез процесі екі сатыға бөлінеді. Жарық және қараңғы фазалары. Жарық фазасының реакциялары хлоропластың бетіндегімембраналық түзілім - ламеллада жүрсе, караңғы фазасының реакциялары хлоропласт денесінде немесе стромасында өтеді. Фотосинтездің жарық фазасы реакцияларының әлементарлық өлшем бірлігі - квантосомалар болып табылады. Оның құрамынахлорофилдің 230 молекуласы және электрон тізбегін тасымалдауға қатысатын нәруыздар - цитохром b, с және ферредоксин кіреді.
Жарық фазасы
Энергетикалық процестер тікелей жарық фазасында жүреді. Жарық кванты хлоропласта орналасқан хлорофилл пигменті арқылы қабылданады. Жарық кванты мен хлорофилдер әрекеттескенде, электрондар пайда болады. Олардың ежелгі және қазіргі өсімдік организміндегі жүру жолдары бірдей емес. Ежелгі фотосинтездеуші бактериялар мен төменгі сатылы.
Балдырларда электрондар электронды тасымалдаушы тізбек арқылы тасымалданғанда, бейорганикалық фосфат пен аденозиндифосфаттан (АДФ) аденозинтрифосфат (АТФ) түзіледі. Бұл процесте электрондар хлорофилге қайтып оралатындықтан, циклдік фотофосфорлану деп аталады. Хлоропласт ламелласының квантосомаларында орналасқан циклді фотофосфорлану тек кана фотосинтездеуші микроорганизмдер мен төменгі сатыдағы балдырларда ғана емес, жасыл өсімдіктерде де жүреді. Жасыл өсімдіктердің фотосинтезін зерттеуде Р. Хилл 1937 жылы үлкен үлес қосты. Ол алғаш рет судың фотолизі кезіндегі молекулалық оттектің бөлінуі фотосинтездің жарық фазасында жүретін реакция екендігін аныңтаған. Бұл реакция жүзеге асу үшін міндетті түрде электрондар акцепторы қатысуы қажет, мысалы, феррицианид немесе энергия жұмсау арқылы жинайды. Осы циклдік емес фотофосфорланудың пайда болуы нәтижесінде жоғары сатыдағы (жасыл) балдырлар мен жасыл өсімдіктер атмосфераға оттек бөле бастады. Ал олардың пайда болуына дейін атмосферада оттек болмаған. Жасыл өсімдіктердің арқасында аэробты тіршілік және аэробты организмдер эволюциясы пайда болды.
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz