Petrosimonia sibirica өсімдігінің жер үсті бөлігінің фитохимиялық құрамы және биологиялық белсенді заттарды бөліп алу


РЕФЕРАТ
Бітіру жұмысы: 53 беттен, 8 суреттен, 9 кестеден, 4 диаграммадан, 2 сызба-нұсқадан, 30 әдебиет көзінен тұрады.
Кілтті сөздер:
Petrosimonia sibirica, экстракция, биологиялық белсенді заттар, сапониндер, флавоноидтың гликозидтері, кумариндер, хроматография, амин қышқылдары, жоғары май қышқылдары, минералды заттар.
Жұмыстың мақсаты:
Petrosimonia sibirica өсімдігінің жер үсті бөлігінің фитохимиялық құрамын зерттеу, биологиялық белсенді кешен алу.
Зерттеу нысаны:
Атырау обылысында 2011жылы тамыз айында жиналған Petrosimonia sibirica өсімдігінің жер үсті бөлігі.
Зерттеу әдістері:
Қағазды, жұқа қабатты және колонкалы хроматографиялар; экстракция жүргізу; титрлеу; фотокалориметр; газды хроматография, атомды адсорбциялау.
Жұмыстың міндеттері:
- Алғаш ретPetrosimonia sibiricaөсімдігі жер үсті бөлігіне фитохимиялық зерттеулер жүргізу; шикізаттың сапалылығы және негізгі биологиялық белсенді заттардың кластарына сандық және сапалық сараптама жасау;
- Petrosimonia sibiricaөсімдік күлінің құрамындағы минералды заттар анықтау;
- Petrosimonia sibiricaөсімдігінен биологиялық белсенді заттарды бөлудің сызба-нұсқасы жасау;
- Этилацетат экстратысынан флавоноидтың моногликозиді бөлу.
Басылымдар:
Берілген жұмыс бойынша « Petrosimonia Sibirica өсімдігін фитохимиялық зерттеу» тақырыбында 1 тезис жарияланды.
РЕФЕРАТ
Выпускная работа изложена на 53 страницах, 8 содержит рисунка,
4 диаграммы, 2 блок-схемы, 30 литературных источников.
Ключевые слова:
Petrosimonia sibirica, экстракция, биологически активные вещества, сапонины, флавоноидные гликозиды, жирные кислоты, аминокислоты, хроматография, кумарины, минеральные вещества
Целью настоящей работы:
Фитохимическое изучение и выделение биологически активного комплекса из надземной части растений Petrosimonia sibiriса.
Объекты исследования
Надземная часть растений Petrosimonia sibiriса собранное в фазу цветения в Атырауской области 2011 году.
Методы иследования:
Бумажная, тонкослойная и колоночная хроматография, экстракция, титрование, фотоколориметрия, высокоэффективная жидкостная хроматография (ВЭЖХ) .
Задачи работы:
Работа посвящена фитохимическому исследованию растений рода Petrosimonia sibiriса, впервые определяется количественное содержание биологически активных веществ. Определить минеральный состав золы растений Petrosimonia sibiriса .
Публикаций:
По дипломной работе опубликован 1 тезис на тему « Petrosimonia sibirica өсімдігін фитохимиялық зерттеу».
Мазмұны
Кіріспе
Қазақстан флорасы пайдалы өсімдіктерге, соның ішінде ерекше маңызды болып саналатын дәрілік өсімдіктерге бай. Көптеген өсімдіктердің құрамын толықтай зерттелмеген, оларда дәрілік препараттардың негізін құрайтын заттар, әр түрлі мөлшерде биологиялық белсенді заттар көп.
Қазіргі кезде әртүрлі ауруларды алдын алу үшін дәрілік өсімдіктерге, медицинаға саласына ерекше көңіл бөліне бастады. Біздің медицина фитопрепараттар шығаруға мүдделі. Фармацевтикалық өндірісін дамыту үшін дәрілік өсімдіктердің табиғи папуляцияларын қорғап және пайдаланудың ерекшеліктерін сақтай отырып тиімді пайдалану керек. Өсімдік нысандарын зерттеу, жаңа, экологиялық таза, улылығы төмен және жоғары эффективті отандық фитопрепараттарды өндіру маңызды мәселе болып табылады
Дәрілік өсімдіктердің фармакологиялық әсері оның құрамындағы биологиялық белсенді заттардың болуына байланысты анықталады . Соңғы жылдары озық технологияның дамуына байланысты жаңа технологиялармен дәрілік өсімдіктер құрамындағы жаңа заттар анықталынып, олардың белсенділіктері де анықталынып жатыр. Өкінішке орай елімізде жаңа озық қондырғылар жоқтың қасы.
Зерттеу жұмысының мақсаты мен міндеттері.
Petrosimonia sibirica өсімдігінің жер үсті бөлігінің фитохимиялық құрамын зерттеу, биологиялық белсенді кешен алу.
Жұмыстың мақсатына жету үшін алға қойған міндеттер:
- Зерттеуге алынған өсімдіктің құрамына сандық және сапалық сараптама жасау;
- Зерттеуге алынған өсімдіктің сараптама нәтижесіне сүйене отырып, биологиялық белсенді заттарды алу технологиясын жасау;
- Жасалған хроматографиялық әдістерді қолдана отырып, оларды бөліп алу.
Зерттеу нысаны:
Атырау өңірінен 2011 жылы тамыз айында, гүлденген кезінде жиналған Petrosimonia sibirica өсімдігінің жер үсті бөлігі.
1 Әдеби шолу
1. 1 Petrosimonia sibirica туралы қысқаша түсінік
Морфологиялық сипаттамасы. Марева тұқымдасының құрамында туыста 11 түр бар, ал Қазақстанның шөл және шөлейт аймақтарында 10 түрі өседі . Өсімдіктің тамыры жуан, ағашты, жерге өте мықты болып келеді. Жапырақтары шоғыр кезектесіп немесе қарама-қарсы тығыз болып орналасқан, жеміс беретін бұтақтарының биіктігі 10-50 см, бұтақтары майысқан немесе тік келеді, жапырақтары 3-6 мм болатын қыл немесе кірпікті түкті; гүлшелері-күрделі масақты, жоғары бөлігінде тығыз орналасқан, гүл жапырақшаларының ұзындығы 2-2, 5мм, сыртынан қарағанда жұмыртқа тәрізді дөңгелек, майысқан, өте көп қылтанақты, күлте жапырақшаларының тісшелері түтікшелерден шамамен 2 есе қысқа, тіке, дәндері дөңгеленген, 1мм, қара қоңыр түсті .
Гүлдеу уақыты: Маусым - қыркүйек айының аралығында өседі . Тамыз айларында гүлдейтіін біржылдық өсімдік.
Климаттық орта жағдайы. Бұл өсімдік жарық сүйгіш, суыққа да төзімді, жас өскіндері жазғы ыстыққа шыдамды оңай төтеп береді.
Жалпы таралуы. Төменде аталған аймақтарда көп кездеседі: Сібірде, Батыс Сібірде, Орталық Азияда, Орталық және Шығыс Европада, Кавказ жерлерінде кездеседі.
Таралуы: Petrosimonia sibirica өсімдігі сортаң топырақта, тақыр жерлерде жақсы өседі. Қазақстанда 10 түрі бар. Олар: Арал теңізі, Каспий теңізі маңында, Сырдария, Амудария, Қызыл-Құмда, Мойын- құмда, Ақтөбе, Қызылорда, Балқаш-Алакөл, жерлерінде кездеседі. Барлық түрлері төменде келтірілген:
- Petrosimonia brachiata
- Petrosimonia glauca
- Petrosimonia triandra(қаңбақ сораң)
- Petrosimonia litwinowi(қызыл тұз шөп)
- Petrosimonia squarrosa
- Petrosimonia monandra(тұз дубрча)
- Petrosimonia crassifolia
- Petrosimonia hirsutissima
- Petrosimonia glaucescens
- Petrosimonia brachyphylla
- Petrosimonia sibirica
Ботаникалық сипаттамасы. Өсімдіктін биіктігі 10-15 см, диаметрі 10-12 см болатын, ұзын, тісшелі, түкшелері немесе қылтанақтары бар, барлық бұтақшаларымен бірге жалаңаш болады; гүл жапырықшалары сыртқа қарай қайырылған қайық тәрізді және ылғал көп болған жағдайда бұтақ тектес болып келеді. Соңғылары 5 ұзыншалы және ланцетті, үстінен кірпікшелі - түкті жапырақшалары бар; аталығы 5 бос тозаңнан тұрады, аналығы VI-VII бағанаға жақын орналасқан [6] .

1 - сурет . Petrosimonia sibirica өсімдігі
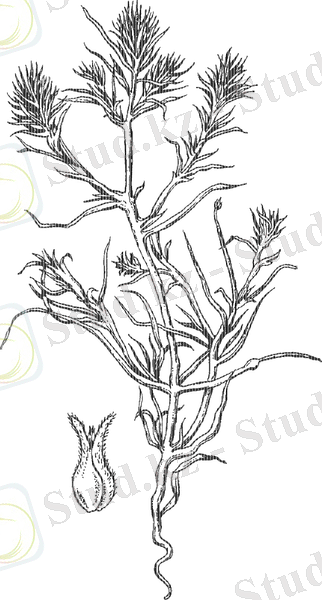
2 - сурет . Petrosimonia sibirica өсімдігі
1. 2 Флавоноиодтар туралы түсінік
Флавоноиодтар табиғатта өте жиі кездеседі. Оның құрамында көптеген әртүрлі бояушы пигменттерге бай, бұл пигменттер өсімдікте өте көп мөлшерде кездесіп отырады. Олар өздерінің атауын « flayus » латын сөзінен алған, сары деген мағынаны білдіреді, себбебі өсімдіктен бөлінген бірінші флавоноиод сары түсті болған. Табиғи флавоноидтардың 7500 құрылысы толығымен зерттелген. Олардың ерекшелігі өсімдікті жағымсыз факторлардан қорғайды.
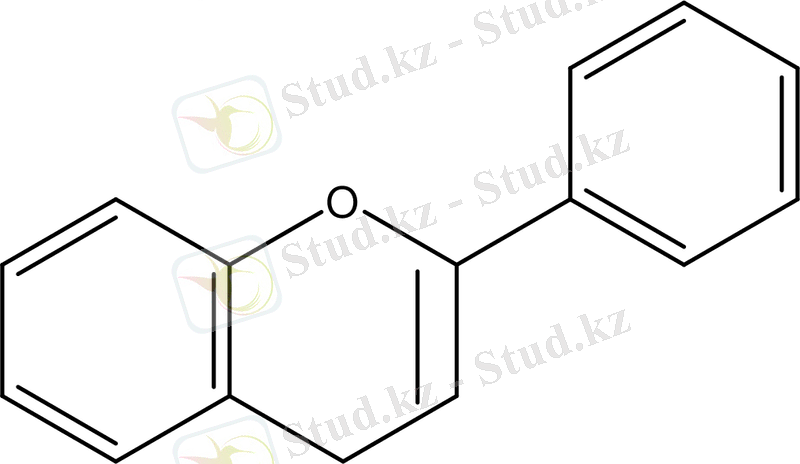
Флавоноидтарды құрамында екі фенилдік қалдықтардан тұрады. Олар ішкі көміртегі атомдарына тізбектеліп жалғанған. Бес немесе алты мүшелі оттек түзуші гетероцикл түзіліп және көптеген флавоноидтарға тұйықталып тізбектелген, бұлар бензол ядросымен жалғанған. Флаваноидтар- пиронның туындылары, 15 көміртегі атомынан тұрады. Құрылысы 2 ароматикалық А және В сақинадан тұрады, әртүрлі гидроксил немесе басқа орынбасарлардан; 2 сақинаның арасы өзара пропанды көпіршемен байланысқан болады. оларға реакция жүргізу үшін пропан сақинасы С қажет.
Флавоноидтарды нөмірлеу молекуладағы гетероатомнан (оттегі) басталады, одан кейін А сақинасына жалғасады. В сақинасын бөлек нөмірлейді, нөмірлеу негізгі молекуламен байланысқан көміртегі атомынан басталады.
Флавоноидтардың ішінен табиғатта эуфлавоноидтар кеңінен таралған. Эуфлавоноидтағы гетероциклды С сақинаның тотығу дәрежесіне байланысты оларды былай ажыратады: Флавондар, флавонолдар, флаванондар, флаванонолдар, антоцианидиндер, халкондар, аурондар .
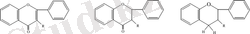
R= H флавон R= H флаванон R= H флаван
R=OH флавонол R=OH флаванонол R=OH флаванол
Флавоноидтарды кластарға бөлу мынадай топ бойынша жүргізіледі: пропан бөлігін тотығу дәрежесі бойынша, гетероциклдік шамасы бойынша, фенильдік орынбасарды жағдайы бойынша және т. б. қазіргі кезде флавондар мен флавонолдарды көп зерттелген.
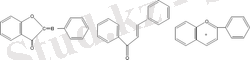
Аурон Халкон Антоцианидин
Флавоноидтар түссіз және сары кристалды заттар, суда және органикалық еріткіштерде еруі, орынбасушы радикалдарды орналасуына және санына байланысты болып келеді.
Флавондар - сары түсті бояғыш зат- ол гликозид түрінде кездеседі. Көп таралған агликондар - апигенин ( R = R 1 = H), лютеолин (R = ОH ; R 1 = Н) және трицин (R = R 1 = ОСH 3 ) . Түссіз флавондар мен флавондар ақ, кремді және пілдің сүйектеріндей түстерді қамтамасыз етеді[2] .
Флавонолдар - сары түсті бояғыш зат, қауіпті өсімдікте кеңінен таралған. Көп мөлшерде әр түрлі гликозидтерді құрайды, көбіне келесі силикондардың туындылары: Кемпферол (R = R 1 = H) ; кверцетин (R=ОН 1 ; R 1 =Н) және мирицитин (R = R 1 = ОH) . Сары түсті флавонолдар түсті қарқындатуға үлес қосады. Флавонолдар түс беруге үлесін қосады бір ғана жағдайда, олар металденген немесе гликозидтер түрінде болуы тиіс.
Көбінесе флавоноидты қосылыстар әр түрлі гликозидтер түрінде кездеседі. Қазіргі кезде белгілі флавоноидты гликозидтер түріндегілері мынандай үш топқа бөлінеді. О- гликозидтер, С- гликозидтер және ацилдеуші О- гликозидтер.
О- гликозидтердің қанттары жартылай гидроксил агликондары оттегі атомы арқылы байланысқан. О- гликозидінің қантының шамасына және орналасу орнына байланысты моногликозидтерге, биозидтерге, дигликозид-терге және аралас гликозидтерге бөлінеді. Олардың ішінде моногликозидтер жай байланыстарға жатады, боизидтер, бірдей қанттармен байланысады, қанттар байланыстың тізбегімен және ретімен, тотыққан сақина шамасымен және гликозидтің байланыстар конфигурациясымен бөлінуі мүмкін.
Гликозидтерге қанттар әр түрлі жағдайларда орналасқан біріншісінде бір қантпен, ал екіншісінде екі қантпен. Барлық О- гликозидтер қышқылдың және ферменттік гидролизге тез ұшырайды.
Херхаммер мен Вагнер қатаң өңдеудің өзінде С - гликозидтер гидролизденбейді, мұндай заттарды С-гликозидтер деп атады, өйткені мұндай заттарда қант флавон сақинасымен тікелей байланысқан. Мұнымен қоса С - гликозидтік байланыстар фенолды гидроксилді топтың молекуласында көршілес болады. Биосинтез О - гликозид сатысы арқылы өту мүмкіндігі туралы жорамал айтылған. С - гликозидтер және гликофлавоноидтарды С - моногликозидтерге, С-гликозидтерге бөлуге болады. Биосинтез О-гликозид сатысы арқылы өту мүмкіндігі туралы жорамалдар бар. С-гликозидтер және гликофлавоноидтарды С-моногликозидтерге, С-гликозидтерге бөлуге болады.
С - гликозидтер О - гликозидтермен бірге кездеседі және олардың бірнеше белгілері арқылы бөлінеді:
1) Сілтілік гидролиздің тұрақтылығы;
2) Қышқылдық гидролизге кәдімгі жағдайда орнықтылығы;
3) Ферменттік гидролизге тұрақтылығы;
4) С-гликозидтердің бөлшектенуден кейінгі және бөлшектенуге дейінгі бос фенолдық окси топтар сандарының тұрақтылығы;
5) Изомерлердің өзара бір-біріне ауысуының қышқылдық гидролиздегі өнімнің пайда болуы.
Егер флавоноидты гликозидтер салыстырмалы аз болатын болса онда екінші топ антоциандарда көптеп кездеседі. Комплексті гликозидтерден бөлінген қышқылдар: бензой қышқылы, п-оксибензой қышқылы, протокатех қышқылы, кофейн қышқылы, ферулл қышқылы, сірке қышқылы, пропион қышқылы және басқа қышқылдарға этерификацияланған.
1. 2. 1 Флавоноидты қосылыстарды сараптау әдістері
Флавонотдтар өсімдіктердің барлық бөліктерінде кездеседі, оларды бөлу тәсілі өсімдіктің мөлшеріне және флавоноидтың түріне байланысты. Егер жаңа терілген шөп өңделетін болса, онда гидролиз тудыратын фермент әсерін тоқтату үшін, экстрауция әдісін өзгертеді. Құрғақ шөп экстрауцияға ұшырайды. Экстракциялау шін еріткішті таңдап алу, флавоноидтардың полярлығына тәуелді болады. Полярлығы көп еріткіштер гликозидтерді және антроциандарды экстрауциялау үшін қолданылады.
Көп жағдайларда тізбектеп экстракциялау үш-төрт еріткіштердің полярлығын пайдаланады. Флавоноидтарды басқалардан бөлу үшін стандартты әдіс жоқ, әрбір нақты жағдайларды таңдап алу бірнеше факторға байланысты: қосылыстардың қасиеттеріне, қоспаның күрделілігіне, компоненттік ара қатынастардың санына, бірге кездесетін заттардың санына байланысты болады. Кейінгі жылдары адсорбциялау (колонкалы жұқа қабат) әдісі және хроматографиялы бөлу әдістері флавоноидтарда бөлу мақсаты үшін кеңінен қолданылады. Бұл тәсілдер тазалығы жоғары дәрежелі заттар алуға мүмкіндік береді. Бұл әдіс өзінің қарапайымдылығымен және ұтымдылығымен ерекшеленеді[27] .
Адсорбенттер үшін мынадай заттар пайдаланылады: полиамид, силикагель, магнезол, целлюлоза, сефадекс, ион алмасу смолалары. Олардың арасынан флавоноидтарды өзара бөлу үшін жоғарыда көрсетілген адсорбенттер ішінен ең тиімді бөлу қабілеті жоғары полиамид. Фенол гидроксилмен және амин тобының поликапролактам арасында қайтымды сутектік байланыстар құрылу нәтижесінде флавоноидтар полиамидке адсорбцияланады да, эдюенттердің көмегімен флавоноидтар колонкадан жуылады. Полиамидті адсорбенттер жеке талғамды тазалау және флавоноидты қосылыстарды бөлінуімен қатар бұлардың құрылысына хромотографиялық бөлінуде ешбір әсер етпейді.
1. 2. 2 Сапалық сараптау
Флавондарды, флавонолдарды және т. б заттарды сапалық реакциялар арқылы бір-бірінен айыруға болады.
Диазоттау реакциясы. Бұл реакция арқылы гидроксил тобын 7-орында байқауға болады. Гидроксил тобы электрондар сияқты азобірігуді 6-ші 8-ші орындарға бағыттайды:
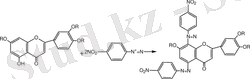
Мысалы, бұл комплекстерді алюминий хлоридімен көрсетуге болдаы.
Флавоноидтардың аммиак және алюминий хлоридімен комплекс түзу реакциясы
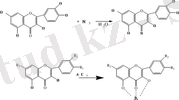
Металл ионымен флавоноидтар А және Б комплексті қосылыстар түзеді. А сақинасындағы комплекс С 5 -ОН, С-сақинасындағы С=0 топ және С 3 -ОН топтар арасында түзеді.
Тұз қышқылын қосқанда А комплексті жойылады да, С-сақинасындағы комплекс сақталады.
Үшхлорлы сүрме реакциясы. 5-оксифлавон және 5-оксифлавонол үшхлорлы сүрмемен әрекеттесіп, комплексті қосылыс түзеді, нәтижесінде сары және қою сары түске флавондар боялады, ал қызыл немесе күлгін қызылға халкондар береді.
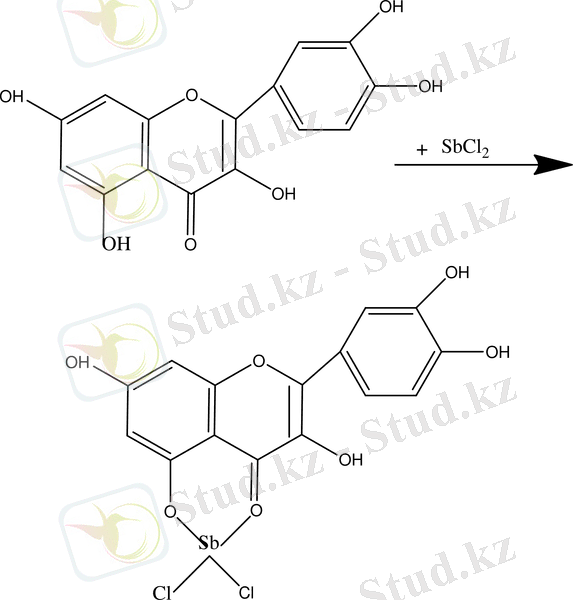
Бор-лимонды реакция (Вильсон- Таубек реакциясы ) .
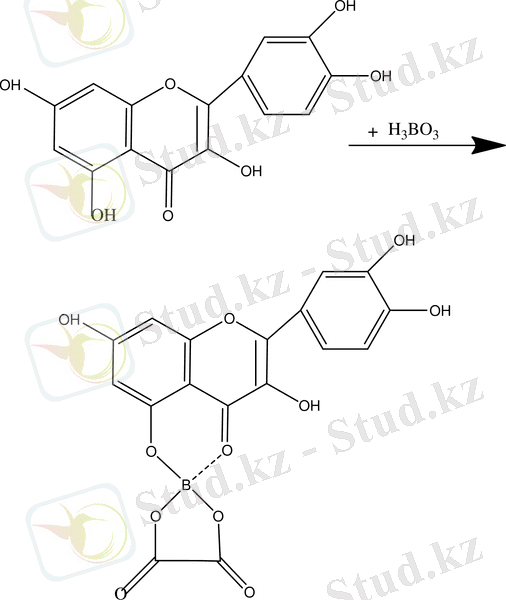
Цианид реакциясы. Магний көмегімен және тұз қышқылының спирттік ортада жүреді, боялған өнімнің түзілуіне байланысты зерттелетін заттың тотықсыздануына негізделген:
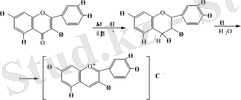
Цианидин хлориді
Магнийді мырышпен алмастырғанда бояуды тек гликозидтер береді.
1. 2. 3 Сілтілік ыдырату
Агликонның құрылысын анықтау үшін сілтілік ыдыратуды жүргізеді. Инертті газ орталығында 170 0 -С-та қыздырғанда агликон 50%-тік сілті ерітіндісімен фенол және фенол қышқылдарына ыдырайды. Этилацетатпен экстракциялап қағазды хроматографияның көмегімен құрылысын белгілі фенол және фенол қышқылдармен салыстырады. Фенолды анықтау шін пайдаланылатын айқындағыштар: 1%-ті ванилин, күміс нитраты; ал фенол қышқылдарды анықтау үшін пайдаланатын айқындағыштар ЖАК, диазотталған п-нитроанилин. Сонымен, анықталған фенол және фенол қышқылы бойынша агликоннның құрылысын шығаруға болады[1] .
Жұмсақ жағдайда ацетофенон және фенол қышқылына ыдырайды.
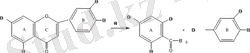
Қатаң жағдайда фенолға және фенол қышқылына ыдырайды.
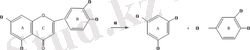
1. 2. 4 Қышқылдық гидролиз
Қышқылдық гидролизге сүйене отырып заттардың қантты бөлігін дәлелдеуге болады. Идентификацияға алынған молекуланың біршама үлкен бөліктері тез ұшырайды және молекулалардың жеке құрамдас бөліктерін талқылауға мүмкіндік береді.
а) Қышқылдық гидролизбен биозид болған кезде қанттардың байланысу жағдайы 0, 1%-ті НСІ -мен сатылай жүретіні түсіндіріледі. Бастапқыдан аралық өнім монозоид, биоза және агликонға дейін толық ыдырауы жүреді. Қышқылдық гидролиз (10мг затты 5мл 2% НСІ сулы немесе спирттегі ерітіндісінде ерітіп, колбаны кері тоңазытқышқа жалғап, 2 сағат бойы сулы моншада қыздырады. Одан кейін ерітіндіні суытып, реакциялық қоспаны нейтралды ортаға дейін келтіреміз. Агликонды этилацетатпен экстракциялап бөліп алады, ал сулы бөлікте қанттар қалады. Қандай қанттардың бар екенін анықтау үшін сулы бөлікті бір жүйелі қағазды хроматографияға «БСС жүйесіне» қойып, одан кейін хроматограмманы о-толуидин және мочевина айқындағыштарымен өңдейді) .
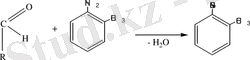
О-тлулдин
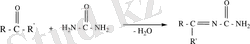
мочевина
ә) Сатылы қышқылдық гидролиз.
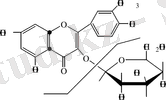
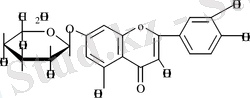
3-О-гликозид 7- О -гликозид
10 мг затты 5 мл 0, 1% НСІ сулы немесе спиртті ерітіндісінде ерітіп, колбаны кері тоңазытқышқа жалғап, сулы моншада 3-4 сағат қыздырады. Әрбір 5 минут сайын проба алып, бір жүйелі ҚХ-ға тамызады. Белгілі уақыт өтіп және реакция аяқталғаннан кейін ҚХ-ны белгілі ерітінділер жүйесіне қойып, о-толуидинмен өңдейді. Бұл кезде рамнозидтер мен арабинозидтер тез гидролизге ұшырайды. Нәтижесінде қанттың яғни көмірсудың агликонға қай гидроксил тобына жалғанғанын тез гидролизденеді. Флавоноидтардың С-гликозидтері үшін Килиан гидролизі қолданылады, ең басты айырмашылығы затқа концетрлі тұз қышқылы мен сірке қышқылының қоспасын пайдаланады.
б) Ферментативті гидролиз. Арнайы спецификалық ферменттерді қолдану арқылы мысалы: β - эмульсин, α-амилаза, рамнодиастазамен жүргізіледі. Нәтижесінде қанттардың конфигурациясын және гликозидтің құрамында бірнеше қант болса сол қанттардың арасындағы байлансыты береді.
1. 3 Флавоноид құрлысын дәлелдеудегі физико- химилық әдістері
1. 3. 1 УК - спектроскопия
УК - спектрі ұзын және қысқа толқынды аймақта екі максимум жұтылу сызығымен сипатталады. Олардың интенсивтілігі және жағдайы орынбасарлардың табиғатына және орналасу реттілігіне байланысты болдаы. Флавониодтардың ұзын толқынды спектр сызығы 340-385 нм, ал қысқа толқынды сызығы 240-270 нм аралығында жатады. УК - спектрлерді көп жағдайда абсолютті метил спиртінде түсіреді. Арнайы спецификалық қоспаларды қосу арқылы функционалды топтардың орналасу орнын анықтауға болады. Флавоноид молекуласындағы оңай иондалып комплекс түзетін топтарды әр функционалдық топқа сәйкес минималды ығысу сызығын тудыратын натрий ацетатының қоспасы және хлорлы алюминий арқылы анықтауға болады. Натрий ацетаты 7- орындағы ОН тобына сапалы реактив болып табылады. Натрий ацетатын қосқанда қысқа толқынды сызықты батохромды ығысуы болады. (8-20 нм) . Натрий этилаты С 7 - орындағы ОН тобына жақсы реактив. Бор қышқылы мен натрий ацетаты қоспасын қосқанда о- дигидроксил тобы бар флавонолдардың ұзын толқынды сызығының батохромды ығысуы болады. Бос ОН тобы бар С 3 және С 5 - атомдары алюмини хлоридімен комплекс түзіп бірінші сызықтың 50-60 нм- ге батохромды ығысумен анықталады немесе цирконий түзумен анықтауға болады. Лимон қышқылын қосқан кезде 5-ОН және карбонил топтары бойынша түзілген 6-мүшелі комплекс әсерінен бұзылып, батохромды ығысу 10-20нм- ге дейін азаяды. Сонымен, УК - спектрі көмегімен флавоноид түрін көміртекті орынбасушылар санын, қант компонентінің орнын анықтауға болады [13] .
1. 3. 2 ИҚ-спектроскопия
ИҚ-спекторскопия көмегімен флавоноидтарды идентификациялау кезінде барлық функционалдық топтарын және С сақинасының орынбасу дәрежесі, көміртек орынбасуларды, агликонмен байланыс типтерін, циклдің тотыққан өлшемдерін, ароматты сақина (А және В сақинаасы) және С-О-С көпірі жұтылу аймағында ауытқусыз байқалады. Орынбасарлардың бар жоқтығы және орналасуы сиректеу алмастырылмаған флавондардың өзіне тән қасиеті бойынша анықталады. Мысалы, алмастырылмаған флавондардың С=О тобы 1650 см -1 аймағында байқалады, 3 жағдайға ОН -тобының кiрiспесi С=О жолақтың екiге бөлiнуiне алып келедi, бұл С сақинасының ароматтылығының өсуіне байланысты. 5-ОН-тобы С=О тобымен ішкімолекулярлық сутектік байланыс түзеді, сондықтан флавондар үшін 1645см -1 және флавонондар үшін 1648см -1 . Ал мастырылмаған флавоноидтар үшін В сақинасындағы С-Н байланысы 730-745 және 684-702 см -1 деформациялық тербелістер көрсетеді. Мысалы басқа топтардың жұтылу аймақтары: 3-ОН тобы 3350-3250 см -1 , 5-ОН тобы 2500-3000см -1 , 7-ОН тобы 3100-3200 см -1 , ал 4 1 -ОН тобы 3450-3350 см -1 байқалады. С-О-С 1000-1100 см -1 , С-Н тобы 2999-2970 см -1 және 1375 см -1 деформациялық тербелісі тән.
1. 4 Флавоноидтарды идентификациялау
1. 4. 1 Қағазды хроматография
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz