Aspergillus туысының эндоглюканаза гендерін прокариоттық жүйеде клондау және экспрессиялау


Жұмыс түрі: Дипломдық жұмыс
Тегін: Антиплагиат
Көлемі: 41 бет
Таңдаулыға:
Қазақстан Республикасының Білім және ғылым министрлігі
Әл-Фараби атындағы Қазақ Ұлттық Университеті
«Қорғауға жіберілді»
Кафедра меңгерушісі, б. ғ. д.,
профессор Айташева З. Г
ДИПЛОМ ЖҰМЫСЫ
Тақырыбы: Aspergillus туысына жататын саңырауқұлақтардың эндоглюконаза гендерін прокариот жүйесінде экспрессиялау және клондау
«Биотехнология» 050701 мамандығы бойынша
4 курс студенті Жанаева А. Б.
(күні, қолы)
Ғылыми жетекшісі:
б. ғ. д. Бисенбаев А. Қ.
(күні, қолы)
Норма бақылаушы: Біләлова Г. Ж. Т (күні, қолы)
Алматы, 2012
РЕФЕРАТ
Дипломдық жұмыс 42 беттен тұратын компьютерлік тексттен тұрады. 16 сурет, 4 кесте келтірілген, 28 әдебиет тізімі қолданылған, оның 11 шетел әдебиет көзі.
Жұмысты жасау үшiн объект ретiнде Aspergillus niger саңырауқұлағынан бөлініп алынған нуклеин қышқылдарының препараттары қолданылады.
Өзектілігі: Мұнай құнының күрт шарықтауы, әлемдік мұнай мен газ қорларының азаюы энергияның альтернативтік көздерін іздестіру жұмыстарына қызығушылықты арттыра түсірді. Соған байланысты көптеген зерттеу жұмыстарының алдына қойған мақсаты қайта қалпына келетін органикалық шикізаттан биотехнологиялық процестер негізінде экономика тұрғысынан арзан биоэтанол алу болды. Этанол бензинге қарағанда жоғары октандық санға ие, адам үшін токсикалық әсері төмен. Осыған орай целлюлозадан алынатын этанолдың бензинге бәсекеге қабілетті альтернатива бола алатындығы және олардың автомобильді транспорттың қажеттілігіне қолданылуы болжалданады.
Жұмыстың мақсаты:
Aspergillus туысы саңырауқұлақтарының эндоглюканаза ферментін сипаттау және оны прокариот жүйесінде клондау.
Жұмыстың міндеттері:
- Aspergillusтуысы саңырауқұлақтарының мицелийінен нуклеин қышқылдарын бөліп алу.
- эндоглюканаза гендерін амплификациялау үшін праймерлерін есептеу және компьютерлік талдау жасау
- Бөлініп алынған нуклеин қышқылдары препараттарын талдау және целлюлаза гендерін PCR көмегімен амплификациялау.
- Генді векторға енгізіп, бактериялық клеткаларды трансформациялау.
- Клондалған гендердің экспрессиясын анықтау.
Жұмыс барысында қолданылған әдістемелер: Aspergillus niger саңырау-құлағынан тотальдік нуклеин қышқылдарының препараттарын бөліп алу, тотальдік нуклеин қышқылдарын poly-A байыту, кері транскрипция әдісімен кДНҚ алу, PCR әдісі арқылы амплификациялау, рекомбинантты ДНҚ молекуласын құрастыру және оны E. сoli клеткаларына трансформациялау, геннің E. сoli клеткасында экспрессиялануын белок препаратын ДСН-ПААГ электрофорезі арқылы анықтау.
Кілтті сөздер: эндоглюканаза, целлюлоза, целлюлазалық комплекс, Aspergillus туысы, биоэтанол, биодеструкция.
МАЗМҰНЫ
КIРIСПЕ
Соңғы жылдары дүние жүзінде этил спирті өндірісінің қарқынды дамуы байқалынды. Бұл этил спиртінің биожанармай ретінде қолданылуына байланысты болып келеді. Бензин-этанол қоспасын жанармай ретінде қолдану бұрыннан белгілі болып келген. Қазіргі кезде де АҚШ пен Еуропа елдерінде 10 % және 20 % этанол бар бензин қоспасын жанармай ретінде кең қолданады. Отынның бұл түрі ішкі жану қозғалтқыштарының құрылымдарын өзгертпей, оларды сол күйінде қолдана беруге мүмкіндік береді. Бразилияда мыңдаған көліктер этанолды жағу арқылы жұмыс істейді. Бұл үрдіске басты себеп ретінде жетпісінші жылдары туындаған кризис болатын. Қазақстан үшін биожанармай өндірісі Батыс елдері үшін сияқты дәл осы уақытта соншама маңызды болып тұрған жоқ (өйткені қазіргі таңда республика үшін ең басты энергия көздері - бұл мұнай мен газ болып отыр) . Дегенмен мұнай мен газ қорларының сарқылатындығына қарағанда, Қазақстанда биоэтанол шикізаты - целлюлозаның қоры шексіз деп айтуға болады. Сол себепті Қазақстан үшін целлюлоза қорларын пайдалану - экономикалық жағынан таптырмайтын пайда болып табылады. [13]
Этил спиртін дәстүрлі жолмен өндіру кезінде құрамында крахмалы бар шикізат және қант (меласса) қолданылады. Крахмалды шикізат - бұл, негізінен, астық тұқымдастары (бидай, арпа, сұлы), күріш, жүгері және көп жағдайда - картоп. Келтірілген шикізаттың барлығы да азық-түлік көздері болып табылады. Азық-түлікке деген сұраныстың жоғарылауын еске алатын болсақ, спиртті целлюлозадан алу - өте перспективті әдіс. Бұл шикізат түрінің артықшылығы - оның қайтадан қалпына тез келуіне байланысты: дүние жүзінде жыл сайын 100 млрд. т. целлюлоза жинақталса, крахмал - 1 млрд., ал қант - 0, 1 млрд. т. Осы фактілерге сүйенетін болсақ, этил спирті өндірісі үшін целлюлозды шикізатты қолдану өте өзекті болып келеді.
Этил спиртін қанттарды, негізінен, глюкозаны, энзимдер мен ашытқылардың қатысымен ашыту арқылы алады. Глюкоза бастапқы шикізатта болуы мүмкін немесе оны полисахаридтерді - крахмал мен клетчатканы гидролиздеу арқылы алады. Қазір спирт өндірісінде азық-түлік өнімдерін целлюлозалы шикізатпен ауыстыру технологиялары белсенді түрде іздестірілуде, ал целлюлоза көптеген өндірістердің қалдығы болып табылады (орман шаруашылығы, ағашты өңдеу өндірісі, қағаз жасау өндірісі, т. б. ) .
Глюкозаны целлюлозаға дейін екі жолмен гидролиздеуге болады: химиялық және ферментативті. Целлюлозаның химиялық гидролизі қышқылдардың қатысуымен жүзеге асады, сол себепті осы процесстен кейін қалдықтарды утилизациялау маңызды проблемалардың біріне айналады. Сонымен қатар реакцияның соңғы өнімін қышқылдар мен бөгде қосылыстардан тазартылуын өте қатаң қадағалау қажет, себебі гидролизден кейін глюкозамен бірге реакторға түскен қышқылдар спирттік ашытуды жүргізетін ашытқыларға кері әсер етіп, реакцияны тежеуі мүмкін.
Ферментативті гидролиз процесстерін практикада қолдану үшін ферменттердің жоғары белсенді формаларын алу қажет, бастапқы субстратты активтендіріп, ферментация процесстерінің параметрлерін оптимумға келтіру қажет. Ферментативті гидролиз процесстері химиялық гидролизге қарағанда күрделірек, дегенмен ферментативті үрдіс гидролизді селективті өткізуге мүмкіндік береді және химиялық гидролизге қарағанда қосымша бөгде заттардың түзілуіне алып келмейді. [7]
Целлюлозаның ферментативті деструкциясын жүзеге асыру үшін целлюлазалық ферменттердің продуценттерін тауып, олардың ішінен ең оптимальды продуцентті таңдау маңызды. Табиғатта целлюлазаларды өндіретін организмдер көп кездеседі, бірақ олардың барлығы өндірістік масштабта қолдануға келмейді. Целлюлаза продуценттері ішінен ең қолайлы объектілерінің бірі - Aspergillus туысына жататын саңырауқұлақтар. Aspergillus саңырауқұлақтары табиғатта көптеп кездеседі, аса күрделі дақылдандыру жағдайларын қажет етпейді. Сонымен қатар, бірқатар дерек көздері бойынша Aspergillus саңырауқұлақтары целлюлазалық ферменттерді түзуге қабілеттілігі және де целлюлазалық комплекстің ішінен эндоглюканаза ферменттерін жоғары деңгейде синтездейтіні белгілі [8] . Сол себепті осы саңырауқұлақтардың эндоглюканаза ферменттерін қолданып, биоэтанол жасау үрдісінде қатыстыру - аса перспективті бағыт.
1 ӘДЕБИЕТКЕ ШОЛУ
1. 1 Aspergillus туысы саңырауқұлақтарына жалпы сипаттама
Аспергилл туысы ( Aspergillus )
Ғылыми классификациясы:
Домен: Eukaryota
Патшалық: Fungi
Бөлім: Ascomycota
Бөлім асты: Pezizomycotina
Класс: Eurotiomycetes
Қатар: Eurotiales
Тұқымдас: Trichocomaceae
Туыс: Aspergillus
Аспергилл туысының саңырауқұлақтары (алғаш рет 1729 ж. итальян микологы П. Микеллимен сипатталған) - ең көп таралған гифомицеттердің бірі. Олардың мекен ету ортасы - топырақтың беткі қабаты, әсіресе оңтүстік өңірлерде. Дегенмен оларды сұр-көгілдір, жасыл колониялар түрінде түрлі тағам беттерінен табуға болады, колониялар пайда болуы үшін бұл саңырауқұлақтарға жоғарғы ылғалдылық жеткілікті. Аспергиллдердің көбісі - сапрофиттер, бірақ бұл туыста адам мен жануарларда паразитті тіршілік ететін түрлер кездеседі. [4]
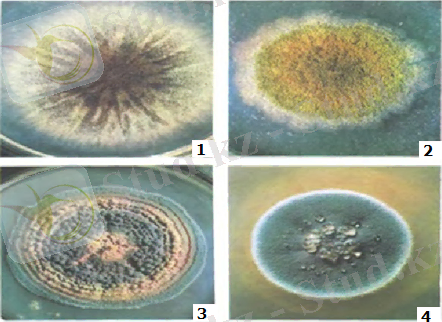
- -Aspergillus niger, 2 -A. flavus, 3- Penicillium expansum, 4 -P. cyclopium.
Сурет 1 - Aspergillus пен Penicillium туысы колониялары
( Aspergillus niger морфологиясы // Internet. - http://dic. academic. ru/dic. nsf/enc_biology/1845/%D0%A0%D0%BE%D0%B4#sel= )
Аэробты микроорганизмдер, әртүрлі субстраттарда жақсы өседі. Алдымен ақ түсті үлпілдек колонияларды түзетін болса, кейін, жатқызылатын түріне байланысты, алуан түрлі түстерге боялуы мүмкін, бұл саңырауқұлақтың метаболиттері мен спора түзу процесстеріне байланысты (Сурет 1) . Саңырауқұлақ мицелийі өте берік, мықты, жоғарғы сатыдағы саңырауқұлақтарға тән пердешелері болады. Барлық класс саңырауқұлақтары сияқты, аспергиллдер де жыныссыз жолмен түзілетін споралармен көбейеді. Дегенмен Aspergillus fumigatus жынысты жолмен көбейе алады.
Табиғатта өте кең таралған, сыртқы факторларға тұрақтылығы жоғары. Ылғалды бөлмелердің қабырғаларында болатын қара “дақтар” - бұл, негізінен, жеміс беру фазасына түскен Aspergillus niger. [5]
Aspergillus niger морфологиясы.
Aspergillus niger қалталы саңырауқұлақтар классына ( Ascomycetes ), аспергиллдер тұқымдасына ( Aspergillaceae ), Aspergillus туысына жатқызылады (бұл түрден басқа осы туысқа 120 түр кіреді) . Саңырауқұлақ денесі түссіз, қатты тармақталған және бір-бірімен өрілген жіпше- гифалардан тұрады, бұл гифалар жиналып, мицелий түзеді. Гифтер септелген - пердешелермен (септермен) клеткаларға бөлінген. Гифтер диаметрі 3-тен 6 мкм-ге дейін (Сурет 2) .
Аспергиллдер үшін беткі өсу тән, бірақ жеткілікті аэрация мен асептика ережелерін өте қатаң сақтаған кезде қатты және сұйық ортаның ішінде де көбейе алады.
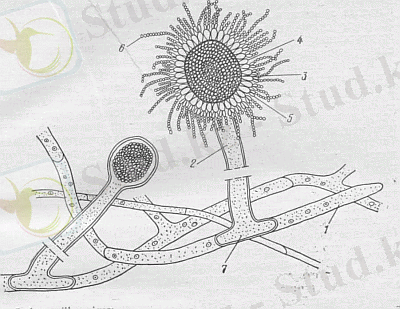
1 - гифтер; 2 - конидий түзуші өскін; 3 - көпіршік; 4 - бірінші қатар стеригмалары; 5 - екінші қатар стеригмалары; 6 - конидии; 7 - тірек клеткалары.
Сурет 2 - Aspergillus niger
(Производство лимонной кислоты // Internet. - http://citricacid. ru/aspergillus-niger/morphology/)
Беттік өсірілу кезінде мицелийден ерекше тірек клеткаларынан тарайтын жемісті денесі - конидийлер орналасатын өсінді бөліктері ортадан көтеріліп тұрады. Конидий орналасатын өсінділер - бұл жуаң, тармақталмаған, септелмеген, сыртқы беті түйіршікті, ұзындығы 2000 және одан да ұзын болатын гифтер. Алдымен конидий орналасатын өсінділерде болашақ конидий жиынтығының негізі болатын “көпіршік” пайда болады. Көбіршік дөңгеленіп, 400 мкм-ге дейін жетеді, оның үстіңгі бөлігінде ұзынша келген бірядролы немесе екіядролы клеткалар - стеригмалар түзіледі. Стеригмалардың бос ұштарында тізбек түрінде одан да ұсақ клеткалар - конидийлер пайда болады. Осылай өсіндінің жалпы көрінісі суы ағып жатқан “субұрқаққа” ұқсайды. Дегенмен аспергилл терминінің дәл аудармасы - “сабалақ жүнді”.
Конидийлер - судың минимальды мөлшері болатын, шар тәрізді немесе эллипс тәрізді, көлденең кесіндісі 4 мкм болатын тыныштықта жатқан клеткалар. Конидийлердің беті - тегіс, кедір-бұдыр немесе тікенді, қара (саңырауқұлақтың niger аталуы да содан) немесе қара-қоңыр түсті. Конидийдің түсі барлық конидий түзуші беттің түсін қамтамасыз етеді. Әрбір басында орналасқан конидийлердің саны 10 мыңға дейін жетеді.
Жетілген конидийлер өскіннің басынан ауаның немесе су ағымы әсерімен өте жеңіл бөлініп кетуі мүмкін. Сұйық қоректік ортаға түскенде, олар алдымен ісінеді, кейін бір немесе екі өскінше (гифтер) түзіп өне бастайды, қатты қоректік ортада ылғалдылық жеткілікті болса, бірден өскін шығара бастайды. Гифа бос ұшында өсе бастайды; ұзарғанда, қосалқы өскіншелер пайда болады да, олар өз алдымен ұзарып, бір-бірімен тығыз байланысып, көзбен көрінетін колонияларды түзеді. 16 - 20 сағ кейін орталық гифада кейін одан конидий түзушілер дамитын ерекше клеткалар пайда болады. Жетілген конидийлердің пайда болуы тек 3 - 4 күннен кейін ғана аяқталады.
A. niger -дің жоғарыда қарастырылған көбею тәсілі “жыныссыз” деп аталады. Жалпы, аспергиллдер жеміс денелерінде пайда болатын аскалар арқылы жынысты жолмен де көбеюге қабілетті. Сонымен қатар гифадан үзілген бір бөліктен жаңа мицелий өсіп шыға алады, бұл аспергиллдердің вегетативті көбеюі. [6]
1. 2 Өсімдік биомассасының негізгі компоненттерінің құрылымы мен қасиеттері
Барлық жер бетіндегі өсімдіктердің структуралық каркасы лигнин, гемицеллюлоза және целлюлоза полимерлерінен тұрады. Олар әртүрлі пропорцияларда біріге отырып, ауыл шаруашылығының, ағаш өңдеу өнеркәсіптерінің және адам күнделікті шаруашылық іс әрекетінің басқа да салаларынан қалатын қоқыс биомассасының басым көпшілігін құрайтын лигноцеллюлозалық материал түзеді.
Целлюлоза ( лат. cellula - бөлме, осында - клетка) - клетчатка, өсімдіктердің клетка жарғақшасының құраушысы, молекулалары глюкза моносахаридынан тұратын полисахарид. Целлюлоза өсімдік тіндеріне механикалық беріктік, серпімділік қасиет береді. Ол өсімдіктерде қарапайым көмірсулардан күрделі биохим. синтез нәтижесінде түзіледі. Целлюлозаның молек. массасы қай өсімдіктен алынғанына байланысты бірнеше миллиондаған көміртектік бірлікке дейін барады. Оның молекуласының құрылымы сызықты тармақталған, сондықтан мақта, зығыр, кендір, т. б. талшықты материалдардың целлюлозадан түзілетіндігі осыған байланысты.
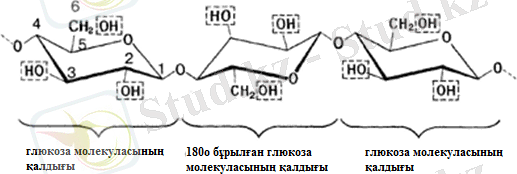
Сурет 3- Целлюлоза молекуласының құрылымы
Әрбір глюкоза молекуласының қалдығы көрші молекулаға қарағанда 180 о бұрылған және онымен -О- оттекті көпірше арқылы гликозидтік байланыспен байланысқан. Осылай бүкіл молекула ұзын тізбек түрінде болады. Тізбектің әрбір бөлігі 6-буынды цикл түрінде болады. Осы 6-буынды циклдың конформациясы кеңістікте жазықтық бойымен түзу орналаспайды, ол целлюлоза молекуласы үшін ең тұрақты әрі қолайлы “кресло” конформациясына өтеді. Әрбір глюкоза қалдығында 3 ОН-гидроксил топтары бар (Сурет 3) .
Гидроксил топтары Н-сутегіні көпір ретінде қолданып, мықты молекула аралық байланыстарды түзуге қабілетті, сол себепті целлюлозада молекулалар арасындағы байланыс энергиясы өте жоғары, ал целлюлоза материал ретінде үлкен беріктік және тығыздық қасиетіне ие болады. Сонымен қатар ОН-топтары ауадан су буларын сіңіріп, целлюлозаға көпатомды спирттердің қасиеттерін тән қылады. Целлюлоза ісінген кезде, оның молекулалары арасындағы сутектік байланыстар ыдырап, молекулалардың тізбектері судың әсерінен (немесе сіңірілген басқа да реагенттен) бір-бірінен алшақтайды да, жаңа байланыстар - су мен целлюлоза молекулалары арасындағы байланыстар пайда болады.
Қалыпты жағдайда целлюлоза - тығыздығы 1, 54-1, 56 г/см 3 болатын қатты зат, еріткіштердің көбісінде - су, спирт, диэтил эфирі, бензол, хлороформда, т. б. ерімейді. Табиғи талшықтарда целлюлозаның кристаллдану дәрежесі 70% жетіп, аморфты-кристаллдық құрылымда болады.
Целлюлозаның қатысуымен жүретін химиялық реакцияларда, негізінен, үш -ОН тобы қатысады. Целлюлозаның басқа элементтері реакцияға басқа өте қатты факторлар әсер еткенде кіріседі, бұл факторлар - жоғарғы температура, концентрлі қышқылдар, сілтілер, тотықтырғыштар. [12]
Осылай целлюлозаны 130 о С дейін қайнатқанда, оның қасиеттері тек аз мөлшерде ғана өзгереді. Бірақ 150-160 о С температурада целлюлозаның баяу ыдырауы - деструкциясы басталады да, 160 о С жоғары температураларда бұл процесс өте тез өтіп глюкозидті байланыстардың бұзылуымен (оттегі атомы бойынша), молекулалардың одан да қатты ыдырауымен сипатталады.
Қышқылдар целлюлозаға әртүрлі әсер етеді. Мақта целлюлозасын концентрлі азот және күкірт қышқылдарымен өңдегенде, реакцияға -ОН гидроксил топтары кірісіп, нәтижесінде целлюлозаның азотқышқылды эфирлері - нитроцеллюлоза пайда болады, ол құрамындағы нитротоптардың санына байлансты әртүрлі қасиеттермен ерекшеленеді. Нитроцеллюлозалардың ішіндегі ең танымал өкілдері - бұл оқ-дәрі жасауда қолданылатын пироксилин мен негізі нитроцеллюлоза болатын бірнеше қоспа қосылған пластмасса - целлулоид. [1]
Химиялық әрекеттесудің тағы басқа түрі бұл целлюлозаны тұз немесе күкірт қышқылдарымен өңдегенде байқалады. Бұл минералды қышқылдардың әсерінен глюкозидтік байланыстарының ыдырауымен жүретін целлюлоза молекулаларының деструкциясы бастау алады, реакцияға су молекулалары да кірісіп, деструкция гидролиз процессімен қоса жүреді (Сурет 4) .
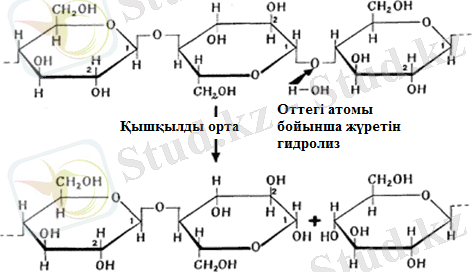
Сурет 4 - Қышқыл ортада жүретін целлюлоза деструкциясы
Минералды қышқылдармен қайнату арқылы жүретін толық гидролиз глюкозаның түзілуіне алып келеді. Целлюлозаның толық емес ыдырауының өнімі - бұл қалыпты целлюлозадан төмен механикалық беріктігімен сипатталатын гидроцеллюлоза, беріктіліктің төмендеуінің себебі - беріктілік қасиеттері полимер молекуласының тізбегі қысқарған сайын төмендей береді. Минералды және органикалық қышқылдардың әлсіз ерітінділері (0, 5%-дық) 70 о С дейінгі температураларда әсер етеді, егер одан кейін оны шаятын болсақ, целлюлозаға мүлдем әсер етпейді.
Сілтілерге (сұйылтылған ерітінділерге) целлюлоза тұрақты болып келеді. Концентрациясы 2-3, 5% болатын күйдіргіш натр ерітінділерін ескірген мата қалдықтарынан қағаз жасау өндірісінде кең қолданады.
Салқын (бөлме немесе одан да төмен) температураларда целлюлозаға концентрлі қышқылдардың әсері ерекше. 1844ж Дж. Мерсермен ашылған бұл мерсеризация құбылысы маталардың қасиеттерін жақсарту үшін қолданылады. Талшықтарды 20 о С 17, 5% күйдіргіш натрмен өңдейді. Целлюлоза молекулалары сілтіні қосып алып, сілтілі целлюлозаға айналады, процесс кезінде целлюлоза көлемін үлкейтіп қатты ісінеді. Осындай өңдеуден өткен целлюлоза талшықтары жұмсақ, жібек тәрізді болып, түрлі бояғыштарды өзіне жақсы сіңіруге өте қабілетті болады.
Жоғары температураларда оттнгінің қатысуымен концентрлі қышқылдар глюкозидті байланыстардың ыдырауымен жүретін целлюлозаның деструкциясын туғызады.
Целлюлоза - глюкоза қалдықтарынан тұратын полимер болыр есептеледі. Дегенмен тек глюкоза қалдықтарынан тұратын целлюлоза моделі - бұл идеальды вариант. Табиғатта өсімдік шикізатында осы модельден көп не аз мөлшерде ауытқитын мысалдар жиі кездеседі. Целлюлоза макромолекуласында урон қышқылдары, моносахаридтердің басқа да қалдықтары болуы мүмкін.
Целлюлоза макромолекуласында глюкоза қалдықтарының саны “полимеризациялану дәрежесі” деп аталады және n индексіменен белгіленеді. Оның мөлшері әртүрлі целлюлозды шикізатта әртүрлі. Мысалы, мақтада n 5000-12 000 болса, зығыр, рамиде бұл көрсеткіш 20 000 - 30 000 дейін барады. n неғұрлым көр болса, целлюлоза соғұрлым мықты әрі берік болады.
Дегенмен егер целлюлозаны белгілі бір өсімдік түрінен алынған материал ретінде қарастыратын болсақ - мақта, зығыр, кендір (конопля) немесе ағаш, онда целлюлоза молекулалары әртүрлі ұзындыққа, әртүрлі полимеризациялану дәрежелеріне ие болатынын байқаймыз, яғни целлюлоза молекуласында қысқа және ұзын тізбектер де болады. Кез келген техникалық целлюлозаның жоғарымолекулалық бөлігін а-целлюлоза деп атау келісілген. а-целлюлоза - бұл 200 немесе одан да көп глюкоза қалдықтарынан тұратын целлюлозаның бөлігі. Целлюлозаның осы бөлігінің ерекшелігі - бұл 17, 5%-дық күйдіргіш натр ерітінділерінде ерімеуі (бұл жоғарыда айтылған мерсеризация процесінің параметрлері) .
Гемицеллюлоза және пектиндер. Техникалық целлюлозаның ерігіш түрін “гемицеллюлоза” деп атайды. Гемицеллюлоза 200-ден 50-ге дейін глюкоза қалдықтарынан тұратын b-фракциясынан және ең төмен молекулалық массасымен сипатталатын, n 50-ден аз болатын y-фракциясынан тұрады. “Гемицеллюлоза” деген атау “а-целлюлоза” деген атау сияқты шартты: гемицеллюлозаның құрамына тек қана молекулалық массасы төмен болатын целлюлоза кірмейді, онымен қоса молекулалары басқа пентоза мен гексоза қалдықтарынан тұратын полисахаридтер кіреді. Олардың ортақ қасиеті - n полимеризация дәрежесінің төмен болуы, 200-ден кем, сол себепті 17, 5%-дық күйдіргіш натр ерітіндісінде еруі.
Өсімдік талшықтарында целлюлозамен бірге басқа да қосымша заттар кездеседі. Олардың бірі пектинді заттар мен пентозандар. Пектинді заттар - көмірсу классының полимерлері, целлюлоза сияқты тізбекті құрылымды болып келеді, бірақ урон қышқылы қалдықтарынан құралған, дәлірек айтқанда - галактурон қышқылы қалдықтарынан. Полигалактурон қышылы пектин қышылы деп аталса, оның метилді эфирлері - пектиндер деп аталады (Сурет 5) .
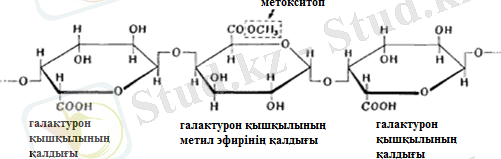
Сурет 5 - Пектин макромолекуласының құрылымы
Пектинді заттар қышқылдарға тұрақты, дегенмен сілтіқоып қайнатқан кезде өте тез ыдырап кетеді. Олардың бұл қасиеті целлюлозаны пектинді заттардан тазартқан кезде қолданылады.
Пентозандар - пентоза қалдықтарынан, негізінен, арабиноща мен ксилозадан тұратын полисахаридтер. Сәйкесінше бұл пентозандар “арабандар” мен “ксиландар” деп аталады. Олардың құрылымы тізбекті немесе әлсіз тармақталған, өсімдіктердің құрамында олар пектинді заттармен қоса (арабандар) немесе гемицеллюлоза құрамына (ксиландар) кіреді. Арабандар суда жақсы еритін болса, ксиландар суда ерімейді.
Лигнин. Целлюлозаның келесі тағы бір серігі - лигнин, тармақталған полимер, ағаштардың сүректенуін тудырады. Негізінен, осы полимер өсімдік клеткалары арасындағы кеңістікті бітеп тастайды да, кейде талшықтардың үстіңгі бөліктеріне өтіп, целлюлоза талшықтарын бірге ұстап тұратын инкрустациялаушы зат сияқты болады. Лигниннің әжептәуір көп мөлшері әсіресе ағашта кездеседі - 30% дейін. Өзінің табиғаты жағынан лигнин полисахаридтер классына жатпайды, осы полимер көпатомды фенолдардың туындысы, яғни майароматты қосылыстарға жатады. Оның целлюлозадан ең негізгі айырмашылығы - лигнин макромолекуласының құрамы тұрақты емес, яғни полимер молекуласын бірдей мономер қалдықтары емес, әртүрлі құрылымдық компоненттер құрастырады. Дегенмен оларды да біріктіретін бір ерекшелік бар - олар ароматты ядро мен бүйірлік пропан тізбегінен тұрады, барлық лигниндерге тән болып келетін осы құрылымдық элементті “фенилпропанды мүше” деп атайды.
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz