Рений және 2,2'-дипиридил негізіндегі әртекті лиганттық комплекстер: физико-химиялық қасиеттер мен аналитикалық спектрофотометриялық әдістерге әдеби шолу


Әдеби шолу
Рений
Жалпы сипаттамасы
1937жылы Э. Сегре мен К. Перье молибденді нейтронмен атқылау арқылы жасанды түрінде алған және нөмері 75 элементі рентгенспектральдық әдіспен анықтады. 922 жылы немістің ағайынды химиктері Вольтер мен Ида Ноддак рентген спектрінің көмегімен колуибиттің құрамынан нөмер 75 элементті тапқан. 1925 Рений деп жариялаған. Ал 1927 жылы олар ренийді молибден концентратының құрамынан бөліп алуға болатындығын айтқан. Бірінші рет ренийді 1930 Германияда Мансфельд заводында өндірген.
Физикалық және химиялық қасиеттері
Рений - пнриодтық жүйенің VII тобының элементі маргенец пен технецийдің аналогы. Ең жақын ренийдің аналогы - технецийдің, нөмер 43 элемент. Атомдық массасы 186, 027 ядроның зарияды - 75. Электрондардың орналасуы келесідей : 2, 8, 18, 32, 13, 2. Электрондық құрылысына байланысты рений ауыспалы валенттік көрсетеді. Ең тұрақты қосылыстар төрт-, алты-, жеті- валентті рений . Рений гидриді - (ReH) қосылысы екені белгілі, оның құрамында ренийдің валенттілігі (-1) .
Рений - жылтыр ақ түсті, платинаға ұқсас металл. Ауада үй температурасында тұрақты, ұнтақ түрінде ауада жануы мүмкін, сондықтан тотығып рений оксиді (Re 2 O 7 ) түзіледі.
Ренийдің тығыздығы 21, 02 г/см 3 (ең ауыр металдардың бірі ), балқу температурасы 3190 o c, қайнау температурасы 5600 o c . льфрамнан кейінгі ең қиын балқитын металдың бірі 20 o c температура шамасында ренийдің меншікті электркедергісі - 19, 14 10 -6 ом. см қыздырғанда рений оттекпен, галогендермен, күкіртпен әрекеттесіп, ұнтақ түрін сутекті окклюзденеді.
Тығысдығы жөнінен осмийден, ирийден және платинкадан кейінгі төртінші орында. Рений ауада тұрақты, тотығу процесі 300 o c - тан басталады да температура жоғарлаған (600 o c) сайын қарқынды жүріп ренийдің (VII) оксидін түзеді . сутегімен рений балқу температурасына дейін әрекеттеспейді де, броммен және иодпен қосылысқа кірмейді. Тұз және фторсутек қышқылдарын қыздырғанда да рений ерімейді. Рений азот, күкірт қышқылдарында және сутегінің диоксидінде сонымен қатар тотықтырғыш қосқан сілтілерде жақсы ериді. Рений химиялық қосылыстарда бір мен жетінің арасындагы тотығу дәрежесін көрсетеді.
Аналетикалық сипаттамасы
Рений аналетикалық химиясы туралы коп жұмыстар көрсетілген. Ренийдің ең белгілі аналетиукалық қасиеттеріне тоқталайық.
Рений сапалық әдіспен анықтау үшін, рений оксидінің Re 2 O 7 ұшқыш қасиетін пайдаланады: күкірт окситін қосқанда рений(VII) тотықсызданып, көк түсты оксид түзіледі. Осы реакциямен малибденның қатысында ренийдің аз мөлшерін анықтауға болады - (5 мкг) . Калий ферроцианиді рениймен қоңыр түсті тұнба береді, бірақ бұл реагентпен көп элементтер әрекеттеседі. Калий роданиді рениймен түз қышқылды ортады қалайы(II) хлоридінің қатысында сарғыш қызыл түсті комплексті қосылыс K[ReO(CNS) 4 ] түзеді, бұл сезмтал реакция ренийдің сапалық және сандық анализіне кең қолданылады. Ренийді анықтау шегі 0, 2 мкг/мл. Ренийді анықтау үшін әр түрлі органикалық реакциялар пайдаланады.
Гавиметрлік әдіспен ренийді анықтау үшін таллийдің тұздармен, күкіртсутекті және әр түрлі органикалық реагенттермен (нитрон, фениларсон қышқылы) түзілетін нашар еритін қосылыстарды пайдаланыды.
Фениларсон қышқылы перрнатпен құрамы тұрақты тұнбалар түзеді, тұнбаның құрамы қыздырғанда (106-185 0 С) өнзгермейді. Рений молибдениттердің концентраттарнда анықтағанда сезгіш әдістер пайдаланыды - спекторлы және фотометрлік. Фотометрлік әдіспен ренийді анықтауға қолданылатын әдістер өте көп және белгілі. Олардің арасында ең кең тарағаны және жиі пайдаланатыны жоғарда аталған “ роданидті’’ реакция.
Қолданылуы
Рений және оның қосылыстары химия, мұнай және металлургия өнеркәсіптеріне катализатор ретінде электротехника салаларында электр шамдарының қылсымын, кедергілері, резисторлар, термо-паралар және қосмоста қолданатын ыстыққа төзімді әртүрлі құймалар жасауға, әсіресе ұшақтар мен зымырандарда кеңінен қолданады.
Дипиридилдер -
молекуласында екі пиридил қалдығы бар гетероциклді аминдер.
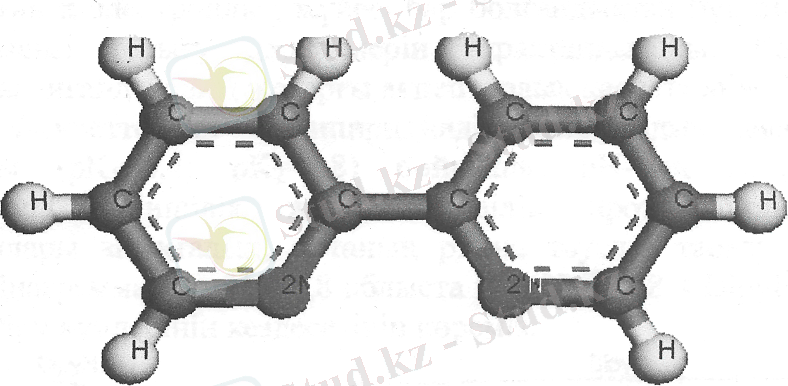
Сурет 6 - 2, 2'-дипиридил молекуласының кеңістіктегі көрінісі
Дипиридилдің алты изомері бар:
I - 2, 2'-дипиридил немесе а, а'-дипиридил; II - 2, 3'-дипиридил немесе а, р'-дипиридил; III - 2, 4'-дипиридил немесе а, у'- дипиридил; IV- 3, 3'-дипиридил немесе 3, р'- дипиридил; Ү-3, 4'-дипиридил немесе (3, ү'- дипиридил, VI - 4, 4'-дипиридил немесе у, у'- дипиридил.
Ерітіндінің рН-ының төмендеуі мен 2, 2'-дипиридилдің УК- спектрлерінің жұгылу жолақтарыньщ ығысуына қарап, протонный, бос негізге сатылап косылады деген шешімге келген. Бірінші сатыда (10) монокатион (И 4 " dipy), екінші сатыда (11) дикатион (Н2 2+ dipy) түзіледі. (КІ=3, 72* 10~ 5 ; К2=1, 66*10~ ) .
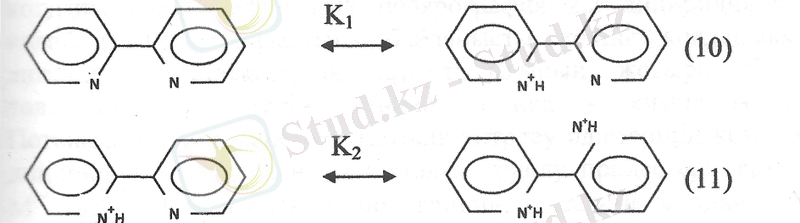
H + dipy монокатионына жазық цис - конфигурация, ал H 2 2+ dipy дикатионына транс -конфигурация тән. Қосылған екІ протонның стериялық әрекеттесуінің нәтижесінде пиридин сақиналарының копланарлығы бұзылады.
Дипиридилдер фенолдармен, аминдермен, металл тұздарымен және басқа да косылыстармен комплекс түзуге бейім. 2, 2'-дипиридил периодтық жүйедегі металл тұздарымен қосылыстар береді. Ол басқа изомерлерімен салыстырғанда активтігі ең жоғарғы қосылыс болып табылады. 2, 2'-дипиридил полидентантты лиганд ретінде зерттеулерде көп қолданылады. Тармақталған π электрондық жүйесі бар болғандықтан бұл лиганд ортальқ атомның төменгі тотығу дәрежелерін тұрақтандырады. Комплекстердің тұрақты болуы лигандтардың жоғаргы акцепторлық қасиеттеріне байланысты.
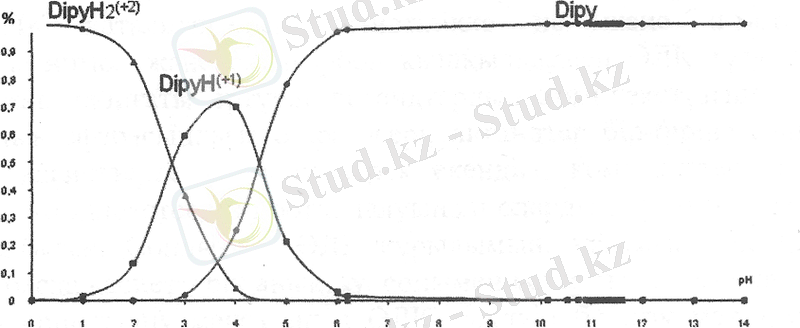
Сурет 7 - 2, 2' - дипиридилдің әртүрлі күйлерінің ерітінді рН-на тәуелді таралу диаграммасы.
Төмендегі 7-суретте 2, 2' - дипиридилдің қышідылдық диссоциациялану константалары (рКІ=4, 4; рК2=2, 8) бойынша, рН-тың әртүрлі мәнінде протондалмаған, біріншілік және екіншілік протондалған лигандтың концентрациялары анықталып, ортаның рН-на тәуелді таралу диаграммасы келтірілген.
Диаграммадан рН < 2, 8 облыста DipyH 2 2+ , 2, 8 < Dipy H + < 4, 4, рН > 4, 4 облыста Dipy күйлерінің кездесетінін көреміз.
Екі валентті металл түздарымен 2, 2'-дипиридилдің комплекс түзуі көп зерттелген. Me (II) : 2, 2'-dipy жүйесінде 1:2 жэне 1:3 қатынастағы комплекстер түзіледі. Металдың 2, 2'-дипиридилмен комплекстері түзілген кезде бесмүшелді хелатты циклдер түзеді, ал 4, 4'-дипиридил молекуласы металл иондарының арасында "көпірше" қызметін атқарады. 2, 2'-дипиридилдің аралас комплекстер түзу қабілеттілігі жоғары. Металдардың 2, 2'-дипиридил қатысындағы әртекті лигандты комплекстерін зерттеуде көбіне потенциометрия жэне рН - метрлік титрлеу эдістері колданылады. Классикалық полярография 2, 2'-дипиридилдің адсорбциялық колайсыздықтар туғызуына байланысты көбіне қолданылмайды. Әртекті лигандты комплекстердің түрақтылығының жоғыры болу себептерінің толықтай мэліметтерін жанама физика - химиялық эдістер береді. Потенциометрлік жэне рН- метрлік титрлеу эдістерінің көмегімен М п+ - 2, 2'-дипиридил - L жүйесіндегі комплекс түзілу процестері зерттелген. Мүндағы М пт - Cu 2+ , L - этилендиамин, глицин, а-аланин, малонат. Бірдей жағдайда анықталған (1=0, 2; 30°С) эртекті комплекстер мен біртекті комплекстердің тұрақтылық костанталарын салыстырғанда [Cudipy] коплекстері тұрақты екенін көрсеткен. Спектроскопиялық зерттеулер қорытындысы бойынша [CuL] және [CuL 2 ] комплекстеінің тұрақтылығының төмен болуы Си(П) -ң dn электрондары мен сэйкес лигандтың L ажырамаған электрон жүптарының тебісуіне байланысты деп түсіндіріледі. [CudipyL] типті комплекс түзілгенде орталық атомның dn электрондары мен 2, 2'-дипиридил молекуласының бос п орбиталдарының арасында дативті байланыс түзу нэтижесінде тебілу төмендейді. Бүл Си(П) -ң dn орбиталінің электрон тығыздығының төмендеуіне экеліп, нэтижесінде әртекті лиандты комплекстердің түзілуін күшейтеді [16] .
1. 1 Әртекті лигандты комплекстердің (ӘЛК) түзілу сипаттамасы
Әрткеті лиганты комплекстүзілу үрдістері аналитикалық химияда элементтерді анықтаудың бөлу және концентрлеу реакцияларының сезгіштігі мен талғанпаздығын арттыру үшін кеңінен қолданылады. Оларды химиялық технология мен гальванотехникада қолдану өндірісті жетілдіруге ықпал етеді. Көптеген ӘЛК каталитикалық активтілікке ие және d-металдардың гетероциклді аминмен және оксикарбон қышқылымен ӘЛК түзу үрдістері, нақтырақ айтсақ табиғаты әртүрлі лигантардың комплекстүзгіш-ионның координациялық сферасындағы өзара әсері, лигандтар бір-біріне сәйкес келу үшін қандай қасиеттерге ие болу керек екендігі, комплекстердің құрамы, лигантар мен комплекстердің протондалуының олардың тұрақтылығына әсері толық зерттелмеген. Сондықтан ӘЛК құрылымын, құрамын, тұрақтылығын және тағы да басқа қасиеттарін анықтау, сонымен қатар ғылым мен практиканың нақты міндеттерін шешу мақсатында ӘЛК түзілуін болжау мен қасиеттерін бағытты түрде өзгерту маңызды және өзекті болып табылады.
ӘЛК түзілгенде маңызды рольді біртекті комплекстердің тұрақтылығын анықтайтын факторлар болып табылады. Сонымен қатар ӘЛК түзілу реакциясылигандтардың үйлесімділігін және олардың тұрақтылығын анықтайтын спецификалық парамерлермен сипатталады. Сондықтан орталық ион, лиганд және ортаның комплементарлық және сәйкестік принципі ӘЛК түзілгенде жақсы көрінеді. Мұндай комплекстерде МА және МА 2 типі комплекстерде байқалмайтын қасиеттер тән болып келеді: стереоселективтілік, кіші молекулаларды (O 2 , N 2 , CO, NO) байланыстыру қабілетілігі, жаңа химиялық қасиеттер, молекулашылық, лигандаралық байланыстардың түзілуі және лигандаралық әрекеттесу, лигандтардың депротондалу процесін және олардың реакциялық қаьілеттілігін, лигандтардың ерекшелігін басқару, белгілі тотығу дәрежесі бар металдармен комплекстерінің тұрақтылығын және координациялық полиэдрдің геометриясы, жеңіл гидролизденетін лигандтардың тұрақтылығы және олардың ерекше құрылымы және т. б. Бұл барлық эффектілер белгілі бір дәрежеде ӘЛК тұрақтылығына әсер етеді.
ӘЛК - дің тұрақтылық константалары (1) - (3) теңдеулерімен анықталады:
... жалғасыM + L + X MLX, =
ML + X MLX, =
MX + L MLX, =
Мұндағы М - металл ионы; L және X - лигандтар. Тәжірибеден анықталатын жалпы тұрақтылық константасы мына теңдеулер арқылы K ML MLX және K MX MLX байланысады:
Lg = lg - lg
lg = lg - lg
мұндағы және - мынадан туындайды:
M + L ML, =
M + X =
ӘЛК - дің салыстырмалы тұрақтылығы ΔAIgK шамасымен анықталыды:
lgK = lg - lg =lg - lg =lg - lg -lg
lgK шамасы лигандтың (мысалы, X) ML комплексіне координациялануының салыстырмалы ( оның акваионға координациялануымен салыстырмалы түрде ) қабілеттілігін сипаттайды.
ӘЛК - дің сандық сипаттамасы үшін қолданылатын тағы бір жақындастыру () - теңдеумен сәйкес “антидиспропорцонирлеу” (сопропорционирлеу) реакциясына негізделген:
ML 2 + MX 2 2MLX, X 11 =
ал Lg X 11 мына теңдеумен анықталады:
lgX 11 = 2lg - (lg lg ) =
(lg - lg ) + (lg - lg )
Мұндағы , , және -(), (), (), () теңдеулеріне сәйкес
- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz