Атом-молекулалық ілім және химияның теориялық негіздері: стехиометриялық заңдар, атом құрылысы, периодтық заң және химиялық байланыс


1. Атом молекулалық ілім. Химияның негізгі түсініктері мен стехиометриялық заңдары (Зат массасының сақталу заңы, құрам тұрақтылық заңы, еселік қатынастар заңы, көлемдік қатынастар заңы, эквиваленттер заңы, Авогадро заңы) .
Ежелгі атомистика теориясы Ломоносовтың атомдар туралы көзқарасынан тым алыстау екені анықталды. Химияның даму тарихының бір дәуірі алхимиямен байланысты. Алхимия өз заманына керек болды. Алхимияның негізгі міндеті-философиялық тастың көмегімен, жай заттарды алтынға айналдыру еді. Олардың негізгі мақсаты-жай металдардың құрамына асыл қасиеттерді кіргізу арқылы алтын алу. Алхимия Аристотельдің жалған теориясына негізделгенімен, зерттеу барысында көптеген химиялық заттар және сол заттарды алу әдістерін ашуға мүмкіндік жасады. Неміс ғалымы Шталь 17 ғасырда флогистон теориясын ұсынды. Бұл теория бойынша, барлық жанатын заттардың және металдардың құрамында ерекше зат-флогистон болатындығын айтты. Мысалы, металдарды қақтағанда флогистон бөлініп шығады деп санады:темір-темір қағы+флогистон. Демек, флогистон теориясы бойынша, темір(күрделі зат) қаққа(жай зат) және флогистонға ыдырайды. Бұл қате теория химияның даму тарихында пайдалы ықпалын жасады. Ф. Энгельс былай жазды:химия флогистон теориясы арқылы, алхимиядан құтылды. 2-нші кезеңі Ломоносовпен Дальтонның жұмыстары жатады. Химияның жекелей ғылым болып дамуы, 17ғ-дың 40жылдары басталды. Осы кезде, Ломоносовтың «Математикалық химияның элементтері» деген жұмысында, молекулярлық-атомистикалық көзқарас бірінші рет ұсынылды. Дальтон 1808ж «Химиялық философияның жаңа жүйесі » деген жұмысында атомдық-молекулярлық көзқарасты мазмұндады.
Химиядағы стехиометриялық заңдар деп, құрам тұрақтылық, еселі қатынастар, эквиваленттер, газдар, Гей-Люссактың көлемдік қатынастар және Авогадро заңдарын айтады. 1. Құрам тұрақтылық заңы. Прусттың 1801ж ашқан құрам тұрақтылық заңы:Әрбір таза заттың элементтік құрамы әрқашанда тұрақты, ол заттардың алу әдісіне байланысты емес. мысалы әр түрлі жолмен алынса да көміртек диоксидінде 27, 29 процент көміртек және 72, 71 оттек бар. 19ғасырдың басында Бертолле кейбір заттардың құрамы ауыспалы болатындығын ескертіп, заңға күмән келтірді. Пруст пен Бертолле арасындағы таласты, орыс ғалымы Курнаков шешті. Курнаков құрамы тұрақты қосылыстарды дальтонидтер деп, дальтонидтерге қарсы құрамы тұрақсыз қосылыстарды бертолидтер деп атады. Эквиваленттер заңы. Эквиваленттер заңы-химиялық заңдардың ең бір негізгісі . Олар химиялық элементтер бір-бірімен өздерінің химиялық эквиваленттеріне сай, белгілі сандық қатынаста әрекеттесетінін белгілейді. Эквивалент дегеніміз бағалары тең деген сөз. Эквивалент деп берілген қышқылдық негіздік реакцияда сутектің 1 катионына, немесе берілген тотығу-тотықсыздану реакциясында 1 электронға сәйкес шартты немесе нақты бөлшекті айтады. Зттың эквивалентінің 1 моль мөлшерінің массасын оның эквивалентінің молярлық массасы деп атайды. оның өлшем бірлігі-г/моль. 3. Еселі қатынас заңы. Дальтон 1803ж еселі қатынастар заңын өрнектеді: егер екі элемент өзара бірнеше химиялық қосылыстар түзсе, онда бір элементтің массасы осы қосылыстардағы екінші элементтің массаларына бүтін сандар ретінде қатынасады. Дальтон айтуы бойынша, атомның абсолюттік массасын анықтау мүмкін емес, сутектің атомдық массасын бірге тенестіріп, салыстырмалы атомдық масса туралы түсінік енгізді. Сутекте, оттекте изотоптар бар болғандықтан оны көміртекке өзгертті. Химиялық элементтің салыстырмалы атомдық массасы-өлшеусіз шама, олар көміртек бірлігімен өлшенетін атомдық масса болады. Атомның массасы көміртек массасы бірлігінің оның салыстырмалы массасының көбейтіндісіне тең. 4. Авогадро заңы. Моль-заттың мөлшері. Көміртектің С 12 изотопының 6, 02*10 23 атомдары бар. Мына сан 6, 02*10 23 Авогадро тұрақтылығы деп аталады. яғни, моль-заттың мөлшері, ол құрылыстық бірлікке 6, 02*10 23 дискретті. Авогадро заңы-бірдей жағдайда алынған газдардың тең көлемінде молекулалар саны да бірдей болады. Авогадро заңынан мына салдар шығады:молекулалық сандар бірдей газдардың, бірдей жағдайда, көлемі де бірдей болады.
2. Эквивалент, эквиваленттік фактор, эквиваленттің молярлық массасы. Эквивален ттер заңы. Атомдық және молекулалық массаларды анықтау әдістері.
Эквиваленттер заңы. Эквиваленттер заңы-химиялық заңдардың ең бір негізгісі . Олар химиялық элементтер бір-бірімен өздерінің химиялық эквиваленттеріне сай, белгілі сандық қатынаста әрекеттесетінін белгілейді. Эквивалент дегеніміз бағалары тең деген сөз. Элементтің химиялық эквиваленті деп сутек массасының 1, 008 бөлігі немесе оттек массасының 8, 0бөлігі қосылатын осы элементтердің мөлшерін немесе қосылыстарында орнын басатын осындай мөлшерді айтады. Эквивалент деп берілген қышқылдық негіздік реакцияда сутектің 1 катионына, немесе берілген тотығу-тотықсыздану реакциясында 1 электронға сәйкес шартты немесе нақты бөлшекті айтады. Бөлшектің берілген қышқылдық- негіздік реакцияда сутектің бір катионына сәйкес, немесе берілген тотығу-тотықсыздану реакциясында 1 электронға сәйкес келетін үлесін эквиваленттік фактор f экв деп атайды. Заттың эквивалентінің 1 моль мөлшерінің массасын оның эквивалентінің молярлық массасы деп атайды. оның өлшем бірлігі-г/моль. Күрделі заттың эквиваленттік массасын есептеу негізіне оның массалық бірлікпен алынған г/моль молярлық массасы алынады. Оксидтің экв. массасы массалық бірлікпен алынған оның молярлық массасының, металдың валенттілігі мен оның атомдар саны арасындағы көбейтіндіге бөлінген теңдеуге тең. Гидроксидтің экв. Массасы оның молярық массасының металдың валенттігіне немесе гидроксил топтарының санына бөлінген теңдеуге тең. Қышықылдың экв. массасы оның молярлық массасының қышқылдың негіздік санына бөлінген теңдеуге тең. Тұздың экв. массасы оның молярлық массасының, металдың валенттігі мен атомдар саны арасындағы көбейтіндіге бөлінген теңдеуге тең.
3. Атом құрылысы. Атом құрылысының күрделілігін дәлелдейтін тәжірибелер: М. Фарадейдің тәжібилері, катод сәулелері, электронның ашылуы, Э. Резерфордтың тәжірибелері және т. б.
Атом құрылысының күрделі екендігі туралы ұғым атом бөлшектерінің бірі болып саналатын электрондар құбылысы ашылғаннан кейін барып қалыптасты. Бірінші рет электрондар ағынын, катод сәулесін ашқан Крукс 1879ж байқаған. Ауасыз түтікшеде, үлкен кернеулікте электр тогы жүре бастағаны байқалады және түтікшенің ішінде сәуле пайда болды. Бұл сәулелер катодтан шыққандықтан, оны катодты сәулелер деп атады. Магнитті немесе электр өрістері болмаған жағдайда катодты сәулелер электр не магнит өрістерінде оң зарядталған электрод жағына ығысады. сол себептен оны теріс зарядталған бөдшектердің ағыны деп айтуға болады. Дж. Томсон 1897ж зарядтың электронның массасына қатынасын өлшеді және осы қатынастың катодтың табиғатына, газдың химиялық құрамына және тәжірибенің жағдайына байланысты еместігін көрсетті. Бір ғана елементарлы бөлшектен тұратын қарапайым ядро- сутек атомының ядросы болып табылады. Сутек атомының иондануы нәтижесінде Крукс түтігінде түзілетін бөлшекті 1920 жылы Э. Резерфорд протон деп атады, яғни бірінші деген мағынада. Бастапқыда басқа да элементтердің атом ядросы протоннан, ал атом электрон мен протоннан тұрады деп есептеді. Резерфордтың тәжірибелері атомның құрылысы планетарлы жүйеге ұқсас екендігін дәлелдеді: ортасында тығыз орналасқан оң зарядты ядро болады, ал ядроның айналасында, ядроның мөлшерімен шамамен 1 есе көп, көп женіл теріс зарядталған бөлшектер -электрондар айналып жүреді. Кемшілігі: Классикалық электродинамиканың заңдары бойынша, егер электронның ядроға кулондық тартылыс күші ортадан тебісу күшіне тең болса, онда ядроның маңындағы шеңбер бойынша электронның қозғалысы тұрақты болады. Резерфордтың моделі сутек атомының тұрақтылығын да немесе оның спектірінің сызықтық қасиеттерін де түсіндіре алмайды.
1933ж Иваненко, Гапон және олардан тәуелсіз Гейзенберг атом я дросының протонды-нейтронды құрылыс моделін құрды. Осы модель бойынша барлық элементтердің атом ядросы протон саны периодтық жүйедегі элементтердің рет номеріне сәйкес, ал нейтрон саны атомның массасынан протон санын алып тастағанға тең.
Ядролық физиканың даму тарихына көз жүгіртсек, оның қайнар көзі 1886 жылы француз ғалымы А. Беккерель ашқан табиғи радиоактивтік құбылысынан басталады. А. Беккерель уран тұзының фотопластинаға әсерін зерттеген. Тәжірибелер барысында ол мына құбылысты байқаған: уран тұздары тығыз қара қағазбен оралған фотопластинаға әсер етіп, оның қараюын туғызатын, өтімділігі жоғары белгісіз сәулелерді шығарады екен. Мұқият зерттеулер нәтижесінде Беккерель өтімділігі жоғары белгісіз сәулелерді уран атомының өзі, ешқандай сыртқы әсерсіз-ақ, өздігінен шығаратынын анықтады. Белгісіз сәулелердің заттармен әрекеттескенде:
1) фотопластинканы қарайтатыны, яғни химиялық әсерінің бары;
2) газдарды иондауы;
3) кейбір қатты денелер мен сұйықтардың люминесценциясын туғызатыны сияқты қасиеттері белгілі болды.
Бұл құбылысты зерттеу жұмыстары бірден басталды. Францияда 1898 жылы М. Склодовская-Кюри мен П. Кюри торий (
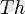 ) элементінің өздігінен сәуле шығаруын ашты. Өздігінен сәуле шығаратын химиялық элементті
радиоактивті
деп, ал сәуле шығару процесін радиоактивтік деп атауды М. Кюри ұсынған еді. Радиоактивтік латынның "
radio
" - сәуле шығару, "
activus
" - әрекетті деген сөздерінен алынған. Осы жылы ерлі-зайыпты ғалымдар тонналаған уран кенін өңдеу арқылы, радиоактивті екі жаңа химиялық элементті бөліп алады. Радиоактивтігі ураннан миллион есе қарқынды элементті (
) элементінің өздігінен сәуле шығаруын ашты. Өздігінен сәуле шығаратын химиялық элементті
радиоактивті
деп, ал сәуле шығару процесін радиоактивтік деп атауды М. Кюри ұсынған еді. Радиоактивтік латынның "
radio
" - сәуле шығару, "
activus
" - әрекетті деген сөздерінен алынған. Осы жылы ерлі-зайыпты ғалымдар тонналаған уран кенін өңдеу арқылы, радиоактивті екі жаңа химиялық элементті бөліп алады. Радиоактивтігі ураннан миллион есе қарқынды элементті (
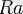 ) радий, екінші элементті М. Склодовскаяның отанының құрметіне полоний (
) радий, екінші элементті М. Склодовскаяның отанының құрметіне полоний (
 ) деп атаған. 1908 жылы Резерфорд спектрлік анализ әдісімен радиоактивті газ - радонды (
) деп атаған. 1908 жылы Резерфорд спектрлік анализ әдісімен радиоактивті газ - радонды (
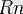 ) ашты. Ауқымды жүргізілген зерттеулер Менделеев кестесіндегі қорғасыннан кейінгі ауыр элементтердің ядроларының бәрінде табиғи радиоактивтік бар екенін көрсетті. Кейбір жеңіл элементтердің де, мысалы, калийдің изотопы
) ашты. Ауқымды жүргізілген зерттеулер Менделеев кестесіндегі қорғасыннан кейінгі ауыр элементтердің ядроларының бәрінде табиғи радиоактивтік бар екенін көрсетті. Кейбір жеңіл элементтердің де, мысалы, калийдің изотопы
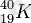 , көміртегінің изотопы
, көміртегінің изотопы
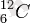 және т. б. табиғи радиоактивтік қасиеттері ашылды.
және т. б. табиғи радиоактивтік қасиеттері ашылды.
4. Атом құрылысының Н. Бор теориясы. Сутек атомының спектрі. Кванттық теорияның негізгі идеялары. Квант сандары.
Сутек спектрі ең қарапайым. Көрінетін денгейде Нα, Нβ, Нγ, Нσ таңбасымен белгіленген тек 4 сызық бар. Соған жақын жатқан ультрафиолет деңгейінде тағы да бір-бірінне жақын жатқан сызықтар бар. Бұл сызықтар алдында көрсетілген 4сызықтармен бірге сызықтар құрамын құрайды, оларды Бальмер сызықтар құрамы деп атайды. Швейцария ғалымы Больмер 1885 жылы осысерия сызықтардың толқындық санын ашты: Мұнда R=109678 см¹, -Ридберг түрақтылығы аталған, тұрақты сан, N=3, 4, 5, 6, . . . Сутек спектрін қарастырғанда оны зерттеген ғалымдардың Лаймен, Пашен, Бреккет атымен аталған басқа сериялары да ашылды. Бұл сериялардағы сызықтардың толқындық сандары төмендегі келтірілген жалпы формуламен есептелінеді:
Сонымен сутек спектріндегі көптеген сызықтар тек бір ғана байланыстылықпен өрнектеледі, ал спектрдің негізінде тек бір құбылыс жатқанын болжамдауға болады. Атомдардың сәуле шығаруы электрондардың қозғалысына байланысты деген көзқарас та болуы мүмкін. Бірақ атомдардың толқын ұзындығы белгілі сәуле шығаратындығы жәнне спектрдің сериялы сызық бойынша көрінетіндігі түсініксіз болатын. Сутек спектрінің сызықтық қасиетін түсіндіретін бірінші ғалым Нильс Бор болды. Ол 1913ж. Резерфордтын болжамын және Планктың кванттық теориясын қолданып, сутек атомының құрылыс теориясын ашты. Бор теориясының негізі ретінде екі постулатты ұсынды:1постулат. Элаектрон ядроның айналасында белгілі тұрақты орбита бой ынша айналып жүреді. Бұл орбитада электрон ешқандай энергия жоғалтпайды және сіңірмейді. Бор тұрақты орбитадағы электронның қозғалыс м-лшерінің моменті n/2π шамасына қатынаста болатындығы туралы болжамдады. Мына тендік:
Орындалған жағдайда, электронның қозғалысы тұрақты болуға тиісті, мұнда
m- электронның массасы,
V- жылдамдық,
r - орбитаның радиусы,
h - Планк тұрақтысы,
n - 1, 2, 3, . . . бүтін сандар.
Сутек атомы үшін, тұрақты орбиталдардың радиустары өзара бүтін сандардың квадраттары сияқты болады:
R1:R1: . . . Rn=1²:2²:3² . . . n²
Бордың болжамы бойынша кез келген тұрақты орбитада айналған кезде электрон энергиясы тұрақты. электронның энергиясы ядроға жақындаған сайын азая береді:
Е1<E2<E3 . . . <En
Бор теориясындағы энергия, қозғалыс мөлшерінің моменті сияқты, квант сандарымен анықталады. Ол мынаған тең:
2постулат. электрон бір орбитадан екіншіорбитаға ауысқагн кезде ғана энергия шығарылуы немесе сіңірілуі болады, мұнда белгілі бір жиілікпен тербелетін квант энергиясы бөлінеді немесе сіңіріледі:
атомның ядроға алыс орбитадағы энергиясы,
ядроға жақын орбитадағы энергиясы
Электрон кіші энегетикалық жағдайдан жоғары деңгейге ауысқан кездеэнергия сіңіріледі. Ал электрон жоғары деңгейден кіші энергетикалық деңгейге ауысқан кезде энергия бөлінеді. Электонның орнына байланысты, екі жағдлайдағы атомның энергиясын білу арқылы, ауысатын электронның тербеліс жиілігін есептеуге болады. Егер бір заттың атомдарына сыртқы энергия көзімен әсер етсе, онда электрон квант энергиясын сіңіріп, жоғарырақ орбитаға ауысады, демек, электрон қозған жағдайда келеді. Егер осындай ауысу жоғары орбитадан ядроға жақынырақ жатқан орбита аралығында болса, онда энергия сәулелік энергия- фотон түріде бөлінеді:
ΔE=Eж−Eа=hν
Спектрде ол белгілі сызықтар түрінде шығады. осы серияның әрбір сызықтарының толқын ұзындығы мына теңдеу бойынша, өте дәл есептелінеді:
Мұнда R- тұрақты шама, Ридберг костантасы.
Сызықтардын жиілігіфизи калық қасиеті ләі беклгісіз бүтін сандарға байланы сты. Бор бойынша, жақын және алыс , N- квантты сандарға жатады. Бор осы теңдеудің және атом құрылысының постулаттары негізінде, сутек атомы спектріндегі барлық сериялардың толқын ұзындығын есептейді. Жоғарыда көрсетілген теңдеулерден келесі өрнек алынады:
Сутек спектріндегі сериялардың сызықтары былай түсіндіріледі:егер электрон кез келген алыс жатқан орбитадан ядроға жақын бірінші орбитаға ауысса, онда спектрдің ультрафиолет ауданындағы жиілік толқындары бөлінеді. көп ұзамай, бұл серияны Лайман ашты . Ол Бор теориясының жақсы жетістігі еді. Егер электрондар кез келген алыс жатқан орбитадан екінші орбитаға ауысса, онда спектрдінң көрінетін сериясы алынады. Тәжірибелер Бор теориясын жақсы дәлелдеді. Есептеу арқылы алынған Ридберг тұрақтылығы, тәжірибе жүзінде алынған шамамен тура келді:
Бұл атомдарда тұрақты орбиталар болатындығын және Бор теңдеулерінің дұрыстығын дәлелдейтін үлкен жетістік еді. Бірақ Бор теориясының жетістігі тек сутек атомымен ғана шектелді. Гелий атомы үшін бул теория жарамады, ал күрделі атомдар үшін Бор теңдеулері бойынша есептеулерді мүлдем жүргізуге болмады. Көп электронды атомдардың спектріндегі сызықтар одан сайын күрделі бола бастады. спектрдің мультиплеттігі магтитті және элекр өрісінде күшейе түсті.
1925-26 жылдары неміс ғалымы Гейзенберг пен австриялық Э. Шредингер өз беттерінше жаңа механиканың екі варианттарын ұсынды. Бұл екі варианттың нәтижесі бірдей, бірақ, есептеуге қолайлы болғандықтан Шредингер теңдеуі жиірек қолданылады. Атом мен молекула құрылыстарының қазіргі теориялары да әдіске сүйенеді. Бұл теория микробөлшектердің қозғалысын және күйін сипаттайтын болғандықтан квант механикасы деп аталады. Ал Ньютон заңдарына негізделген микроденелерге арналған механика - классикалық механика д. а.
Квант сандары тек сутек атомындағы электронды сипаттап қоймайды, кез келген басқа атомдардағы электрондарды да қамтиды. Олар атомның қасиеті және химиялық байланыстың табиғатын түсіну үшін аса маңызды роль атқарады. Квант сандары электрон қозғалысын физикалық тұрғыдан сипаттайды, әрі электрон бұлтының геометриялық ерекшеліктерін бейнелеп береді. Бас квант саны Бор теориясынан шығатын санмен бір мәндес. Кванттық механикалық көзқарас бойынша бас квант саны орбитальдағы электронның энергиясын және орбитальдардың көлемін көрсетеді.
5. Көп электронды атомдардың орбитальдарының электрондармен толу принциптері: Энергияның минимум принципі, Паули принципі, Хунд ережесі. Клечковский ережелері. Элементтердің электрондық формулалары.
Элементтердің және оның қосылыстарының химиялық қасиеттері электрондық құрылысына байланысты. Атомдағы электрондардың энергетикалық орбитальдар бойынша орналасуы былай жүреді:1 энергия минимумы принципы; 2Паули принципі 3 Гунд және Клечковский ережелеріне сай.
Энергияның минимум принципі бойынша, электрондар әуелі энергиясы ең кіші орбитальдарға орналасады. Ең кіші энергия n=1 энергетикалық деңгей, осы орбитальда электрон өте тұрақты жағдайда болады. Сондықтан, көп электронды атомда әуелі n=1 деңгейі, сонан кейін n=2, n=3 . . . деңгейлері толтырылады. Бір бас квант саны шектігінде «n» орбитальдарының электронға толуы мына тәртіппен жүреді. s→p→d→f Кейбір уақытта бұл ережеден ауытқу байқалады. Кейбір жағдайда электрондар бір типті орбитальдан екінщі типті орбитальға ауысып кетуі мүмккін.
Паули принципі. Көпэлектронды атомдарда электронның жағдайы Паули ашқан квантты -механикалық заңмен өрнектеледі. Бұл заң бойынша, төрт квант сандарымен суреттелетін бір кванттық жағдайда тек бір ғана электрон болады. S-орбитальда спиндері антипараллель тек екі электрон ғана орналасады. Салдары: 1. Деңгейдегі электрондардың максимал саны негізгі кванттық санның екі еселенген квадратына тең 2. Деңгейшедегі электрондардың саны 2 (2l+1) ге тең.
Гунд ережесі. Бір деңгейшелер аралығында сәйкес орбитальдарды электрондармен толтырған кезде, электрондар спиндерінің қосындысы максимал болуы керек. Барлық орбиталдарда бір электроннан орналасқаннан кейін, келесі электрондар жұптасып орналасады.
Клечковский ережесі. Орыс ғалымы Клечковский өте қарапайым және нақты ереже ұсынды:элементтердегі атомдар электрондарының толтырылуы, квант сандары n+1 қосындысының өсуі тәртібі бойынша жүреді; егер екі деңгейдің қосындысы тең болса, онда бірінші n шамасы кіші деңгей толтырылады.
6. Периодтық заң мен периодтық жүйе. Периодтық заң. Атомдардың электрондық құрылымы және Д. И. Менделеев жасаған элементтердің периодтық жүйесі. Атомдар мен иондардың периодты түрде өзгеретін қасиеттері. Элементтердің периодтық кестесінің түрлері: олардың артықшылытары мен кемшіліктері.
Атом-молекулалық теориядан кейінгі химия тарихындағы ерекше маңызды ірі табыс Д. И. Менделеев ашқан периодтық заң болды. Осы заң негізінде элементтердің периодтық жүйесі жасалы. Периодтық заң-жаратылыстың негізгі заңдарының бірі, оның ашылуы химияда жаңа дәуір туғызды. Периодтық заң химиялық элементтерді, олардың қосылыстарын зерттеуге, заттың құрылысының қалай екенін іздеуге теориялық негіз болды. Осымен бірге атом құрылысының күрделілігін теория жүзінде жәнетәжірибе арқылызерттеу процесіндегіашылған жаңалықтар периодтылықтың мазмұның терең түсінуге мүмкіншілік туғызды. Химия тарихында ерекше табысты ғасыр, химияның теориялық негіздері атом-молекулалықтеория жәнеэлементтердің периодтық жүйесі ашылған - XIXғ-да химияда элемент жайындағы білім аса көбейді. Осы кезде белгілі болған элементтер саны 28 болса, Д . И. Менделеевтің заманыңда 63, ғасырдың аяғында 83
Болды. Осы кезде 109 элемент белгілі. Период ішіндегі элементтердің қасиеттерікүшті сілтілік металдан басталып, бірте-бірте металдық қасиеті кеміп, амфотерлі қасиеті артып, ақыры, бейметалдардың ең күштілерігалогендерге келіп. яғни инертті газбен бітеді. Горизонталь бағыт, период бойымен солдан оңға қарай. Бұл бағытта атомдық салмақ, ядро заряды, э лектрон саны біртіндеп өседі, осы ған сай металдық қасиет әлсіреп, бейметалдық қасиет күшейеді. Мундай өзгеру алғашқы периодтарда айқынырақ, кей інгі периодтарда баяуырақ болады. Мысалы, C мен Nқарағанда Sn менSb айырмашылығы аз. Вертикаль бағыт, негізгі және қосымша топшалар бойымен жоғарыдан төмен қарай. Бұл бағытта атомдық салмақ, ядро заряды, электрон саны сылыстырмалы түрде өзгереді, бірақ электрондық кұрылымының ұқсастығына байланысты және квант қабаттары санының артуына сай элементтердің қасиеті өте баяу өзгереді, айырмашылықтан ұқсастық көп. Гортизонталь жәнне вертикаль бағыттағы өзгерушілікті ұластыра қарасақ, кестенің сол жақ төменгі бұрышында негізгі топшаларда нағыз күшті металдар, оң жақ бұрышындағы негізгі топшаларды нағыз бейметалдар орналасқан.
7. Химиялық байланыс және зат құрылысы. Льюис пен Коссель теориялары. Коваленттік байланыс. Гайтлер мен Лондонның жұмыстары. Валенттік байланыс әдісі.
Химиялық байланыс - атомдардың химиялық қосылыс түзіп әрекеттесуі.
19 ғасырдың басында К. Бертолле Химиялық байланыс түзілуінің гравитациялық,
1810 жылы Й. Я Берцелиус электрхимиялық,
1861 жылы орыс ғалымы А. Н Бутлеров заттардың химиялық құрылыс теориясын,
1915 жылы неміс физигі Кассель,
1916 жылы ағылшын ғалымы Г. Льюис электрондық теорияларын ұсынды.
Кванттық механика көзқарасы тұрғысынан Хиялық байланыс валенттілік сұлба және молекулалық орбиталдар әдісімен түсіндіріледі. Химиялық байланыс түзілуіне қарай төртке бөлінеді: иондық ковалентті металдық сутектік
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz